微小RNA-490-3p靶向FK506相关蛋白14表达抑制骨肉瘤MG63细胞侵袭和迁移的实验研究
陈夫圆,孙利平,朱远见,孟猛
骨肉瘤是一种好发于青少年或儿童的恶性骨肿瘤。虽然手术、化疗和放疗等常规治疗方法使病人预后的生存率有所改善,但对多数已发生转移病人的治疗作用并不理想[1-2]。因此,如何有效地抑制肿瘤细胞恶性转移是治疗骨肉瘤的重要策略。研究显示,微小RNAs(microRNAs,miRNAs)可通过调控相关靶基因在骨肉瘤在内的多种肿瘤的发生发展过程中发挥着致癌或抑癌作用[3-8]。微小RNA-490-3p(miR-490-3p)是miRNAs中的重要一员,被证实在结肠癌、胃癌和肝癌等多种肿瘤组织或细胞中异常低表达,且可通过调控细胞增殖、侵袭、迁移和凋亡等过程发挥着重要的抑癌作用[9-11]。已有研究指出,miR-490-3p在骨肉瘤组织中表达下调,且其表达水平与远处转移、临床晚期、整体生存率和无复发生存率显著相关[12];而上调其表达可通过靶向调控高迁移率族蛋白A2(HMGA2)表达抑制癌细胞增殖并诱导细胞凋亡[13];然而,其对骨肉瘤细胞侵袭和迁移的作用并不明确。因此,本研究于2019年9月至2020年4月进行体外细胞实验,观察miR-490-3p对骨肉瘤MG63细胞侵袭和迁移的影响,旨在探究miR-490-3p在骨肉瘤转移中的作用及其可能机制,以期为骨肉瘤的治疗提供分子靶点。
1 材料与方法
1.1 主要试剂与仪器人骨肉瘤细胞株MG63购于中科院上海细胞库,miR-490-3p模拟物(miR-490-3p mimics)、miR-490-3p抑制剂(anti-miR-490-3p)及其相应的模拟物阴性对照miR-NC、抑制剂阴性对照(anti-miR-NC)和PCR引物购于上海吉玛公司。RPMI-1640培养基购于美国Hyclone公司,Transwell小室购于美国Costor公司,胰蛋白酶和胎牛血清购于美国Gibco公司,cDNA第一链合成试剂盒购于美国Thermo公司,LipofectamineTM2000转染试剂购于美国Invitrogen公司,双荧光素酶报告基因检测试剂盒购于美国Promega公司,兔抗人β-肌动蛋白(β-actin)单克隆抗体购于北京中杉金桥公司,兔抗人FK506相关蛋白14(FKBP14)、基质金属蛋白酶-2(MMP-2)多克隆抗体购于美国Abcam公司,鼠抗人钙黏蛋白E(E-cadherin)单克隆抗体和Twist多克隆抗体购于美国Santa Cruz公司。人FKBP1基因ORF全长cDNA克隆表达载体及其空载体对照购于北京义翘神州科技有限公司。二氧化碳培养箱,美国Thermo公司;PCR仪,美国MJ Research公司;凝胶成像系统,美国BioRad公司;光学显微镜和荧光显微镜,日本Olympus公司。
1.2 细胞培养、分组与转染以含10%胎牛血清、100 U/mL链霉素和100 U/mL链霉素的RPMI-1640完全培养基于5%二氧化碳、37℃和饱和湿度的细胞培养箱内常规培养,待细胞贴壁生长至90%时,采用0.25%胰蛋白酶消化传代。将生长状况良好的指数期MG63细胞分为对照组(未处理)、miR-NC组(转染miR-NC)和miR-490-3p组(转染miR-490-3p mimics)。当细胞汇合度达70%时,参照转染试剂LipofectamineTM2000说明书步骤将miR-490-3p mimics及miR-NC根据实验分组转染至MG63细胞中。转染48 h后收集细胞进行后续miR-490-3p表达检测、侵袭和迁移实验检测以及MMP-2、E-cadherin、上皮间质转化因子Twist转录因子(Twist)蛋白检测。实验后期另设miR-490-3p+pcDNA组(共转染miR-490-3p mimics和空载体对照)、miR-490-3p+FKBP14组(共转染miR-490-3p mimics和FKBP14表达载体),参照上述方法转染48 h后,收集对照组、模拟物阴性对照(miR-NC)组、miR-490-3p模拟物(miR-490-3p)组、miR-490-3p模拟物+空载体对照(miR-490-3p+pcDNA)组和miR-490-3p模拟物+FKBP14表达载体(miR-490-3p+FKBP14)组细胞进行侵袭和迁移实验以及MMP-2、E-cadherin、Twist、FKBP14蛋白检测。
1.3 实时荧光定量PCR检测miR-490-3p的表达收集“1.2”中转染48 h后的待测细胞,加入1mL Trizol试剂提取总RNA,并对RNA的浓度进行检测。再按照cDNA第一链合成试剂盒说明书将RNA逆转录合成单链cDNA,将1 μL cDNA作为模板,加入Maxima SYBR Green qPCR Master Mix 10 μL、浓度为10 μmol PCR正反引物各0.5 μL和双蒸水8 μL制成20 μL PCR反应体系,上PCR仪,并设定反应程序为95℃、3 min(1个循环),95℃、30 s,58℃、30 s,72℃、30 s(共40个循环),待循环结束后记录数据,以U6为内参基因,2-ΔΔCt法计算miR-490-3p的表达水平。
1.4 Transwell小室法检测细胞侵袭和迁移收集“1.2”中转染48 h后的细胞,调整细胞密度为1×105个/毫升。实验前提前1 d将Transwell小室放入24孔板内,加入100 μL稀释的Matrigel基质胶(无血清培养基稀释)室温下充分凝固。次日,取细胞悬液200 μL加入到Transwell小室上层,并在小室下层加入500 μL含血清的培养基,每组设3个复孔。在细胞培养箱中常规培养24 h后,吸去上室液体并以棉签小心擦去残留的细胞,以4%多聚甲醛对下室细胞进行固定30 min。去固定液后,以0.1%结晶紫染色15 min。去染色液后,在显微镜下随机选取3个视野统计穿膜细胞数,结果以3个视野细胞数的均值表示侵袭细胞中。迁移实验中无需对Transwell小室铺Matrigel基质胶,其余步骤同侵袭实验。
1.5 蛋白质印迹法检测MMP-2、E-cadherin、Twist和FKBP14蛋白的表达向待测细胞中加入通用蛋白裂解液于冰上裂解抽提总蛋白后,BCA法检测总蛋蛋白浓度与纯度。向蛋白样品中加入1/4体积的5×上样缓冲液于100℃中变性6 min。取蛋白样品80 μg加入到SDS-PAGE凝胶孔中进行电泳。电泳结束后,转膜。将PVDF膜放入脱脂奶粉中封闭2 h。经1×TBST溶液洗膜后,放入MMP-2(1∶800)、E-cadherin(1∶800)、Twis(t1∶1 000)、FKBP14(1∶1 000)和β-actin(1∶1 000)一抗工作液中,并于4℃下孵育过夜。次日,经1×TBST溶液洗膜后,加入辣根过氧化酶标记的二抗(1∶2 000)室温孵育1 h。ECL显影后,凝胶成像系统扫描,并以β-actin为内参分析目的蛋白的表达水平。
1.6 荧光素酶实验测定miR-490-3p和FKBP14的靶向关系采用TargetScan、miRanda和miRBase三大生物信息学软件预测到FKBP14的3’UTR存在能够与miR-490-3p互补结合的位点,为了验证miR-490-3p与FKBP14是否存在靶向关系,构建含FKBP14 3’UTR野生结构(野生型FKBP14-WT)和FKBP14 3’UTR突变结构(FKBP14-MUT)的FKBP14 3’UTR荧光数酶报告载体。按照转染试剂说明书步骤 行miR-NC+FKBP14-WT、miR-490-3p(mimics)+FKBP14-WT、miR-NC+FKBP14-MUT、miR-490-3p(mimics)+FKBP14-MUT四组共转染,在培养箱中培养48 h后,收集各组细胞检测其荧光素酶活性,具体步骤参照双荧光素酶报告基因检测试剂盒说明书。
1.7 统计学方法实验数据以形式表示,采用SPSS 22.0进行统计学分析,多组间比较使用单因素方差分析,组间多重比较采用SNK-q。miR-NC+FKBP14-WT组与miR-490-3p+FKBP14-WT组及miR-NC+FKBP14-MUT组 与miR-490-3p+FKBP14-MUT组 荧 光素酶活性比较采用独立样本t检验。P<0.05为差异有统计学意义。
2 结果
2.1 转染miR-490-3p模拟物后MG63细胞中miR-490-3p表达升高与对照组1.02±0.10比较,miR-490-3p在miR-NC组细胞中的表达0.96±0.09未见明显改变(P>0.05),但在miR-490-3p组细胞中的表达水平3.68±0.37明显升高(P<0.05)。
2.2 上调miR-490-3p抑制MG63细胞侵袭和迁移与对照组(76.52±6.00、97.85±6.45)比较,miR-490-3p组中侵袭细胞数和迁移细胞数(73.48±5.35、98.02±5.84)均 明 显 增 多(P<0.05);但miR-NC组(73.48±5.35、98.02±5.84)和对照组相比数量差异无统计学意义(P>0.05)。三组侵袭细胞数与迁移细胞数比较差异无统计学意义(F=76.42、94.45,均P<0.001),见图1。
2.3 上调miR-490-3p抑制MG63细胞中E-cadherin、MMP-2、Twist和FKBP14蛋白的表达与对照组比较,miR-490-3p组细胞中MMP-2、Twist和FKBP14蛋白的表达水平明显降低,而E-cadherin蛋白的表达水平明显升高(P<0.05),但miR-NC组与对照组比较未见明显改变(P>0.05)。见图2,表1。

图2 蛋白质印迹法检测E-cadherin、MMP-2、Twist和FKBP14蛋白的表达
表1 各组细胞中E-cadherin、MMP-2、Twist和FKBP14蛋白的表达水平/

表1 各组细胞中E-cadherin、MMP-2、Twist和FKBP14蛋白的表达水平/
注:E-cadherin为钙黏蛋白E,MMP-2为基质金属蛋白酶-2,Twist为上皮间质转化因子Twist转录因子,FKBP14为FK506相关蛋白14,miR-NC为模拟物阴性对照,miR-490-3p为miR-490-3p模拟物。①与对照组比较,P<0.05。
组别对照组miR-NC miR-490-3p F值P值重复次数333 E-cadherin 0.12±0.03 0.13±0.02 0.46±0.03①153.14<0.001 MMP-2 0.76±0.05 0.78±0.06 0.38±0.03①65.31<0.001 Twist 0.72±0.06 0.74±0.05 0.33±0.03①68.70<0.001 FKBP14 0.68±0.04 0.73±0.06 0.27±0.03①93.98<0.001
2.4 FKBP14是miR-490-3p潜在靶基因FKBP14 3'UTR与miR-490-3p存在互补的结合位点。与miR-NC+FKBP14-WT组比较,miR-490-3p+FKBP14-WT组细胞的荧光素酶活性明显降低(0.34±0.03比1.02±0.06,t=17.56,P<0.05),但miR-NC+FKBP14-MUT组 和miR-490-3p+FKBP14-MUT组 细 胞 的 荧 光素酶活性未见显著差异(0.97±0.06比0.99±0.07,t=0.38,P=0.726)。FKBP14引物序列为5'UACCACGACAUGAGACCAGGUUA3',miR-490-3p引物序列为3'GUCGUACCUCAGGAGGUCCAAC5',结合位点为319-326 of FKBP14 3'UTR。
2.5 上调FKBP14表达逆转miR-490-3p对MG63细胞侵袭和迁移的抑制作用与对照组比较,miR-490-3p组中侵袭细胞数、迁移细胞数和FKBP14、MMP-2、Twist蛋白的表达水平明显降低,E-cadherin蛋白的表达水平明显升高(P<0.05);而miR-NC组与miR-490-3p组之间差异无统计学意义(P>0.05);与miR-490-3p组比较,miR-490-3p+FKBP14组中侵袭细胞数、迁移细胞数和FKBP14、MMP-2、Twist蛋白的表达水平明显升高,E-cadherin蛋白的表达水平明显降低(P<0.05),但miR-490-3p组与miR-490-3p+pcDNA组之间上述指标差异无统计学意义(P>0.05)。见图3,表2。
表2 各组侵袭细胞数、迁移细胞数和FK506相关蛋白14、上皮间质转化因子Twist转录因子、基质金属蛋白酶-2和钙黏蛋白E蛋白表达水平/
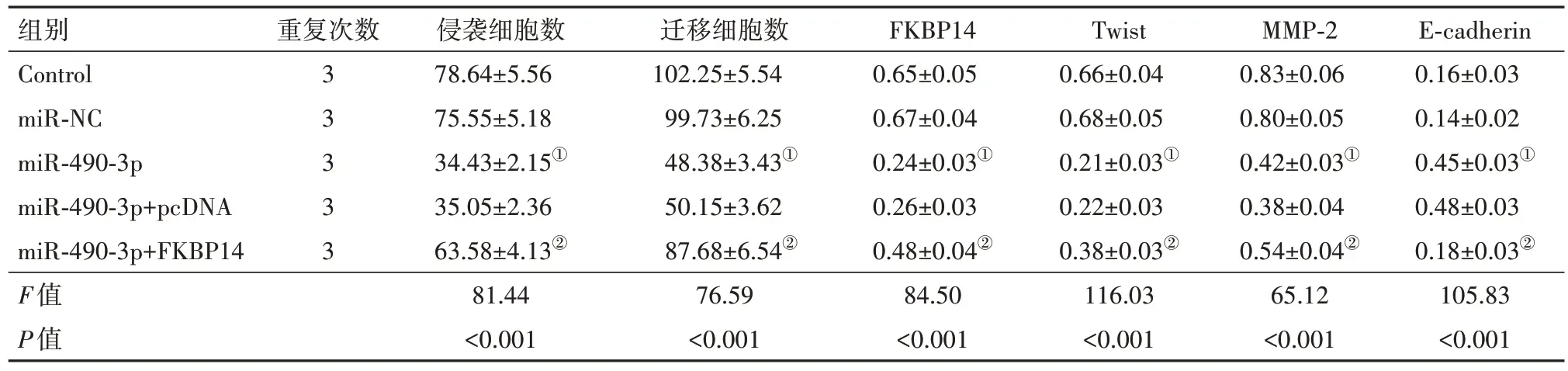
表2 各组侵袭细胞数、迁移细胞数和FK506相关蛋白14、上皮间质转化因子Twist转录因子、基质金属蛋白酶-2和钙黏蛋白E蛋白表达水平/
注:FKBP14为FK506相关蛋白14,Twist为上皮间质转化因子Twist转录因子,MMP-2为基质金属蛋白酶-2,E-cadherin为钙黏蛋白E。①与miR-NC组比较,P<0.05。②与miR-490-3p+pcDNA组比较,P<0.05。
组别Control miR-NC miR-490-3p miR-490-3p+pcDNA miR-490-3p+FKBP14 F值P值重复次数33333侵袭细胞数78.64±5.56 75.55±5.18 34.43±2.15①35.05±2.36 63.58±4.13②81.44<0.001迁移细胞数102.25±5.54 99.73±6.25 48.38±3.43①50.15±3.62 87.68±6.54②76.59<0.001 FKBP14 0.65±0.05 0.67±0.04 0.24±0.03①0.26±0.03 0.48±0.04②84.50<0.001 Twist 0.66±0.04 0.68±0.05 0.21±0.03①0.22±0.03 0.38±0.03②116.03<0.001 MMP-2 0.83±0.06 0.80±0.05 0.42±0.03①0.38±0.04 0.54±0.04②65.12<0.001 E-cadherin 0.16±0.03 0.14±0.02 0.45±0.03①0.48±0.03 0.18±0.03②105.83<0.001
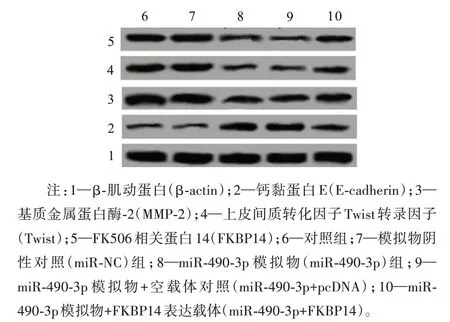
图3 蛋白质印迹法检测FKBP14、Twist、MMP-2和E-cadherin蛋白的表达
3 讨论
本研究成功上调骨肉瘤MG63细胞中miR-490-3p表达后发现,MG63细胞侵袭和迁移能力明显受到抑制。miR-490-3p是一种进化上高度保守的miRNA,定位于人17号染色体上;被证实可通过调控相关靶基因在肿瘤恶性转移过程中发挥着重要的抑制作用[14]。Kang等[15]在食管鳞状细胞癌研究指出,上调miR-490-3p表达可通过靶向调控HMGA2抑制肿瘤细胞的侵袭、迁移和上皮间质转化。Fan、Zhang[16]研究指出,miR-490-3p在前列腺癌PCa细胞中表达下调,下调其表达可靶向调控HDAC2促进癌细胞的侵袭和迁移。本研究结果在骨肉瘤中进一步证实miR-490-3p抗肿瘤细胞转移的作用。这提示,miR-490-3p可能在骨肉瘤恶性转移过程中发挥着重要的抑制作用。
为了探讨miR-490-3p抑制MG63细胞转移的分子机制,本研究采用蛋白质印迹法检测发现,上调miR-490-3p表达后可使MG63细胞中MMP-2和Twist表达降低,而E-cadherin表达升高。MMP-2是基质金属蛋白酶家族成员,可降解细胞外基质中的胶原蛋白,在骨肉瘤细胞侵袭和迁移过程中发挥着重要作用[17-18];上皮间质转化是赋予细胞侵袭和迁移能力的生物学过程,而E-cadherin是重要的上皮标志物,Twist是细胞发生上皮间质转化的重要诱导因子,主要功能是抑制E-cadherin表达[19]。E-cadherin和Twist均在骨肉瘤组织中异常表达,在肿瘤细胞侵袭和转移过程中发挥着重要作用[20-21]。结果提示,miR-490-3p可能通过抑制MG63细胞上皮间质转化进而减弱癌细胞侵袭和迁移。
另外,本研究还发现,miR-490-3p表达上调还可以引起MG63细胞中FKBP14表达降低。FKBP14是FK506结合蛋白家族成员,具有受体信号传导、激酶活性和蛋白折叠等多种生物功能,其在胃癌和卵巢癌等多种肿瘤中异常高表达,可通过调控细胞侵袭、迁移等过程促进肿瘤的发生发展[22-23]。同时,本研究采用生物信息学软件预测发现,FKBP14 3’UTR区域存在能够与miR-490-3p互补的结合位点。双荧光素酶实验证实,FKBP14是miR-490-3p的潜在靶基因。Huang等[24]和Wang等[25]研究证实FKBP14在骨肉瘤组织和细胞系中过度表达,其表达水平与肿瘤转移、复发和不良生存时间等有关;可通过促进癌细胞侵袭和粘附等在骨肉瘤的恶性进展中发挥着积极作用。本研究转染FKBP14表达质粒成功上调FKBP14表达后发现,FKBP14可逆转miR-490-3p对MG63细胞侵袭、迁移以及FKBP14、Twist、MMP-2和E-cadherin蛋白表达的调控作用。这提示,miR-490-3p可通过靶向调控FKBP14表达抑制骨肉瘤MG63细胞侵袭和迁移。
本研究首次通过体外细胞实验探究了上调miR-490-3p可靶向抑制FKBP14的表达降低骨肉瘤细胞的迁移和侵袭能力,miR-490-3p/FKBP14轴可能为骨肉瘤的治疗提供了潜在的分子靶标。但本研究仅在细胞层面进行了探究,且miR-490-3p/FKBP14轴下游信号通路对骨肉瘤转移的影响也还未进行探究,因此,本研究接下来将进一步通过动物实验在体内验证miR-490-3p/FKBP14轴在骨肉瘤发生发展中的作用,并深入探究其下游信号通路对骨肉瘤发生发展的影响,为深入了解骨肉瘤发生发展的机制及其治疗靶点的选择提供实验依据。

