温敏性W/O/W型多重乳液的制备及其对维生素C的控释性
符 叶, 周 庄, 王 大 鸷
( 大连工业大学 轻工与化学工程学院, 辽宁 大连 116034 )
0 引 言
多重乳液作为一种优良的缓释载体材料,因其特殊的物理结构及优良的缓释效果已在化妆品行业等众多领域引起广泛关注。传统W/O/W多重乳液具有双层界面膜,不仅可保护其内水相中包裹的水溶性活性物质在使用前不被氧化而保持活性,而且在使用中活性物需要通过两层界面膜被释放,具有活性物释放速度稳定及活性物作用时间延长的理想效果[1-2]。近年来,为推动多重乳液在实际生产中的应用,替代现有缓释手段,越来越多的具有更佳缓释效果的多重乳液体系被提出。Zhang等[3]以多元醇替换传统内水相,利用多元醇较高的黏度来提高多重乳液的稳定性及缓释效果。Faghmous等[4]在多重乳液中加入壳聚糖,利用壳聚糖在油和内水相之间形成刚性界面层增强缓释作用。现有研究大多基于提高多重乳液内水相黏度,通过增加内水相内部释放阻力实现W/O/W型多重乳液缓释作用的增强。但是内水相黏度的过度增加会因其对多重乳液内部渗透压的影响,导致内外水相间的水传递加强,易引起多重乳液溶胀及失稳[5-6],不利于多重乳液的长期存放,限制应用前景。温敏性高分子是对温度刺激具有响应性的智能高分子材料,如泊洛沙姆、聚乙烯吡咯烷酮等。温敏性高分子在水溶液中存在一个低临界溶解温度(LCST),当温度低于或高于LCST时,整个大分子结构随温度响应分别产生线团或胶粒的构象转变[7],产生对高分子水溶液物理特性(如黏度)的变化。温敏高分子因其特有的温度响应性而广泛应用于药物缓释及物料分离提纯等领域。在化妆品领域,如面膜等化妆品一般在常温下储存而使用时是作用在具有一定温度(37 ℃)的人体皮肤表面。因此,可利用该类化妆品储存和使用时的不同环境温度,利用温敏性材料的温度响应机制,选用适合的温敏性高分子材料构建多重乳液内水相,制备面向化妆品应用的具有温度响应特性的新型多重乳液,可使该多重乳液在长期常温(低于LCST)储存中保持内水相低黏度、低渗透压,利于多重乳液长期稳定;当该多重乳液作用于人体皮肤表面时(高于 LCST),内水相温敏性高分子随温度响应凝胶化,大幅改变内水相传质阻力,从而增强内部活性物质的缓释效果,达到延长作用时间及增加释放量的目的。
本研究以泊洛沙姆水溶液(P)构建内水相、碳酸二辛酯(DHC)为油相、去离子水为外水相制备出具有温度响应特性的W/O/W型多重乳液体系,确定了多重乳液最佳制备条件。同时将维生素C包裹于多重乳液中,对维生素C进行模拟体外释放实验,验证该温敏性W/O/W新型多重乳液在化妆品领域中应用的可行性。
1 实 验
1.1 材料与仪器
材料:碳酸二辛酯、聚甘油-3二异硬脂酸酯、泊洛沙姆407、泊洛沙姆188,德国BASF公司;大豆卵磷脂,分析纯,天津市光复精细化工研究所;六聚甘油单硬脂酸酯、十聚甘油单硬脂酸酯,山东滨州金盛新材料科技有限公司;抗坏血酸(维生素C),分析纯,国药集团化学试剂厂;透析袋(截留相对分子质量200),北京瑞达恒辉科技发展有限公司。
仪器:高剪切均质乳化机、相差显微镜,上海弗鲁克流体机械制造有限公司;Zeta电位仪,英国马尔文仪器公司;紫外分光光度计,上海山岳科学仪器有限公司。
1.2 实验方法
1.2.1 多重乳液的制备
采用如图1所示两步乳化法制备多重乳液:

图1 W/O/W多重乳液制备示意图
(1)将泊洛沙姆混合水溶液(23%泊洛沙姆407,1.18%泊洛沙姆188,其余为去离子水[8])在5 ℃下滴入含大豆卵磷脂、TGI的DHC中乳化5 min,制得W/O型乳液,记为E1。
(2)将制好的W/O乳液在5 ℃下滴加至含有6-PGFE、10-PGFE的外水相中,乳化3 min,制得W/O/W型多重乳液[9-10]。消泡后,测量多重乳液的粒径及电位。
1.2.2 包裹维生素C多重乳液的制备
分别将不同含量的维生素C低温下溶解在内水相中[11],采用两步乳化法制备包裹维生素C的多重乳液。同时制备维生素C水溶液、未添加泊洛沙姆的多重乳液进行比对实验,组分如表1所示。
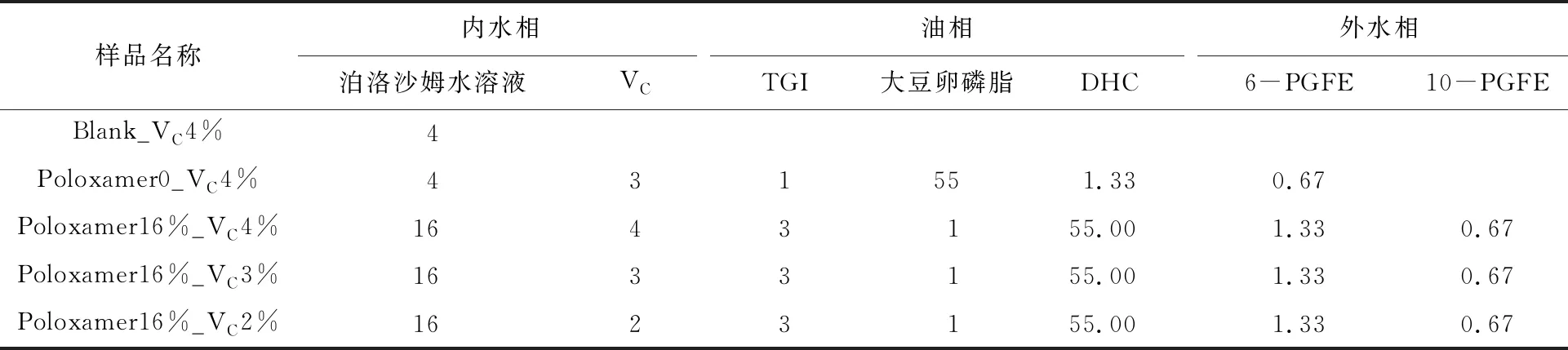
表1 维生素C多重乳液组分的质量分数
1.3 粒径的测定
取一定量的多重乳液稀释10倍,滴在载玻片上,用相差显微镜观察其结构,计算多重乳液的平均粒径。计算公式:
式中:Di为粒子的直径;Ni为直径为Di的粒子个数。
1.4 Zeta电位的测定
将制备的多重乳液稀释至0.05 mg/mL,通过Zeta电位仪测定其电位,经过3次测量取平均值[12-14]。
1.5 乳液的外观观察
将乳液置于40 ℃真空干燥箱中24 h,观察其稳定性。
1.6 维生素C标准曲线的测定
准确称取0.1 g维生素C定容于100 mL容量瓶中,超声10 min使其完全溶解,再分别移取0.125、0.250、0.375、0.500、0.625、0.750 mL至25 mL容量瓶中,加磷酸盐缓冲溶液定容。其吸光度与浓度的关系式为Y=77.437X-0.000 7,R=0.999 88。
1.7 累积释放率的测定
因为维生素C易溶于水,因此选择磷酸盐缓冲液作为透析液,pH为5.8(与人体皮肤表面的pH相近)。取5 g多重乳液放入透析袋,浸于200 mL pH=5.8的磷酸盐缓冲溶液释放介质中,在37 ℃、避光、搅拌条件下透析12 h。分别在10 min、30 min、1 h、2 h、4 h、6 h、8 h、10 h、12 h取透析袋外缓冲溶液5 mL,用紫外分光光度计在波长266 nm处测定其吸光度,同时补入同温度的释放介质5 mL[15-17]。
式中:Q为累积释放率,%;ρn为第n个时间点所取样品质量浓度,mg/mL;V为释放介质总体积,mL;Vi为第i个时间点所取样品体积,mL;ρi为第i个时间点所取样品质量浓度(V0和ρ0均为0),mg/mL;m为投入的多重乳液质量,mg;x为多重乳液的载药量,%。
2 结果与讨论
2.1 多重乳液的显微结构
由图2(a)可以明显看到DHC中分散着泊洛沙姆小颗粒,粒径均一,分散均匀,加强了乳液的稳定性。图2(b)、(c)分别为多重乳液在不同倍数下的显微镜图片,可以明显地看到大的液滴里包含着许多泊洛沙姆小颗粒,证明W/O/W型多重乳液已成功制备。

(a) P/O乳液
2.2 多重乳液的稳定性
2.2.1 TGI质量分数对乳液稳定性的影响
E1质量分数为40%,其中P质量分数为40%,大豆卵磷脂质量分数为1%,DHC质量分数为55%,6-PGFE与10-PGFE总质量分数为2%,6-PGFE与10-PGFE质量比为3∶1。如图3(a)所示,乳液粒径随体系中TGI含量的增加而少量增加;而电位的绝对值在前期呈现快速增大趋势,但当TGI质量分数超过3%后,电位变化趋于稳定。图3(a)照片为样品在40 ℃下放置24 h后的稳定性结果,可观察到当体系中TGI质量分数低于3%时,样品出现了明显分层现象(样品1、样品2箭头所标示);当样品中TGI质量分数高于3%(样品3~5)时,乳液较稳定。观测结果与图中电位的变化趋势一致。由于多重乳液液滴间静电斥力的大小(电位绝对值越大,静电斥力越大)影响乳液稳定性[18],因此样品1及样品2所显示出的较差的乳液稳定性可归因于其较弱的液滴间静电斥力。
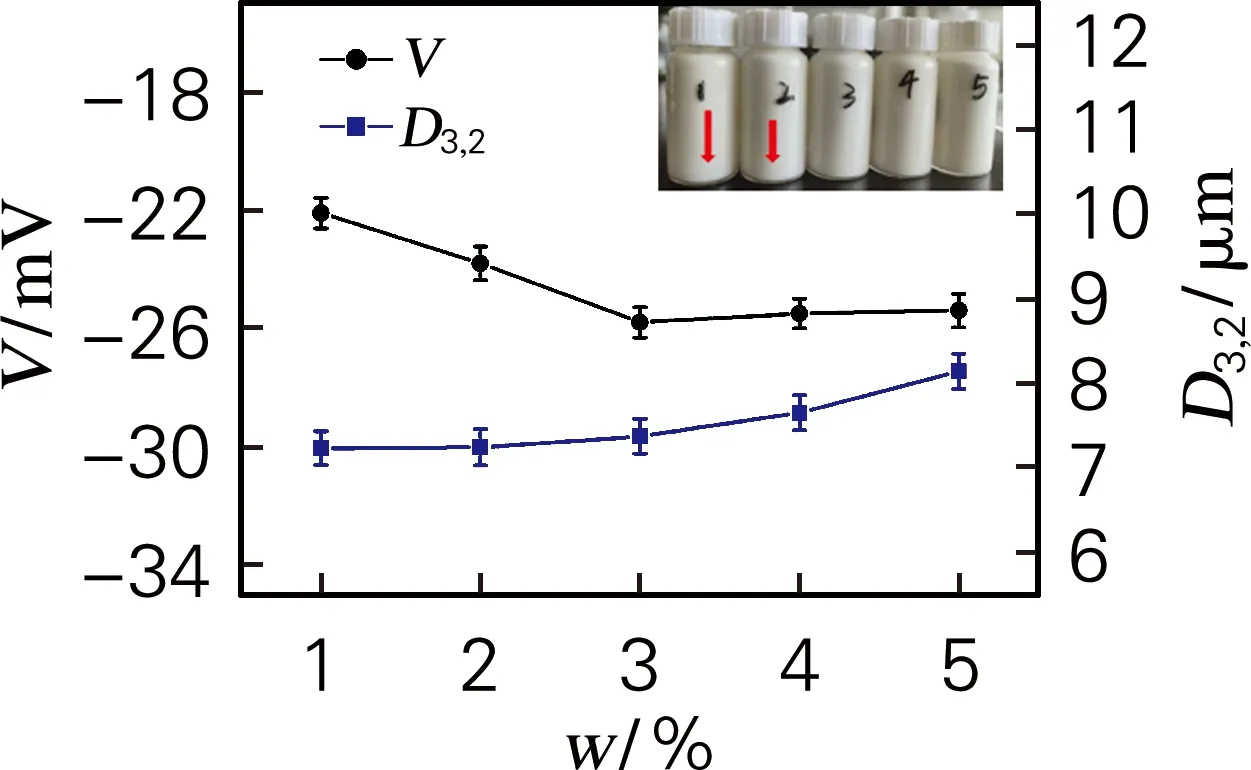
(a) TGI质量分数
2.2.2 6-PGFE与10-PGFE总质量分数对乳液稳定性的影响
E1质量分数为40%,其中P质量分数为40%,大豆卵磷脂质量分数为1%,TGI质量分数为3%,DHC质量分数为55%,6-PGFE与10-PGFE 比例为3∶1。图3(b)显示,当6-PGFE+10-PGFE质量分数由0.5%提高到3.0%后,乳液粒径从20 μm左右逐渐减小到5 μm以下;同时电位绝对值也随之逐渐增加,但当6-PGFE+10-PGFE超过2.0%后,电位变化不明显。观测结果也表明当体系中6-PGFE+10-PGFE质量分数大于2.0%时,乳液稳定性较好(样品4~6所示)。虽然样品3中乳液电位的绝对值也相对较大,但依然观测到了分层现象。考虑到液滴粒径及乳液黏度对多重乳液稳定性的作用[19-20],样品3中相对不理想的乳液稳定性可能来自其相对较大的液滴粒径及较小的乳液黏度的影响(相比较于样品4~6)。
2.2.3 6-PGFE与10-PGFE质量比对乳液稳定性的影响
E1质量分数为40%,其中P质量分数为40%,大豆卵磷脂质量分数为1%,TGI质量分数为3%,DHC质量分数为55%,6-PGFE与10-PGFE总质量分数为2%。图3(c)结果表明,随着6-PGFE与10-PGFE质量比的增大,粒径及电位均呈现先减小后增加的趋势,都于二者质量比为2∶1时出现拐点。当6-PGFE与10-PGFE质量比小于2∶1时,40 ℃环境温度下乳液放置24 h后出现分层现象。
2.2.4 DHC质量分数对乳液稳定性的影响
E1质量分数为40%,其中P质量分数为40%,大豆卵磷脂质量分数为1%,TGI质量分数为3%,6-PGFE与10-PGFE总质量分数为2%,6-PGFE与10-PGFE质量比为2∶1。图3(d)中,随着DHC质量分数的增大,粒径及电位均总体呈现缓慢下降趋势,当DHC质量分数大于55%后,电位有所上升,同时乳液出现分层现象。这是由于随着DHC质量分数的增大,乳液油滴界面不断增大,吸附更多的乳化剂TGI,使油滴表面所带电荷增多,有利于乳液稳定。当DHC质量分数持续增大接近某一边界值后,根据DLVO理论,颗粒在布朗运动等作用下相互靠近,同时存在着范德华引力和静电斥力,继续添加DHC,双电层斥力被压缩,双电层变薄,乳液稳定性变差,引起乳液分层[21]。
2.2.5 E1质量分数对乳液稳定性的影响
P质量分数为40%,大豆卵磷脂质量分数为1%,TGI质量分数为3%,6-PGFE与10-PGFE总质量分数为2%,6-PGFE与10-PGFE质量比为2∶1。从图3(e)可看到,随着E1质量分数的增大,粒径缓慢小幅增大;电位的绝对值虽然在前期有所增大,但当E1质量分数高于40%后,电位的绝对值快速减小。E1质量分数低于40%时,乳液中可观测到分层现象。
综合以上结果,当该新型多重乳液体系中TGI质量分数为3%、6-PGFE+10-PGFE质量分数为2%、DHC质量分数为55%、E1质量分数为40%时,乳液稳定性理想,且乳液制备经济性较好。
2.3 维生素C的模拟体外释放
通过透析袋法评价维生素C的体外释放情况。图4显示对照组维生素C水溶液快速释放,未加泊洛沙姆的多重乳液在释放到80%时就不再释放,而维生素C质量分数为4%的添加泊洛沙姆的多重乳液在12 h内缓慢持续释放,最终累积释放率高于90%。
由图4可以看出,维生素C在1 h内有突释,随后趋于平缓,随着维生素C含量的增加,释放速率逐渐增大。维生素C水溶液在1 h内释放率达到80%,未加泊洛沙姆的多重乳液在1 h内释放60%左右,而且在释放到80%时就不再释放。添加泊洛沙姆的多重乳液在1 h内对维生素C的释放率在40%左右,随后释放率缓慢增大,当维生素C质量分数为4%时,最终释放率高于90%,对比说明添加泊洛沙姆的多重乳液对维生素C具有很好的缓释作用。这是因为未加泊洛沙姆多重乳液中的维生素C从内水相透过油膜,由Fickian定律扩散到外水相[22],然后释放到缓冲溶液中,释放到一定程度内外渗透压达到了平衡状态时将不再释放。而添加泊洛沙姆的多重乳液由于泊洛沙姆在37 ℃时会形成凝胶状内界面[23],有利于控制维生素C的释放。此外,泊洛沙姆有强的亲水性,它与维生素C的羟基之间形成额外的分子间氢键[24],提高了内水相的黏度,从而阻止维生素C向外释放,减慢维生素C的氧化速度。
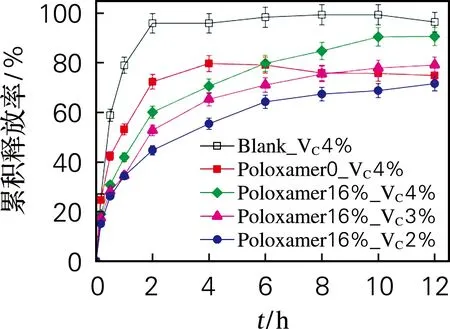
图4 维生素C的累积释放曲线
3 结 论
利用温敏性泊洛沙姆材料采用两步乳化法成功制备了具有温敏特性的W/O/W新型多重乳液。研究结果表明,当TGI的质量分数为3%、大豆卵磷脂的质量分数为1%、DHC的质量分数为55%、6-PGFE+10-PGFE的质量分数为2%、6-PGFE 与10-PGFE的质量比为2∶1、E1的质量分数为40%的制备条件下,得到稳定性最佳的新型多重乳液,乳液平均粒径为(6.4±0.5) μm,电位绝对值为(33.3±0.3) mV。体外释放模拟实验表明,该温敏性多重乳液具有理想的维生素C缓释效果,12 h内的累积释放率高于90%,在化妆品领域具有较好的应用前景。

