慢加急性肝衰竭肝移植围手术期康复评估与干预专家共识
中国医师协会器官移植医师分会移植免疫学专业委员会 中国康复医学会器官移植康复专业委员会广东省医师协会器官移植医师分会
肝移植是治疗慢加急性肝衰竭(acute on chronic liver failure,ACLF)唯一有效的方法,但长期慢性肝病状态以及手术打击导致的营养障碍和器官功能不全仍严重影响患者术后恢复。康复干预在肝病和外科手术患者中的应用已经得到国内外的认可,早期康复不仅可降低患者重症监护室(intensive care unit,ICU)入住时间和住院时间,还可以减少再入院机会[1-2]。ACLF肝移植患者中如何实施康复,目前尚缺乏统一的共识,为进一步规范并推广康复治疗在ACLF患者肝移植围手术期的应用,改善ACLF患者肝移植预后,中国医师协会器官移植医师分会移植免疫学专业委员会、中国康复医学会器官移植康复专业委员会和广东省医师协会器官移植医师分会在前期ACLF围手术期综合管理共识的基础上[3-6],进一步提出围手术期康复评估与干预的重要性,并组织相关专家制定该共识。共识主要包括ACLF患者肝移植围手术期的康复评估以及在此基础上制定的个体化康复方案。
本共识的循证医学证据质量等级和推荐强度等级按照证据推荐分级的评估、制订与评价(Grading of Recommendations Assessment,Development and Evaluation,GRADE)进行分级(表1)[7]。
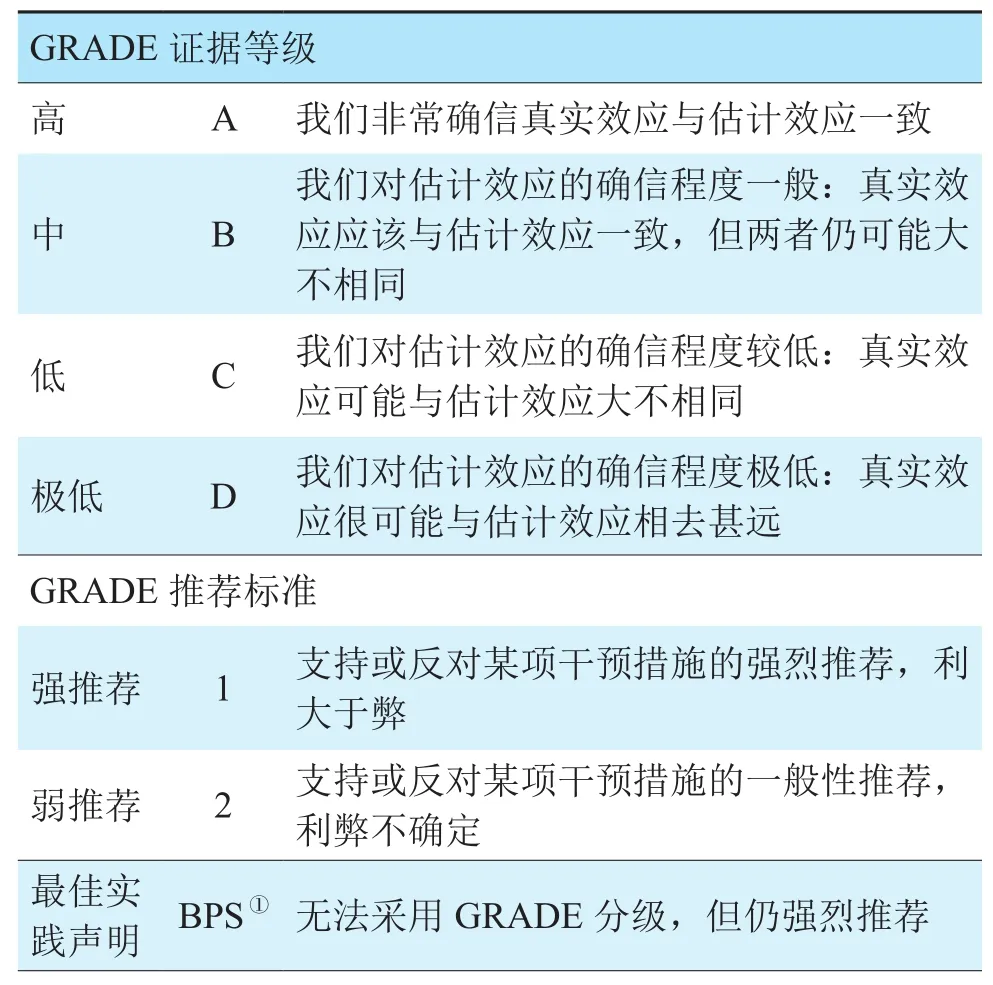
表1 证据等级和推荐标准Table 1 Level of evidence and recommended grades
1 慢加急性肝衰竭肝移植围手术期康复评估
ACLF患者肝移植围手术期病情复杂、个体化差异大,难以统一康复方案。康复评估一方面可以排除肝移植禁忌,预测预后,另一方面康复评估分级可以为个体化康复方案的制定提供重要依据,并对康复效果进行评价[8-10]。康复评估的内容包括:呼吸系统功能评估、心脏功能评估、躯体功能评估。
1.1 呼吸系统功能评估
肺部是ACLF患者最常受到累及的重要器官之一。慢性肝病患者常存在不同程度的精神神经系统异常、心肺血管重构和营养不良等并发症,心肺功能储备显著下降[11-12]。急性加重和肝移植围手术期新的诱发因素作用显著影响患者呼吸驱动、气体交换和气道保护能力,是ACLF发生围手术期肺部并发症的重要危险因素[13-14]。因此,ACLF患者的呼吸系统功能评估需从中枢神经系统、气道通畅程度、呼吸肌肉、肺损伤程度和肺储备功能来进行。
1.1.1 常规检查 ACLF常合并不同程度的肝肺综合征(hepatopulmonary syndrome,HPS)、肺部感染和肺不张等并发症和合并症[15],肝移植后并发症和病死率明显增加[16]。其中,不可逆或者难以逆转的呼吸衰竭[如重度急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS),HPS合并严重低氧血症、重度门静脉性肺动脉高压(portopulmonary hypertension,POPH)]移植后生存率尤为低下,已成为多数移植中心的禁忌证[10,17]。通过影像学可初步筛查出潜在感染或者基础肺部疾病,脉搏血氧饱和度和血气分析了解患者血氧含量和氧合水平,肺功能可初步了解通气和换气功能,心脏超声检查了解心肺交互作用、是否存在肺内分流以及肺动脉压水平,有助于识别禁忌证和预测肺部并发症发生风险[10]。
推荐意见1:除了常规病史采集和体格检查外,ACLF患者应进行感染筛查和胸部影像学、血气分析、肺功能、心脏超声检查,以了解通气和换气功能。如存在肺损伤或HPS或POPH,应对氧合指数[动脉血氧分压(partial arterial pressure of oxygen,PaO2)/吸入氧浓度(fraction of inspired oxygen,FiO2)]、肺动脉压和通气血流比例进一步分级评估。(推荐等级:BPS)
1.1.2 呼吸驱动 合并肝细胞明显损害的ACLF患者,肝性脑病的发生率明显升高[18]。肝性脑病的级别越高,发生脑水肿的风险越高,严重者可累及呼吸中枢,引起呼吸抑制、气道保护性反射减弱,进而继发缺氧和肺部感染[19]。头颅CT检查可了解明显的颅内病变,如出血、梗死和脑水肿。经颅彩色多普勒超声(transcranial color-coded duplex Doppler,TCCD)具有无创和可重复性的特点[20-23],可用于严重肝性脑病颅内血流、颅内高压中线是否偏移的评估。脑电图监测可提供更多神经元电生理信息。
推荐意见2:ACLF合并严重肝性脑病患者,应常规进行头颅CT筛查,必要时行TCCD和脑电图监测,以了解中枢呼吸驱动是否受损。(推荐等级:1C)
1.1.3 呼吸动度和气道自我保护能力 除了中枢驱动的影响,胸廓肌肉和膈肌的运动决定着气道是否能完成自我保护和正常通气[24-25]。常用的指标有胸廓柔韧性和活动度(diaphragmatic stretch)、主被动咳嗽力量分级、膈肌活动度和增厚率[26-28],均与患者发生肺部感染和插管风险有良好的相关性。机械通气患者还需监测气道压、胸腔内压,大量腹腔积液或中毒性鼓肠患者还需监测腹内压,以了解影响呼吸动度的因素,评估撤机风险。
推荐意见3:建议常规采用主观胸廓柔韧性和活动度、主被动咳嗽力量分级、咳嗽峰流量、超声膈肌活动度和增厚率等了解气道分泌物廓清能力、评估膈肌移动度、厚度和增厚率。对机械通气的患者需每日进行撤机评估。(推荐等级:1B)
1.1.4 肺功能储备测试 肺功能检查是对通气功能的全面评估,有助于识别基础肺病如慢性阻塞性肺病(chronic obstructive pulmonary disease,COPD)等,肺活量、第1秒用力呼气容积(forced expiratory volume in one second,FEV1)(最大吸气压更常见用于评估吸气肌肌力)均能较好的预测移植预后和评估康复实施效果[29]。亚极量的运动实验是反映肺功能重要的综合测试方法[30]。较为常用的简便方法有6分钟步行试验(6-minute walk test,6MWT)以及对应的改良Borg评分(目前通用的是改良Borg评分),通过患者行走距离运动前呼吸困难和全身疲劳情况,可以反映患者的呼吸运动储备和耐受能力。其中Borg评分≤4分提示略严重的呼吸困难或疲劳,Borg评分为4~10分是严重的呼吸困难或疲劳。无论在术前还是术后使用6MWT,都能较好预测肝移植受者的预后和评估康复实施效果[31]。其他还有增量往返步行试验(incremental shuttle walk test,ISWT)和耐量往返步行试验(endurance shuttle walk test,ESWT)较为少用,亦有一定价值。
推荐意见4:对于非机械通气并可以配合患者,建议采用改良Borg量表联合6MWT评估患者的呼吸运动储备和耐受能力。利用肺通气功能测试仪器检测肺活量、FEV1、呼气峰流速等指标可以动态评估患者康复效果。(推荐等级:2B)
1.2 心脏功能评估
围手术期心血管事件是肝移植术后早期最常见的致死性并发症之一[32-33]。ACLF患者心功能异常可能与基础心脏病、肝病所致的心血管改变有关。肝移植是有基础心脏疾病患者的高风险手术,因此,术前心脏的评估应结合术前检查和术中事件进行详细评价[34-36]。
1.2.1 冠状动脉粥样硬化性心脏病 冠状动脉粥样硬化性心脏病(冠心病)是移植术前最常见的心脏基础疾病,在酒精性和非酒精性脂肪变性引起的慢性肝病中均较为常见[37-38]。冠心病的危险因素包括:年龄>50岁,吸烟史,高血压,血脂异常、2型糖尿病和冠心病家族史等[10]。除此之外,心肌酶、心电图和心脏超声作为筛查措施必不可少。此外,对于有高危因素患者应在术前常规行冠状动脉CT血管造影(CT angiography,CTA)或数字减影血管造影检查,以明确血管是否存在严重狭窄或多支病变。
1.2.2 肝硬化性心肌病 约有一半的肝移植受者术前合并了不同程度的心肌异常。长期慢性肝病引起的神经体液调节紊乱,心脏逐渐重塑,最终表现为不同程度的收缩、舒张障碍和电生理异常[39-40]。这些患者心功能储备能力低但术前常无明显的临床表现,对手术、感染等应激诱发事件极其敏感,可能是影响术后超早期康复最重要的因素之一。术前心脏超声可识别结构重塑,如室壁增厚,收缩功能异常。常规和动态心电图可识别潜在的电生理改变,如QTc间期延长、心律失常等[41]。
1.2.3 门静脉性肺动脉高压 POPH尽管发生率不高(约4%~8%),但显著影响受者术后生存和生活质量[42],也是心脏功能评估的重要一部分。如前述,术前常规的心脏超声检查,通过三尖瓣反流可初步了解右室和肺动脉收缩末压力,对于肺动脉收缩压≥45 mmHg(10 mmHg=1.33 kPa),建议术中放置右心导管进一步明确并准确评估肺动脉压[10],根据不同等级的肺动脉高压,制定相应水平的康复计划[43-45]。
1.2.4 围手术期心血管事件 肝移植是普外科最大的手术之一,手术麻醉和创伤、大量的失血和输血、下腔静脉的阻断与开放以及移植物产生的代谢毒素等应激和损伤机制的作用下,表现为特有的血流动力学状态。常出现各种类型的心血管事件,如心脏骤停、心律失常、充血性或泵功能衰竭等。因此,需详细评估移植手术中每个环节因素,围手术期采用各类血流动力学监测手段,如即时超声、右心导管等,及时诊断评估和干预。
推荐意见5:(1)应通过详细的病史询问和体格检查,了解ACLF患者的基础心脏情况;(2)建议ACLF患者术前常规行心肌酶学、心电图、心脏超声检查,长期肝硬化患者建议行动态心电图检查、心脏超声评估肺动脉压;(3)存在冠心病高危因素患者,应常规行冠状动脉CTA或造影以明确是否存在血管病变和程度,对于严重冠状动脉病变,应请心血管内科评估血管重建指征;(4)围手术期评估心脏功能,还应结合手术麻醉时长、出血量、输血量、无肝期时间和移植物冷缺血时间等因素,严密监测血流动力学和内环境改变。(推荐等级:BPS)
1.2.5 围手术期心脏的综合评价 心脏是最重要的氧输送器官,根据Fick定律,氧消耗VO2=1.34×[动脉血氧饱和度(saturation of arterial oxygen,SaO2)-静脉血氧饱和度(saturation of venous oxygen,SvO2)]×血红蛋白(hemoglobin,Hb)+0.003 1×[PaO2-静脉血氧分压(partial venous pressure of oxygen,PvO2)]×心输出量(cardiac output,CO)。因此,采用血气分析和血流动力学监测可较好地反映氧输送和氧消耗水平。心肺功能储备高,就能随时适应机体对氧的需求。采用亚极量运动时氧摄取率的改变,可评估心脏的储备功能。功能状态可用代谢当量(metabolic equivalent,MET)来表达,MET是反映患者活动耐量和运动强度的标准指标,1 MET定义为每公斤体质量每分钟耗氧量为3.5 mL,可作为大手术患者心功能储备的初筛测试[46]。4 MET≤心脏耐受耗氧量<10 MET的患者可以进行手术,无须进一步的运动试验和心脏影像学检查。当心脏耐受耗氧量<4 MET时就需要量化的风险评估。心肺运动测试(cardiopulmonary exercise testing,CPET)通过从静息状态到亚极量运动负荷下定量评估峰值摄氧量(peak VO2)、无氧阈值(anaerobic threshold,AT)、二氧化碳排出量(CO2output,VCO2)等代谢指标反映患者运动耐量和运动时心肺峰值反应水平[47]。CPET能反映终末期肝病患者等待期的病情严重程度。研究发现,肝硬化患者中,VO2max与终末期肝病模型(model for end-stage liver disease,MELD)评分负相关[31],peak VO2与AT受损和等待期病死风险密切相关[30]。术后AT也可有效预测短期生存[47-50]。在临床康复实施过程中,可依据不同的分级,采取不同剂量水平康复措施。此外,6MWT亦可作为半定量的心脏储备功能测试,peak VO2的改善可预测8~16周运动疗效,有助于指导分级干预和随访观察[32-33]。
推荐意见6:在血流动力学稳定的ACLF患者中,建议采用MET或6MWT对心脏储备功能进行初筛,对于储备异常的患者,建议行进一步心肺运动测试,定量评估peak VO2、AT等指标,指导分级康复干预。(推荐等级:2C)
1.3 躯体功能评估
躯体功能是人体维持独立日常生活的综合能力。肝性脑病、运动耐量减低、乏力、骨密度减低、体质量下降和营养不良、肌肉丢失和质量下降以及心肺储备下降等因素,是影响ACLF躯体功能的重要因素,同时显著影响移植的结局[51]。目前缺乏针对ACLF患者的躯体功能单独的评估方案,因此需根据患者的营养状态和全身状况,从肌肉含量和质量、肌力、运动耐量、生活自理能力几个维度,进行综合分级评估。
1.3.1 对于意识不清、镇静、或心肺功能不稳定的患者 临床上可通过测量上臂肌围(mid-arm muscle circumference,MAMC)粗略评估肌肉质量和营养状态,标准值:男性25.3 cm和女性23.2 cm。依据MAMC和进食状况的主观营养评定(subjective global assessment,SGA)及皇家自由医院全面评定(Royal Free Hospital-global assessment,RFH-GA)方案[52-53],是评价肝病患者营养状态的常用方法[54]。常采用超声、CT或MRI可客观定量反映肌肉含量和质量。超声可用于评估肱二头肌、股四头肌和腓肠肌厚度,利用羽状角评估肌肉质量,有简便、经济和无创等优点,但可重复性仍有待进一步研究;CT下第三腰椎骨骼肌指数(skeletal muscle index,SMI)与危重患者的营养状态具有独立的相关性,当男性SMI<42 cm2/m2和女性<38 cm2/m2可诊断肌少症,肝移植受者SMI与移植预后存在一定相关性,可用于躯体康复干预动态评估[55-57]。
1.3.2 对于意识逐渐改善,能够配合,局限于床上活动的患者 握力测试和肌力分级是最常用的评估方法[58]。手握力(hand grip strength,HGS)男性<28 kg,女性<18 kg,即为肌肉力量低下。英国医学研究委员会(medical research council,MRC)评分是用牛津肌力等级评分对躯体六大肌群进行评估,总分<48分诊断为ICU获得性肌无力。MRC评分已被用于多种危重病的预后预测和康复干预疗效评价[59]。
1.3.3 对于意识清楚、能够良好配合,具备离床步行能力的患者 运动耐力测试是最常用的方法。6MWT最常用于肝移植术前和术后的躯体功能评估。6MWT与肝移植术前等待期生存和术后生活质量均显著相关[31-32,50,60],术前6MWT<250 m与病死率显著相关,每增加100 m的距离可提高短期50%的生存机会[50],无论是术前或是术后的6WMT与术后并发症或生存质量结局呈明显的正相关[31-32]。简易机体功能评估量表(short physical performance battery,SPPB)评分0~6分提示肌肉功能很差,7~9分提示肌肉功能中级,10~12分提示肌肉能力良好[61]。近年来,肝脏衰弱指数(liver frailty index,LFI)在ACLF患者应用较多,由握力、定时站立和平衡测试3个指标构成,评分≥4.5即为衰弱。衰弱表型(fried frailty phenotype,FFP)内容包括步速下降、疲乏、体力活动减少、体质量下降和握力下降5个方面,有≥3个症状即为衰弱。术前和术后应用LFI均可较好地预测肝移植受者预后和指导康复治疗[62-64]。
另外,一些综合评估量表,如卡氏功能状态评分(Karnofsky score,KPS)和日常生活自理能力评分(activities of daily living,ADL),也可作为快速躯体功能评估筛查工具[64]。
推荐意见7:ACLF的躯体功能应在评估营养状态和全身状况的基础上,从肌肉含量和质量、运动耐量和生活自理能力这三个维度进行等级评价。依据各中心特点,选用合适的评估量表和方法。(推荐等级:1B)
2 慢加急性肝衰竭肝移植围手术期康复治疗
肝移植受者进行早期快速康复治疗能显著减少并发症发生,降低ICU入住时间[65]。ACLF患者肝移植围手术期的康复涉及多个器官系统,应依据前述评估分级、病情演变和严重程度,合理制定不同耐受程度的个体化康复方案。
2.1 呼吸功能康复
呼吸功能康复应强调以控制原发病和营养支持为基础,从被动体位或运动、刺激,到尽可能诱导主动锻炼,循序渐进,从而达到提高呼吸肌肉力量、减少肺不张,最终避免肺部并发症的主要目标[66-67]。根据患者病情从重至轻的等级,呼吸功能康复可分为昏迷或机械通气期、撤机过渡期和主动锻炼期三个阶段。
2.1.1 昏迷或机械通气(完全机控模式)期 主要以被动的胸肺部物理治疗为主,包含多角度侧卧位、俯卧位等利于气道分泌物引流,半坐位和坐位可减少反流误吸风险;必要时行纤维支气管镜检查清除气道分泌物。
2.1.2 撤机过渡期 在被动物理治疗(如变换体位、叩击、胸廓振动等)的基础上,通过减少镇静、降低辅助通气的力度,逐渐增加主动循环呼吸技术(如坐位深呼吸、站立位、带机行走)、指导用力呼气法等能提高咳嗽排痰的效率[68-69];功能性电刺激膈神经能有效提高膈肌收缩力,利于调整呼吸节律,增强呼吸动力;当咳嗽能力3~5级,咳嗽峰流量>60 L/min时,可尝试撤机拔管;因原发病无法解除,评估短期(一般>1周)内无法撤机者应考虑气管切开;撤机后仍需维持1~2周辅助与主动相结合的训练模式,避免再次插管。
2.1.3 主动锻炼期 待患者原发病趋于稳定,可完全遵嘱配合并能完成6MWT或改良Borg评分<4分时,指导主动呼吸功能锻炼,包括呼吸方式锻炼(缩唇呼吸、腹式呼吸、吹气球锻炼),呼吸肌肌力训练(吸气肌训练和呼气肌训练),改善胸廓活动度的训练和主动循环呼吸技术的锻炼[25,70]。逐渐增加锻炼时间和强度,提高无氧运动耐受。
推荐意见8:建议根据患者病情严重程度进行个体化的康复方案制定。昏迷和完全机控通气患者,采用被动的体位、纤维支气管镜和胸部物理治疗方式;撤机过渡期应减少镇静和降低呼吸肌辅助力度,在被动物理治疗的基础上,逐渐增加包含咳嗽和膈肌刺激的主动循环呼吸技术,每日进行神志、气道自我保护能力、膈肌功能等相关的撤机评估,撤机后仍维持一段时间被动与主动相结合的康复模式;完全主动的锻炼模式则要求患者病情稳定后完全遵嘱配合,通过康复师指导、逐级提高时间和强度的形式,提高患者无氧运动耐受。(推荐等级:1B)
2.2 心功能康复
ACLF患者心脏的康复,主要参考心脏术后患者的康复训练。在保证氧输送的前提下,依据不同代谢当量级别,以提高氧摄取,耐受低氧或无氧运动为目标,根据评估分级指导康复方案的制定[71-72]。
(1)对于术前评估无心脏基础疾病的患者,术前6~12周,每日进行60~120 min训练强度为40%~65%最大心率值(maximum heart rate,HRmax)的有氧运动。(2)术后早期耐受耗氧量<4 MET的患者指导从床上进行的肢体被动或主动活动,也可逐步过渡至床旁活动,但控制代谢当量在2~4 MET。(3)移植后恢复期耐受耗氧量>4 MET患者的心脏康复主要以有氧运动耐力训练为主。低中等强度的有氧运动,如床旁踏车(cycling)训练或下地步行。逐渐增加运动时间,从5 min进阶至10~20 min。在运动过程中,控制患者的疲劳指数在11~13分,控制运动中的最大心率不超过静息心率增加20次/分[46-47]。(4)心脏康复终止指标:平均动脉压<65 mmHg或>110 mmHg,心率<50次/分或>130 次/分,呼吸频率<12次/分或>40次/分,氧饱和度<88%,出现明显的人机对抗,患者主观感受状态很差等。同时治疗师在康复过程中应个性化地调整运动剂量和周期,使其既可以接近最大摄氧量,又不至于太过密集,以避免出现心肺相关的不良事件。
推荐意见9:心脏康复干预,应以基础心脏病评估为基础,在保障氧输送前提下,采用逐级升高强度或频率的躯体运动方式,如床旁踏车→坐立→站立→辅助步行→自主步行→慢走→快走→慢跑,同时适当增加阻抗运动,如提重物、抗阻踏车或行走,以提高氧摄取率,最终达到能生活自理、低氧或无氧运动耐受的目标,均适用于术前预康复和术后心脏康复。(推荐等级:1B)
2.3 躯体功能康复
肝移植受者术后早期实施躯体康复训练是安全有效的,早期躯体功能康复有利于肠道功能恢复,缩短机械通气时间和ICU入住时间,减少30 d再住院率,促进患者恢复生活自理能力,而无不良反应[73-74]。因此应在躯体功能评估的基础上根据肝移植受者的意识、配合程度对其实施术后目标导向性早期康复训练,监督患者每日完成规定剂量或者一定康复目标以最大程度地获取康复效益。
推荐意见10:(1)对于昏迷或意识不清的患者可针对其股四头肌等负重的大肌群实施每日30 min的神经肌肉电刺激。并进行每日唤醒,根据病情开展四肢关节被动活动。(推荐等级:1C)
(2)对于清醒可配合患者,术前指导其进行30~60 min、达到≥150分钟/周的有氧运动或有氧运动与抗阻训练相结合的训练方案。术后根据肌力情况进行四肢的被动关节活动训练级床上被动脚踏车训练。(推荐等级:1C)
(3)对于意识清楚且有一定肌力的患者围手术期进行四肢的主动关节活动度训练,借助motomed智能运动训练系统进行床上踏车训练,并指导患者进行床上活动、床边坐起等的功能活动训练。(推荐等级:2C)
3 ACLF患者肝移植围手术期康复的安全性
在心肺移植和一般重症患者中,围手术期康复显示良好的安全性[75-76]。而ACLF患者肝移植围手术期病情复杂多变,康复干预带来的安全性隐患必然是我们关注的重点,如诱发低氧、血流动力学不稳定、出血和疼痛不适等是临床医师最关心的问题[77]。因此,有必要建立外科、重症医学科、呼吸科、康复运动科和心理科等多学科一体参与的康复团队。然而,从对重症患者实施干预的证据表明,早期康复和活动诱发低氧和血流动力学不稳定的风险极低(分别为1.9‰、3.8‰),总体不良事件仅0.6%[76]。术前腹部大手术的预康复能有效提高者摄氧水平,改善高风险手术患者结局的同时并不增加术后出血风险,这种干预在肝移植术后也被证实是安全有效的[65,75,78]。
呼吸和康复的物理治疗更有利于患者血氧改善,促进早期撤机。甚至有学者认为,对于呼吸和血流动力学稳定的患者,肝移植术后实施即刻(<1 h)撤机也是安全的[79]。依据康复评估的等级实施个体化干预,对患者血流动力学的影响甚微,已有的肝移植早期康复研究并未报道类似不良事件[80-82]。由于肝移植手术创伤大,术后创面血栓形成不稳定,大多数移植中心不建议术后24 h内进行较为激进的体位和活动,如俯卧位、站立和行走,这对于移植物功能恢复延迟,凝血功能较差者风险更高。除此之外,早期的康复有利于促进血液流动,减少预防性抗凝的使用,也部分间接避免了出血的风险。
推荐意见11:建议对ACLF患者围手术期早期康复阶段实施呼吸、血流动力学和出血风险监测。建议康复运动在术后24 h后实施。存在氧输送不足如急性呼吸窘迫、血流动力学不稳定、严重凝血紊乱如活动性出血、大量深静脉栓塞脱落风险和切口广泛愈合不良者,应暂缓实施运动康复。(推荐等级:1B)
执笔作者:
吕海金 郑海清 刘剑戎 蔡 庆 任宇基 易慧敏
杨 扬 胡昔权 陈规划
审稿专家:
毕 艳 南京鼓楼医院
蔡 明 浙江大学医学院附属第二医院
蔡金贞 青岛大学附属医院
曹荣华 广东省中医院
陈必成 温州医科大学附属第一医院
陈规划 中山大学第三附属医院
陈 昊 兰州大学第二医院
陈焕伟 佛山市第一人民医院
陈静瑜 无锡市人民医院
陈立中 中山大学附属第一医院
陈 明 东南大学附属中大医院
陈小平 中国人民解放军南部战区空军医院
陈 正 广州医科大学附属第二医院
程 颖 中国医科大学附属第一医院
邓德成 中山市人民医院
丁晨光 西安交通大学第一附属医院
丁泓文 暨南大学附属第一医院
方驰华 南方医科大学珠江医院
丰 琅 首都医科大学附属北京友谊医院
付绍杰 南方医科大学南方医院
富大智 中国医科大学附属第一医院
高 伟 天津市第一中心医院
郭文治 郑州大学附属第一医院
何 军 苏州大学附属第一医院
胡泽民 中山市人民医院
黄 洁 中国医学科学院阜外医院
黄劲松 广东省人民医院
黄 磊 北京大学人民医院
霍 枫 中国人民解放军南部战区总医院
贾瑞鹏 南京市第一人民医院
姜 楠 深圳市第三人民医院
姜海明 中山市人民医院
巨春蓉 广州医科大学附属第一医院
郎 韧 首都医科大学附属北京朝阳医院
李 宁 山西省第二人民医院
李川江 南方医科大学南方医院
李 健 空军成都医院
李建军 南华大学附属第二医院
李劲东 广东省红十字会器官捐献办公室
李先亮 首都医科大学附属北京朝阳医院
李 霄 空军军医大学西京医院
李新长 江西省人民医院
栗光明 首都医科大学附属北京佑安医院
梁朝阳 中日友好医院
林民专 广州医科大学附属第三医院
刘 超 中山大学孙逸仙纪念医院
刘 东 广东省第二人民医院
刘 芳 上海长征医院
刘 永 上海交通大学附属第一人民医院
刘致中 内蒙古包钢医院
鹿 斌 复旦大学附属华山医院
吕 凌 南京医科大学第一附属医院
马 麟 广东省中医院
马俊杰 广州医科大学附属第二医院
马现仓 西安交通大学第一附属医院
门同义 山东医科大学第一附属医院
苗 芸 南方医科大学南方医院
聂海波 中国人民解放军南部战区总医院
潘光辉 深圳市第三人民医院
彭延文 中山大学附属第三医院
秦 彦 山西医科大学第二医院
邱 江 中山大学附属第一医院
沈 恬 浙江大学医学院附属第一医院
石 伟 复旦大学附属华山医院
侍晓敏 中山大学附属第一医院
史颖弘 复旦大学附属中山医院
司中洲 中南大学湘雅二医院
孙丽莹 首都医科大学附属北京友谊医院
孙启全 广东省人民医院
孙其鹏 中山大学附属第三医院
孙煦勇 广西医科大学第二附属医院
田 川 山东大学第二医院
王健东 上海交通大学附属新华医院
王胜军 江苏大学附属人民医院
王彦峰 武汉大学中南医院
王远涛 吉林大学第一医院
王长安 郑州市第七人民医院
王长希 中山大学附属第一医院
王正昕 复旦大学附属华山医院
谢琴芬 树兰(杭州)医院
熊 俊 华中科技大学同济医学院附属协和医院
熊 艳 武汉大学中南医院
徐 健 南方医科大学南方医院
徐 鑫 广州医科大学附属第一医院
杨海彦 哈尔滨医科大学附属第一医院
杨浣情 广东省人民医院
杨家印 四川大学华西医院
杨 军 华中科技大学同济医学院附属同济医院
杨 扬 中山大学附属第三医院
叶俊生 北京清华长庚医院
伊焕发 吉林大学白求恩第一医院
殷伟强 广州医科大学附属第一医院
于立新 北京清华长庚医院
袁 铭 中国人民解放军总医院第八医学中心
曾 浔 浙江大学
张 斌 南方医科大学南方医院
张 明 上海交通大学医学院附属仁济医院
张胥丰 西安交通大学第一附属医院
张英才 中山大学附属第三医院
赵 明 南方医科大学珠江医院
赵 磊 北京大学第三医院
赵 勇 中国科学院动物研究所
甄作均 佛山市第一人民医院
郑海清 中山大学附属第三医院
周 杰 南方医科大学南方医院
周光文 上海交通大学附属第六人民医院
周江桥 武汉大学人民医院
周 琳 浙江大学医学院附属第一医院
周佩军 上海交通大学医学院附属瑞金医院
朱晓丹 青岛大学附属医院
朱晓峰 中山大学附属第一医院
朱玉连 复旦大学附属华山医院
庄 莉 树兰(杭州)医院
邹义洲 中南大学湘雅医学院

