砷化氢发生-砷钼蓝分光光度法测定钢铁中砷
罗嗣兴,王飞飞,孙效轩,刘凯,司圳棋,张琦,孙士超,陈达
(山东众标企信检测科技有限公司,济南 250100)
社会发展对钢铁性能的要求与日俱增。作为钢铁有害残余元素,砷在钢铁中极易发生偏析而对钢材性能产生不利影响。例如导致晶体发生改变造成金属的不连续性;使热加工性能变差如焊接时产生裂痕;对钢的硬度产生不利影响;使钢铁产生冷脆性导致其延展性及韧性变差等[1-4],因此准确快速分析钢铁中的砷含量非常重要。
钢铁分析中常用的砷分析方法有蒸馏分离AsCl3-砷钼蓝光度法[5]、二乙基二硫代胺基甲酸银盐(DDTC-Ag)法[6]、砷锑钼蓝光度法[7]、电感耦合等离子体发射光谱(ICP-AES)法[8-10]、电感耦合等离子体质谱(ICP-MS)法等[11-12]。上述方法中,蒸馏分离AsCl3-砷钼蓝光度法操作繁琐,耗时长且重复性较差;DDTC-Ag 法需要使用有害试剂氯仿,且在实验过程中易析出DDTC-Ag 而堵住通气管;ICP-AES 法因砷的发射强度较弱易造成测定结果精密度较差及共存离子干扰;而ICP-MS 法则受限于仪器过于昂贵。笔者提出一种方法即通过AsH3发生实现砷与其它共存离子分离,以高锰酸钾的硫酸溶液吸收AsH3并形成砷钼蓝络合物,通过测定其吸光度达到检测钢铁中砷含量的目的。该方法操作简便,能消除共存离子干扰,具备较好的选择性和稳定性,灵敏度较高。该法应用于钢铁中砷含量的测试,结果满意。
1 实验部分
1.1 主要仪器及试剂
紫外可见分光光度计:TU-1810 型,北京普析通用仪器有限责任公司。
电子分析天平:AB204-S 型,感量为0.1 mg,梅特勒-托利多国际贸易(上海)有限公司。
纯水机:GWB-UP 型,北京普析通用仪器有限责任公司。
盐酸、硝酸:均为分析纯,天津市科密欧化学试剂有限公司。
高氯酸、硫酸:均为优级纯,天津市科密欧化学试剂有限公司。
碘化钾、酒石酸、钼酸铵、盐酸羟胺、氯化亚锡(SnCl2·2H2O)、硫酸肼:均为分析纯,国药集团化学试剂有限公司。
碘化钾溶液:0.30 g/mL,称取30 g 碘化钾溶于100 mL 水中溶解完全,置于棕色玻璃瓶备用,现用现配。
酒石酸溶液:0.50 g/mL。
高锰酸钾溶液:10 g/L。
钼酸铵溶液:0.5 g/mL。
盐酸羟胺溶液:0.10 g/mL。
氯化亚锡溶液:0.40 g/mL,称取40 g 氯化亚锡,加50 mL 盐酸加热溶解完全,用水稀释至100 mL。
硫酸肼溶液:10 g/L。
无砷锌粒:分析纯,粒径为2~5 mm,天津市科密欧化学试剂有限公司。
三乙醇胺、乙酸、乙酸铅:均为分析纯,莱阳市康德化工有限公司。
乙酸铅棉:将脱脂棉浸浴在0.10 g/mL 乙酸铅溶液[用乙酸(1∶200)配制]中,取出挤干,于室温风干或50 ℃干燥,保存于玻璃瓶中备用。
砷标准储备溶液:1 000 μg/mL,标准物质编号为GBW(E) 080989,济南众标科技有限公司。
砷标准工作溶液:8 μg/mL,取适量砷标准储备溶液,用质量分数为5%的稀硫酸溶液稀释并定容而得。
实验用水:电阻率大于18.2 MΩ·cm,用纯水机制备。
AsH3气体发生分离吸收装置:装置图见图1。
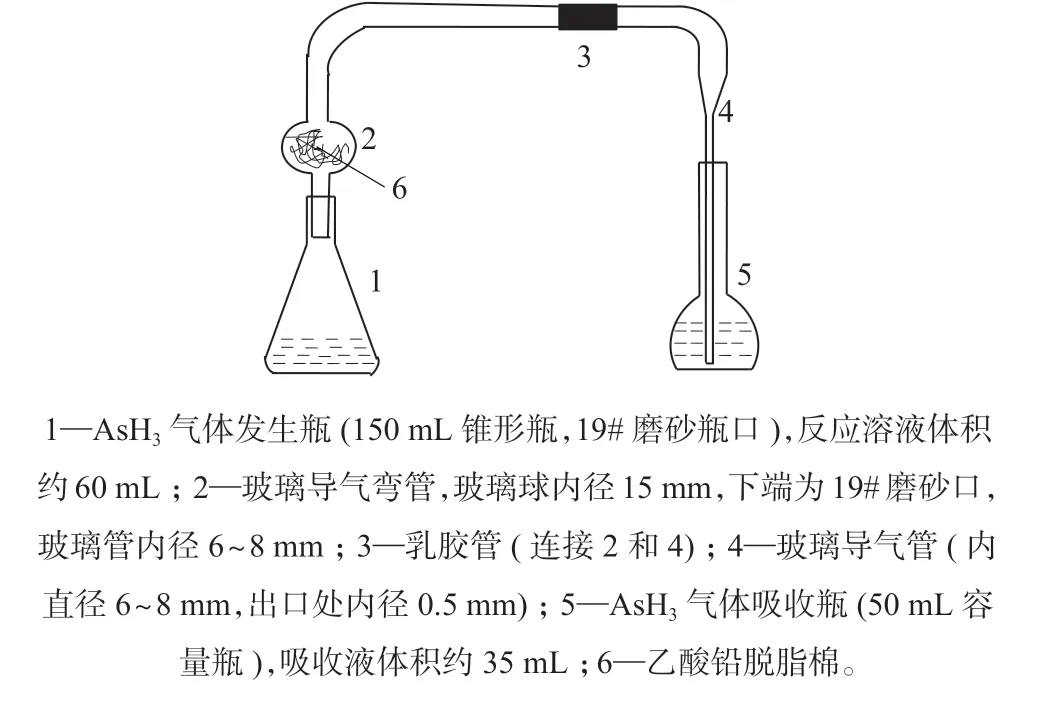
图1 AsH3 发生分离吸收器装置图
1.2 实验方法
准确称取适量钢铁样品于150 mL砷发生瓶(即图1 中的装置1,150 mL 锥形瓶)中,加入10 mL王水,将锥形瓶置于电炉板上加热至样品溶解完全。加入5 mL 高氯酸,继续加热到冒高氯酸烟至瓶口,取下冷却,加入10 mL 水溶解盐类完全后加入8 mL硫酸溶液(1∶1)。
在上述溶液中加入3 mL 碘化钾溶液,摇匀,再边摇边滴加氯化亚锡溶液直至黄色褪去并过量1.5 mL,再加入5 mL 酒石酸溶液和5 mL 三乙醇胺溶液,用水冲洗瓶壁并稀释至60 mL,摇匀,静置15~20 min[13]。
在AsH3气体吸收瓶(50 mL 容量瓶)中依次加入3 mL 硫酸溶液(1∶9)、1 mL 高锰酸钾溶液和30 mL 水[14],插入导气管。
在静置时间结束后向AsH3气体发生瓶中加入5 g 无砷锌粒,立即将导气管与发生瓶连接,保证反应器密闭。在室温下反应45~60 min。
反应结束后取出气体导管,用少量水冲洗导管出口位置,冲洗液并入气体吸收瓶中,滴加1 滴盐酸羟胺溶液并用少量水冲洗容量瓶壁,摇匀静置1 min(若溶液未褪色或MnO2沉淀有残余则再加1 滴盐酸羟胺溶液摇匀并静置1 min,重复操作至溶液呈无色透明状态),再加入5 mL 钼酸铵溶液,摇匀放置5 min,最后加入0.5 mL 硫酸肼溶液,用水定容至50 mL,摇匀,沸水浴3 min 后取出,流水冷却至室温[13]。
以随同空白为参比,使用紫外可见分光光度计在波长840 nm 处测量上述溶液的吸光度,以砷的质量为横坐标、吸光度为纵坐标绘制标准工作曲线,在标准工作曲线上查得样品中砷的质量,按照式(1)计算其质量分数:
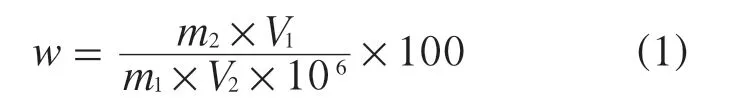
式中:w——砷的质量分数,%;
m1——样品称样量,g;
m2——标准工作曲线上查得的砷质量,μg;
V1——样品溶液总体积,mL;
V2——分取样品溶液体积,mL。
2 结果与讨论
2.1 分析波长的选择
称取适量钢铁样品,按1.2 实验方法处理并显色,用紫外可见分光光度计连续测量样品在不同波长下的吸光度,吸收光谱如图2 所示。由图2 可知,显色液在840~848 nm 处有最大吸收峰,故选择测定波长为840 nm。
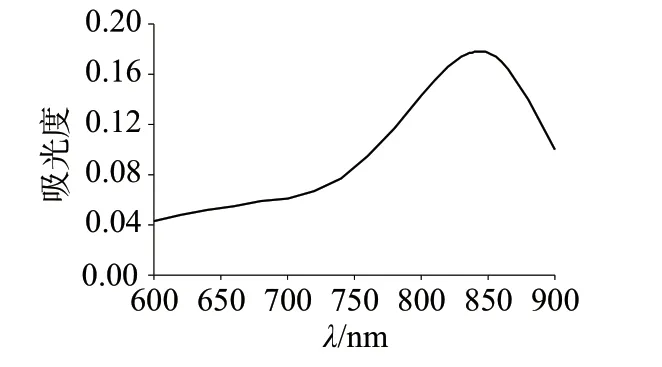
图2 砷钼蓝络合物吸收光谱
2.2 温度对AsH3 发生的影响
当室温太低时,反应速率过慢,易造成AsH3发生不完全,使结果偏低;夏季时室温过高,又因为反应为放热反应,使溶液温度进一步升高造成反应速率过快,使AsH3吸收不完全而逃逸,造成结果偏低,故室温应保持在10~30 ℃之间为宜[15]。
2.3 酸度
2.3.1 AsH3的生成
实验表明,砷转化为AsH3适宜的硫酸浓度为0.80~2.0 mol/L。硫酸浓度低于此范围则不能使砷完全变成AsH3逸出,高于此浓度范围时则生成硫化氢干扰测定[16]。移取含有10 μg 砷的砷标准溶液,在不同硫酸浓度条件下考察AsH3的分离效果(以砷的回收率反映),结果见表1。

表1 不同硫酸浓度时砷的回收率
由表1 可知,当硫酸溶液的浓度在0.80~2.0 mol/L 范围内时,砷的回收率较高。本实验选择硫酸浓度为1.20 mol/L,即加入8 mL 硫酸溶液(1∶1)可以使AsH3分离完全。
2.3.2 AsH3吸收液显色酸度
酸度低则钼酸铵在加热条件下会被硫酸肼还原为钼蓝,随钼蓝增加溶液颜色逐渐变深而无法测试;酸度太高则络合物显色不完全[12]。移取含有20 μg 砷的砷标准溶液,以不加砷标准溶液随同操作样品为空白,以空白为参比,在不同硫酸浓度条件下考察显色效果,结果见表2。
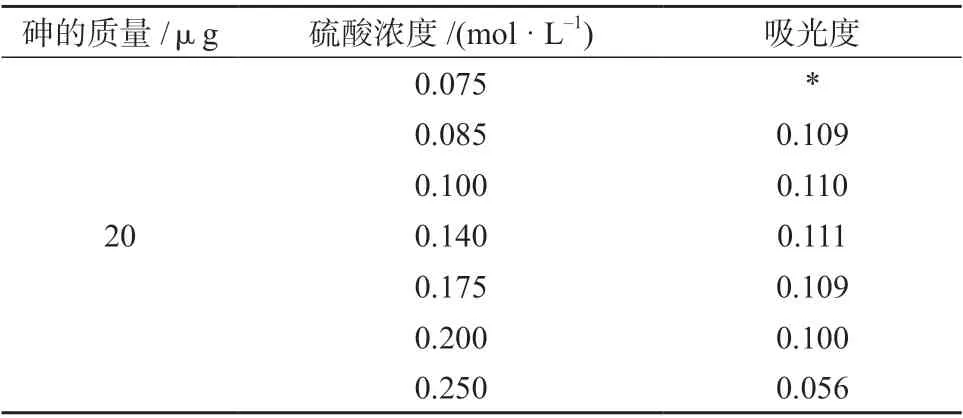
表2 不同硫酸浓度时的溶液吸光度
由表2 可知,在0.085~0.175 mol/L 的硫酸溶液中显色时吸光度较大且基本一致。笔者选取硫酸浓度为0.108 mol/L,即加入3 mL 硫酸溶液(1∶9)。
2.4 高锰酸钾用量
由于水对AsH3的吸收不完全,因而采用高锰酸钾将AsH3氧化成H3AsO4留在溶液中,其反应式如下:
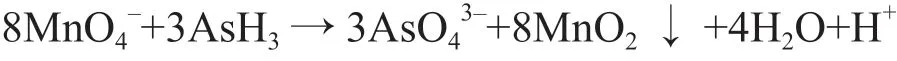
移取含有10 μg 砷的砷标准溶液,考察不同高锰酸钾浓度对AsH3吸收的影响,结果见表3。由表3 可知,当高锰酸钾的质量分数大于0.008%时可使AsH3被完全吸收,而过量的高锰酸钾要用盐酸羟胺清除,为减少盐酸羟胺的用量,选用高锰酸钾的质量分数为0.02%,即加入1 mL 高锰酸钾溶液。
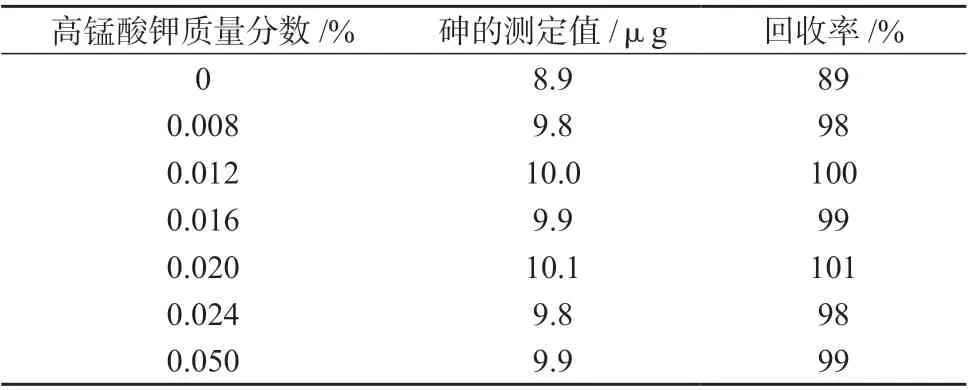
表3 不同高锰酸钾浓度下砷的回收率
2.5 盐酸羟胺用量
盐酸羟胺用于清除过量的高锰酸钾,在吸收瓶中滴加1 滴盐酸羟胺,摇匀静置1 min,若溶液不能褪色成无色透明溶液,则补加1 滴直至无色透明。
2.6 钼酸铵浓度对显色的影响
钼酸铵浓度太高则空白值很大,而浓度太低则络合物吸光度偏低。移取含有20 μg 砷的砷标准溶液,加入不同量的钼酸铵溶液,以不加砷标准溶液的随同操作样品为空白,其余按分析步骤1.2 进行,以空白为参比测定吸光度,结果见表4。由表4可知,当钼酸铵质量分数为0.04%~0.05%时测定结果一致,故选择钼酸铵质量分数为0.05%,即加入5 mL钼酸铵溶液。

表4 不同钼酸铵浓度时的吸光度
2.7 硫酸肼浓度对显色的影响
移取含有20 μg 砷的砷标准溶液,加入不同量的硫酸肼溶液,以不加砷标准溶液的同步操作溶液为空白,其余按分析步骤进行,以空白为参比测定吸光度,结果见表5。

表5 不同硫酸肼浓度时溶液的吸光度
由表5 可知,硫酸肼质量分数为0.001%~0.010%时测定结果一致,实验选择硫酸肼的质量分数为0.005%,即加入0.5 mL 硫酸肼溶液。
2.8 显色液稳定性
移取含有20 μg 砷的砷标准溶液,按分析步骤1.2 进行试验,显色完成后测量在室温下放置不同时间的吸光度,结果表明,显色液显色完全后,在25 h内吸光度基本不变,显色液的稳定性相对较好。
2.9 共存离子的干扰试验
称 取 多 组0.500 0 g 纯 铁ZBG 2181 (As:0.002 4%),分别加入含有20 μg 砷的砷标准溶液,再分别加入常见干扰元素,其余按分析步骤1.2 进行试验,结果见表6。由表6 可知,经AsH3发生分离后,一定含量的常见元素对砷的分析结果无影响。
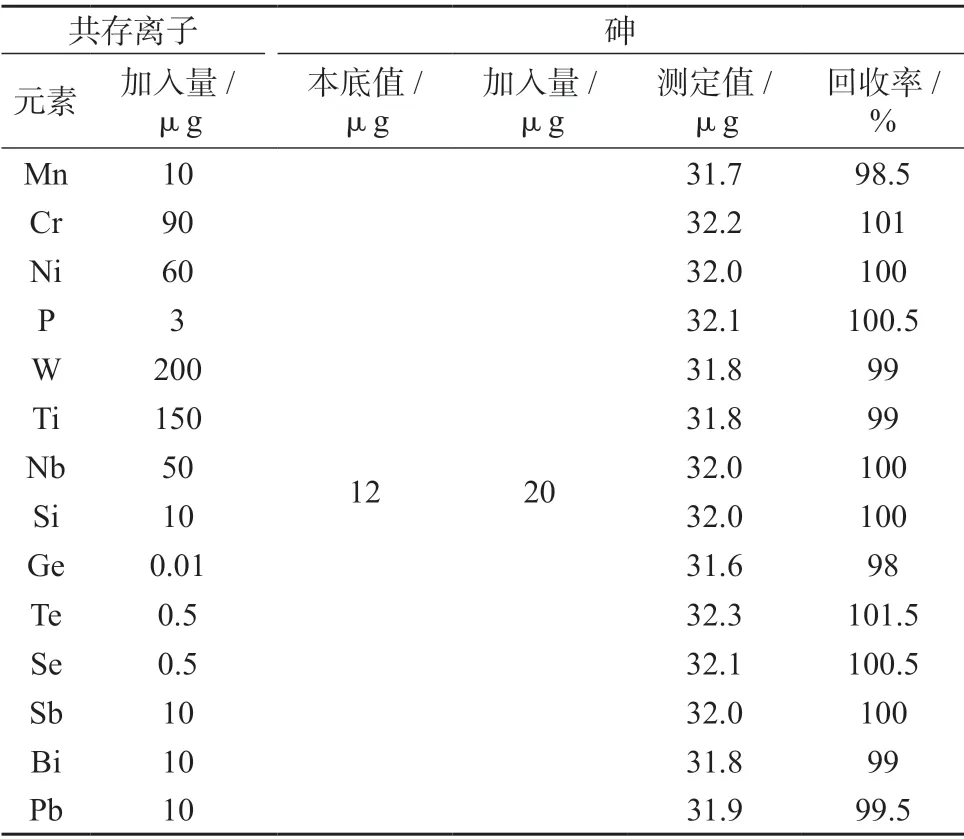
表6 共存离子的干扰试验结果
2.10 标准工作曲线
称 取0.500 0 g 高 纯 铁GBW 01402 g (As:<0.000 1%)置于AsH3气体发生瓶中,分别加入砷标准工作溶液(8 μg/mL) 0、0.625、1.25、2.50、3.75、5.00、6.25 mL,此时含砷质量分别为0、5.00、10.00、20.00、30.00、40.00、50.00 μg,其余步骤按实验方法1.2 进行操作,以不加砷标准溶液样品为空白做参比溶液,测得吸光度。以砷的质量(x)为自变量、吸光度(y)为因变量进行线性回归,计算得标准曲线线性方程为y=0.007 1x-0.001 6,相关系数为0.999 5。结果表明,在50 mL 显色液中,砷的质量在0~50 μg 范围内符合朗伯-比耳定律,线性良好。
2.11 精密度试验
利用本法测定不锈钢标准物质GBW(E)010583、碳钢标准物质GBW(E) 010276a 各10 次,砷含量测定结果列于表7。由表7 可知,两种标准样品测定结果的相对标准偏差分别为2.84%、1.48%,表明本方法的精密度良好。
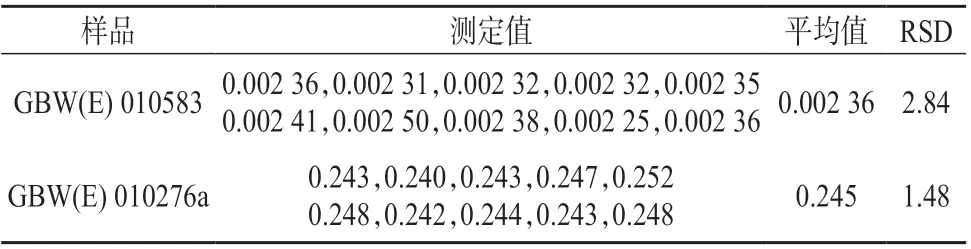
表7 精密度试验结果 %
2.12 样品加标回收试验
称取四组碳钢标准物质[标准物质编号为GBW(E) 010276a],同时加入不同量砷标准溶液得到3 个加标样品,按1.2 实验方法进行操作,测定并计算砷的回收率,结果见表8。由表8 可知,砷的回收率为98.1%~101.7%,平均回收率为100.7%,表明本方法准确度较高。
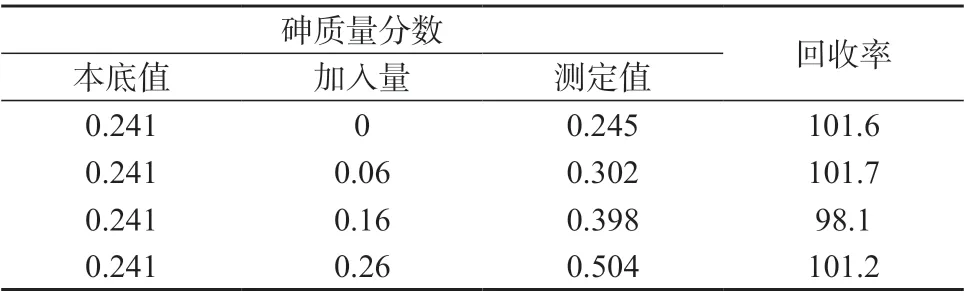
表8 样品加标回收试验结果 %
2.13 准确度试验
称取不同砷含量的碳钢、合金钢、不锈钢和生铸铁标准物质,按分析步骤进行实验,测定结果与标准物质的标准值见表9。由表9 可知,测试结果与标准值吻合,方法准确性良好。
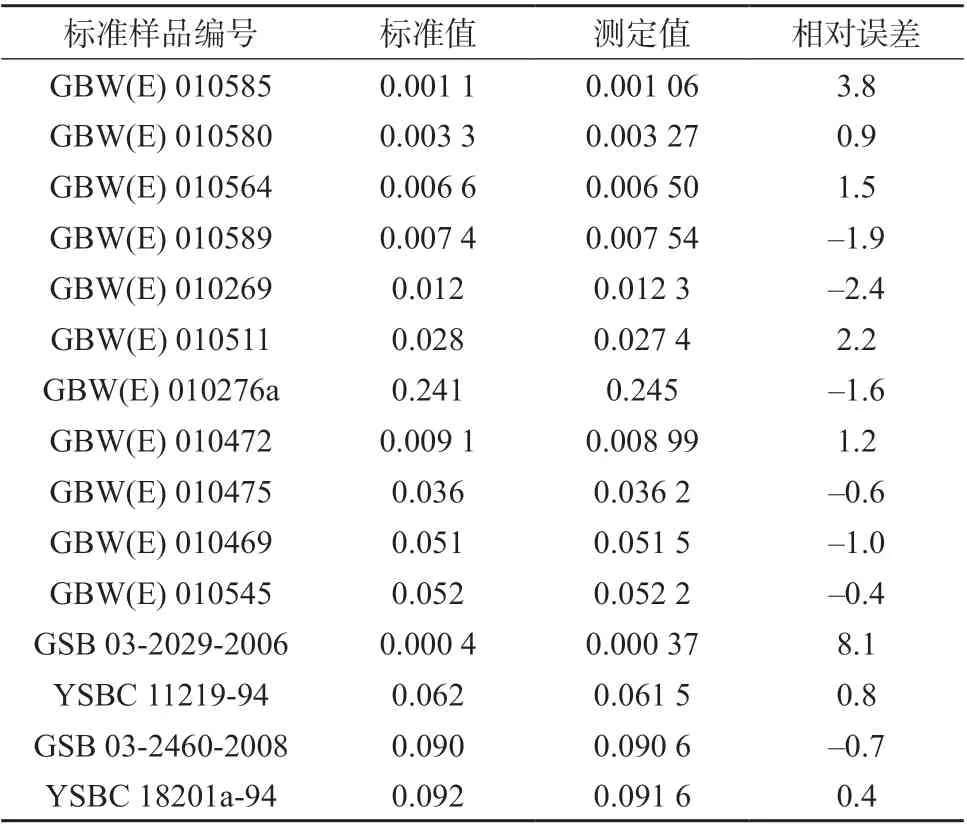
表9 钢铁标样中砷测试结果比对表 %
3 结语
砷作为钢铁中的有害元素,其含量快速准确的检测是有必要的。鉴于此,笔者利用砷的特性设计了一种砷化氢发生-分离-吸收装置,利用该装置建立了砷化氢发生-砷钼蓝分光光度法测定钢铁中砷含量的方法。通过线性拟合得显色液中砷质量与吸光度变化的校准曲线,其相关系数达0.999 5。并且测试回收率介于98%与102%之间;显色液稳定性大于25 h。在实际分析检测过程中,该方法成本低、易于操作、普适性广、应用性强,可以快速实现砷含量的准确分析。

