HIV/AIDS患者二线抗病毒治疗后发生免疫重建不良及影响因素研究
王东利,艾艳珂,袁君,马秀霞,郭会军,许前磊,,金艳涛*
艾 滋 病(acquired immune deficiency syndrome,AIDS)是由于感染人类免疫缺陷病毒(human immunodeficiency virus,HIV)引起的一种致死性传染病,是全球面临的重大公共卫生和社会问题。HIV侵入人体后,主要侵犯和破坏人体的CD4+T淋巴细胞,在侵入的细胞内大量复制,使机体丧失免疫能力,发生多种难以治愈的感染性疾病或肿瘤,最终导致患者死亡。目前公认治疗AIDS最有效的药物疗法是高效抗反转录病毒疗法(highly active antiretroviral therapy,HAART),该疗法可以有效抑制HIV的复制,提升CD4+T淋巴细胞计数水平,重建HIV/AIDS患者的免疫功能[1]。但研究发现,HAART治疗后的免疫重建具有局限性,在病毒载量(viral load,VL)控制良好的情况下,仍有20%~30%的患者并没有获得理想的免疫功能重建,这种现象被称为免疫无应答或免疫重建不良(immunological nonresponse,INR)[2]。研究表明,INR患者仍有较高的死亡率和感染AIDS相关或非相关疾病的风险[3],INR已成为AIDS临床研究热点之一。
为有效控制AIDS,2004年我国开始为符合国家抗病毒治疗标准的HIV/AIDS患者提供主要由2种核苷类抑制剂+1种非核苷类抑制剂组成的一线抗病毒治疗方案。2004年国家中医药管理局启动“中医中药治疗艾滋病试点项目”(以下简称中医项目),为HIV/AIDS患者免费提供中医药临床救治。随着治疗时间的延长,受患者依从性、HAART治疗不良反应及耐药性等多种因素的影响,一线抗病毒治疗失败的患者逐渐增多[4],相关研究表明我国特定人群一线抗病毒治疗失败率高达20.8%[5]。2009年,我国开始采用由1种蛋白酶抑制剂+2种核苷类抑制剂组成的二线抗病毒治疗方案[6]。洛匹那韦/利托那韦(lopinavir/ritonavir,LPV/r)是第一个利托那韦增强的蛋白酶抑制剂[7],也是我国HIV/AIDS免费治疗二线治疗方案中唯一的蛋白酶抑制剂类药物[8]。以LPV/r为基础的二线抗病毒治疗方案已经实施10余年,但有关二线抗病毒治疗后INR的研究较少。本研究采用回顾性队列研究的方法,对河南省中医药治疗艾滋病项目地区HIV/AIDS患者更换二线抗病毒治疗方案后随访3年,分别观察其满1、2、3年免疫重建情况,了解更换二线抗病毒治疗方案3年内INR的发生率,并分析其影响因素。
1 对象与方法
1.1 研究对象 以艾滋病综合防治数据信息系统和中医药治疗艾滋病数据库为数据来源,选取河南省某AIDS高发区常规治疗库中2009年1月至2015年12月更换为二线抗病毒治疗方案的HIV/AIDS患者3 016例为研究对象。纳入标准:(1)数据库中有患者信息;(2)年龄18~65岁;(3)更换为二线抗病毒治疗方案前或后6个月有VL记录,前或后3个月有CD4+T淋巴细胞计数记录;(4)接受二线抗病毒治疗起始基线CD4+T淋巴细胞计数<200个/μl。排除标准:基线信息有缺失的HIV/AIDS患者。本研究经河南中医药大学第一附属医院伦理委员会批准(2019HL-068),免除患者知情同意。
1.2 方法
1.2.1 资料收集 收集HIV/AIDS患者的基线资料,包括性别、年龄、婚姻状况、受教育时间、感染途径、HIV阳性时间、更换二线抗病毒治疗方案前接受HAART治疗时间(简称HAART治疗时间)、二线抗病毒治疗时间、接受二线抗病毒治疗起始基线CD4+T淋巴细胞计数(选取距离更换二线抗病毒治疗方案前后3个月内最近一次检测结果)和接受二线抗病毒治疗时是否参与中医项目。收集接受二线抗病毒治疗满1、2、3年时的CD4+T淋巴细胞计数、VL,以及随访期间是否死亡及死亡时间。
1.2.2 治疗方法 纳入患者均接受以LPV/r为基础的二线抗病毒治疗,具体治疗服药方法见《国家免费艾滋病抗病毒药物治疗手册》[9]。参与中医项目的患者另外服用中成药益艾康胶囊(河南省中医药研究院,豫药制字Lz05002,成分:人参、黄芪、炒白术、茯苓、当归、川芎、白芍、黄芩等),服用方法:3次/d,5粒/次,温开水送服,患者一旦参与中医项目会长期服用益艾康胶囊,除非自愿退出。
1.2.3 随访方法和结局事件 随访起点:以更换二线抗病毒治疗方案时间为随访起点,末次随访时间是接受二线抗病毒治疗满3年,以死亡或者3年随访结束为随访终点。CD4+T淋巴细胞计数取每年随访时间点前、后3个月内最近一次检查结果记录,如无,则为缺失;VL为随访时间点前、后6个月内最近一次检查结果记录,如无,则为缺失。
1.3 INR及INR发生率 关于INR的定义目前尚无统一标准,本研究以CD4+T淋巴细胞计数<200个/μl同时 VL<400拷贝 /ml定义为 INR[10]。INR 缺失定义为CD4+T淋巴细胞计数或者VL缺失。VL<400 拷贝/ml表示VL控制良好[10]。INR发生率=随访期符合INR的患者例数/随访期VL<400拷贝/ml的患者例数×100%[11]。
1.4 统计学方法 采用R 4.1.1软件进行数据分析,符合正态分布的计量资料以(±s)表示,计数资料以相对数表示。分别计算接受二线抗病毒治疗满1、2、3年HIV/AIDS患者INR发生率。采用多因素Logistic回归分析探究HIV/AIDS患者发生INR的影响因素。以P<0.05为差异有统计学意义。
2 结果
2.1 患者基线资料 3 016例HIV/AIDS患者中男1 638例(54.31%),女1 378例(45.69%);平均年龄(46.8±8.4) 岁,<40岁 647例(21.45%),40~50岁1 408例(46.69%),>50岁961例(31.86%);有配偶2 383例(79.01%),无配偶633例(20.99%);受教育时间≤6年864例(28.65%),受教育时间>6年2 152例(71.35%);血液途径感染2 357例(78.15%),其他途径感染659例(21.85%);HIV阳性时间<3年532例(17.64%),3~6年1 067例(35.38%),>6年1 417例(46.98%);参与中医项目466例(15.45%),未参与中医项目2 550例(84.55%);HAART治疗时间<3年1 042例(34.55%),3~5年776例(25.73%),>5年1 198例(39.72%);治疗起始平均基线CD4+T淋巴细胞计数(118±55)个/μl,其中151~200个/μl 1 044例(34.62%)、101~150个/μl 871例(28.88%)、50~100个 /μl 635例(21.05%)、<50个 /μl 466例(15.45%)。
2.2 随访情况及INR发生率 3 016例HIV/AIDS患者随访第1年死亡232例(7.69%),INR缺失566例(18.77%);第2年累积死亡341例(11.31%),INR缺失462例(15.32%);第3年累积死亡447例(14.82%),INR缺失540例(17.90%),见表1。第1、2、3年INR发生率分别为42.34%(774/1 828)、32.31%(608/1 882)和24.11%(421/1 746)。

表1 HIV/AIDS患者随访情况〔n(%),N=3 016〕Table 1 The three-year follow-up information in HIV/AIDS patients switching to second-line antiretroviral therapy
2.3 二线抗病毒治疗后HIV/AIDS患者发生INR的影响因素 剔除INR缺失、死亡的患者,对HIV/AIDS患者接受二线抗病毒治疗后发生INR的影响因素进行分析,以是否发生INR为因变量(赋值:是=1,否=0),以性别、年龄、受教育时间、感染途径、婚姻状况、HIV阳性时间、参与中医项目、HAART治疗时间、基线CD4+T淋巴细胞计数为自变量,进行多因素Logistic回归分析,结果显示,性别、基线CD4+T淋巴细胞计数是HIV/AIDS患者接受二线抗病毒治疗后第1年发生INR的影响因素(P<0.05),见表2;性别、年龄、感染途径、HIV阳性时间、HAART治疗时间、基线CD+4T淋巴细胞计数是HIV/AIDS患者接受二线抗病毒治疗后第2年发生INR的影响因素(P<0.05),见表3;年龄、感染途径、基线CD4+T淋巴细胞计数是HIV/AIDS患者接受二线抗病毒治疗后第3年发生INR的影响因素(P<0.05),见表4。
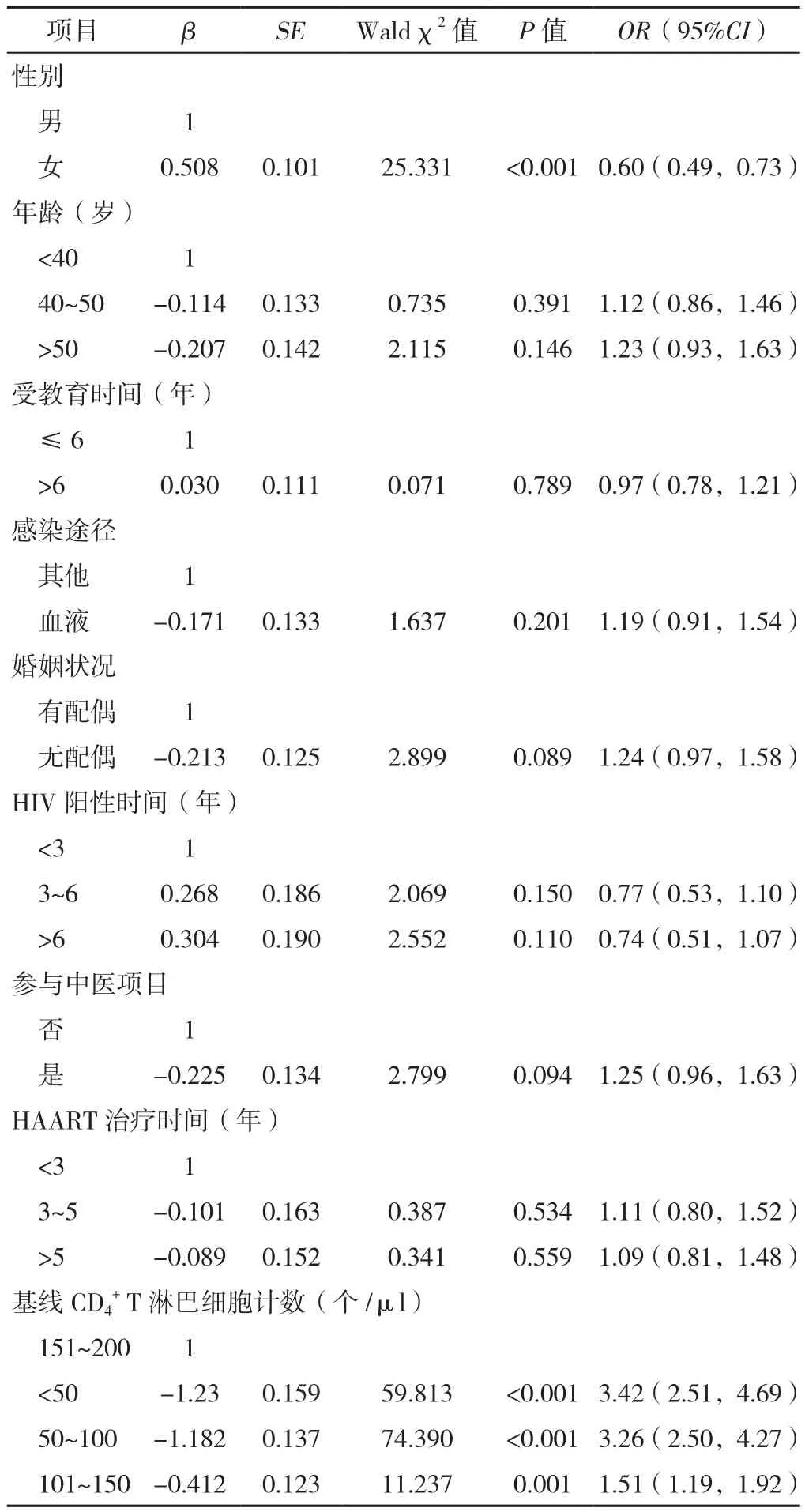
表2 HIV/AIDS患者接受二线抗病毒治疗第1年发生INR影响因素的多因素Logistic回归分析Table 2 Multivariate Logistic regression analysis of influencing factors of INR in HIV/AIDS patients in the first year of second-line antiretioviral therapy

表3 HIV/AIDS患者二线抗病毒治疗第2年发生INR影响因素的多因素Logistic回归分析Table 3 Multivariate Logistic regression analysis of influencing factors of immunological non-response in HIV/AIDS patients in the second year of second-line antiretioviral therapy

表4 HIV/AIDS患者接受二线抗病毒治疗第3年发生INR影响因素的多因素Logistic回归分析Table 4 Multivariate Logistic regression analysis of influencing factors of immunological non-response in HIV/AIDS patients in the third year of second-line antiretioviral therapy
3 讨论
据联合国艾滋病规划署统计,2020年全球HIV感染人数已达到3 770万,其中73%的患者接受了抗反转录病毒治疗[12]。绝大多数患者经过治疗取得了较好的免疫重建效果,仍有部分患者出现INR。INR不仅造成患者心理上的压力,也给患者及其家庭带来沉重的经济负担。近年来,国内外学者围绕INR的定义、病因、病机、临床表现、疾病诊断、治疗原则和方案等进行了大量研究,取得了一定进展。研究发现,年龄、基线CD+4T淋巴细胞计数、丙型肝炎病毒(HCV)共感染是INR的影响因素;骨髓造血功能降低和胸腺输出减少造成的CD4+T淋巴细胞产生减少、免疫活化和凋亡增加造成的CD4+T淋巴细胞破坏增多及体内细胞白介素7(IL-7)等细胞因子水平紊乱是发生INR的内在机制。尽早开始HAART治疗、采用生长激素疗法、免疫抑制剂疗法、细胞因子疗法和中医、中药疗法能够促进免疫重建,但INR的定义、机制、治疗方法等仍尚未完全明确[13]。随着更换二线抗病毒治疗方案的HIV/AIDS患者人数逐渐增多,以往多数研究主要关注的是患者更换二线抗病毒治疗后的CD4+T淋巴细胞计数、VL及耐药情况[14],有关患者更换二线量病毒治疗后INR的发生情况少见报道。了解患者开始二线抗病毒治疗后INR的发生率及影响因素,可为临床防治INR提供参考。
关于INR的定义目前尚无统一标准,其界定主要包含3个要素:HAART治疗时间、VL和CD4+T淋巴细胞计数。对INR的这3个要素界值的界定,学者存在不同的观点,关于HAART治疗时间包括:3、6、12、24、36、60个月等;关于VL包括:HAART后一段时间内VL被抑制和HAART后某个时间节点VL被抑制;VL被抑制的界值包括:<20拷贝/ml、<50拷贝/ml、<60拷贝 /ml、<400拷贝 /ml、<500拷贝/ml等;CD4+T淋巴细胞计数包括:CD4+T淋巴细胞计数<200个/μl、<250 个 /μl、<350 个 /μl、<500 个 /μl等,增加数量<50个 /μl、<100个 /μl,增长率低于 20%、30% 等[13,15-16]。本研究采用的标准依据HAN等[10]的研究制定。
关于INR发生率的计算有两种方式:(1)随访期发生INR的HIV/AIDS患者例数/随访期所有坚持治疗的HIV/AIDS患者例数×100%;(2)随访期发生INR的HIV/AIDS患者例数/随访期VL控制良好HIV/AIDS患者例数×100%[11]。本研究将CD4+T淋巴细胞计数 <200个 /μl同时 VL<400拷贝 /ml定义为 INR,以VL控制良好(CD4+T淋巴细胞计数<400拷贝/ml)HIV/AIDS患者例数为分母计算INR的发生率。
本研究发现,HIV/IDS患者接受二线抗病毒治疗后的满1、2、3年INR发生率分别为42.34%、32.31%和24.11%。表明HAART后大部分患者可以获得良好的免疫重建,且随着治疗时间的延长INR发生率下降,与既往研究结论一致[13]。乌干达的一项队列研究发现,在接受一线抗病毒治疗的第1、2年,CD4+T淋巴细胞计数<200个/μl同时VL<400拷贝/ml的患者所占的比例分别为42%和19%[15]。在泰国的1项基于375例HIV/AIDS患者的回顾性队列研究中,CD4+T淋巴细胞计数<200个/μl的患者在接受一线及二线抗病毒治疗的1、2和3年,CD4+T淋巴细胞计数<200个/μl同时VL<400拷贝/ml的患者占比分别39.7%、19.7%和7.7%[10]。尽管有研究证明接受二线抗病毒治疗的HIV/AIDS患者可以获得更好的免疫重建效果[14,17],但本研究得出的INR发生率略高于其他研究,原因可能与延迟启动二线抗病毒治疗有关,部分患者在接受二线抗病毒治疗前已经存在一线抗病毒治疗失败,继续使用一线抗病毒药物可能会引起耐药突变的累积,降低二线抗病毒治疗的有效性[18],导致患者在接受二线抗病毒治疗后INR的发生率较高。
本研究表明,随访第1、2年女性发生INR的风险均低于男性;随着基线CD4+T淋巴细胞计数的降低,发生INR的风险增高,随访第2年,年龄>40岁、第3年年龄>50岁的患者发生INR的风险较高,这一结果与既往研究一致[19-20],原因可能与女性患者依从性更好,老年HIV/AIDS患者的胸腺功能弱化,CD4+T淋巴细胞再生减弱,基线CD4+T淋巴细胞计数较低的患者,免疫系统已受损严重等因素有关。此外,本研究发现经血液途径感染的HIV/AIDS患者在随访第2、3年更容易发生INR。随访第2年HIV阳性时间为3~6年、HAART治疗时间>3年的患者更容易发生INR。先前研究同样发现感染途径、HAART治疗时间会对INR的发生产生影响,但研究结果并不一致。魏秀青等[21]的研究发现,与感染途径为性传播、输血及血制品和其他的患者相比,静脉注射吸毒的患者发生INR的风险更高。一项大型队列研究发现男性异性恋和注射吸毒传播是INR的危险因素[2]。蒋春云等[22]认为在治疗前期CD4+T淋巴细胞计数增长较快,随着时间的延长,增长速度下降,发生INR的患者大多是经过HAART治疗时间较长的人群。而梅馨尹等[23]的研究发现HAART持续治疗时间≥24个月与治疗时间不足24个月的患者相比,发生INR的风险更低。HIV确诊时间对INR的影响研究较少。不同研究结果间存在差异的原因可能与地域差异、生活方式不同、种族不同以及诊断标准不一致有关。因此,感染途径、HAART治疗时间及HIV阳性时间对INR的影响仍需进一步探索。既往研究显示中医药在治疗INR方面发挥了独特的优势,中医药可以降低INR患者的VL、提高CD4+T淋巴细胞计数、提升免疫重建的有效率[24],但本研究并未发现中医药与INR发生率之间的关系,原因可能与本研究中仅有15.45%的患者参与中医项目有关。
综上所述,男性、年龄50岁以上、经血液传播途径感染、基线CD4+T淋巴细胞计数较低的HIV/AIDS患者接受二线抗病毒治疗后更容易发生INR。本研究为回顾性队列研究,一些与INR相关的基线变量没有完整记录,可能存在选择偏倚和信息偏倚。同时,由于未限制一线、二线抗病毒治疗中的核苷类抑制剂的种类及组合方式,也无法获得与依从性相关的有效信息,因而不能推论INR发生率较高的原因来自蛋白酶抑制剂。今后尚需要加强对二线抗病毒治疗后INR的研究。
作者贡献:金艳涛负责文章的构思、研究的设计、实施与可行性分析,对论文整体负责、监督管理;袁君、马秀霞进行数据收集与整理;王东利、艾艳珂、金艳涛进行统计学处理、论文撰写;郭会军、许前磊对结果进行分析与解释,负责文章的质量控制。
本文无利益冲突

