基于CT诊断的肌少症对结直肠癌患者发生手术部位感染的影响因素分析
张芳芳,胡雅静,黄华勇,倪锦晖,尤泽,常巧玲,廖力*
结直肠癌是常见的消化道肿瘤之一,全球发病率居第三位;我国结直肠癌新发例数及死亡例数分别占全球总例数的23.7%和30.2%,均位居全球第一位;结直肠癌对人类健康造成极大威胁[1-2]。目前根治性手术切除是治愈结直肠癌的主要治疗方法,然而手术部位感染(surgical site infection,SSI)是结直肠癌术后常见的并发症之一[3]。尽管有多种预防SSI措施,但结直肠癌术后SSI发生率仍然很高,国外发生率为23%~26%,国内为11%~30%[4-5]。SSI会降低患者生活质量、延长住院时间、增加住院费用、延迟辅助治疗,给患者带来巨大的身心负担[6]。研究表明,肌少症会增加结直肠癌患者术后并发症的发生风险、延长术后康复时间[7-8]。肌少症是一种可导致骨骼肌质量和总量进行性和全面性丧失的综合征,并导致身体残疾、生活质量下降等不良后果[9],与衰老、营养不良、炎症性疾病和癌症等因素有关[10]。与其他癌症相比,肌少症在结直肠癌等消化道肿瘤中的发生率更高[11]。通过计算机断层扫描(CT)评估第三腰椎骨骼肌质量是目前国内外诊断肌少症的金标准[12]。本研究回顾性分析结直肠癌手术后患者的手术相关结局,评估肌少症对SSI的影响。
1 资料与方法
1.1 一般资料 回顾性收集2019年7月至2021年12月在南华大学附属第一医院胃肠外科接受根治性结直肠癌切除术328例患者的临床资料。研究对象纳入标准:(1)术后经病理检查证实为原发性结直肠癌[2];(2)行结直肠癌根治术;(3)手术前30 d内行腹部CT扫描;(4)术后至少1个月的随访;(5)病历资料完整。排除标准:(1)行急诊手术或姑息性手术者;(2)合并其他部位恶性肿瘤者。所有手术由经验丰富的医师进行。
1.2 观察指标 通过医院电子病历查询系统收集患者性别、年龄、疾病史、NRS2002营养筛查指数[13]、内科合并症指数[14]、美国麻醉师协会(ASA)分级[15]、腹部手术史、化疗史、术前血清白蛋白水平、术前血红蛋白水平、术前C反应蛋白水平、肿瘤分化程度、神经侵犯、脉管癌栓侵犯、AJCC肿瘤分期及手术结局(术中出血量、术后输白蛋白与输血、肠造口、SSI、再手术、总住院天数、术后住院天数)等资料。
1.3 SSI的诊断 参照《医院感染诊断标准(试行)》[16],患者住院期间若符合以下任何一项即可判断为术后SSI:(1)切口深部引流出或穿刺出脓液;(2)切口出现疼痛或压痛,表浅部位脓性分泌物,或体温≥38 ℃;(3)组织病理学或影像学检查发现切口深部脓肿或具有其他感染证据;(4)切口分泌物细菌培养阳性。
1.4 肌肉质量的评估方法和诊断标准 通过医院影像科提取患者CT检查的原始文件,选取第三腰椎水平层面,由影像学图像处理软件(Slice Omatic,Canada,V 2.4b)进行半自动画图。骨骼肌包括腰肌、腰椎肌、竖脊肌、腹横肌、内外斜肌和腹直肌,肌肉组织单位组织阈值范围为-29~150 HU。L3骨骼肌肌肉质量指数(SMI)(cm2/m2)=L3层面所有骨骼肌总面积(cm2)/身高2(m2),软件自动获取L3层面肌肉平均密度(L3 SMD)[17]。按性别划定肌少症的判断标准[18]:男性SMI<40.8 cm2/m2,女性 SMI<34.9 cm2/m2。上述所有测量和计算由两名经过训练的人员进行,在量化时均对手术结果不知情,所有评估独立进行。
1.5 统计学方法 采用SPSS 23.0统计软件进行数据分析。符合正态分布的计量资料以(±s)表示,两组间比较采用独立样本t检验;非正态分布的计量资料以M(P25,P75)表示,两组间比较采用非参数检验;计数资料的分析采用χ2检验;采用单因素和多因素Logistic回归分析探讨结直肠癌患者术后发生SSI的影响因素。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般资料比较 328例患者中,肌少症组44例(13.5%),非肌少症组284例(86.5%)。肌少症组和非肌少症组糖尿病发生率、高血压发生率、冠心病发生率、脑血管疾病发生率、内科合并症指数、ASA分级≥3级、化疗史所占比例、术前血红蛋白水平、术前C反应蛋白水平、神经侵犯所占比例、脉管癌栓侵犯所占比例、AJCC肿瘤分期比较,差异均无统计学意义(P>0.05);肌少症组和非肌少症组性别、年龄、NRS2002≥3分、腹部手术史、术前血清白蛋白水平、肿瘤分化程度比较,差异均有统计学意义(P<0.05),见表1。

表1 肌少症组和非肌少症组一般资料比较Table 1 Comparison of general data between colorectal cancer patients with and without CT-assessed sarcopenia
2.2 两组患者手术结局比较 肌少症组和非肌少症组术后输血发生率、肠造口、再手术发生率比较,差异均无统计学意义(P>0.05);肌少症组术中出血量≥200 ml、术后输白蛋白、SSI发生率均高于非肌少症组,总住院天数、术后住院天数均长于非肌少症组,差异有统计学意义(P<0.05),见表2。
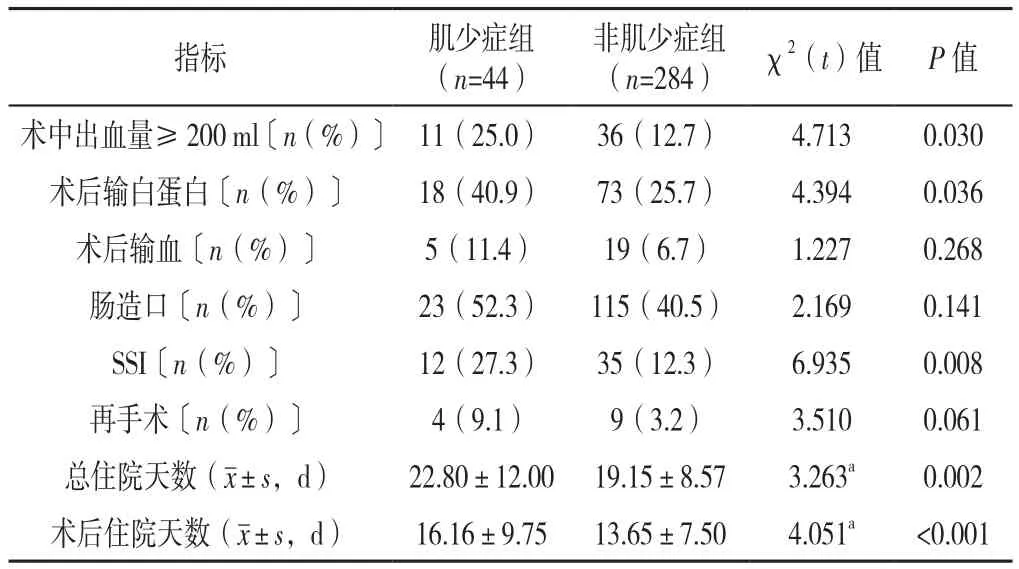
表2 肌少症组和非肌少症组手术结局指标比较Table 2 Comparison of surgical outcome indicators between colorectal cancer patients with and without CT-assessed sarcopenia
2.3 结直肠癌患者术后发生SSI的影响因素分析
2.3.1 单因素Logistic回归分析 将SSI作为因变量(赋值:是=1,否=0),将可能影响SSI的肌少症(赋值:是=1,否=0)、性别(赋值:是=1,否=0)、年龄、内科合并症指数、NRS2002≥3分(赋值:是=1,否=0)、ASA分级≥3级(赋值:是=1,否=0)、血清白蛋白、血红蛋白、C反应蛋白、术中出血量≥200 ml(赋值:是=1,否=0)、肠造口(赋值:是=1,否=0)等11个因素为自变量(其他指标赋值为实测值),分别进行单因素Logistic回归分析,结果显示,肌少症、ASA分级≥3级、肠造口是结直肠癌患者术后发生SSI的危险因素(P<0.05),见表3。
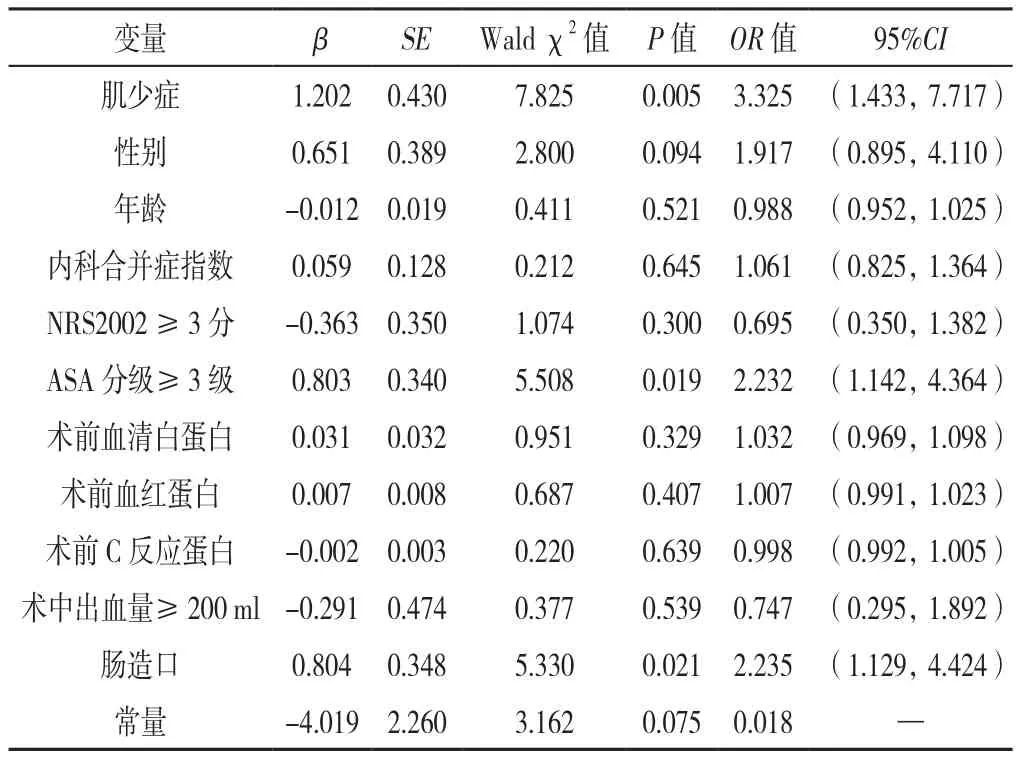
表3 结直肠癌患者术后发生SSI影响因素的单因素Logistic回归分析Table 3 Univariate Logistic regression analysis of the influencing factors of postoperative surgical site infection in patients with colorectal cancer
2.3.2 多因素Logistic回归分析 以SSI为因变量,以单因素Logistic分析中有统计学意义的变量作为自变量,进行多因素Logistic回归分析,结果显示,肌少症、ASA分级≥3级、肠造口是结直肠癌患者术后发生SSI的危险因素(P<0.05),见表4。

表4 结直肠癌患者术后发生SSI影响因素的多因素Logistic回归分析Table 4 Multivariate Logistic regression analysis of the influencing factors of postoperative surgical site infection in patients with colorectal cancer
3 讨论
由于结直肠癌患者发病部位的特殊性,机体的消化吸收功能降低,术前营养不良的发病率高达20%[19]。术前营养不良可降低结直肠癌手术患者的免疫功能,增加术后SSI的风险,延长患者住院时间,增加患者死亡风险[20-21]。因此,鉴别营养不良对于结直肠癌患者的治疗策略的制定和后续干预具有重要意义。最近研究提出,与体质指数等营养指标相比,基于骨骼肌质量诊断肌少症可更直接反映癌症患者的营养状况,用于预测癌症患者的临床结局[6,19,22]。但这一观点仍尚有争论[23-24]。此外,以往研究肌少症对于术后并发症的影响因素分析较为笼统,而本研究针对性地分析肌少症对于结直肠癌患者术后发生SSI的影响。
CT能精准区分肌肉、皮下脂肪及其他软组织,而且可以评估肿瘤的生长情况,不加重患者的经济负担,所以在癌症患者中测量骨骼肌质量主要采用CT检查[12]。目前国际上肌少症诊断采用欧洲肌肉减少症工作小组定义的骨骼肌质量减少的标准,其数据是基于西方人群的CT图像分析得出的L3骨骼肌质量密度,因此不适用于直接作为中国人群诊断肌少症的标准[6,22-24]。然而,亚洲肌肉工作小组推荐评估骨骼肌密度的方法是双能X线吸收法,其易受到组织纤维化的影响,降低测量的准确性。因此本研究采用我国研究者普遍使用的ZHUANG等[18]进行的一项前瞻性队列研究经最佳分层获得骨骼肌减少症的临界值为标准,男性SMI<40.8 cm2/m2,女性SMI<34.9 cm2/m2诊断为肌少症。基于上述标准,13.4%的结直肠癌手术患者在术前诊断出肌少症,其中男性20例,女性24例。与奚秋磊等[25]研究报道的我国结直肠癌患者术前诊断肌少症发病率为15.7%相近。
本研究对结直肠癌患者按肌少症标准分组后,两组患者在术前状态及术后恢复情况存在多项差异。肌少症最早被定义为随年龄增长而骨骼肌质量减少及肌力下降[26],本研究中肌少症组患者的平均年龄更高,然而两组患者的年龄差异并无统计学意义,与OLMEZ等[23]研究结果不一致,可能与本研究纳入的结直肠癌患者年龄较为集中有关。本研究显示性别是发生肌少症的危险因素,在女性中肌少症患病率更高,可能与年龄的增加导致女性雄激素水平下降有关[27]。多项研究显示,结直肠癌患者发生肌少症与营养缺失存在着密切的联系[9-10]。NRS2002营养风险筛查作为临床常用的营养评分工具,可较好地评估患者的营养状态,本研究使用该标准对结直肠癌患者进行评分分层,结果显示两组之间存在差异,肌少症组存在营养风险比例更高;其次是肌少症组术前血清白蛋白水平低于非肌少症组,提示术前营养不良与肌少症的发生有关。
肌少症是恶性肿瘤患者的重要预后因素,本研究发现肌少症组术后输白蛋白较多、SSI发生率较高、总住院及术后住院时间延长。LIEFFERS等[28]首次探讨肌少症与结直肠癌患者术后感染之间的关联,发现肌少症患者术后感染率高达23.7%(P=0.025),与本研究感染率为27.3%较接近,其结论表明肌少症可以预测术后感染,影响住院康复护理,从而延长术后住院时间。随后DOLAN等[29]与REISINGER等[30]证明了肌少症与结直肠癌术后炎症指标增加有关。我国学者HUANG等[8]研究发现术后感染在结直肠癌肌少症患者中的发病率高达41.2%,此研究术后感染发病率高于本研究结果(27.3%),可能与本研究开展术后快速康复有关,降低了术后感染。但本研究中患者总住院与术后住院天数接近田浩等[31]研究结果,这主要与SSI的治疗方式有关,本研究中由国际伤口造口治疗师采用自制的简易负压伤口吸引器对感染部位清创,因负压来自中心负压管道装置,患者需住院进行治疗从而延长住院时间;其次是部分结直肠癌患者在术前接受化疗增加营养消耗,术中应激反应增加代谢,术后增加蛋白质合成[32],导致结直肠癌患者术后需通过输注血清白蛋白等营养支持方式增加能量供给。
经过多因素Logistic回归分析提示:肌少症、ASA分级≥3级以及肠造口是结直肠癌术后发生SSI的危险因素,这一结论与以往研究结果相符。本研究结果显示肌少症是结直肠癌术后发生SSI的危险因素,与LIEFFERS等[28]一致,但OLMEZ等[23]认为肌少症与SSI之间并无关系。目前关于术前肌少症与SSI发生风险的病理机制仍尚未阐明,多数研究认为骨骼肌质量减少可导致炎性因子增加,抗炎细胞减少,使肌少症患者一直处于促炎状态中,患者的免疫系统受损,对手术创伤及术后感染更加敏感,发生SSI的风险提高[29-30,33]。同时,肌肉作为人体最大的蛋白质库,是应激氨基酸的主要来源,当身体遇到手术创伤等应激源时,肌肉蛋白便迅速分解成氨基酸,分配到免疫系统、胃肠等器官以提供能量[34]。然而,肌少症患者用于修复组织的氨基酸数量低于需求量,导致伤口愈合减缓,进一步导致SSI的发生。ASA分级用于评估患者手术和麻醉的风险及风险大小,但既往研究表明ASA分级也可以作为结直肠癌患者发生SSI的危险因素[35],本研究结果与之一致。刘芯妤等[36]进一步探究了不同ASA分级对SSI的风险,结果表明随着级别的升高,结直肠癌患者术后SSI的发病率逐步升高。当ASA分级≥3级时,外科医生需要与麻醉医生交流,积极改善患者术前的全身情况,可有效降低术后SSI的发生。肠造口增加了手术创伤与手术时间,也提高了细菌感染的风险,因此术后有造口患者发生SSI的风险高于无造口患者。本研究结果与牟丹辉等[37]一致,表明肠造口是导致结肠癌患者术后发生SSI的独立危险因素。
本研究的局限性:本研究为回顾性分析,在收集资料的过程中删除了缺失病例,导致选择偏倚,对结果及结论造成一定影响;本研究为单中心研究,存在人群偏倚,未来可开展多中心研究;本研究对肌少症的诊断只有骨骼肌数量减少一项指标,未获取到骨骼肌功能数据,如行走速度、握力。
综上所述,本研究表明肌少症是结直肠癌手术患者术后发生SSI的独立危险因素。在结直肠癌患者手术前,通过腹部CT筛查肌少症并采取针对性措施,可能降低患者术后SSI的发生、改善患者的预后、提高生活质量。
作者贡献:张芳芳、廖力负责文章的构思与设计,对文章负责;胡雅静、黄华勇负责文章的质量控制;张芳芳、倪锦晖、尤泽、常巧玲负责文章的数据收集与整理;张芳芳负责数据分析、论文撰写与修订。
本文无利益冲突。

