瑞香素对人类风湿关节炎滑膜成纤维细胞凋亡的影响及其与内质网应激的关系*
敖琴,刘俊,胡欢,李培霆,秦龙燕,蒙富雪,李龙*** ,曾家顺***
(1.贵州医科大学 临床医学院,贵州 贵阳 550004;2.贵州医科大学附属医院 风湿免疫科,贵州 贵阳 550004;3.贵州医科大学 第三附属医院,贵州 都匀 558000)
类风湿关节炎(rheumatoid arthritis,RA)是一种慢性、自身免疫性和多系统的炎症性疾病[1],病变主要侵犯四肢小关节,可促使滑膜增生、关节滑膜炎及骨与软骨进行性破坏[2],其中炎症的产生以及骨和软骨的破坏与滑膜成纤维细胞(fibroblast-like synoviocytes,FLS)肿瘤样增殖相关,RA-FLS的异常增殖主要因为其具有抗凋亡的特性[3-5]。瑞香素(daphnetin,DAP),又名祖师麻甲素,是一种香豆素类衍生物,具有抗炎、抗肿瘤及抗氧化等作用[6-8]。在胶原诱导性关节炎(collagen-induced arthritis,CIA)大鼠中,DAP可减弱辅助性T细胞2(helper T cell,Th2)、辅助性T细胞17(helper T cell,Th17)型应答,抑制白细胞介素1β(interleukin 1β,IL-1β)、白细胞介素6(interleukin 6,IL-6)及白细胞介素12(interleukin 12,IL-12)的表达,从而起到抗炎作用[9-11];DAP还可促进促凋亡基因死亡受体3(death receptor 3,DR3)、细胞程序性死亡受体5(programmed cell death 5,PDCD5)、人凋亡相关因子配体(human factor-related apoptosis ligand,FasL)和人抑癌基因P53去甲基化,增加细胞凋亡[12-14]。目前,DAP在炎症性疾病中研究相对较少,且作用机制还未明确。本研究基于内质网应激(endoplasmic reticulum stress,ERS),探讨DAP对人RA-FLS增殖、凋亡的影响,旨在进一步明确DAP作用机制,为将其应用于临床提供参考依据。
1 材料与方法
1.1 实验材料
1.1.1细胞株 人类风湿关节炎成纤维样滑膜细胞(人RA-FLS),由贵州医科大学第三附属医院中心实验室蒙富雪老师惠赠,购于北京北纳生物(BNCC340356)。
1.1.2主要药物和试剂 DAP(上海源叶,纯度≥98%)和Cell Counting Kit-8试剂盒(CCK-8,大连美伦),胎牛血清和青霉素/链霉素(美国BI),二甲基亚砜(中国索莱宝),高糖Dulbeccos Modified EagleMedium(DMEM,美国Gibco),兔多克隆抗体蛋白激酶R样内质网激酶抗体(protein kinase-like ER kinase,PERK)、兔多克隆ERS相关蛋白葡萄糖调节蛋白78抗体(glucose regulated protein 78,GRP78)、兔多克隆凋亡蛋白C/EBP同源蛋白抗体(C/EBPhomologous protein,CHOP)及兔多克隆含半胱氨酸的天冬氨酸蛋白水解酶12抗体(cysteinyl aspartate specific proteinase 12,Caspase12;武汉三鹰),B细胞淋巴瘤/白血病-2(B-cell lymphoma gene-2,BCL-2;中国华安生物),凋亡试剂盒(美国BD)。
1.1.3主要仪器 倒置显微镜(日本Nikon),酶标仪(美国Thermo),曝光机(美国Bio-rad),培养箱(美国Biobase),流式细胞仪(美国Beckman coulter)。
1.2 实验方法
1.2.1细胞培养 细胞培养于含15%胎牛血清和1%青霉素/链霉素的DMEM培养基,培养箱条件为37 ℃、5%CO2,2 d换1次液,细胞长满90%左右进行1∶3传代。
1.2.2CCK-8检查细胞存活率 取对数增长期细胞,按100 mL/孔加入96孔板,每组种4个孔,37 ℃、5%CO2培养箱孵育24 h,去掉培养基,用0(对照组)、10、20、30、40、50、60及70 mg/L DAP的培养基处理细胞,24 h后加CCK-8增强剂10 μL、孵育2 h,于酶标仪上波长460 nm处检测吸光度(opticail density,OD)值,记录结果,计算细胞存活率[细胞存活率(%)=(OD实验组-OD空白组)/(OD对照组-OD空白组)×100%],统计分析后以0、20、40及60 mg/L DAP为实验分组,后续实验分组相同。
1.2.3流式细胞术检测细胞凋亡率 取对数增长期细胞接种于6孔板,按1.2.2项下分组处理24 h,冷磷酸缓冲液(phosphate buffer saline,PBS)洗涤细胞2次,PE AnnexinV和7-AAD溶液避光染色15~30 min;流式细胞仪于30 min内对样本进行检测,数据用FlowJo V10软件进行分析。
1.2.4免疫荧光检测蛋白表达 提前在6孔板中放入细胞玻璃爬片,取对数增长期细胞接种于6孔板,待细胞贴壁后,0、20 mg/L DAP处理24 h;清洗、固定、通透、封闭,PERK、GRP78及Caspase12抗体稀释液孵育过夜;次日清洗,荧光二抗避光孵育2 h,DAPI染色5 min,于荧光显微镜下观察。
1.2.5Western blotting检测蛋白表达 取对数增长期细胞接种于6孔板,按1.2.2项下分组处理24 h;PBS清洗细胞,常规方法提取总蛋白,通过蛋白定量试剂盒对蛋白浓度进行定量;经蛋白变性、电泳及转膜后,于5%脱脂奶粉封闭1.5~2.0 h,用PERK、p-PERK、GRP78、CHOP、Caspase-12、Bcl-2及GAPADH一抗4 ℃孵育过夜,次日清洗,辣根过氧化物酶(horseradish peroxidase,HRP)偶联的二抗处理2 h;显色液将信号可视化,使用Image J进行灰度值定量分析。
1.3 统计学分析
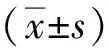
2 结果
2.1 人RA-FLS增殖活性及浓度确定
经0、10、20、30、40、50、60、70 mg/L DAP处理RA-FLS 24 h后,CCK-8检测各组细胞存活率,与0 mg/L DAP组比较,细胞的存活率随DAP浓度增加而受抑制,差异有统计学意义(P<0.05);当药物质量浓度超过60 mg/L时,细胞存活率<50%;0、20、40及60 mg/L DAP组细胞存活率比较,差异均有统计学意义(P<0.05),因此0、20、40及60 mg/L DAP为后续实验分组。见图1。
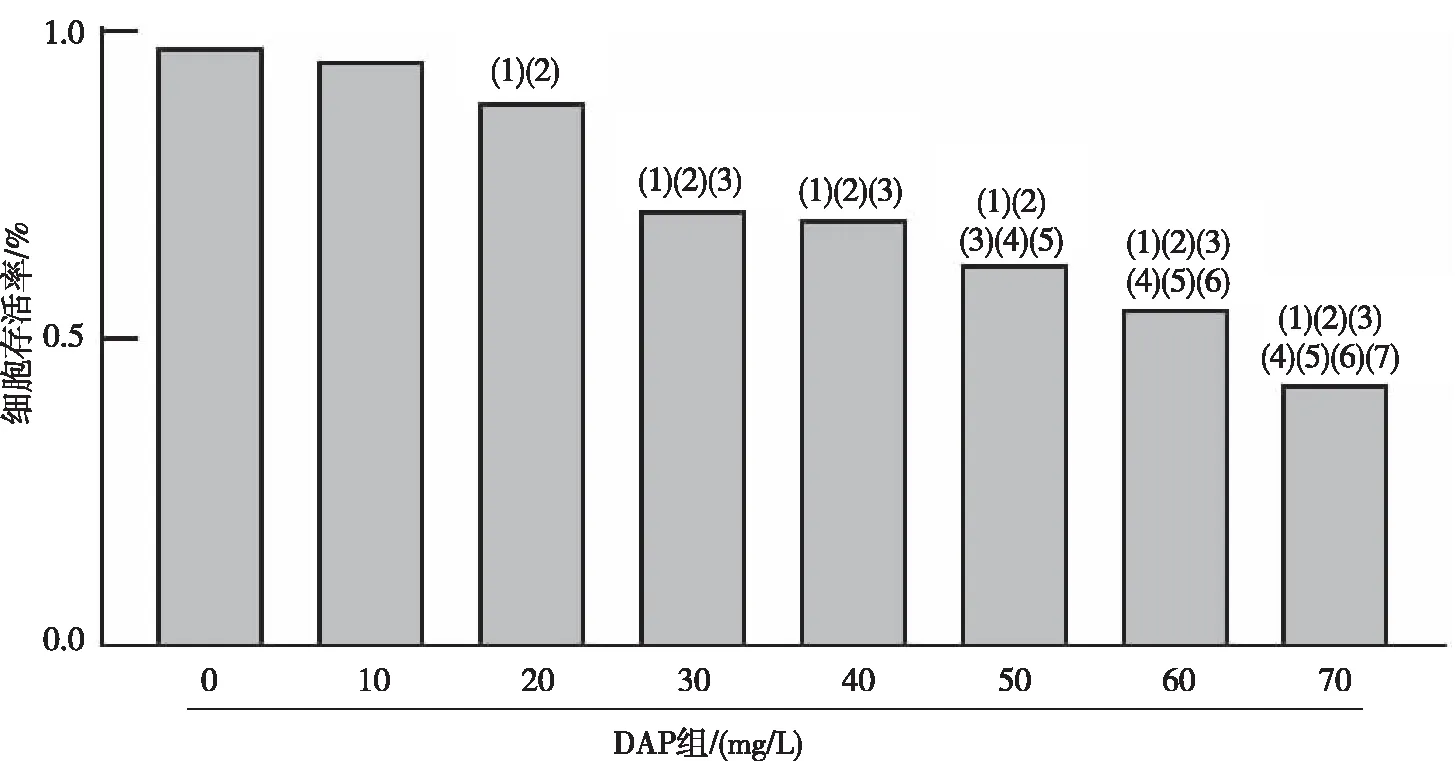
注:(1)与0 mg/L DAP组比较,P<0.05;(2)与10 mg/L DAP组比较,P<0.05;(3)与20 mg/L DAP组比较,P<0.05;(4)与30 mg/L DAP组比较,P<0.05;(5)与40 mg/L DAP组比较,P<0.05;(6)与50 mg/L DAP组比较,P<0.05;(7)与60 mg/L DAP组比较,P<0.05。
2.2 人RA-FLSA凋亡
结果显示与0 mg/L DAP组比较,在药物处理培养24 h后,随着DAP药物浓度增加人 RA-FLS细胞凋率逐渐增大(P<0.05),结果呈剂量依耐性改变。见图2。
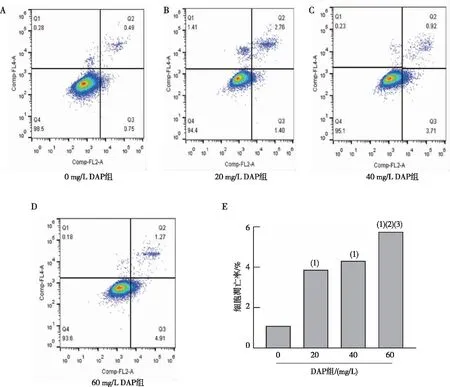
注:A~D分别为0、20、40及60 mg/L DAP组人RA-FLS细胞凋亡的流式图,E为细胞凋亡率的定量结果;(1)与0 mg/L DAP组比较,P<0.05;(2)与20 mg/L DAP组比较,P<0.05;(3)与40 mg/L DAP组比较,P<0.05。
2.3 免疫荧光检测人RA-FLS细胞ERS相关蛋白表达
采用免疫荧光的方式初步观察ERS相关蛋白在DAP处理细胞后的表达情况,结果显示,20 mg/L DAP组处理的人RA-FLS细胞中PERK、GRP78及Caspase-12荧光强度均高于0 mg/L DAP组。见图3。
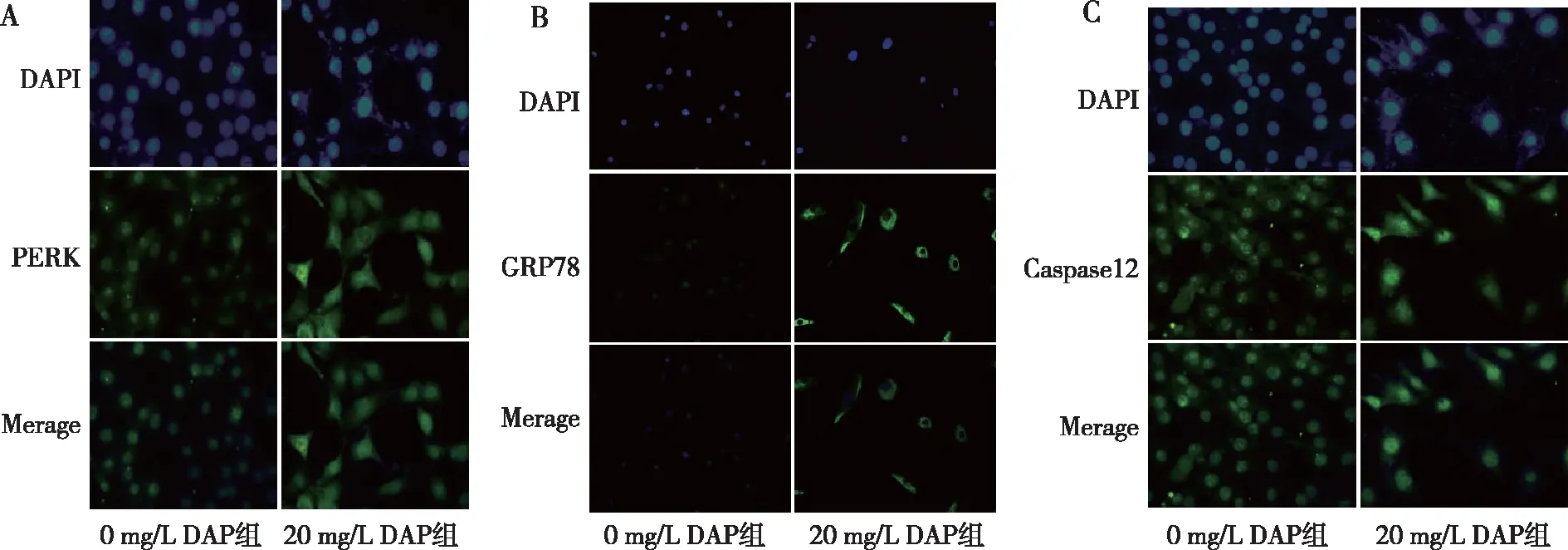
注:A、B、C分别为PERK、GRP78及Caspase-12的蛋白表达;蓝色为细胞核显色,绿色为目的蛋白荧光显色。
2.4 Western blot 检测ERS相关蛋白的表达
Western blot检测结果显示,与0 mg/L DAP组比较,其余质量浓度DAP组对人RA-FLS细胞中ERS相关蛋白PERK、p-PERK、GRP78、CHOP及Caspase-12表达随DAP质量浓度增加而增加,差异均有统计学意义(P<0.05);与0 mg/L DAP组比较,其余质量浓度DAP组对人RA-FLS细胞中ERS抑制凋亡蛋白Bcl-2的表达随质量浓度增加而减少,差异均有统计学意义(P<0.05)。见图4。
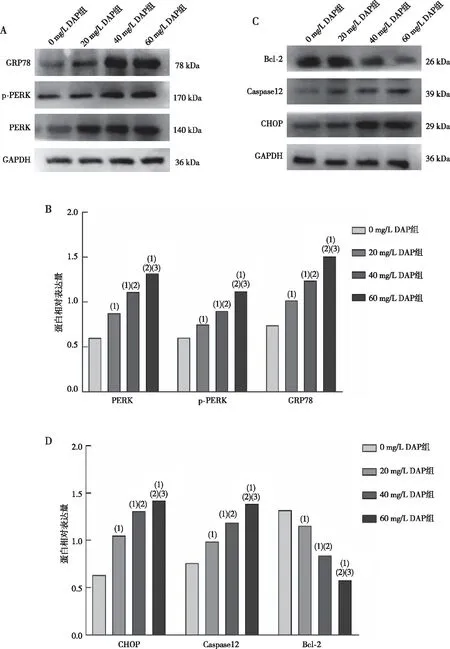
注:A、B分别为PERK、p-PERK及GRP78蛋白电泳和定量表达结果,C、D分别为CHOP、Caspase12及Bcl-2的蛋白电泳和定量表达结果;(1)与0 mg/L DAP组比较,P<0.05;(2)与20 mg/L DAP组比较,P<0.05;(3)与40 mg/L DAP组比较,P<0.05。
3 讨论
甲氨蝶呤、羟氯喹目前作为RA在临床上常用药[15],能快速缓解疾病症状,再加上生物制剂的加持,使得RA的治疗更近一步改善,患者病情可得到极大控制,但部分患者因个体差异对药物的敏感性及耐药性的不同,疗效不一,还会出现不同程度副作用[16-18]。因此,找到一种合适、更有效的治疗方式是至关重要的[19]。近年来,中草药类药物研发和应用不断发展,与化学类药剂相比,具有毒性及副作用小的优势,因此发掘中草药类抗炎制剂将更加造福于人类[20-22]。已有相关研究表明,DAP在CIA中可调节辅助性T(helper T cell,Th)细胞,并通过线粒体自噬途径调节CIA小鼠FLS炎症介质表达、促进其凋亡[23-25]。本研究结果显示,DAP可成剂量依耐性地诱导人RA-FLS细胞凋亡,与前期诱导CIA-FLS凋亡结果一致。
ERS是细胞自我调节功能的体现,适当的应激可通过ERS提高细胞存活率,起到细胞保护作用,但当过度刺激超过内质网自身调节能力时,ERS反而加重细胞内环境稳态的不平衡,通过诱发下游凋亡信号通路,从而导致细胞凋亡[26]。PERK/GRP78/CHOP是ERS中的一条通路,可介导下游凋亡基因的表达,当启动ERS时,PERK与GRP78解离,以磷酸化活性状态激活下游CHOP、Caspase-12及Bcl-2表达,促进细胞凋亡[27-29]。本研究首先通过免疫荧光初步检测20 mg/LDAP对人RA-FLS细胞ERS相关蛋白表达的影响,再通过蛋白印记进一步定量印证,结果显示,20 mg/L DAP可上调人RA-FLS细胞表达PERK、GRP78以及Caspase-12,对应的蛋白印记结果也进一步证明DAP可成剂量依耐性诱导ERS相关蛋白表达。
综上所述,DAP对人RA-FLS的抑制作用可能与ERS介导的凋亡相关,但本研究仅先探讨DAP在人RA-FLS细胞中与ERS的初步联系,后续仍需加入抑制剂进行验证,同时还需进一步在动物体内加以研究,深入探讨潜在分子机制,为DAP治疗RA提供更具说服力的理论支撑。

