血清hs-CRP、Hcy、Cys-C水平与2型糖尿病周围神经病变的相关性
蔡文婷
(江南大学附属医院内分泌科,江苏 无锡 214000)
糖尿病周围神经病变(diabetic peripheral neuropathy,DPN)作为2型糖尿病(diabetes mellitus type 2,T2DM)较为常见的一种慢性并发症,是导致足部溃疡、坏疽、感染的重要因素,严重者甚至面临截肢,影响患者生命质量[1]。DPN的发病机制复杂,由代谢紊乱所致的炎症反应、氧化应激、血管内皮损伤等多种因素均参与其发生发展[2-3]。超敏C反应蛋白(hypersensitive C-reactive protein,hs-CRP)是敏感的炎症指标,可参与糖尿病微血管病变的发生发展[4]。同型半胱氨酸(homocysteine,Hcy)作为一种血管损伤性氨基酸,可反映血管病变状况,与T2DM血管病变紧密相关[5]。胱抑素C(cystatin-C,Cys-C)是判断肾小球滤过率的敏感指标,其表达水平与糖尿病心血管事件和糖尿病神经病变密切相关[6-7]。但目前关于Hcy、Cys-C与T2DM患者周围神经病变的相关性的文献报道尚少,现存报道结论也不尽相同。本研究拟明确hs-CRP、Hcy、Cys-C与T2DM周围神经病变的相关性。
1 资料与方法
1.1 一般资料
选取2020年1月至2021年6月江南大学附属医院收治的148例T2DM患者作为研究对象。纳入标准:符合1999年WHO制定的T2DM诊断标准[8],且各项临床检测资料完整。排除标准:(1)合并其他代谢性疾病者;(2)合并慢性炎症性疾病者;(3)严重肝肾功能不全者;(4)合并自身免疫性疾病者;(5)活动性感染者;(6)恶性肿瘤患者;(7)终末期疾病者。所有T2DM患者中,单纯T2DM患者92例(T2DM组);T2DM合并DPN患者56例(DPN组),DPN诊断参照《糖尿病神经病变诊治专家共识(2021年版)》[9]。根据多伦多神经病变评分(TCSS)[10]将DNP患者分为不同病情亚组:6~8分(轻度)、9~11分(中度)、12~19分(重度)。另选取同期与T2DM患者性别、年龄相匹配的50名健康体检者作为对照组。本研究经医院医学伦理委员会批准,入组对象均签署知情同意书。
1.2 研究方法
1.2.1 一般资料收集 收集患者一般资料,包括性别、年龄、糖尿病病程、吸烟史、饮酒史,测量身高、体重,计算身体质量指数(BMI)。
1.2.2 生化指标检测 受试对象均禁食8 h以上后采集肘静脉血5 mL,离心(3 000 rpm,10 min)留取血清,采用全自动生化分析仪(AU5800型,美国贝克曼)进行空腹血糖(FPG)、总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白胆固醇(HDL-C)及低密度脂蛋白胆固醇(LDL-C)的测定,应用高效液相色谱进行糖化血红蛋白(HbA1c)的测定,并采用增强免疫比浊法进行hs-CRP水平的测定,采用酶联免疫吸附法进行Hcy水平的测定,采用微粒子增强比浊法进行Cys-C水平的测定,试剂盒购自上海景源医疗器械有限公司。
1.3 统计学分析
2 结果
2.1 各组一般资料比较
DPN组血清hs-CRP、Hcy、Cys-C、FPG及HbA1c水平高于T2DM组和对照组(P<0.05),且T2DM组血清hs-CRP、Hcy、Cys-C、FPG及HbA1c水平高于对照组(P<0.05),DPN组糖尿病病程长于T2DM组(P<0.05)。见表1。
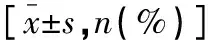
表1 各组一般资料比较
2.2 DPN影响因素的Logistic回归分析
将DPN作为因变量,以hs-CRP、Hcy、Cys-C、糖尿病病程、FPG、HbA1c等为自变量行Logistic回归分析。结果显示,hs-CRP、Hcy、Cys-C、糖尿病病程是DPN发生的独立危险因素(P<0.05)。见表2。
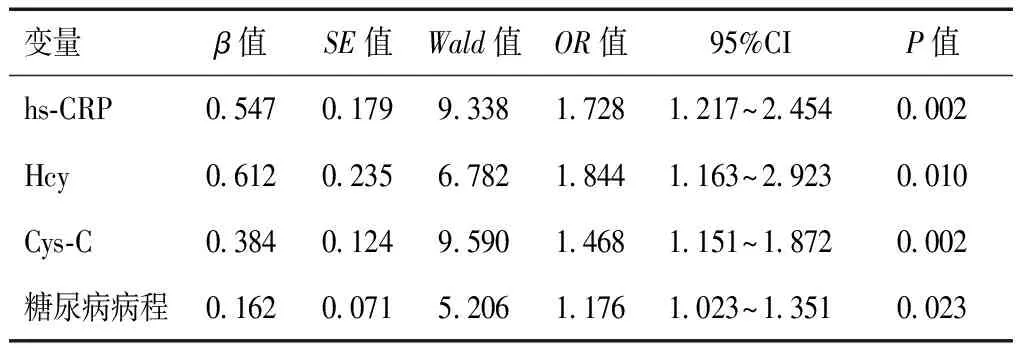
表2 DPN影响因素的Logistic回归分析
2.3 hs-CRP、Hcy、Cys-C与DPN严重程度的相关性
不同病程DPN患者之间血清hs-CRP、Hcy、Cys-C水平比较,差异有统计学意义(P>0.05);随着病情程度加重,血清hs-CRP、Hcy、Cys-C水平逐渐增高。见表3。
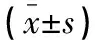
表3 hs-CRP、Hcy、Cys-C与DPN严重程度的相关性
3 讨论
DPN诱因包括代谢紊乱、炎症反应、氧化应激、血管损伤、微循环障碍等[11]。T2DM患者处于长期高血糖状态,致使微血管壁重构,诱发透明性病变,血管壁增厚,导致管腔狭窄,微循环障碍,进而神经纤维缺血缺氧,引发DPN[12]。随着糖尿病病程进展,DPN的发生风险显著提高[13],因此T2DM患者DPN病变的早期诊断以及尽早干预对改善患者生活质量和预后至关重要。
DPN的发生机制尚未完全阐明,既往研究[14-16]表明,hs-CRP、Hcy、Cys-C可能参与了T2DM的微血管病变过程。本研究发现,DPN组血清hs-CRP、Hcy、Cys-C水平高于T2DM组和对照组,且T2DM组血清hs-CRP、Hcy、Cys-C水平高于对照组;此外,Logisitic回归分析显示,hs-CRP、Hcy、Cys-C是DPN发生的独立危险因素,提示hs-CRP、Hcy、Cys-C可能在DPN的发病过程中发挥关键作用。炎症反应在T2DM及其并发症发生发展过程中的作用备受关注,hs-CRP是由白细胞介素-6诱导产生的血浆蛋白,可作为敏感的炎症标志物之一,能够通过激活核因子κB(NF-κB)通路诱导多种炎症介质的产生,调控细胞凋亡,促进DPN的发生[17]。魏微等[18]研究报道,hs-CRP等炎症因子与DPN发生密切相关,与本研究基本一致。另外,研究[19]表明,Hcy是T2DM微血管病变的危险因素。本研究也显示,Hcy与DPN密切相关,这可能是由于Hcy通过诱导氧化应激和直接细胞毒性作用等机制对血管内皮细胞造成损伤,譬如诱导微血管平滑肌细胞增殖,进而参与血管硬化、管腔狭窄等过程;Hcy可影响凝血功能,促进血栓形成,引发微循环障碍[20-21]。
Cys-C是一种半胱氨酸蛋白酶抑制剂,可作为肾功能的敏感标志物之一[22];并且血清Cys-C水平与T2DM慢性并发症相关[23],其表达增高与动脉粥样硬化紧密联系,能够通过炎症反应、血管重构等机制在糖尿病血管并发症的发病过程中发挥关键作用[24]。本研究显示,Cys-C可能参与了DPN的发病过程,其作用机制可能为:(1)Cys-C激活中性粒细胞,介导炎症反应,促使hs-CRP水平增高,引起血管内皮损伤[25];(2)Cys-C可抑制Hcy分解相关酶,使得Hcy水平增高[26],而高水平Hcy能够通过诱导氧化应激等诱导血管内皮损伤,导致神经损伤。本研究还发现,随着病情程度加重,DPN患者血清hs-CRP、Hcy、Cys-C水平逐渐增高,进一步表明hs-CRP、Hcy、Cys-C与DPN的发生发展密切相关。但本研究存在一定的局限性,首先样本量较小,其所得结论仍需大样本量研究进一步验证;其次,仅将hs-CRP、Hcy、Cys-C作为主要观察指标,关于其他细胞因子与DPN的相关性仍待探讨,为临床诊治提供更全面指导。
综上,血清hs-CRP、Hcy、Cys-C水平与DPN的发生发展紧密关联,可为病情评估及临床诊治提供参考依据。

