Bi3TaO7/MXene纳米片异质结的制备及光催化降解磺胺嘧啶钠
石 丹 黄章律 严素定 王 娟 王国宏
(湖北师范大学化学化工学院,污染物分析与资源化湖北省重点实验室,黄石 435002)
0 引言
近几十年来,由于代谢物排泄和工业废物的大量排放,人类和动物的生活环境不断恶化。因此,我们需要开发一种生态环境友好的方法,来有效地消除大多数不可生物降解的污染物[1-3]。在现有的各种技术中,半导体光催化技术作为一种理想的“绿色”策略,具有低能耗、无二次污染的特点,受到研究学者们的广泛关注[3-4]。二氧化钛(TiO2)是一种常见的能在紫外光照射下分解有机污染物的光催化剂[5]。然而,TiO2的实际应用受到其较宽禁带宽度(不能利用太阳光中的可见光部分)、电子-空穴对复合速率快的制约[6-7]。因此,有必要开发具有优良光催化活性的新型可见光驱动光催化剂[8-9]。近些年来,一些钽酸盐光催化剂(如 Bi3TaO7、AgTaO3和InTaO4),因其在可见光光催化降解有机污染物和光催化制氢方面具有优异的性能,引起了人们的广泛关注[10-12]。
Bi3TaO7作为一种潜在降解污染物的光催化剂,因其无毒、耐光性和特殊的结构引起了人们的研究兴趣[13]。具有萤石型结构的Bi3TaO7的禁带宽度约为2.95 eV,能吸收可见光并降解有机污染物[11-14]。然而,Bi3TaO7的光生电子-空穴对复合速率快,严重限制了其实际应用[11]。因此,我们需要寻求一种提高Bi3TaO7光催化性能的有效策略。通常,Bi3TaO7通过与其它半导体光催化剂复合形成异质结或通过贵金属修饰来提高Bi3TaO7光生电子-空穴对的分离效率,从而提高其光催化性能[11]。例如,Luo等采用简单的光还原法制备了一种新型Ag/Bi3TaO7光催化剂,负载1%Ag的Bi3TaO7对四环素(TC)的降解效率最高,达到85.42%,光催化活性的明显增强可能是Ag纳米粒子引起表面等离子共振的协同作用导致的[11]。而Wang等通过简单的超声法成功合成了Z型g-C3N4/Bi3TaO7复合光催化剂,构筑的Z型异质结能有效地快速分离光生电子-空穴对,负载20%g-C3N4的样品光催化降解环丙沙星(CIP)的效率分别是纯Bi3TaO7和g-C3N4的4倍和12.2倍[15]。
Mxenes是一类二维过渡金属碳化物和碳氮化物,通常是通过选择性刻蚀其母相MAX制备而成,由于其独特的特性,在光催化方面显示出巨大的潜力[16]。Ti3C2是一种已经得到大量研究的MXenes材料,其电导率为(4 600±1 100)S·cm-1,具有高度各向异性的载流子迁移率,有利于光生电子的捕获和转移[17-18]。此外,Ti3C2表面上的末端基团不仅提供了表面活性位点,而且还在助催化剂和光催化剂之间提供了致密的界面接触[19-20]。因此,将半导体光催化剂与Ti3C2耦合是加快光生电子-空穴对分离效率和提高光催化性能的有效方法。例如,Peng等制备的Cu/TiO2@Ti3C2Tx光催化剂有效改善了光生电子-空穴对的分离效率,表现出高效的光催化制氢性能[21]。此外,Cao等构建的2D/2D Ti3C2/Bi2WO6纳米片通过致密的界面接触有效改善了光生电子-空穴对的分离效率,同时显著增强了CO2还原能力[22]。
在本工作中,我们分别以五水合硝酸铋(Bi(NO3)3·5H2O)和五氯化钽(TaCl5)作为 Bi源和 Ta源,采用静电吸附和溶剂热法在2D Ti3C2的表面原位生长0D Bi3TaO7纳米颗粒制备Bi3TaO7/Ti3C2复合光催化材料,并通过在可见光下降解磺胺嘧啶钠(SD-Na)溶液来评价其光催化性能。实验结果表明,0D/2D Bi3TaO7/Ti3C2复合材料的光催化性能明显增强,并且具有良好的稳定性。在Bi3TaO7/Ti3C2复合光催化材料中,Ti3C2的存在有效抑制了Bi3TaO7光生电子-空穴对的复合,并且使复合物中的电导率增强,电子迁移速率加快。
1 实验部分
1.1 试 剂
氢氟酸(HF,AR)购于科密欧化学试剂有限公司,Ti3AlC2(325目,98%)购于上海卜汉化学技术有限公司,二甲亚砜(DMSO,AR)、氢氧化钾(KOH,AR)购于国药集团化学试剂有限公司,五水合硝酸铋(Bi(NO3)3·5H2O,AR)购于西陇化工股份有限公司,五氯化钽(TaCl5,AR)购于阿法埃莎(中国)化学有限公司,SD-Na购于上海国药集团试剂有限公司。实验用水为去离子水。
1.2 表征仪器
利用X射线衍射仪(XRD,Bruker D8 ADVANCE,Germany)测定样品的晶型,CuKα辐射(λ=0.154 06 nm),管电压40 kV,管电流40 mA,扫描范围2θ=10°~80°,扫描速率 5(°)·min-1;利用扫描电子显微镜(SEM,Gemini SEM 300,工作电压15 kV,德国)和场发射透射电子显微镜(FETEM,FEI Tecnai G2 F30,加速电压为50和300 kV)观察样品的形貌;利用原子力显微镜(AFM,MFP-3D)观察Ti3C2纳米片的微观结构和形貌;利用X射线光电子能谱仪(XPS,Thermo Scientific K-Alpha,美国)检测样品的化学元素组成;使用BaSO4作为参比,利用紫外可见光谱仪(UV-2550,中国)研究合成样品的光吸收特性;利用电化学工作站(CHI660E,中国)记录光催化剂的光电响应性能;利用高效液相色谱仪(HPLC,Agilent 1260,德国)测定SD-Na的浓度;利用稳态荧光光度计(F-4700,日本)和瞬态荧光光度计(Edinburgh,FLSP920,英国)分析样品的荧光性质。
1.3 样品制备
1.3.1 Ti3C2及其纳米片的制备
Ti3C2的制备:MXene材料的制备技术已经非常完善,根据Cao等的制备方法成功得到了“三明治”结构的Ti3C2和Ti3C2纳米片[21]。首先用塑料量筒量取20 mL HF溶液(含量不低于40.0%,浓度约为22.5 mol·L-1),再将其转移至聚四氟乙烯容器中,称取1 g Ti3AlC2固体粉末缓慢加入上述容器中,室温下缓慢搅拌72 h。待反应完成后,将悬浮液过滤得到黑色的固体,再用去离子水多次洗涤直至其pH≥6,然后在60℃真空干燥箱中干燥12 h,最后得到黑色样品,即层状Ti3C2。
Ti3C2纳米片的制备:首先,在室温下将上述得到的层状Ti3C2重新分散至20 mL DMSO溶液中,充分搅拌12 h。搅拌完成后,对悬浮液进行离心处理,用去离子水洗涤4~5次,以除去残留的DMSO溶液,最后在60℃真空干燥箱中干燥12 h。将干燥的固体样品按照与去离子水的质量比1∶100重新分散至去离子水中,在氮气气氛下对分散液进行超声处理。待超声分散4 h后,对其进行离心分离,设置转速3 500 r·min-1,离心分离1 h以达到除去未剥离块体Ti3C2。最终收集离心分离后的上层液,得到Ti3C2纳米片分散液,其浓度约为1.5 mg·mL-1。
1.3.2 Bi3TaO7/Ti3C2复合材料的制备
通过简单的溶剂热法制备Bi3TaO7/Ti3C2复合材料。首先,称取 0.728 g Bi(NO3)3·5H2O(1.5 mmol)固体溶于20 mL无水乙醇中,再向其中加入一定量的Ti3C2纳米片,搅拌1 h后得到均匀的悬浮液A。再称取0.179 g TaCl5(0.5 mmol)固体溶于20 mL无水乙醇中,搅拌1 h后同样得到均匀的悬浮液B。然后边搅拌边将A逐滴地加入到B中,再使用7 mol·L-1的KOH将以上混合液的pH值调至10。最后,在上述混合液搅拌1 h后,将其转移至聚四氟乙烯作内衬的反应釜中进行水热反应。设置水热反应温度为230℃,水热反应时间为24 h。水热反应完成后自然冷却到室温后再离心分离,用去离子水和乙醇交替洗涤3~4次,再将其放入60℃真空干燥箱中干燥12 h,最终得到Bi3TaO7/Ti3C2复合材料。通过控制Ti3C2的含量制备了一系列Bi3TaO7/Ti3C2,将Ti3C2与Bi3TaO7的质量比为0、0.01、0.02和0.05时所得样品分别标记为BT0、BT1、BT2和BT5。具体的制备流程如图1所示。
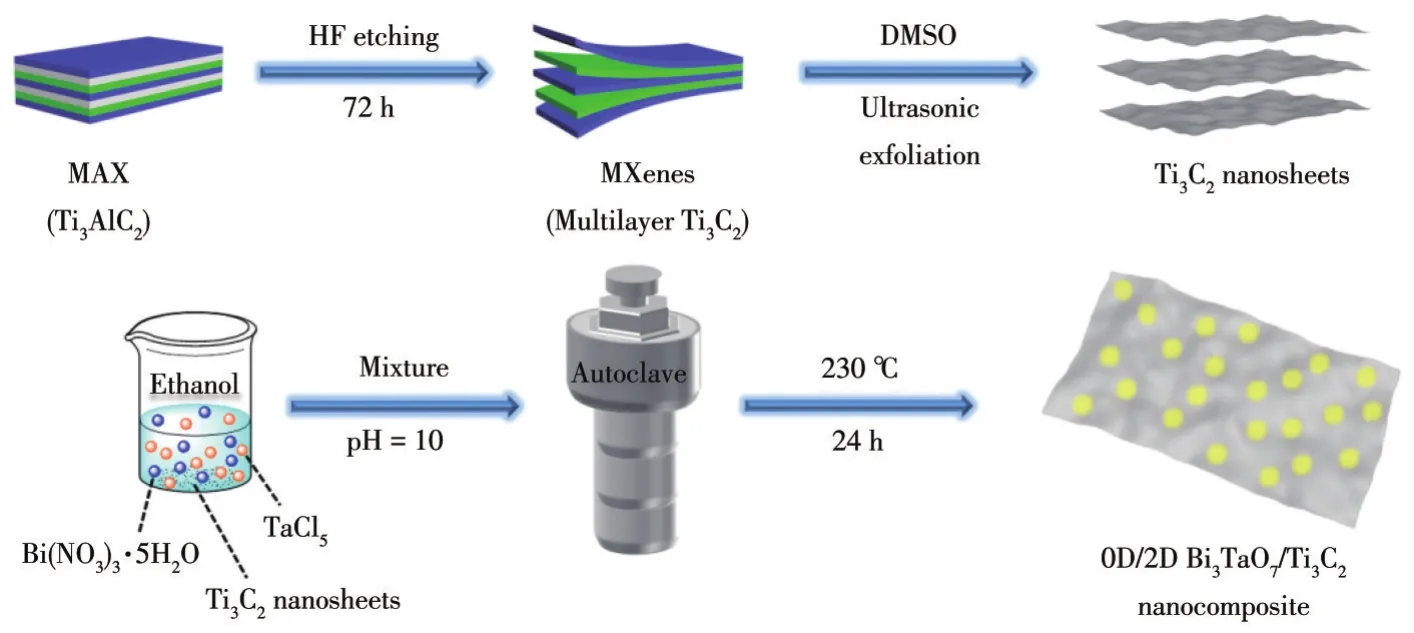
图1 Bi3TaO7/Ti3C2复合材料合成过程示意图Fig.1 Schematic illustration of the synthetic process of the Bi3TaO7/Ti3C2composites
1.4 光催化活性测试
通过对SD-Na在4个LED灯(波长λ=420 nm,每个灯的光强为0.4 W·cm-2)照射下进行Bi3TaO7/Ti3C2复合光催化剂的光催化降解测试。具体步骤如下:首先,准确称取一定量SD-Na固体溶于100 mL去离子水中,定容,得到5 mg·mL-1的SD-Na溶液。其次,取100 mL去离子水和200 μL SD-Na溶液于200 mL烧杯中混合均匀(此时SD-Na溶液浓度为10 mg·L-1),再向其中加入20 mg光催化剂。在光照射前,将悬浮液在黑暗中搅拌1 h,以保证光催化剂与SD-Na达到吸附-解吸平衡。在光催化过程中,分别间隔10、10、10、15、15、30、30 min移取1.5 mL悬浮液,再用0.22 μm过滤膜将其过滤后装入液相色谱瓶中。最后,采用高效液相色谱法测定SD-Na的浓度。光催化降解SD-Na的过程可以看作是一个准一级反应,其遵循动力学方程:ln(c0/c)=kt,其中c为SD-Na在不同光照时间时的浓度,c0为暗吸附平衡后溶液的浓度,k为表观速率常数,t为反应时间。
1.5 电化学测试
采用常规三电极系统,通过CHI660E电化学工作站记录光催化剂的光电响应性能。在电化学体系中,将光催化剂镀膜电极、Ag/AgCl电极和铂电极分别作为工作电极、参比电极和辅助电极。另外,采用0.5 mol·L-1的Na2SO4作为电解质溶液,并用420 nm的LED光源对样品照射,测试其光电流和电化学阻抗谱(EIS)。
1.6 活性基团超氧自由基(·O2-)和羟基自由基(·OH)的测定
以 5,5-二甲基-1-吡咯啉-氧化物(DMPO)作为·O2-和·OH的捕获剂,采用电子顺磁共振(ESR,Bruker A 300S)技术分别检测 DMPO-·O2-和DMPO-·OH配合物的信号。具体测试过程如下:将10 mg样品和40 μL DMPO溶于0.5 mL甲醇中,搅拌5 min,得到溶液C;将10 mg样品和40 μL DMPO溶解于0.5 mL去离子水中,搅拌5 min,得到溶液D。使用溶液C和D分别检测DMPO-·O2-和DMPO-·OH 的ESR信号。
2 结果与讨论
2.1 样品的微观结构和形貌分析
通过SEM对样品的形貌进行了表征。从图2a中前驱体MAX(Ti3AlC2)的SEM图可以明显看到,在HF蚀刻之前,Ti3AlC2呈现块状的结构。由图2b可知,HF刻蚀后MAX的层间产生了层间距,随着层间Al原子层的去除,原本的结构被破坏形成了疏松的“三明治”层状结构,呈现出典型的Ti3C2形貌。图2c为Ti3C2纳米片的SEM图,多层的Ti3C2经过超声剥离后得到Ti3C2纳米片,其独特的“三明治”层状结构消失,呈现出薄层结构,证明成功制得了Ti3C2纳米片。由图2d可知,纯Bi3TaO7颗粒主要是由不规则的小纳米粒子团聚形成,其颗粒平均尺寸为6 nm。

图2 (a)Ti3AlC2、(b)Ti3C2、(c)Ti3C2纳米片和(d)BT0的SEM图Fig.2 SEM images of(a)Ti3AlC2,(b)Ti3C2,(c)Ti3C2nanosheets,and(d)BT0
采用AFM观察Ti3C2纳米片的微观结构和形貌。图3a表明Ti3C2具有典型二维层状结构的超薄纳米片,同时也表明利用超声处理成功剥离了Ti3C“2三明治”层状结构。纳米片的厚度在1.89~2.71 nm(图3b),说明大约有4层Ti3C2[23]。
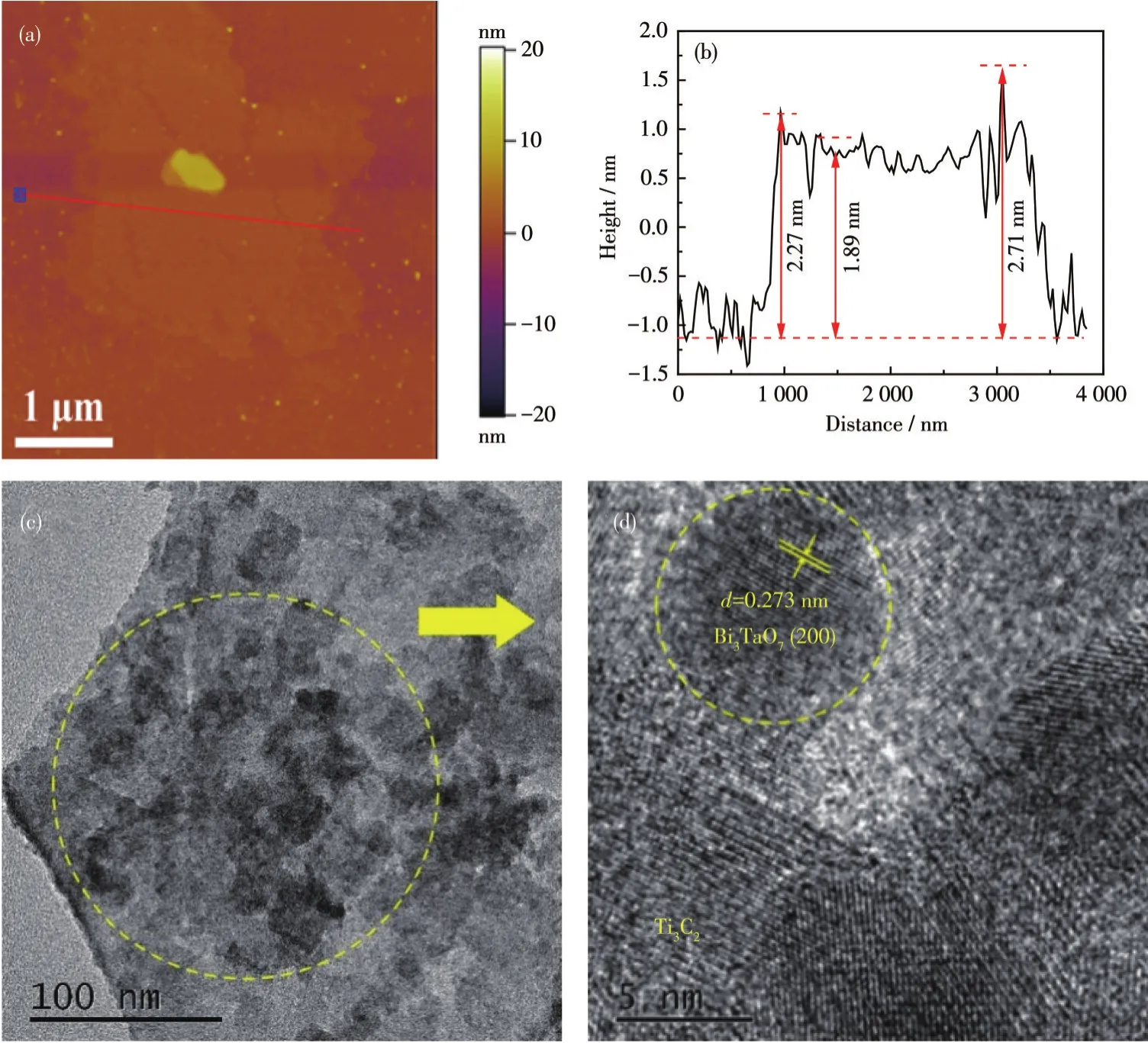
图3 Ti3C2纳米片的(a)AFM图和(b)高度剖面图;BT2的(c)TEM图和(d)HRTEM图Fig.3 (a)AFM image and(b)height cutaway view of Ti3C2nanosheets;(c)TEM image and(d)HRTEM image of BT2
通过TEM分析证明Bi3TaO7/Ti3C2异质结的形成。如图3c所示,Bi3TaO7颗粒均匀分散在透明的Ti3C2纳米片上[24-27]。图3d中BT2的高分辨TEM图(HRTEM)中晶格间距d=0.273 nm对应Bi3TaO7的(200)晶面[28]。这些结果都进一步证实了Bi3TaO7与Ti3C2之间具有致密的接触界面,也证明了成功制备出0D/2D的Bi3TaO7/Ti3C2异质结光催化剂。
2.2 样品的结构和光学性质分析
利用XRD分析测试了所合成样品的晶体结构。图4a为Bi3TaO7和Bi3TaO7/Ti3C2复合物的XRD图。BT0为纯Bi3TaO7,28.1°、32.7°、47.1°、55.8°和58.5°的衍射峰分别对应 Bi3TaO7的(111)、(200)、(220)、(311)和(222)晶面(PDF No.44-0202),说明 Bi3TaO7为立方相结构。值得注意的是,与BT0相比,所有Bi3TaO7/Ti3C2复合物峰中Bi3TaO7衍射峰的位置并没有变化,表明Ti3C2的加入并没有改变Bi3TaO7的晶体结构。进一步观察发现,随着Ti3C2加入量的增多,Bi3TaO7衍射峰强度逐渐降低,这是因为Ti3C2的加入抑制了Bi3TaO7晶粒的生长[29-30]。同时在图4a中未观察到明显的Ti3C2衍射峰,这可能是Ti3C2在Bi3TaO7/Ti3C2复合材料中含量较低,且分散均匀[22]。
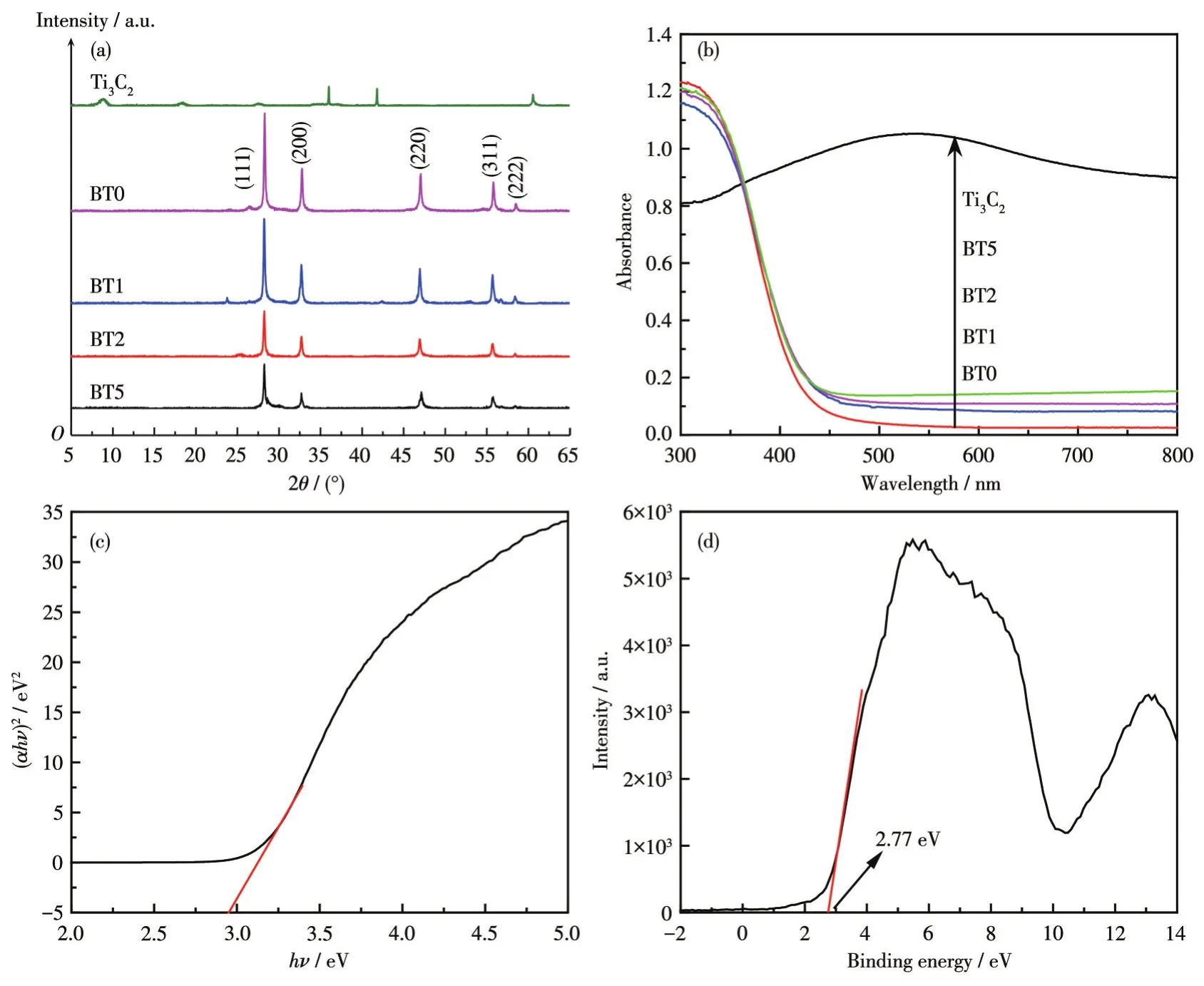
图4 (a)新制纯Ti3C2和Bi3TaO7/Ti3C2复合物的XRD图;(b)样品的UV-Vis DRS谱图;(c)Bi3TaO7的(αhν)2vs hν关系图;(d)Bi3TaO7的VB-XPS谱图Fig.4 (a)XRD patterns of as-prepared pure Ti3C2and Bi3TaO7/Ti3C2composites;(b)UV-Vis DRS spectra of all samples;(c)Plots of(αhν)2vs hν of Bi3TaO7;(d)VB-XPS spectra of Bi3TaO7
通过UV-Vis漫反射光谱(DRS)研究了所制备样品的光吸收特性。由图4b可以看出,纯Bi3TaO7的吸收边阈值大约是425 nm。同时,Ti3C2在300~800 nm范围内具有较强的吸收强度,这是Ti3C2的金属性质导致的[31]。在450~800 nm可见光区域内,随着Ti3C2纳米片含量的逐渐增加,复合物的吸收强度逐渐增加,这种现象可归因于Ti3C2的较强吸收能力。此外,半导体的禁带宽度可以由经验公式确定:

其中,α、h、ν、A和Eg分别代表吸收系数、普朗克常数、光子频率、常数和禁带宽度[32-33]。对于Bi3TaO7,n=4,再通过(αhν)2-hν曲线的切线截距可得到BT0的Eg=2.92 eV,如图4c所示。
为进一步探索光生电子-空穴对的激发、分离、转移和反应过程,阐明制备的光催化剂的能带结构[34],我们测定了Bi3TaO7的价带(VB)-XPS,如图4d所示。由图可知,Bi3TaO7的VB能量为2.77 eV。结合图4c所示的Eg值(2.92 eV),可以计算出Bi3TaO7的导带(CB)能量为-0.15 eV。
2.3 样品的化学组成分析
使用XPS可以很好地阐明所制备Bi3TaO7/Ti3C2复合光催化剂的化学元素价态。图5a是BT0、BT2和Ti3C2纳米片的全谱图,BT2中与Ti3C2和Bi3TaO7相关的所有元素(Bi、Ta、O、Ti和C)均存在。BT0、BT2和Ti3C2纳米片的高分辨C1s谱图如图5b所示。校准的C1s峰的结合能位于284.8 eV。BT0的C1s谱图中位于286.0 eV处的峰属于C—O键,其来自XPS仪器本身的污染碳水化合物[35]。BT2的C1s谱图中显示了2个典型的峰281.6和286.1 eV,分别归属于C—Ti和C—O键。Ti3C2纳米片的3个特征峰在281.8、286.3和 288.9 eV处,分别对应 C—Ti、C—O和C—F键。BT2中的C—Ti和C—O键的结合能相对Ti3C2纳米片都减少了0.2 eV。图5c为BT0和BT2的Bi4f高分辨XPS谱图。BT0的Bi4f5/2和Bi4f7/2分别位于165.0和159.7 eV,说明存在三价态的Bi,而BT2的Bi4f峰出现在更高的结合能处(165.2和159.9 eV)[36]。此外,BT0的Ta4f谱图中出现了位于26.6、28.5 和 29.8 eV的3个峰(图5d),分别对应Ta4f7/2、Ta4f5/2和 Ta4f5/2,同时也验证了 Ta是由 Ta5+组成[37-38]。与BT0相比,BT2的Ta4f7/2(26.8 eV)、Ta4f5/2(28.7 eV)和Ta4f5/2(30.0 eV)的结合能都增加了0.2 eV。通常,当电子密度减少时,电子的屏蔽效应会减弱,结合能会增加,而电子密度增加时,电子的屏蔽效应会增强,结合能会降低[39-40]。以上结果都揭示了在BT2中电子从Bi3TaO7转移到Ti3C2,同时在Ti3C2和Bi3TaO7之间形成了强的相互作用。
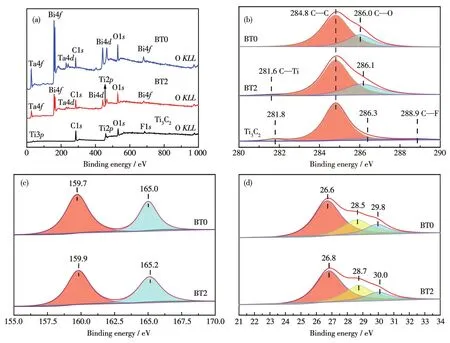
图5 BT0、BT2和Ti3C2纳米片的(a)全谱图和(b)C1s XPS谱图;BT0和BT2的(c)Bi4f和(d)Ta4f XPS谱图Fig.5 (a)Survey and(b)C1s XPS spectra of BT0,BT2,and Ti3C2nanosheets;(c)Bi4f and(d)Ta4f XPS spectra of BT0 and BT2
2.4 光催化性能测试
为了评价所制备Bi3TaO7/Ti3C2的光催化降解活性,在可见光照射下对典型的抗生素SD-Na溶液进行了光催化降解。如图6a所示,经过1 h的暗吸附后发现,BT0、BT1、BT2、BT5和Ti3C2对SD-Na几乎没有降解和吸附效果。此外,从没有光催化剂的空白对照可以看出,SD-Na的光分解作用可以忽略不计。图6b给出了不同样品对SD-Na的光催化降解率。由图6b中可知,在可见光光照2 h之后,BT0仅降解了40%的SD-Na,而Ti3C2对SD-Na没有光降解活性。与此同时,与BT0相比,所有Bi3TaO7/Ti3C2复合样品的光催化活性明显增强,BT1、BT2和BT5对SD-Na的降解率分别为70%、74%和58%。同时,使用Langmuir-Hinshelwood模型来考察SD-Na在不同样品上的光降解过程,如图6c所示。结果表明,光催化降解过程符合准一级动力学方程,BT0、BT1、BT2、BT5 相应的k值分别为 3.82×10-3、9.49×10-3、1.08×10-2和 7.17×10-3min-1(图6d)。值得注意的是,BT2展现出最高的光催化活性,其k值是BT0的2.8倍左右。Bi3TaO7光催化降解SD-Na性能的有效提高归因于Bi3TaO7/Ti3C2异质结的形成,同时具有以下优点:(1)Bi3TaO7CB上的光生电子可以通过Ti3C2和Bi3TaO7之间的界面进行有效转移,并在Ti3C2纳米片表面上积累,而在Bi3TaO7VB上留下光生空穴。(2)Ti3C2特殊的光热转换特性可以将Ti3C2纳米片表面上的光生电子与SD-Na溶液中O2分子反应生成超氧负离子(·O2-);同时,Bi3TaO7VB上光生空穴与水分子生成·OH。具有强氧化能力的·O2-和·OH共同促进光催化降解SD-Na反应[22]。

图6 (a)SD-Na在黑暗下的吸附性能;(b)可见光照射下所制备样品对SD-Na的光降解;(c)可见光照射下制备样品的SD-Na降解曲线的一级动力学;(d)所制备样品的反应速率常数;(e)在可见光照射下用BT2循环降解SD-Na;(f)循环4次后BT2降解前后的XRD图;(g)不同催化剂在可见光照射120 min后对SD-Na的TOC去除率Fig.6 (a)Absorption properties of SD-Na in the dark;(b)Photodegradation of SD-Na under visible light irradiation over as-prepared samples;(c)First-order kinetics of SD-Na degradation curves over as-prepared samples under visible light irradiation;(d)Reaction rate constants over as-prepared samples;(e)Cycling degradation of SD-Na with BT2 under visible light irradiation;(f)XRD patterns of BT2 before and after degradation for the four cycles;(g)TOC removal of SD-Na in the presence of various photocatalysts under visible light irradiation for 120 min
光催化剂的稳定性是影响其实际应用的重要因素。图6e为BT2对SD-Na的降解循环实验。在4个循环之后BT2光催化性能没有表现出明显的变化,表明其在降解SD-Na过程中具有很好的光催化稳定性。图6f为光催化降解后BT2的XRD图,由图可知,光催化反应前后BT2的XRD图没有明显的改变。由此可见,所制备的Bi3TaO7/Ti3C2复合材料具有显著的结构稳定性。
用TOC分析仪对光催化反应120 min前后的SD-Na溶液进行总有机碳(TOC)分析,TOC去除率如图6g所示。TOC去除率大小顺序为BT2(15.7%)>BT1(8.7%)>BT5(3.4%)>BT0(2.0%),与上述光催化剂降解效率的顺序是一致的(图6d)。
2.5 电化学、荧光和ESR测试
为了研究样品的电子转移能力,我们进行了EIS测试,相应的Nyquist谱图如图7a所示。通常,光催化剂的电荷转移阻力越小,其EIS曲线的半径就越小[41]。从图7a中可以清楚地看到BT2的半径比BT0的小,这说明BT2的电化学阻抗明显降低,同时表明Ti3C2的引入提高了光生电子-空穴对的转移和分离效率。另外,利用光电流实验研究了所制备样品电子-空穴对的分离效率,如图7b所示,发现BT2上的瞬态光电流明显高于BT0和Ti3C2,这也意味着BT2能更有效地分离光生电子-空穴对。此外,Ti3C2的光电流可以忽略不计(图7b),意味着Bi3TaO7/Ti3C2复合材料中光生电子是由Bi3TaO7产生的。Ti3C2是电子受体,将Bi3TaO7中光生电子有效转移到Ti3C2纳米片的表面,有效抑制了光生电子-空穴对的复合。
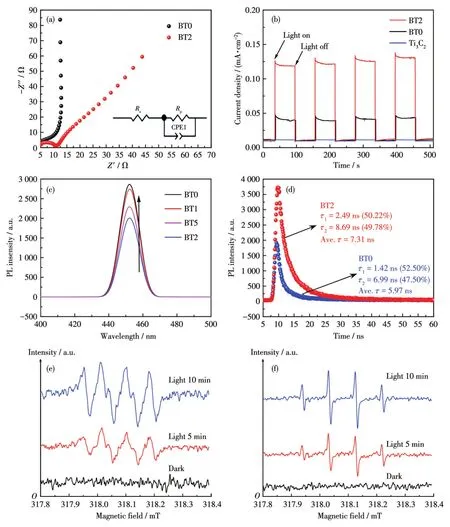
图7 (a)BT0和BT2的EIS谱图;(b)BT0、BT2和Ti3C2纳米片的光电流响应图;(c)BT0、BT1、BT2和BT5的PL谱图;(d)BT0和BT2的TRPL谱图;BT2在暗处和可见光照射5、10 min后(e)甲醇分散液中DMPO-·O2-和(f)水分散液中DMPO-·OH的ESR谱图Fig.7 (a)EIS spectra of BT0 and BT2;(b)Photocurrent response curves of BT0,BT2,and Ti3C2nanosheets;(c)PL spectra of BT0,BT1,BT2,and BT5;(d)TRPL spectra of BT0 and BT2;ESR spectra of BT2 under dark and under visible-light irradiation(5 and 10 min)for(e)DMPO-·O2-in methanol dispersion and(f)DMPO-·OH in aqueous dispersion
为了进一步解释Bi3TaO7/Ti3C2光催化降解性能提升的原因以及深入了解电荷转移动力学以及光生电子-空穴对的分离效率,利用光致发光(PL)和时间分辨光致发光(TRPL)谱对样品进行了分析。首先,利用PL谱研究了半导体光催化中的光生载流子的激发和转移,如图7c所示。由图可知,纯Bi3TaO7在450 nm处出现了较强的峰,这表明Bi3TaO7中电子-空穴对复合速率较快。当Bi3TaO7分散到Ti3C2纳米片表面形成界面紧密的异质结时,该发射峰强度明显下降,说明复合材料中Ti3C2的引入有效抑制了光生电子-空穴对的复合速率,这与光催化降解SD-Na的结果是一致的。进一步观察发现,BT2复合材料的PL强度最低,这也意味着BT2的光生载流子复合速率更低。与此同时,为了更好地探索光催化剂光生电子的分离过程,我们测试了纯Bi3TaO7和BT2的TRPL谱图,如图7d所示。通常,材料内部的电子被激发,在吸收光子后跃迁到激发态。当这些激发态电子返回到热平衡态时,多余的能量可以通过辐射和非辐射衰变过程释放出来[42-44]。由图7d可知,BT2(辐射跃迁寿命τ1=2.49 ns,非辐射跃迁寿命τ2=8.69 ns,平均寿命为 7.31 ns)比 BT0(τ1=1.42 ns,τ2=6.99 ns,平均寿命为5.97 ns)的荧光寿命明显延长,在Ti3C2的其他复合光催化剂如Ti3C2/g-C3N4[16]、Bi-VO4/Ti3C2[23]和Ti3C2/metal sulfide[31]中也报道了相似的结果。因此,BT2荧光寿命的延长进一步证实了Bi3TaO7中光生电子-空穴对的有效分离。
利用ESR技术确定了光催化反应体系中BT2上活性物质的存在,如图7e和7f所示[45-46]。在黑暗条件下,DMPO-·O2-复合物或者DMPO-·OH复合物都没有明显的信号。然而,当其暴露在可见光条件下时,可以明显地发现DMPO-·O2-和 DMPO-·OH 的特征峰,并且随着光照时间的增加,其特征峰的强度逐渐增加。这一结果表明,BT2复合材料在可见光照射下产生的·O2-和·OH是光催化降解过程中的主要活性物质。
2.6 光催化机理分析
基于上述实验结果,我们提出了Bi3TaO7/Ti3C2光催化剂降解SD-Na的可能机理(图8)。UV-Vis DRS结果表明,Bi3TaO7由于其适当的禁带宽度(2.92 eV),可以吸收可见光产生的光生电子-空穴对。在可见光照射下,Bi3TaO7的VB的电子被激发到CB,在Bi3TaO7的VB上留下光生空穴。由于Ti3C2纳米片是较好的电子受体,能快速将Bi3TaO7的CB上的光生电子转移到Ti3C2纳米片的表面,实现Bi3TaO7的光生电子-空穴对的有效分离。Bi3TaO7的CB电位(-0.15 V(vs NHE))比 O2/·O2-的电位(-0.046 V(vs NHE))更负,其光生电子被溶解在水中的O2捕获,产生·O2-。另外,Bi3TaO7的VB电位(2.77 V(vs NHE))高于H2O/·OH电位(2.69 V(vs NHE)),其光生空穴直接氧化水分子生成·OH。·O2-和·OH都是强氧化物质,可以将污染物SD-Na氧化为无毒无害的无机小分子。结合相关文献[11,47]和上述实验结果,Bi3TaO7/Ti3C2复合材料光催化降解SD-Na的过程可以描述如下:

图8 Bi3TaO7/Ti3C2光催化降解SD-Na的机理示意图Fig.8 Mechanism schematic diagram of photocatalytic degradation SD-Na of Bi3TaO7/Ti3C2
3 结论
通过溶剂热法制备了一种0D/2D Bi3TaO7/Ti3C2异质结复合材料,并将其应用于可见光光催化降解磺胺嘧啶钠水溶液。BT2表现出最佳的可见光光催化降解性能,其表观速率常数是纯Bi3TaO7的2.8倍左右。ESR实验表明,·O2-和·OH是光催化降解磺胺嘧啶钠的主要活性物质。与纯Bi3TaO7相比,Bi3TaO7/Ti3C2复合光催化剂光生电子-空穴对的分离能力得到明显增强。Ti3C2作为转移光生电子的助催化剂,有效分离了光生电子-空穴对,从而提高了Bi3TaO7/Ti3C2的光催化性能。这项工作为开发新型可见光响应的光催化剂提供了新思路。

