肾茶袋泡茶质量标准的提升研究
王 剑 杨文玉 普天彪 李晓花,2*
1.西双版纳版纳药业有限责任公司,云南 景洪 666100;2.滇西应用技术大学 傣医药学院,云南 景洪 666100
肾茶为唇形科植物Clerodendranthusspicatus(Thunb.)C. Y. Wu的全草,傣医应用历史悠久[1-2]。现代药理学和化学研究[3-4]显示:肾茶中含有黄酮、二萜、酚类、三萜类等化学成分,具有抗炎、抗菌、利尿、免疫调节、改善慢性肾功能衰竭等药理活性。肾茶袋泡茶(国药准字Z20026660)由云南西双版纳版纳药业有限责任公司生产,是将肾茶切段粉碎成粗粉,过筛,混匀,灭菌后低温干燥制得,具有清热解毒、利水通淋的功效,用于膀胱湿热所致的尿急、尿热、尿痛,非特异性下尿路感染见上述证候者[5]。
肾茶袋泡茶质量控制的文献报道较少,仅见王剑等[6]采用薄层色谱法对肾茶中熊果酸的含量进行了改进。肾茶袋泡茶现行质量标准WS-11108(ZD-1108)-2002中,包括薄层色谱的定性鉴别方法,采用HPLC法对熊果酸含量进行测定等方法[5]。根据文献报道,迷迭香酸(RA)是一种天然存在的羟基化合物,具有抗炎、抗氧化、抗抑郁、抗菌作用和抗病毒的活性[7-8],是肾茶主要有效成分之一,目前未见以肾茶袋泡茶中迷迭香酸作为含量测定指标的质量标准研究。本项目以肾茶袋泡茶的临床应用为基础,采用TLC法对肾茶袋泡茶进行定性鉴别,并建立肾茶袋泡茶中迷迭香酸的高效液相色谱法,以期使该制剂具备更好的质量可控性,使检测标准更加全面和完善,提高现行质量标准。

A.肾茶生药;B.肾茶药材;C.肾茶袋泡茶图1 肾茶图
1 仪器与材料
1.1 仪器 1260型高效液相色谱仪(美国Agilent公司);LC-2030型高效液相色谱仪(日本SHIMADZU公司);DFY-600D型粉碎机(温岭市林大机械有限公司);ZF-2三用紫外分析仪(上海安亭电子仪器厂);XMTD-701型薄层电动点样器(上海科哲生化科技有限公司)ZDHW型调温电热套(河北省黄骅市中兴仪器有限公司);MS-105DU型电子天平(梅特勒-托利多仪器(上海)有限公司);DK-98-Ⅱ型电热恒温水浴锅(天津泰斯特仪器有限公司);DFY-600型摇摆式高速万能粉碎机(温岭市林大机械有限公司);岛津InertSustain C18液相色谱柱;Agilent 5 TC-C18液相色谱柱。
1.2 药品与试剂 10批肾茶袋泡茶(西双版纳版纳药业有限责任公司,批号:160803、160805、170131、170901、170903、180610、180701、180704、180911、181004;规格:每袋装3 g);肾茶对照药材(中国药品生物制品检定所,批号:121326-200502);迷迭香酸对照品(中国食品药品检定研究院,批号:111871-201706;纯度:90.5%);硅胶G薄层色谱板(青岛谱科分离材料有限公司,批号:20200421);纯乙腈(Merk)和磷酸(J.T.Baker)为色谱纯;盐酸、乙酸乙酯、三氯甲烷、甲醇、甲酸等均为分析纯试剂,水为超纯水。
2 方法与结果
2.1 外观性状 原标准对肾茶袋泡茶的性状描述为“本品为袋泡茶,内容物为植物茎、叶混合粗粉;气微香,味微苦”,缺少色泽描述,笔者对样品进行观察后,将肾茶袋泡茶的外观性状描述修改为“本品为袋泡茶,内容物黄褐色至深褐色的粗粉及颗粒;气微香,味微苦”。
2.2 TLC鉴别[9-11]精密称取肾茶袋泡茶(批号:180701)粉末约1.0g,置于圆底烧瓶中,加入20倍量30%甲醇,回流提取60 min,滤过,滤液作为供试品溶液;另取迷迭香酸对照品,加30%甲醇超声处理5 min,摇匀,制成50 μg /mL对照品溶液;30%甲醇作为阴性对照。照薄层色谱法 (通则 0502) 试验, 吸取上述3种溶液各2 μL,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-异丙醇-甲酸(10∶2∶2∶0.5) 为展开剂展开,取出晾干,置紫外光灯 (365 nm) 下检视,供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点,阴性样品无干扰。结果表明不同批次肾茶袋泡茶中均含有迷迭香酸。TLC色谱图如图2所示。
2.3 迷迭香酸的含量测定[8,12-15]
2.3.1 溶液制备 精密称取肾茶袋泡茶(批号:180701)约1.0 g,置于圆底烧瓶中,加入20倍量30%甲醇,称定质量,回流提取60 min,放冷,再次称定质量,30%甲醇补足减失质量,摇匀,过滤,取续滤液,得到供试品溶液。取迷迭香酸对照品10.79 mg,置50 mL容量瓶中,加30%甲醇适量,超声处理5 min,加30%甲醇至刻度,摇匀,制成195.3 μg /mL对照品储备液。乙腈-0.1%磷酸水溶液(20∶80,V/V)为阴性对照溶液。

1.肾茶对照药材;2.迷迭香酸对照品;3.阴性对照(30%甲醇);4~13号样品
2.3.2 色谱条件 高效液相色谱仪:Agilent 1260和岛津LC-2030;检测器:紫外检测器;色谱柱:岛津InertSustain C18(250 mm×4.6 mm,5 μm)和Agilent 5 TC-C18(250 mm×4.6 mm,5 μm);流动相:乙腈-0.1%磷酸水溶液(20∶80,V/V);流速:1.0 mL/min;检测波长:330 nm;柱温:30 ℃;进样量:10 μL。
2.3.3 系统适用性及专属性试验 取阴性对照溶液(流动相)、对照品溶液和供试品溶液各适量,按照“2.3.2”项下色谱条件进样测定,结果显示:肾茶袋泡茶中迷迭香酸的保留时间约为21.9 min,与其余色谱峰的分离度均大于1.5,基线分离度良好,阴性对照溶液在供试品和对照品色谱峰相应位置无干扰色谱峰,本方法系统适用性及专属性良好。色谱图如图3所示。
2.3.4 线性关系考察 精密量取对照品储备液 0.5 mL、1 mL、2 mL、4 mL、6 mL、8 mL、10 mL,置25 mL容量瓶中,加30%甲醇稀释至刻度,摇匀。分别取上述制备的对照溶液10 μL注入液相色谱中,按“2.3.2”项下色谱条件进行检测,测定峰面积,以进样量(μg)横坐标,峰面积为纵坐标,绘制标准曲线。线形方程为Y=28988.0569967X+3434.4871968(r=0.9999)。迷迭香酸在3.906~78.12μg范围内线性符合要求。结果如图4所示。
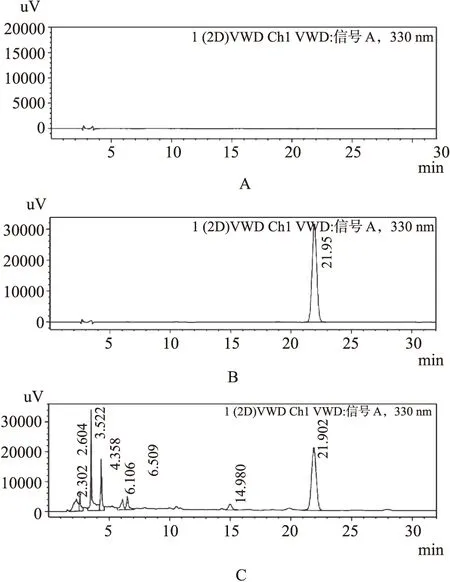
A. 阴性对照;B. 对照品;C.样品
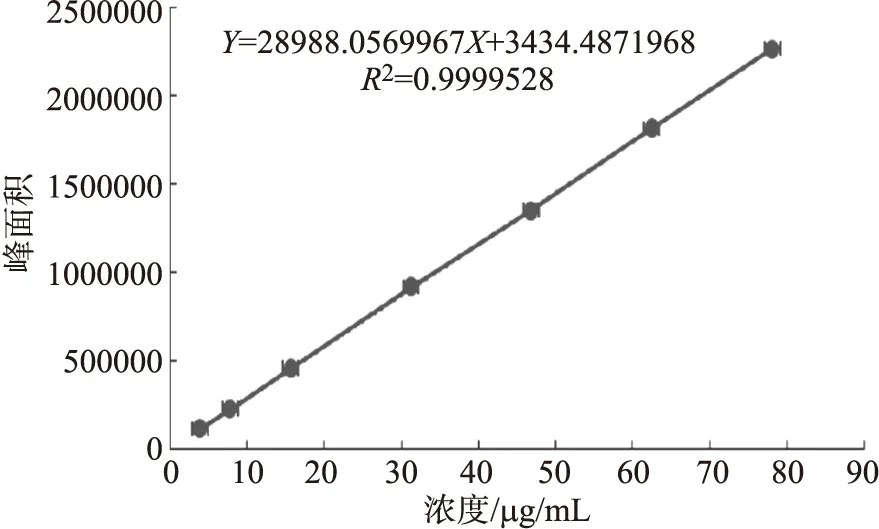
图4 迷迭香酸线性曲线图
2.3.5 中间精密度试验 精密称取同一批的肾茶袋泡茶(批号180701),采用Agilent1260高效液相色谱仪和岛津LC-2030高效液相色谱仪,按“2.3.2”项下方法试验,试验结果表明,两个型号高效液相色谱仪,两个不同操作人员检测结果分别为3.70mg和3.79mg,RSD分别为1.56%和1.45%,表明该方法中间精密度良好,结果符合要求。
2.3.6 重复性试验 分别称取肾茶袋泡茶(批号:180701),按照“2.3.1”项下制备方法获得6个供试品,按“2.3.2”项下检测方法测定迷迭香酸峰面积,计算质量分数,测定结果RSD为1.59%,重复性符合要求。
2.3.7 加样回收试验 取已知含量的供试品(批号:180701)9份,随机分为3组,分别加入含有401.2 μg/mL的迷迭香酸对照品溶液4 mL、5 mL和7 mL后,加30%甲醇补充至20 mL,精密称定,按“2.3.1”项下样品溶液制备方法进行提取,按“2.3.2”项下检测方法进行含量测定,结果表明:本法回收率在98.07%~101.45%之间。平均回收率为99.47%。结果符合要求。结果见表1。
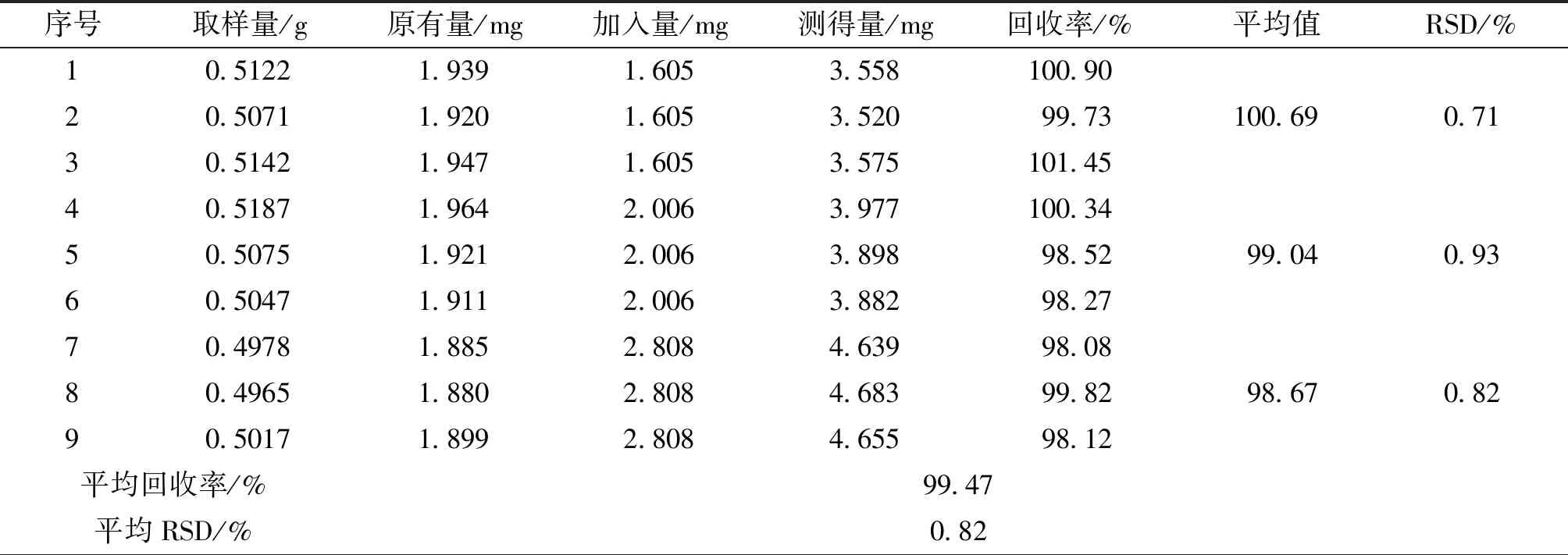
表1 迷迭香酸回收率试验
2.3.8 检测限与定量限考察 检测限和信噪比以3倍和10倍噪声水平所相当的待测物质的量计算,按照“2.3.2”项下迷迭香酸的检测方法对对照品溶液进样检测,结果迷迭香酸的检测限为195.3 ng /mL,定量限为664.02 ng /mL。
2.3.9 稳定性试验 取肾茶袋泡茶(批号:180701)样品3份,按“2.3.1”项下方法制备供试品溶液,与对照品溶液分别于0、3、6、9、12、18、24 h测定,每个样品3个重复,考察溶液稳定性,结果显示:RSD为0.57%,表明样品溶液在24 h内稳定。
2.3.10 耐用性试验 取三份样品,按“2.3.1”项下方法进行样品制备,选用Agilent 5 TC-C18色谱柱和岛津InertSustain C18色谱柱,按“2.3.2”项下方法测定含量,比较不同厂家同型色谱柱对测定结果的影响。结果显示,用岛津InertSustain C18色谱柱和Agilent 5 TC-C18色谱柱所测的样品含量均为3.55 mg/g,RSD分别为0.81%和0.96%,两种品牌的色谱柱对迷迭香酸的含量测定结果无显著影响,本方法耐用性良好。
2.3.11 样品含量测定 按“2.3.2”项下检测方法测定10批肾茶袋泡茶,迷迭香酸含量在8.13~11.54 mg/袋之间。平均含量为9.05 mg/袋。

表2 10批次肾茶袋泡茶迷迭香酸含量测定结果 (n=2)

续表2 表2 10批次肾茶袋泡茶迷迭香酸含量测定结果
3 讨论
3.1 供试品溶液制备方法的选择 在薄层鉴定和含量测定试验中,笔者分别考察了不同提取方法(超声提取、回流提取)、不同提取溶剂(10%、30%、50%、70%和100%甲醇-水)、不同液料比(10、20、30、40、50倍50%甲醇)、不同提取时长(0.5 h、1 h、1.5 h和2 h)对肾茶袋泡茶中迷迭香酸提取率的影响,并通过正交试验进行了提取工艺优化。结果显示,采用20倍30%甲醇,回流提取60 min,为肾茶袋泡茶中迷迭香酸的的最佳提取工艺。
3.2 质量标准性状描述的改进 将原标准中肾茶袋泡茶的性状“本品为袋泡茶,内容物为植物茎、叶混合粗粉;气微香,味微苦”改为“本品为袋泡茶,内容物黄褐色至深褐色的粗粉及颗粒;气微香,味微苦”,增加了色泽描述,使肾茶袋泡茶的性状特征更完善。
3.3 质量标准中TLC鉴别项的改进 以甲苯-乙酸乙酯-甲酸(9∶4∶1)、正己烷-乙酸乙酯-甲酸 (3∶10∶0.2)、甲苯-乙酸乙酯-甲酸 -水(5∶4∶0.5∶0.5)、甲苯-三氯甲烷-乙酸乙酯-甲醇-甲酸 (2∶3∶4∶0.5∶2)、环己烷-乙酸乙酯-异丙醇-甲酸(10∶2∶2∶0.5),对展开剂进行了筛选,结果显示:展开剂为环己烷-乙酸乙酯-异丙醇-甲酸系统时,TLC图谱中斑点清晰,分离度好。在方法学研究中,分别考察了温度、湿度及不同厂家薄层板对迷迭香酸展开情况的影响,结果显示,色谱斑点与分离度均符合要求,耐用性良好,确定环己烷-乙酸乙酯-异丙醇-甲酸(10∶2∶2∶0.5)为肾茶袋泡茶的TLC鉴别条件。
3.4 HPLC含量测定方法的考察
3.4.1 流动相的选择 通过查阅相关文献资料,笔者主要考察了乙腈-0.1%乙酸(18∶82),乙腈-0.1%乙酸(20∶80)和乙腈-0.1%乙酸(22∶78)等3种流动相对迷迭香酸出峰时间、峰形及样品峰的影响。结果显示,乙腈-0.1%磷酸溶液(20∶80)为流动相,迷迭香酸的出峰时间为21.9 min左右、峰形呈正态分布、分离度好、样品峰的纯度最优。
3.4.2 流速的选择 比较0.8 mL/min、1.0 mL/min和1.2 mL/min下对迷迭香酸出峰时间、峰形等的影响。结果所示,流速为1.0 mL/min时,样品中迷迭香酸的保留时间为21.9 min左右,与其他杂锋分离度较好;流速越低,保留时间越长,流速快则影响迷迭香酸的分离度。综合以上因素,选择流动相的流速为1.0 mL/min。
3.4.3 柱温的选择 比较28 ℃、30 ℃和32 ℃ 3种柱温条件对样品中迷迭香酸含量测定结果的影响。结果显示,不同温度条件下所测的样品含量范围为3.81~3.94 mg/g,RSD为1.18%,符合要求,综合考虑操作条件的可控性,选择检测柱温为30 ℃。
3.4.4 检测波长的选择 色谱图和光谱图的检测结果显示,迷迭香酸在328 nm、330 nm和332 nm处均有吸收,检测结果的RSD为0.76%,符合要求。当检测波长为330 nm时,色谱图基线更平稳、色谱峰分离度更好,灵敏度更高,因此确定检测波长为330 nm。
3.5 含量限度的拟定 肾茶袋泡茶现行质量标准WS-11108(ZD-1108)-2002中,每袋肾茶以熊果酸(C30H48O3)计,含量不得少于2.4 mg。为了使肾茶袋泡茶质量标准更能与临床应用相结合,本试验采用HPLC法建立了肾茶袋泡茶中迷迭香酸的检测方法。根据肾茶袋泡茶的处方(肾茶3000 g)和制法(切段,粉碎成粗粉,过筛,混匀,灭菌后低温干燥,分装,制成袋泡茶1000袋,即得),本研究对10批肾茶袋泡茶进行检测,迷迭香酸含量范围为8.13~11.54 mg/袋。平均含量为9.05 mg/袋,根据10批产品的含量测定结果及《中国药典》2015版四部通则9000制定原则9101药品质量标准分析方法验证指导原则七“原料药和制剂含量测定,范围一般为测定浓度的80%~120%”,以及公司对肾茶袋泡茶含量控制要求,暂定本品含量为平均含量的80%,即本品每袋含肾茶以迷迭香酸(C18H16O8)计,不得少于7.2 mg。
综上,笔者在肾茶袋泡茶原有质量标准基础上修订了性状描述,改进了TLC检测条件,并采用HPLC法测定了迷迭香酸的含量,方法简便可行,准确性、重复性高,能够有效地提高肾茶袋泡茶的质量控制标准,为该制剂的临床应用提供依据。

