贝那普利联合酒石酸美托洛尔对老年高血压合并心力衰竭患者血压控制及心室重塑的影响
陈 伟 撒翠翠
山东省龙口市第二人民医院药剂科,山东龙口 265700
高血压多发于老年人群,是导致心力衰竭、脑卒中等心脑血管疾病发生的重要危险因素[1]。近年来,受生活饮食习惯改变、 老龄化进程加快等多种因素影响,高血压合并心力衰竭的发生率明显增加。 研究显示,持续性高血压状态会引起左心室负荷增加,导致舒张性心力衰竭,并随着心脏射血功能不断减退而出现收缩性心力衰竭,严重威胁患者生命安全,有效控制血压在改善老年高血压合并心力衰竭患者预后方面的意义重大[2-3]。 目前,临床多采用药物控制血压水平,贝那普利是临床常用药物,能够抑制神经系统血管紧张素分泌,降低血管阻力,具有降压、恢复心肌供血之效[4]。 但老年高血压合并心力衰竭患者的病情复杂,单一用药降压效果不够平稳,临床应用受限。倍他乐克又名美托洛尔,属β 受体阻滞剂,在心血管疾病治疗中广泛应用[5]。鉴于此,本研究选取龙口市第二人民医院收治的84 例老年高血压合并心力衰竭患者作为研究对象,探讨贝那普利联合酒石酸美托洛尔在老年高血压合并心力衰竭患者中的应用效果。
1 资料与方法
1.1 一般资料
选取2019年1月至2021年1月龙口市第二人民医院收治的84 例老年高血压合并心力衰竭患者作为研究对象,按照随机数字表法将其分为对照组(42例)和研究组(42 例)。 对照组中,男27 例,女15 例;年龄63~74 岁,平均(68.23±3.19)岁;美国纽约心脏病协会(American Heart Association of New York,NYHA)分级:Ⅱ级17 例,Ⅲ级19 例,Ⅳ级6 例。 研究组中,男25 例,女17 例;年龄62~73 岁,平均(67.98±3.16)岁;NYHA 分级:Ⅱ级16 例,Ⅲ级21 例,Ⅳ级5 例。 两组患者的一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经龙口市第二人民医院医学伦理委员会审核及同意,患者均知晓本研究情况并签署知情同意书。
纳入标准:①患者均符合《老年高血压的诊断与治疗中国专家共识(2017 版)》[6]中高血压诊断标准,以及《中国心力衰竭诊断和治疗指南2018》[7]中心力衰竭诊断标准;②患者均可正常沟通、交流。 排除标准:①对贝那普利和酒石酸美托洛尔过敏者;②既往有内分泌系统疾病史、药物滥用史者;③孕妇;④合并糖尿病者。
1.2 方法
所有患者入院后均予以常规检查,要求低盐低脂类饮食,并予以利尿剂、强心剂等控制病情。
对照组采用贝那普利(上海新亚药业闵行有限公司,国药准字H20044840,生产批号:20181203,规格:10 mg/片)口服治疗,起始剂量10 mg/次,1 次/d,若降压效果不明显,可增加至20 mg/d,并根据血压波动调整剂量,一般每隔7~14 d 调整1 次,最高剂量不超过40 mg/d。 在此基础上, 研究组采用酒石酸美托洛尔(商品名:倍他乐克,阿斯利康制药有限公司,国药准字H32025391,生产批号:20181120,规格:25 mg/片)口服治疗,起始剂量6.25 mg/次,2 次/d,连续用药14 d 后若无不良反应,可根据病情恢复情况,逐渐加大服药剂量,最大剂量至12.5 mg/次,2 次/d。
两组患者均持续用药6 个月。
1.3 观察指标及评价标准
比较两组患者治疗前、治疗6 个月后的血压控制及心室重塑情况、心功能、半乳糖凝集素-3(galectin-3,Gal-3)、 微量白蛋白尿(microalbunminuria,MAU),并记录不良反应发生情况。 ①血压控制:使用U80AH型电子血压计(上海海尔医疗科技有限公司)测定两组患者的舒张压(diastolic blood pressure,DBP)、收缩压(systolic blood pressure,SBP)。 ②心室重塑情况:使用DT-578 型彩色多普勒超声仪 (上海聚慕医疗器械有限公司)测定两组患者的左室后壁厚度(left ventricular posterior wall thickness,LVPWT)、左室心肌重量指数(left ventricular mass index,LVMI)、舒张末期室间隔(interventricular septal thickness,IVST)。 ③心功能:采用DW-T8 型心脏彩超机(江苏大为医疗有限公司)测定两组患者的左室射血分数(left ventricular ejection fractions,LVEF)、左室舒张期内径(left ventricular end-diastolic diameter,LVEDD)、 左室收缩期内径 (left ventricular end-systolic dimension,LVESD)。④Gal-3、MAU 水平: 抽取患者静脉血3 ml, 转速为2000 r/min,离心时间为3 min,离心半径为15 cm,分离血清,Gal-3 用酶联免疫法测定,MAU 用免疫比浊法测定。 ⑤不良反应,包括头痛、恶心、腹痛等情况。
1.4 统计学方法
采用SPSS 20.0 统计学软件进行数据分析, 符合正态分布的计量资料用均数±标准差(±s)表示,两组间比较采用独立样本t 检验,组内比较采用配对样本t 检验;计数资料采用率表示,组间比较采用χ2检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者治疗前后血压及心室重塑情况的比较
治疗前,两组患者的DBP、SBP、LVPWT、LVMI、IVST 比较,差异无统计学意义(P>0.05);治疗后,两组患者的DBP、SBP、LVPWT、IVST 低于治疗前,LVMI高于治疗前, 且研究组患者的DBP、SBP、LVPWT、IVST 低于对照组,LVMI 高于对照组, 差异有统计学意义(P<0.05)(表1)。
表1 两组患者治疗前后血压及心室重塑情况的比较(±s)

表1 两组患者治疗前后血压及心室重塑情况的比较(±s)
注 DBP:舒张压;SBP:收缩压;LVPWT:左室后壁厚度;LVMI:左室心肌重量指数;IVST:舒张末期室间隔;1 mmHg=0.133 kPa
组别 DBP(mmHg) SBP(mmHg) LVPWT(mm) LVMI(g/m2) IVST(mm)对照组(n=42)治疗前治疗后t 值P 值研究组(n=42)治疗前治疗后t 值P 值91.35±8.42 85.59±7.30 3.350 0.001 146.23±11.20 129.81±10.13 7.047<0.001 10.12±1.64 8.69±0.35 5.526<0.001 93.32±7.58 102.41±3.45 7.034<0.001 10.82±2.13 8.79±0.85 5.737<0.001 t 治疗前组间比较值P 治疗前组间比较值t 治疗后组间比较值P 治疗后组间比较值92.01±9.26 71.75±6.54 11.582<0.001 0.342 0.733 9.151<0.001 147.18±11.59 108.52±9.43 16.768<0.001 0.382 0.704 9.969<0.001 10.14±1.66 8.07±0.38 7.878<0.001 0.056 0.956 7.778<0.001 92.28±8.10 108.96±4.18 11.860<0.001 0.608 0.545 7.832<0.001 10.83±1.96 8.11±0.57 8.636<0.001 0.022 0.982 4.306<0.001
2.2 两组患者治疗前后心功能及Gal-3、MAU 水平的比较
治疗前,两组患者的LVEF、LVEDD、LVESD、Gal-3、MAU 比较,差异无统计学意义(P>0.05);治疗后,两组患者的LVEDD、LVESD、Gal-3、MAU 低于治疗前,LVEF 高于治疗前, 且研究组患者的LVEDD、LVESD、Gal-3、MAU 低于对照组,LVEF 高于对照组,差异有统计学意义(P<0.05)(表2)。
表2 两组患者治疗前后心功能及Gal-3、MAU 水平的比较(±s)
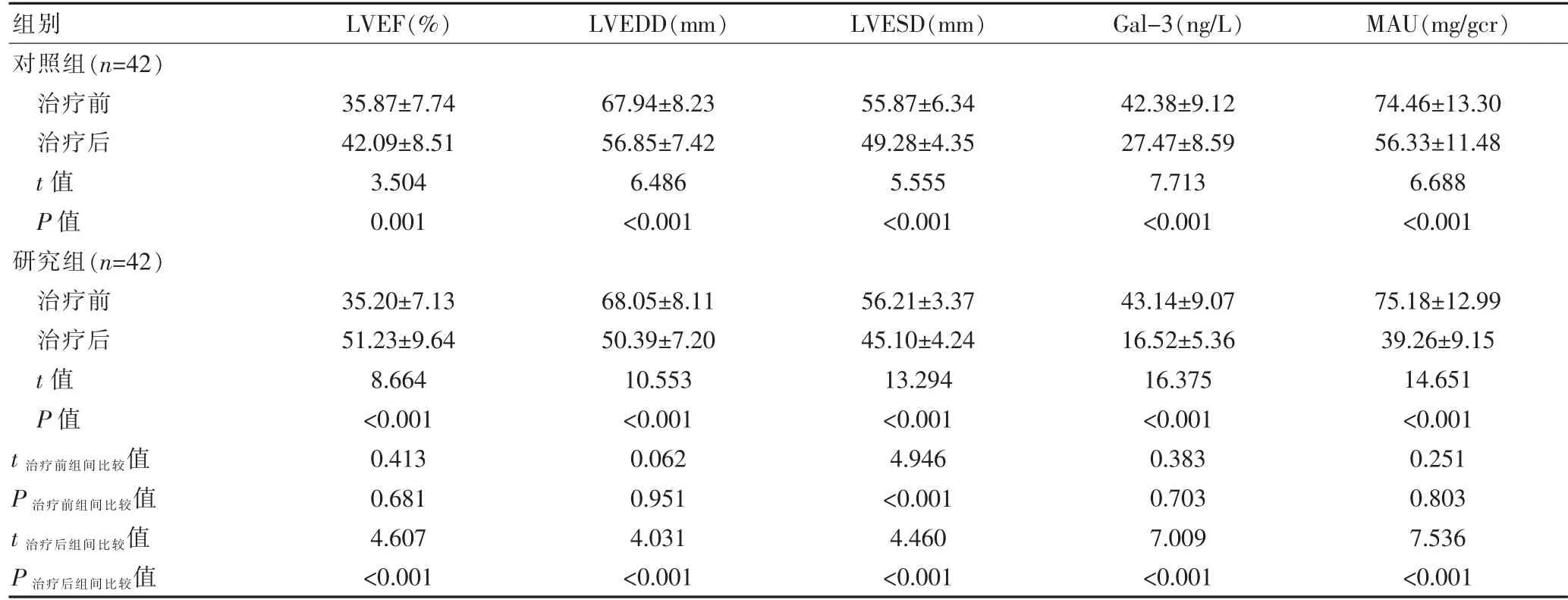
表2 两组患者治疗前后心功能及Gal-3、MAU 水平的比较(±s)
注 LVEF:左室射血分数;LVEDD:左室舒张期内径;LVESD:左室收缩期内径;Gal-3:半乳糖凝集素-3;MAU:半乳糖凝集素-3
组别 LVEF(%) LVEDD(mm) LVESD(mm) Gal-3(ng/L) MAU(mg/gcr)对照组(n=42)治疗前治疗后t 值P 值研究组(n=42)治疗前治疗后t 值P 值35.87±7.74 42.09±8.51 3.504 0.001 67.94±8.23 56.85±7.42 6.486<0.001 55.87±6.34 49.28±4.35 5.555<0.001 42.38±9.12 27.47±8.59 7.713<0.001 74.46±13.30 56.33±11.48 6.688<0.001 t 治疗前组间比较值P 治疗前组间比较值t 治疗后组间比较值P 治疗后组间比较值35.20±7.13 51.23±9.64 8.664<0.001 0.413 0.681 4.607<0.001 68.05±8.11 50.39±7.20 10.553<0.001 0.062 0.951 4.031<0.001 56.21±3.37 45.10±4.24 13.294<0.001 4.946<0.001 4.460<0.001 43.14±9.07 16.52±5.36 16.375<0.001 0.383 0.703 7.009<0.001 75.18±12.99 39.26±9.15 14.651<0.001 0.251 0.803 7.536<0.001
2.3 两组患者不良反应发生情况的比较
研究组患者的不良反应总发生率为9.52%(4/42),具体包括头痛2 例,恶心1 例,腹痛1 例;对照组患者的不良反应总发生率为4.76%(2/42), 包括头痛1 例,腹痛1 例。 两组患者的不良反应总发生率比较,差异无统计学意义(χ2=0.180,P=0.672)。
3 讨论
高血压是一种以体循环动脉压增高为主要症状的综合征,可引起心、肾、脑多器官损害[8]。研究发现,高血压合并心力衰竭的发病机制较为复杂,与血流动力学异常、心肌间质纤维化、心肌细胞肥大等因素相关[9]。老年高血压合并心力衰竭患者由于机体长期受高血压、炎症侵袭,易出现心室重构,导致心功能进一步损害。 LVPWT、LVMI、IVST 与心室肥厚联系密切,能够充分反映患者心室重构情况[10-11]。
贝那普利是一种血管紧张素转化酶抑制药,主要通过抑制血管紧张素Ⅰ生成血管紧张素Ⅱ,发挥舒张血管、降低血管阻力的作用,还可增加血浆肾素、活肾素活性,起到降低血压、减轻心脏负担等作用,有利于改善患者心排血量[12-13]。 但临床为更稳定地控制血压水平,常选择联合用药。本研究结果显示,治疗前,两组患者的DBP、SBP、LVPWT、LVMI、IVST、LVEF、LVEDD、LVESD、Gal-3、MAU 比较,差异无统计学意义(P>0.05);治疗后,研究组患者的DBP、SBP、LVPWT、IVST、LVEDD、LVESD、Gal-3、MAU 低于对照组,LVMI、LVEF 高于对照组,差异有统计学意义(P<0.05);两组患者的不良反应总发生率比较,差异无统计学意义(P>0.05)。提示贝那普利联合酒石酸美托洛尔在老年高血压合并心力衰竭患者中具有较高的应用价值。 周全[14]研究指出,贝那普利和美托洛尔(倍他乐克)联合用于治疗老年高血压合并心力衰竭患者, 可有效改善其血压,下调Gal-3、MAU 水平,与本研究结果类似。原因在于酒石酸美托洛尔可通过选择性阻断β 受体,降低交感神经活动,减少血管阻力,以达到控制血压、减少心肌耗氧量的效果[15-16]。 酒石酸美托洛尔还能够提高心肌细胞β 受体敏感性,降低心脏负荷,改善左心室舒张功能,提升患者运动耐力,进而促进心功能恢复[17-18]。而酒石酸美托洛尔与贝那普利联合用药后,可发挥协同作用,可从阻断β 受体、抑制血管紧张素Ⅱ的生成等多个方面降低血压,有助于改善患者高血流动力状态,抵抗心室重塑,且效果优于单一用药。联合用药还能够有效调节Gal-3 水平,并通过抑制血管紧张素Ⅱ的生成,可有效减少肾上腺素的释放,降低肾小球内压,降低MAU 水平,有利于病情的控制,进而提高患者生存质量。 另外,临床用药时根据患者情况及医嘱严格控制、调整剂量,安全性较高,不会增加不良反应的发生。 然而本研究纳入样本量较少,可能造成试验结果出现偏差, 对此临床需进一步完善试验设计,扩大样本量以证实贝那普利联合酒石酸美托洛尔对老年高血压合并心力衰竭患者的具体影响。
综上所述,贝那普利联合酒石酸美托洛尔应用于老年高血压合并心力衰竭患者中效果良好,能够增强血压控制效果, 降低Gal-3、MAU 水平, 延缓心室重塑,改善患者心功能,安全可行。

