全血糖化血红蛋白、Lp(a)联合检测在糖尿病血管并发症诊治中的应用价值
杨曦
北京怀柔医院检验科,北京 101400
糖尿病的发病率仅次于脑血管疾病和肿瘤。据相关部门估计,2050 年糖尿病患病人数在全球范围内将超过3 亿[1]。结合我国最新的调查研究结果,我国的糖尿病患病人群超过3 000 万,且近几年发病概率不断攀升[2]。其中2 型糖尿病患者占比95%。长期的高血糖状态会损伤微血管与大血管,诱发严重的心、脑、肾、足并发症,降低了患者的生活质量,对患者的生命安全是极大的威胁。因此,糖尿病临床诊治的关键在于早发现、早确诊、早治疗。基于此,研究选取该院2021 年1—12 月86 例糖尿病血管并发症患者,对其临床资料进行回顾性分析,并选取同期86名健康体检者作为对照,以此研究全血糖化血红蛋白与血清脂蛋白联合检测在糖尿病血管并发症诊治中的作用,现报道如下。
1 资料与方法
1.1 一般资料
选取该院86 例糖尿病血管并发症确诊患者为观察组,男46 例,女40 例;年龄40~70 岁,平均(55.32±1.45)岁;病程2~10 年,平均(6.09±1.23)年;并发症包括:冠心病36 例、脑梗死20 例、颈动脉狭窄10 例。全部患者经临床确诊糖尿病且临床治疗完整。
选取同期86 名健康体检者为对照组,男44 名,女42 名;年龄41~70 岁,平均(55.67±1.12)岁。全部健康体检者均接受血液生化、彩色多普勒超声、头颅CT、眼底镜检查。
纳入标准:临床确诊2 型糖尿病且合并血液并发症者;知情同意该项研究者,临床资料完整者。
排除标准:靶器官病变或外周动脉疾病、颈动脉疾病、视网膜眼底病变者;意识不清者;对研究不予以支持者。
两组一般资料对比,差异无统计学意义(P>0.05)。具有可比性。该院研究经过医院医学伦理委员会批准。
1.2 方法
①标本处理:全部研究目标在空腹状态采集4~5 mL 静脉血。取1 mL 注入常规采血管(含混凝剂),混匀数次,以免血液凝固,以此测定GhbA1c。2~8℃环境下可保存全血标本7 d,室温15~30℃,可保存全血标本3 d。剩余静脉血注入不含抗凝剂的干燥试管,3 000 转离心10 min,取血清测定Lp(a),确保所有血液标本均无溶血、无脂血、无黄疸。所有测定项目操作均严格按照说明,确保检测结果准确可靠,重复性好。
②GhbA1c 测定:方法学采用亲和层析高压液相色谱法,试剂选用普莱默斯医疗器械(上海)有限公司生产,仪器选择美国普莱默斯Hb9210 血红蛋白测试系统,GhbA1c 分为四组:<6.0%、6.1%~8.0%、8.1%~9.9%、≥10%,阳性阈值为全血GhbA1c≥6.1%。
③Lp(a)测定:试剂选择中生北控生物科技股份有限公司生产,仪器选择贝克曼AU5800,使用免疫比浊法,将Lp(a)分为两组:<30 mg/dl、≥30 mg/dl,阳性阈值为≥30 mg/dl。
1.3 统计方法
采用SPSS 21.0 统计学软件处理数据,符合正态分布的计量资料用(±s)表示,采用t 检验;计数资料用[n(%)]表示,采用χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组检测者GhbA1c 检测结果比较
观察组全血GhbA1c 百分比高于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组检测者GhbA1c 检测结果比较

续表1
2.2 两组检测者Lp(a)检测结果比较
观察组Lp(a)浓度高于对照组,差异有统计学意义(P<0.05),见表2。
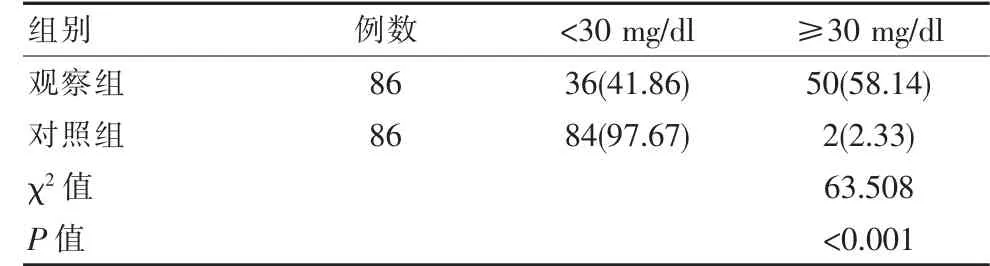
表2 两组检测者Lp(a)检测结果比较

续表2
3 讨论
2 型糖尿病患者更容易发生脂质代谢失调,原因在于:体内胰岛素分泌减少,导致血脂异常。长期高血糖可导致相关血管并发症和动脉粥样硬化。2型糖尿病血脂代谢异常的原因可能与胰岛素抵抗有关。胰岛素激活脂蛋白脂肪酶(LPL)活性,促进游离脂肪酸的增加,血脂中TC 含量也明显增加。血液中的葡萄糖含量过高,会加快结构蛋白糖基化。在糖化结构蛋白的反应影响下,形成进行性糖化终末产物(AGE)[3]。该产物溶解度很差,在各组织中形成巨分子,同时产生交联,可阻碍可溶性蛋白,减少蛋白分解,导致核酸功能与免疫性异常,增加血液组织毒性。同时,毛细血管基底膜中的胶原蛋白还有大量羟赖氨酸,羟赖氨酸可以促进糖类物质结合,增加血管基底膜中糖化胶原蛋白的合成量,从而引发强大的交联作用[4]。促进AGE 与糖化胶原蛋白深入交联,激活巨噬细胞,联合血管内皮细胞发生反应,减少低密度脂蛋白的清除,强化血小板粘附性,改变血管基底膜的形态,引发功能障碍,诱发视网膜血管异常、糖尿病肾病等微血管和小血管病变[5]。同时,糖化血红蛋白还会影响氧气携带能力,导致心血管病变、脑血管病变、外周血管病变等大血管病变,及糖尿病肾病、糖尿病视网膜病、糖尿病神经病变等微血管病变,大血管病变与微血管病变均为糖尿病血管并发症[6]。高糖状态下,合成大量的粘多糖,患者血液中粘多糖含量过多会使在主动脉与较小血管沉积大量的粘多糖,加之高脂蛋白血症,从而诱发动脉硬化疾病。早期2 型糖尿病具有隐匿性,不易被确诊,且血管并发症风险较大,严重降低了糖尿病患者的生活质量,且致残率、致死率较高。所以,相关领域一直致力研究糖尿病血管并发症。
人体血液中含有葡萄糖成分。葡萄糖与蛋白质可发生缓慢的、不可逆的非酶促反应,从而形成糖化蛋白。血糖浓度与高血糖存在时间均会影响合成的速率。血糖水平正常时,可糖化少量的蛋白,其中部分糖化后的蛋白由于降解作用而消失。但是长时间的高血糖状态会加大血液和组织蛋白糖化的比例,蛋白质降解之后才可将其释放,因此,在蛋白质整体的发生发展中均可持续[7]。通常情况下,糖化作用分为两个阶段,第一,葡萄糖分子上的酮基通血红蛋白分子上的胺基发生反应形成Schiff 碱或醛亚胺,该反应具有可逆性;第二,Amadori 将Schiff 碱重排,形成醛亚胺,该反应可逆。人体红细胞的血红蛋白由HbA、HbA2、HbF 组成,GHb 包括:HbAlb1、HbAib2、HbA1b3、HbA1c、HbA1d,其中核心在于HbA1c。结合国外相关前瞻性研究可知[8],高血糖状态可诱发心绞痛与心肌梗死,每增加1%HbA1c,危险性可增加11%。并且,HbA1c 每下降1%,与糖尿病相关的任何危险性将下降21%,与糖尿病相关的相关心肌梗死危险性下降14%。不仅如此,想要控制糖尿病并发症的发生、延缓糖尿病并发症的发展,必须严格控制HbA1c。结合相关学者的研究可知,与无病变组相比较,糖尿病视网膜病变合并肾病患者的HbA1c 与Lp(a)水平均显著更高,提示HbA1c 与Lp(a)与糖尿病微血管病变并发症之间存在紧密的联系[9]。结合文章研究结果,86 例糖尿病合并血管病发作患者中,51例HbA1c 水 平(HbAl ≥10.0%)显著升高,占59.30%;全血HbA1c 百分比水平(全血HbAl8.1%~9.9%)升高22 例,占比25.58%;全血HbA1c 百分比(全血HbA6.1%~8.0%)升高11 例,占12.79%;全血HbA1c 百分比水平低于阳性阈值2 例,占比2.33%。对这2 例患者进行了追踪调查,发现患者的血红蛋白指数为56 g/L,属于重度贫血,对其予以2 单位红细胞悬液输注治疗来纠正贫血,所以其全血HbA1百分比水平低于阳性阈值。86 名健康体检者中,其HbA1 百分比水平均低于阳性阈值,占比100.00%。结果显示,与健康体检人群相比较,糖尿病合并血管并发症患者的HbA1 百分比水平显著更高,文章研究结果与国内外相关研究结果一致[10]。
Lp(a)是从血液中分离出来的一种脂蛋白,具有特殊性,结构类似于LDL,带有富含碳水化合物,且具备高清水性的APO(a)蛋白。血清Lp(a)浓度受基因控制,与患者性别、年龄、体质量、适度体育锻炼、降胆固醇药物无关。结合相关研究可知,Lp(a)可与纤溶酶原、纤维蛋白以及细胞表面结合竞争,一致纤维蛋白的水解作用,由此可认定动脉粥样硬化血管疾病的独立危险因素之一为Lp(a)[11]。结合文章研究结果,86 例糖尿病合并血管并发症患者其Lp(a)含量均高于健康体检者,该项研究结果与国内外相关研究成果一致[12]。
糖尿病血管并发症患者的全糖化血红蛋白和血清脂蛋白水平高于健康人群。这提示,针对糖尿病血管并发症患者,需要同时检测其全糖化血红蛋白水平和血清脂蛋白水平,并积极采取控制措施,以实现糖尿病血管并发症的有效防治,为糖尿病血管并发症的诊断、治疗提供有力的依据。

