NaBH4/MClx体系对液体端羧基氟橡胶的还原及还原机理
常云飞, 廖明义, 温佳明
NaBH4/MCl体系对液体端羧基氟橡胶的还原及还原机理
常云飞, 廖明义, 温佳明
(大连海事大学交通运输工程学院, 大连 116026)
以液体端羧基氟橡胶(LTCFs)为原料, 硼氢化钠与金属氯化物(NaBH4/MCl)为还原体系, 采用一锅法成功将LTCFs还原为液体端羟基氟橡胶(LTHFs). 研究了多种稀土金属氯化物(LaCl3, CeCl3, NdCl3和SmCl3)和过渡金属氯化物(MnCl2, NiCl2, CoCl2和CuCl2)对LTCFs还原效果的影响及变化规律. 采用傅里叶变换红外光谱(FTIR)、 核磁共振氢谱(1H NMR)、 核磁共振氟谱(19F NMR)和化学滴定法对原料和产物的分子链结构和官能团含量进行了表征. 结果表明, 稀土金属MCl还原体系对LTCFs的还原效果均高于过渡金属MCl还原体系, LTCFs中的—C=C—和—COOH均可以被还原为—C—C—和—OH, 其中NaBH4/SmCl3还原体系还原效率最高, 达到92%. 机理研究表明, NaBH4/MCl对—COOH的还原性能与MCl中金属阳离子和羰基氧间的结合力有关, 结合力越大越有利于—COOH的还原.
液体端羧基氟橡胶; 金属氯化物; 硼氢化钠(NaBH4); 羧基; 还原机理
氟橡胶作为广泛使用的原材料, 其稳定的碳氟单键(C—F, 485 kJ/mol)以及氟原子对主链的屏蔽作用[1~3]使得氟橡胶比其它橡胶化学性质更稳定, 因此在化学工程、 机械及航空等[4~6]领域成为重要的基础有机材料. 液体氟橡胶是一种具有流动性的低分子量含氟聚合物, 不仅具有固态氟橡胶的耐燃烧、 耐油、 耐高温和抗氧化性等优异性能, 并且易于加工成型, 可以克服传统固体氟橡胶在挤出成型和模压中对形状与尺寸的限制, 因此受到越来越多的关注[7~9]. 液体氟橡胶主要通过聚合法和氧化降解法制备, 但通过氧化降解法制备的液体氟橡胶, 分子链中会引入—C=C—和—COOH等不饱和基团, 影响其耐热、 耐油和耐老化等性能, 因此, 需要进一步对—C=C—和—COOH进行还原改性.
众所周知, 羧基中的羰基由于与羟基氧原子上的未共用电子对共轭, 降低了羰基碳原子的亲电能力, 因此羧酸的化学性质稳定, 难与还原试剂发生还原反应[10], 通常还原效果不佳[11~14]. 为实现羧基的还原, 一般采用强还原剂或通过添加催化剂来提高还原剂的还原能力, 常用的还原试剂有氢化铝锂(LiAlH4)、 乙硼烷(B2H6)和硼氢化钠(NaBH4). 其中, LiAlH4还原能力强[15], 但选择性差、 化学性质活泼、 易燃易爆、 操作条件苛刻且价格较高, 不利于大规模应用. B2H6与LiAlH4相似, 也是一种强还原剂, 室温下即可将羧酸还原成醇[16], 但选择性差, 不适合用于还原含有碳氧不饱和键、 杂原子不饱和键、 羟基、 卤素和环烷烃基的化合物, 并且B2H6沸点低, 易燃易爆, 限制了其使用范围. NaBH4反应条件温和, 化学选择性强, 价格便宜, 性质稳定, 有利于安全生产, 因此成为广泛使用的一种有机还原试剂, 得到了越来越多的关注. NaBH4作为金属复氢化物, 具有四氢硼离子(BH4-)的复盐结构, 这种复合负离子具有亲核性, 可攻击极性不饱和键中带正电的碳原子, 发生负离子转移而进行还原. 与LiAlH4和B2H6相比, NaBH4还原能力中等, 一般不能用来直接还原羧酸, 常与金属盐催化剂配合来提高NaBH4还原羧酸及羧酸衍生物的能力, 如NaBH4/ZnCl2[17], NaBH4/ZrCl4[18], NaBH4/AlCl3[19]和NaBH4/CoCl2[20]等还原体系. 对于NaBH4/金属盐还原体系的还原机理, 目前有两种解释. 第一种解释认为NaBH4与金属盐发生原位反应, 生成了还原能力更强的硼氢化物, 从而实现了对羧基及其衍生物的还原. 对NaBH4/ZnCl2体系, NaBH4与ZnCl2反应生成的Zn(BH4)2对羧酸酯具有很好的还原效果[21]. 另一种解释则认为, 还原反应并非生成还原能力更强的硼氢化物, 而是通过金属盐与羰基的络合, 促进还原反应的进行[19].
目前, 对于液体端羧基氟橡胶(LTCFs)端羧基的还原及还原机理的研究还鲜有报道. 由于LTCFs的分子量明显高于低分子量有机化合物, 并且分子链上分布着众多强极性的F原子, 简单采用传统的还原体系难以对其进行有效还原, 还原机理也尚不清楚. 本课题组曾利用NaBH4/SmCl3还原体系将LTCFs高效地还原为液体端羟基氟橡胶(LTHFs)[22], 并对还原机理进行了初步研究, 但研究还缺少系统性, 未与其它金属盐催化剂进行比较, 对还原机理的研究还不够深入. 因此, 本文系统研究了NaBH4/LaCl3, NaBH4/CeCl3, NaBH4/NdCl3和NaBH4/SmCl3稀土金属氯化物还原体系将LTCFs还原为LTHFs的性能, 并与NaBH4/MnCl2, NaBH4/NiCl2, NaBH4/CoCl2和NaBH4/CuCl2过渡金属氯化物还原体系进行了对比, 深入研究了还原反应机理.
1 实验部分
1.1 试剂与仪器
甲醇、 丙酮、 溴百里香酚蓝指示剂、 酚酞指示剂、 浓盐酸和四氢呋喃(THF), 分析纯, 天津科密欧化学试剂有限公司; 氢氧化钾、 乙醇、 邻苯二甲酸氢钾、 硼氢化钠、 氯化锰、 氯化镍、 氯化铜、 氯化钴、 氯化钐、 氯化镧、 氯化钕和氯化铈, 分析纯, 上海阿拉丁化学试剂有限公司.
Frontier型傅里叶变换红外光谱仪(FTIR), 美国PerkinElmer公司, 扫描范围为650~4000 cm-1, 扫描次数32次, 分辨率4 cm-1, 衰减全反射(ATR)模式; AC-80型核磁共振波谱仪[1H NMR, 500 MHz, 内标物为四甲基硅烷(TMS);19F NMR, 470 MHz, 内标物为一氟三氯甲烷(CFCl3)], 瑞士Bruker公司.
1.2 LTCFs的制备
参照文献[22]方法制备LTCFs.
1.3 LTHFs的制备
将5.0 g(羧基含量为2.8 mmol)LTCFs加入15 mL THF和15 mL二甘醇二甲醚的混合液中进行溶解; 控制反应温度为0 ℃, 将NaBH4加入到200 mL反应釜中, 随后加入5.0 g LTCFs溶液, 搅拌反应 1 h; 再按照(COOH)/(NaBH4)/(MCl)=1/4/2的比例加入相应量的MCl, 待混合均匀后, 升温至90 ℃反应6 h; 反应结束后, 加入30 mL 2.0 mol/L的盐酸淬灭反应, 用去离子水反复洗涤产物, 并在60~65 ℃下真空干燥至恒重, 得到乳白色LTHFs.
1.4 LTCFs/Co2+和LTCFs/Sm3+络合物的制备
将0.5 g LTCFs溶解在4 mL THF中, 按照(COOH)/(MCl)=1/2的比例加入相应量的MCl, 搅拌0.5 h后放入鼓风干燥箱中, 于60 ℃下除去溶剂, 得到LTCFs/金属盐络合物.
1.5 SmCl3催化剂的钝化
将3.0 g SmCl3溶解在12 mL甲醇中, 待SmCl3完全溶解后于50 ℃下真空干燥除去甲醇, 得到钝化的SmCl3催化剂.
1.6 化学滴定定量分析
1.6.1KOH/C2H5OH溶液的配制与标定按照GB/T 601-2002和GB/T 603-2002配制0.1 mol/L的KOH/C2H5OH溶液. 将0.2 g邻苯二甲酸氢钾溶解于50 mL去离子水中, 加入约0.1 mL浓度为10 g/L的酚酞指示剂, 用配制好的KOH/C2H5OH溶液进行滴定, 滴定至溶液由无色变为粉红色, 即为滴定终点, 同时做空白实验. KOH/C2H5OH标准滴定溶液的浓度(, mol/L)根据下式进行计算:

式中:1(mL)为试样消耗KOH/C2H5OH溶液的体积;V(mL)为空白试样消耗KOH/C2H5OH溶液的体积;(g)为邻苯二甲酸氢钾的精确质量;(204.22 g/mol)为邻苯二甲酸氢钾的摩尔质量.
1.6.2羧基含量测试将0.2 g LTCFs溶解于4 mL丙酮中, 加入约0.1 mL浓度为10 g/L的溴百里香酚蓝指示剂, 用KOH/C2H5OH对其进行标定, 当溶液变为绿色时即为滴定终点. 根据下式计算LTCFs的羧基含量(0, %):
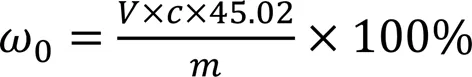
式中:(mL)为试样消耗KOH/C2H5OH溶液的体积;(g)为测试样品的质量.
1.6.3羧基还原率测试采用化学滴定定量法, 分别对LTCFs和LTHFs中的羧基含量进行测试, 进一步计算可得出羧基还原率(, %):
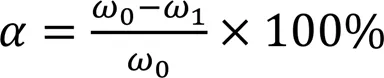
式中:0(%)为LTCFs中的羧基含量;1(%)为LTHFs中的羧基含量.
2 结果与讨论
2.1 反应条件的影响
以NaBH4/LaCl3还原体系为例, 研究了反应温度、 反应时间和LaCl3使用量对LTCFs还原的影响. 由图1(A)可见, LTCFs的还原率随着反应温度的升高而增加, 在90 ℃下还原率达到80%, 继续升高温度还原率不再显著增加, 说明90 ℃为最优实验温度. 由图1(B)可见, LTCFs的还原率随着反应时间的延长而增加, 反应时间为6 h时羧基的还原率达到最大, 继续延长还原反应时间还原率不再增加, 说明6 h为最佳还原反应时间.

Fig.1 Effect of temperature(A) and time(B) on the reductive rate of LTCFs
催化剂LaCl3使用量对LTCFs还原的影响见图2. 由图2可见, 当(R0COOH)/(NaBH4)/(LaCl3)从1/4/0增加到1/4/2时, LTCFs的还原转化率随LaCl3量的增加而增加, 说明LaCl3用量的增加对羧基的还原起促进作用. 当(R0COOH)/(NaBH4)/(LaCl3)增加到1/4/2时其还原率达到最大值(80%). 当(R0COOH)/(NaBH4)/(LaCl3)增加到1/4/2.5时, 还原率却下降到74%. 原因是LaCl3过量会包裹NaBH4颗粒, 阻碍NaBH4的溶解, 从而使LTCFs的还原转化率降低. 因此, 确定最佳还原条件为反应温度90 ℃, 反应时间6 h, 最佳(R0COOH)/(NaBH4)/(LaCl3)为1/4/2, 在此条件下羧基还原率达到80%.
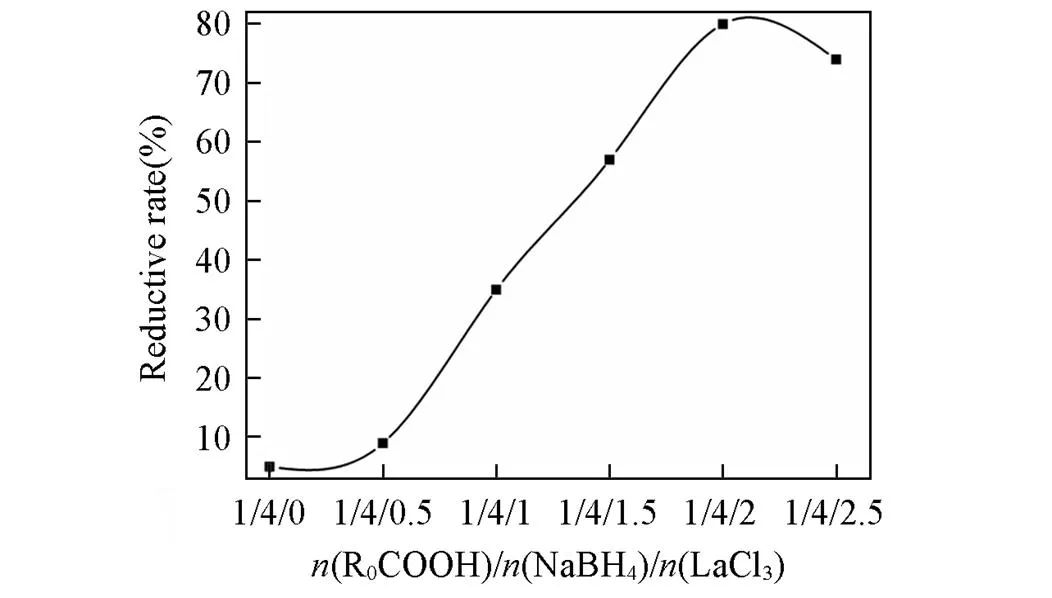
Fig.2 Effect of amount of LaCl3 on the reductive rate of LTCFs
2.2 不同MClx催化剂的影响
在使用NaBH4/LaCl3时得到的最佳还原条件下, 继续研究不同MCl催化剂对LTCFs还原率的影响及变化规律. 分别利用其它稀土金属MCl(CeCl3, NdCl3和SmCl3)和过渡金属MCl(MnCl2, CoCl2, NiCl2和CuCl2)与NaBH4组成还原体系还原LTCFs, 结果列于表1.
由表1中结果可知, NaBH4/稀土金属MCl还原体系的还原效果明显优于NaBH4/过渡金属MCl还原体系, 还原率均大于80%, 远高于NaBH4/过渡金属MCl体系. 对于NaBH4/稀土金属MCl还原体系, 还原能力从大到小的顺序为:NaBH4/SmCl3>NaBH4/NdCl3>NaBH4/CeCl3>NaBH4/LaCl3. 稀土金属阳离子半径从大到小的顺序为:La3+>Ce3+>Nd3+>Sm3+, 可见, NaBH4稀土金属MClx还原体系的还原性能随稀土金属阳离子半径的减小而增加. 对于NaBH4/过渡金属MCl还原体系, 还原能力从大到小的顺序为: NaBH4/CuCl2>NaBH4/NiCl2>NaBH4/CoCl2>NaBH4/MnCl2. 同样, 过渡金属阳离子半径从大到小的顺序为: Mn2+>Co2+>Ni2+>Cu2+, 过渡金属MCl还原体系的还原性能随过渡金属阳离子半径的减小而增加. 以上还原结果也说明, NaBH4/过渡金属MCl催化剂体系不适用于还原LTCFs.
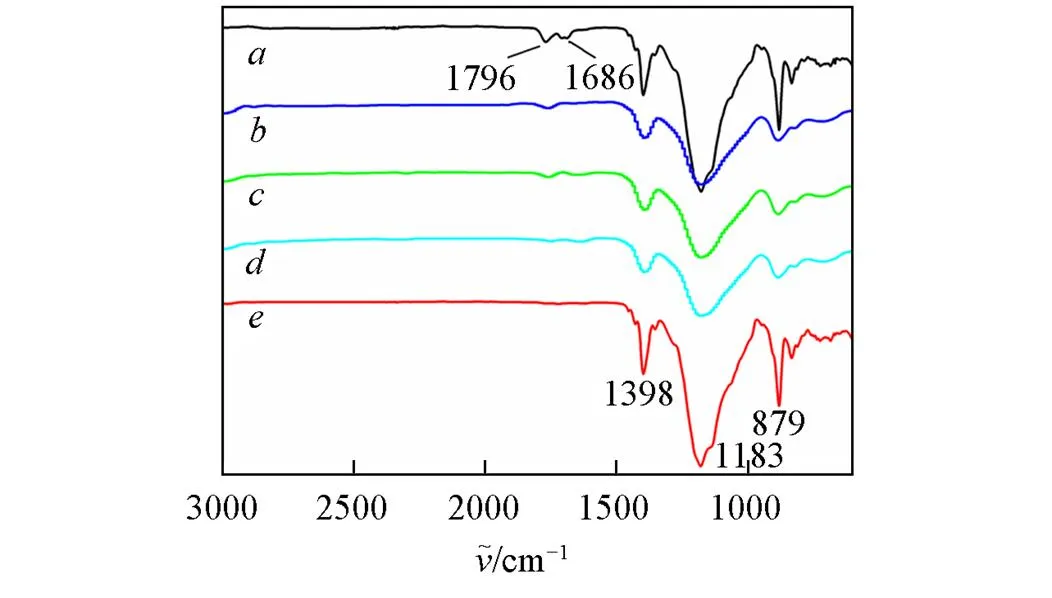
Fig.3 FTIR spectra of LTCFs(a) and LTHFs reduced by NaBH4/LaCl3(b), NaBH4/CeCl3(c), NaBH4/NdCl3(d) and NaBH4/SmCl3(e)
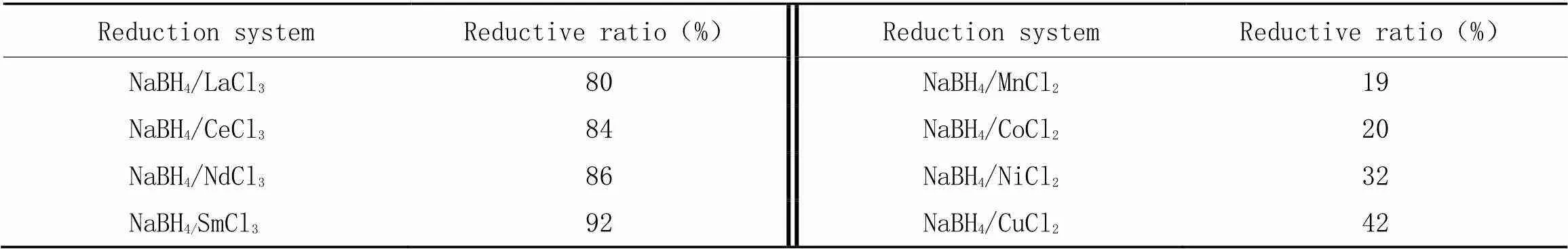
Table 1 The MClx/NaBH4 system and the reductive rate of LTCFs
2.3 结构表征
由LTCFs的FTIR谱图(图3谱线)可见, LTCFs在1769, 1686, 1398, 1183和879 cm-1处 出现吸收峰, 分别为—CF2COOH, —C=C—, —FCH2—, —CF2—和—CF3的伸缩振动峰[23,24]. LTCFs还原产物的FTIR谱图(图3谱线~) 在1398, 1183和879 cm-1处也出现了吸收峰, 表明LTHFs与LTCFs具有相同的骨架结构, 但其 —C=C—和—CF2COOH的吸收峰消失, 说明NaBH4/稀土金属MCl还原体系对—C=C—和—CF2COOH均具有良好的还原效果.
在LTCFs的1H NMR谱图(图4谱线)中,3.51~2.86处的多重峰为—CH2CF2—的特征峰,1.55处为—CF=C(CF3)CH2—的特征峰,4.68处为—(CF3)C=CH—的结构特征峰,7.50~7.70处 为—CH=CF—的特征峰[25,26]. 与LTCFs相比, 在NaBH4/MCl还原产物的1H NMR谱图中(图4谱 线~),1.55,4.68和7.50~7.70处的特征峰均基本消失, 说明—C=C—被还原, 这与FTIR分析结果一致. 同时, 还原产物在3.63和3.75处均出现新的化学位移峰, 它们归属于—CH2OH[22].1H NMR谱图证实了羟基的形成, 说明LTCFs被有效还原为LTHFs.
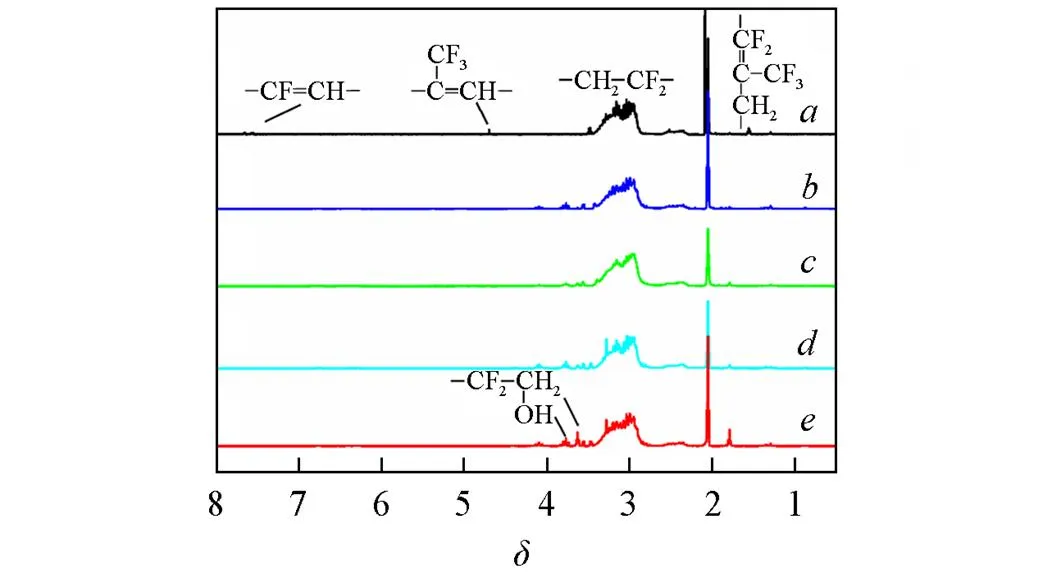
Fig.4 1H NMR spectra of LTCFs(a) and LTHFs reduced by NaBH4/LaCl3(b), NaBH4/CeCl3(c), NaBH4/NdCl3(d) and NaBH4/SmCl3(e)

Fig.5 19F NMR spectra of LTCFs(a) and LTHFs reduced by NaBH4/LaCl3(b), NaBH4/CeCl3(c), NaBH4/NdCl3(d) and NaBH4/SmCl3(e)
进一步采用19F NMR对LTCFs结构进行研究(图5). 由图5谱线可见, LTCFs在-63.67, -73.71, -80.66和-81.30处出现特征峰, 分别为—CF2COOH, —(CF3)C=CH—, —CH=CF— 和—CF=C(CF3)CH2—的特征峰[27,28], 详细归属列于表2. 图5谱线~为NaBH4/稀土金属MCl还原产物的19F NMR谱图. 与图5谱线相比, 图5谱线~在-63.67处—CF2COOH的特征峰明显减弱, 图5谱线在-63.67处—CF2COOH的特征峰基本消失, 表明端羧基被成功还原, 这与FTIR分析结果一致. 继续对比图5谱线~发现, —CF2COOH的特征峰由谱线到谱线出现逐渐减弱直至基本消失的变化规律, 说明所对应的NaBH4/稀土金属MCl体系的还原能力逐渐增强, 这与表1不同NaBH4/稀土金属MCl的还原结果一致. 同时-73.71, -80.66和-81.30处的特征峰也基本消失, 表明分子链中的双键被还原, 与FTIR和1H NMR分析结果一致.1H NMR, FTIR和19F NMR结果充分证明已成功将LTCFs还原为LTHFs.
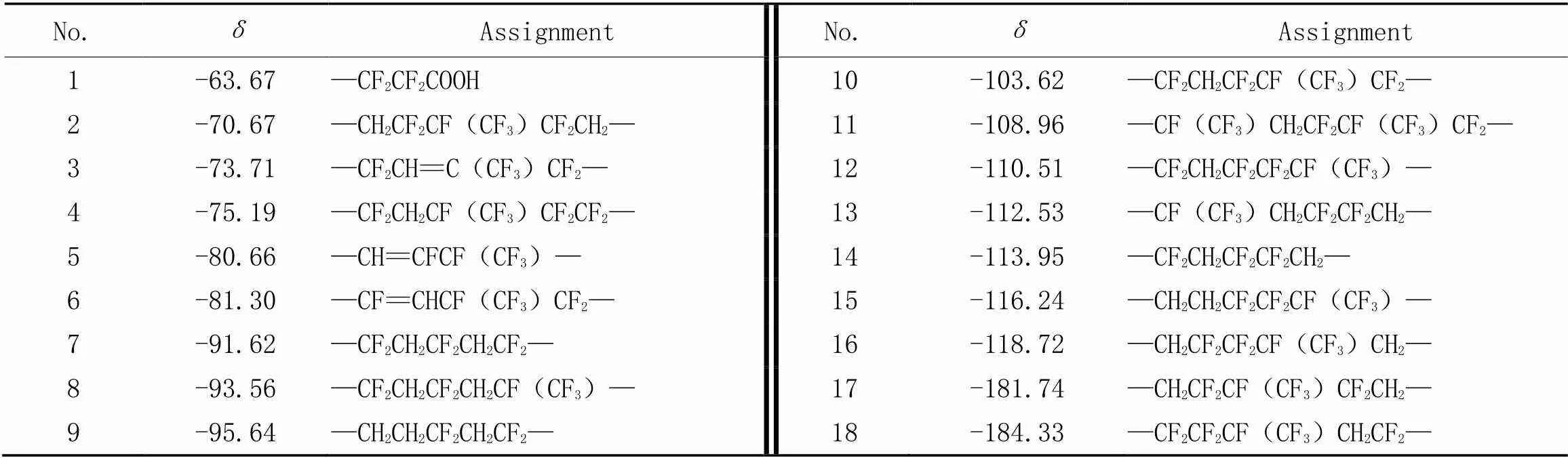
Table 2 Assignments of 19F NMR peaks in liquid fluoroelastomers
2.4 还原机理
NaBH4/金属盐还原体系还原羧酸及其衍生物一般通过两种途径: 第一种是NaBH4与金属盐发生原位反应将钠置换为其它金属, 生成还原能力更强的硼氢化物; 第二种是通过金属盐与羰基氧络合对羰基进行活化, 而后BH4-直接进攻反应底物提供负氢而将底物还原.
首先, 为了确定LTCFs是通过哪种途径被还原为LTHFs的, 研究了不同加料顺序对端羧基转化率的影响. 结果表明, 保持其它条件不变, 当将NaBH4和SmCl3一同加入LTCFs溶液中(No.1)(这种加料顺序有利于NaBH4与SmCl3先发生原位反应并对羧基进行还原)时, 还原率仅为33%. 而当先加入SmCl3与LTCFs中的羰基氧络合而后加入NaBH4进行还原(No.2)时, 还原效果要优于No.1加料顺序的效果, 还原率为48%. 因此, 可以确定LTCFs的还原应该符合第二种途径. 但是No.2加料顺序的还原效果依然不理想, 这可能因为LTCFs中含有亲核的C=C以及溶剂中含有少量的水会使SmCl3催化剂中毒, 导致还原效果不理想. 采用先加入NaBH4与LTCFs反应, 再加入SmCl3的加料顺序(No.3)时, 先加入的NaBH4可以对LTCFs中的C=C进行还原[22]同时除去溶剂中的水, 后加入的SmCl3再与羰基氧络合, 对羧基显示出高的还原活性(92%).

Fig.6 FTIR spectra of LTCFs(a), LTCFs/Co2+ complex(b) and LTCFs/Sm3+ complex(c)

Fig.7 FTIR spectra of LTCFs(a) and intermediate products(b)
其次, 分析不同MCl催化剂对LTCFs还原能力的影响, 特别是NaBH4/稀土金属MCl与NaBH4/过渡金属MCl还原体系还原性能差别的原因. 如表1所示, 不同NaBH4/稀土金属MCl还原体系均比NaBH4/过渡金属MCl还原体系的还原性能强很多, 同时NaBH4/稀土金属MCl和NaBH4/过渡金属MCl还原体系的还原性能均随金属阳离子半径的减小而增加. 一般认为, 这与金属阳离子对羰基氧的结合力大小有关, 金属阳离子与羰基氧结合能力越大, 羰基双键电子越容易向氧原子偏移, 越有利于NaBH4分离的BH4-攻击显正电性的羰基碳原子[29], 还原体系的还原性能越强. 对此, 本文进行了深入研究. 以 过渡金属CoCl3和稀土金属SmCl3为例, 分别在LTCFs的THF溶液中加入CoCl3和SmCl3催化剂, 搅拌0.5 h, 待金属阳离子与羰基氧充分络合后加热除去THF, 得到LTCFs/Co2+和LTCFs/Sm3+络合物. 利用FTIR分别研究LTCFs/Co2+和LTCFs/Sm3+络合物中羰基吸收峰的吸收频率变化并分析稀土金属阳离子和过渡金属阳离子对羰基氧结合力大小的差异(图6). 图6谱线为LTCFs的FTIR谱图, 在1769 cm-1处出现羰基吸收峰. 图6谱线和分别为LTCFs/Co2+和LTCFs/Sm3+络合物的FTIR谱图. 与图6谱线相比, 图6谱线和中的羰基吸收峰都发生了明显的红移, 分别位于1726和1646 cm-1, 这是由于金属阳离子与羰基氧存在较强的络合, 使羰基双键上的电子向氧原子发生偏移, 从而导致吸收峰发生红移. 由图6谱线和可见, 与LTCFs/Co2+络合物比较, LTCFs/Sm3+络合物羰基吸收峰的吸收频率更低, 说明Sm3+与羰基氧的结合力要大于Co2+离子, 这有利于还原反应, 这就解释了NaBH4/稀土金属MCl比NaBH4/过渡金属MCl还原体系的还原性能强的原因. 根据文献[30]可知, 金属盐阳离子半径越小, 极化能力越强, 与羰基氧间的结合力越大, 羰基双键电子越容易向氧原子偏移, 越有利于NaBH4分离的BH4-攻击显正电性的羰基碳原子. 本文研究也证实了这一规律, NaBH4/稀土金属MCl和NaBH4/过渡金属MCl还原体系的还原性能均随金属阳离子半径的减小而增加.
然后, 对还原过程中间产物进行针对地研究, 以证明还原机理的正确性. 根据机理推测, 在LTCFs被还原为LTHFs的过程中, 应该有羧基先还原为醛基的中间产物生成, 但由于中间产物醛基的活性高, 很容易被NaBH4/SmCl3还原体系直接还原为最终产物LTHFs, 在反应条件下很难检测到. 为此, 本文使用甲醇对SmCl3催化剂进行钝化, 以降低NaBH4/SmCl3还原体系的还原活性, 结果在还原产物中成功地检测到端醛基(图7). 图7谱线和分别为LTCFs和中间产物的FTIR谱图, 与图7谱线相比, 图7谱线在808和2963 cm-1处出现新的吸收峰, 分别为醛基的C—H面外弯曲振动和C—H伸缩振动的吸收峰. FTIR结果清晰地证明, 在LTCFs被还原为LTHFs的过程中经历了生成端醛基氟橡胶中间产物的过程, 随后LTCFs继续被还原为LTHFs.
最后, 根据以上研究结果, 提出了NaBH4/MCl还原LTCFs的还原机理, 如Scheme 1所示. 首先, LTCFs中的C=C被NaBH4还原, 并且R0COOH与NaBH4反应生成(R1COO)4BNa(A→B); 然后, 金属阳离子M3+与羰基氧络合产生诱导效应, 使羰基电子向羰基氧移动, 从而导致羰基碳的缺电子性增加, 这有利于NaBH4分离的BH4-攻击羰基碳, 进而羰基被还原(B→C); 接下来, 金属离子M3+与羰基氧分离, 另一个碳氧键发生均裂断键, 形成液体端醛基氟橡胶(C→E); 最后, 再次通过金属离子的络合作用对醛基进行还原, 最终得到LTHFs(E→G).
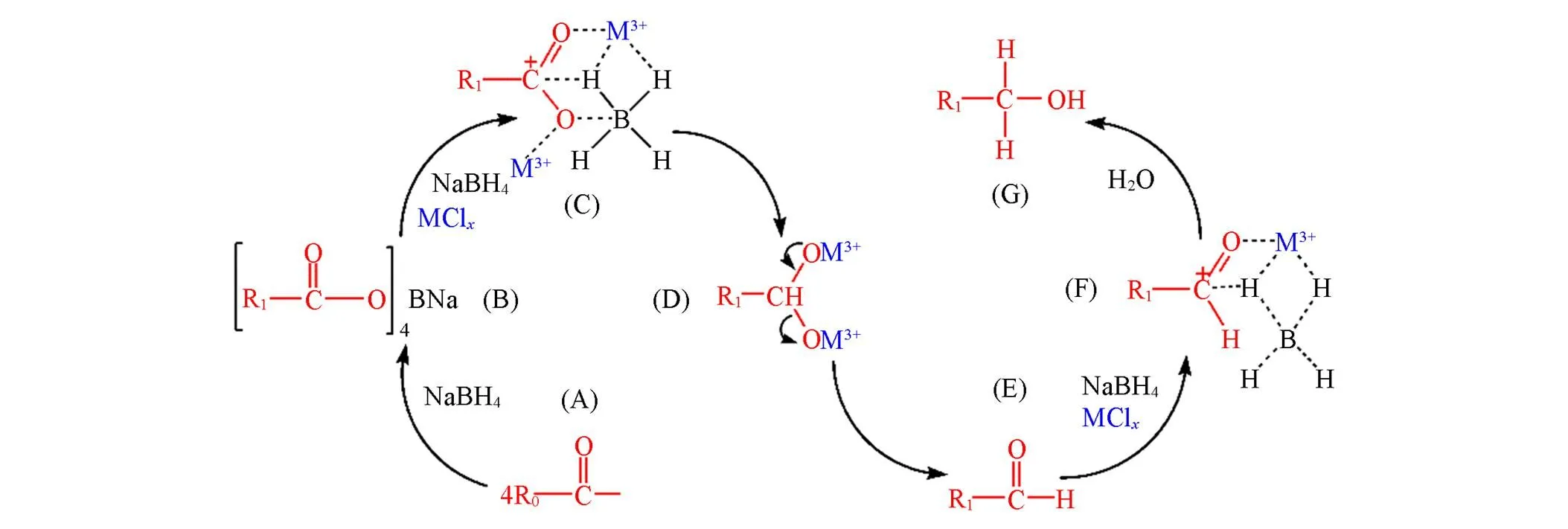
Scheme 1Reduction mechanism of TCLFs
R0is composed of —CH2CF2—, —CF2CF(CF3)—, —CFCHCHF(CF3)—, —CF2C(CF3)CHCF2—, and —CFCH—; R1is composed of —CH2CF2— and —CF2CF(CF3)—.
3 结 论
研究了不同NaBH4/稀土金属MCl还原体系对LTCFs还原能力的变化规律, 为高效筛选MClx催化剂提供了理论依据, 得出以下结论: (1) 在反应温度为90 ℃、 反应时间为6 h,(R0COOH)/(NaBH4)/(MCl)=1/4/2时, LTCFs中的碳碳双键及羧基被还原, 并且NaBH4/稀土金属MCl还原体系的还原效果明显好于NaBH4/过渡金属MCl还原体系, 更适合用作LTCFs还原的催化剂, 其中NaBH4/SmCl3还原体系的还原效果最好, 羧基的还原率达到了92%. (2) FTIR和NMR分析表明, LTCFs中的碳碳双键和端羧基被NaBH4/MCl还原体系还原, 生成碳碳单键和端羟基. (3) 机理研究表明, 在LTCFs还原反应中催化剂的金属阳离子与羰基氧间的结合力越大, NaBH4/MCl体系对LTCFs的还原效果越好, 这有助于在众多金属盐催化剂中筛选出具有高效催化作用的催化剂, 同时证明了还原过程会有液体端醛基氟橡胶中间产物生成.
[1] Ameduri B., Boutevin B.,, Elsevier, Amsterdam, 2004, 187—230
[2] Ameduri B., Boutevin B., Kostov G.,., 2011,, 105—187
[3] Mitra S., Siahkali A. G., Kingshott P., Hvilsted S., Almdal K. J.,., 2004,, 6216—6229
[4] Ferrandez P.; Robert, C. K.(Ed.),Taylor & Francis Group, New York, 2008, 133—154
[5] Maclachlan J. D.,., 1978,, 41—53
[6] Ameduri B.,., 2009,, 6632—6686
[7] Robinson M. I., Kochi J. K.,, 1983,, 526—532
[8] Li D. H., Liao M. Y.,., 2017,, 55—67
[9] Li D. H., Liao M. Y.,., 2018,, 116—125
[10] Bodnar B. S, Vogt P. F.,, 2009,, 2598—2600
[11] Findlay N. J., Park S. R., Schoenebeck F., Cahard E., Zhou S., Berlouis L. E. A., Spicer M. D., Tuttle T., Murphy J. A.,, 2010,, 15462—15464
[12] Pelletier G., Bechara W. S., Charette A. B.,, 2010,, 12817—12819
[13] Das S., Addis D., Zhou S., Junge K., Beller M.,, 2010,, 1770—1771
[14] Das S., Möller K., Junge K., Beller M.,., 2011,, 7414—7417
[15] Ganewatta M. S., Ding W., Rahman M. A., Yuan L., Wang Z., Hamidi N., Robertson M. L., Tang C.,, 2016,, 7155—7164
[16] Brown H. C., Subbe R. B., Subba Rao B. C.,., 1960,, 681—686
[17] Narasimhan S., Madhavan S., Prasad K. G.,, 1995,, 5314—5315
[18] Itsuno S., Sakura Y., Ito I. K.,, 1988,, 995—996
[19] Hida T., Mitsumori S., Honma T., Hiramatsu Y., Hashizume H., Okada T., Kakinuma M., Kawata K., Oda K., Hasegawa A., Masui T., Nogusa H.,, 2009,, 1413—1418
[20] Ashot M., Rafael T., Sahak G., Marina A., Henry P., Vahan M., Raymond S.,, 2010,, 231—233
[21] Yamakawa T., Masaki M., Nohira H.,, 1991,, 2730—2734
[22] Chang Y. F., Liao M. Y., Li X. Y.,, 2020,, 10932—10938
[23] Pianca M., Barchiesi E., Esposto G., Radice S.,, 1999,, 71—84
[24] Saint L. R., Manseri A., Ameduri B., Lebret B., Vignane P.,, 2002,, 1524—1536
[25] Ross G. J., Wattsa J. F., Hill M. P., Morrissey P.,, 2000,, 1685—1696
[26] Gondi S. R., Vogt A. P., Sumerlin B. S.,, 2007,, 474—481
[27] Wormald P., Ameduri B., Harris R. K., Hazendonk P.,, 2008,, 3629—3638
[28] Souzy R., Ameduri B., Ahsen S. V., Willner H., Arguöello G. A.,., 2003,, 85—93
[29] Brown H. C., Narasimhan S., Choi Y. M.,., 1982,, 4702—4708
[30] Meksi N., Ticha M. B., Kechida M., Mhenni M. F.,, 2010,, 12333—12338
Reduction Performance and Mechanism of Liquid Terminated-carboxyl Fluoroelastomers Using NaBH4/MClReduction System
CHANGYunfei, LIAOMingyi*, WENJiaming
(,,116026,)
Using a simple one-pot method, direct transformation of liquid terminated-carboxyl fluoroelastomers(LTCFs) to the corresponding liquid terminated-hydroxyl fluoroelastomers(LTHFs) was easily realized with sodium borohydride(NaBH4) in the presence of metal chloride(MCl). The structure and functional group content of LTCFs and LTHFs were analyzed by Fourier transform infrared spectroscopy(FTIR),1H nuclear magnetic resonance(1H NMR) spectrocopy,19F nuclear magnetic resonance(19F NMR) spectrocopy and chemical titration. The results showed that —C=C— and carboxyl groups of LTCFs were reduced efficiently. The effect of different rare-earth chlorides(LaCl3, CeCl3, NdCl3and SmCl3) and transition metal chlorides(MnCl2, NiCl2, CoCl2and CuCl2) on the performances of the LTCFs reduction was discussed. The NaBH4/SmCl3system was the best and the reduction rate reached 92% under optimum reaction conditions. Mechanism research showed that the stronger binding force of metal ion and carbonyl oxygen was beneficial to the reduction of LTCFs.
Liquid terminated-carboxyl fluoroelastomer; Metal chloride; NaBH4; Carboxyl; Reduction mechanism
O632.21
A
10.7503/cjcu20210835
2021-12-16
2022-02-22.
廖明义, 男, 博士, 教授, 主要从事橡胶合成、 液体氟橡胶的制备和应用及聚合物基纳米复合材料方面的研究. E-mail: liaomy@dlmu.edu.cn
国家自然科学基金(批准号: 51873026)资助。
Supported by National Natural Science Foundation of China(No.51873026).
(Ed.: W, K, M)

