Sn-Al-β分子筛酸性在葡萄糖转化反应中作用的固体NMR研究
李志光, 齐国栋, 徐君, 邓风
Sn-Al-分子筛酸性在葡萄糖转化反应中作用的固体NMR研究
李志光1,2, 齐国栋1, 徐君1, 邓风1
(1. 中国科学院精密测量科学与技术创新研究院, 武汉物理与数学研究所,波谱与原子分子物理国家重点实验室, 武汉磁共振中心, 武汉 430071; 2. 中国科学院大学, 北京 100049)
制备了一系列具有不同酸性质的分子筛催化剂, 通过固体核磁共振(NMR)探针分子技术对其酸性质进行了表征, 并考察了其催化葡萄糖转化为乙酰丙酸甲酯的性能. 吸附三甲基磷的31P NMR实验结果表明, 含有骨架Sn以及Al原子的Sn-Al-催化剂同时具有Brønsted与Lewis酸性. 通过2-13C-丙酮探针分子区分出 3种酸强度的Brønsted酸位, 其中一种酸强度接近“超强酸”, 可能是由于空间临近的Brønsted酸位和Lewis酸位发生协同作用产生的. 葡萄糖转化为乙酰丙酸甲酯的催化反应结果表明, 相比于分别只含有Lewis酸位和Brønsted酸位的Sn-和Al-样品以及两者的物理混合样品, Sn-Al-分子筛催化剂具有高催化活性与产物选择性, 这主要是由于Brønsted酸位和Lewis酸位的协同作用产生了强Brønsted酸位, 这种强Brønsted酸位进一步导致了更高的催化活性.
分子筛; 探针分子; 酸性; 固体核磁共振; 葡萄糖转化
生物质资源在地球上储量丰富, 价格低廉, 是替代传统化石资源的最具潜力的可再生能源. 将生物质资源高效地转化为平台化合物或者高附加值化学品, 在应对未来的能源危机具有重要意义[1~3]. 目前, 制约生物质转化的一个重要原因是缺乏高活性的催化剂, 近年来该类催化剂的开发备受关注[4~6]. 分子筛类催化剂具有可调变的酸性和孔结构、 较好的热稳定性、 可择形催化及分离简单等特点, 在生物质转化中拥有广阔的研究前景[7~10].

本文合成了具有不同酸性质的分子筛催化剂, 利用吸附2-13C-丙酮和三甲基磷(TMP)的固体核磁共振(NMR)探针分子技术, 对所合成催化剂的酸性质(包括种类和强度)进行了表征, 研究了催化剂的酸性质与葡萄糖转化反应活性间的关系.
1 实验部分
1.1 试剂与仪器
正硅酸四乙酯(TEOS, 分析纯)、 结晶四氯化锡(SnCl4·5H2O, 分析纯)、 硝酸(HNO3, 分析纯)、 氯化钠(NaCl, 分析纯)、 氟化铵(NH4F, 分析纯)、 氢氟酸(HF, 分析纯)、 葡萄糖(C6H12O6·H2O, 分析纯)、 无水甲醇(CH3OH, 分析纯)和萘(C10H8, 分析纯)均购于国药集团化学试剂有限公司; 四乙基氢氧化铵(TEAOH, 质量分数25%)购于北京百灵威科技有限公司; H-分子筛(Si/Al摩尔比12.5)购于天津南化催化剂有限公司; 2-13C-丙酮(CH313COCH3, 纯度99%)购于美国剑桥同位素公司; 三甲基磷(TMP, 纯度97%)购于美国Sigma-Aldrich公司; 对硝基甲苯(C7H7NO2, 纯度99%)和对硝基氯苯(C6H4ClNO2, 纯度99.5%)购于上海阿拉丁试剂公司.
X'Pert3Powder型X射线粉末衍射仪(XRD, 荷兰PANalytical公司); Agilent ICP-OES 720ES电感耦合等离子体发射光谱仪(ICP-OES, 美国Agilent公司); GC-2014型气相色谱仪(GC, 配备RXI-5ms色谱柱, 日本岛津公司); Caries G9824 A型固体紫外-可见漫反射光谱仪(UV-Vis, 美国Agilent公司); Bruker Avance III 500 MHz 型固体核磁共振波谱仪(NMR, 德国Bruker公司); Varian Infinity plus 600 MHz型固体核磁共振波谱仪(NMR, 美国Agilent公司).
1.2 实验过程
1.2.1催化剂的制备采用两步法合成Sn-Al-分子筛[26]. 第一步对商业H-分子筛进行硝酸脱铝处理: 按照每克H-分子筛与20 mL 1 mol/L HNO3溶液的比例混合, 于室温下搅拌6 h, 然后过滤分离固体产物, 用超纯水洗涤至中性, 随即在100 ℃烘箱中干燥10 h, 得到的部分脱铝样品记为Al-, ICP元素分析其Si/Al摩尔比为30. 第二步是Sn物种的引入: 将2.4 g Al-加入到装有11.79 g TEAOH的聚四氟乙烯烧杯中, 加入1 mL SnCl4溶液(0.143 g SnCl4·5H2O溶于1mL超纯水中), 在70 ℃水浴条件下搅拌约1 h, 蒸发多余的水, 使最终凝胶中SiO2/Al2O3/SnCl4/TEAOH/H2O摩尔比为1.0∶0.017∶0.01∶0.5∶7.5. 然后将凝胶转移到25 mL聚四氟乙烯内衬的不锈钢反应釜中, 置于140 ℃烘箱中预处理1 h, 冷却至室温, 加入0.78 g NH4F, 搅拌均匀后, 继续在140 ℃烘箱中晶化1 h. 最终产物经过滤分离, 用超纯水洗涤3遍, 直至滤液中无Cl‒离子,将产物置于100 ℃烘箱中干燥10 h, 最后将所得到的样品置于管式炉中, 于550 ℃下焙烧6 h, 最终得到Sn-Al-分子筛, 经ICP元素分析其Si/Al摩尔比为29, Si/Sn摩尔比为91.
Sn-分子筛采用传统水热法合成[11]. 将8.5 g TEOS加入到装有11.72 g TEAOH的聚四氟乙烯烧杯中, 室温下搅拌90 min. 然后滴加1 mL SnCl4溶液(0.095 g SnCl4·5H2O溶于1 mL 超纯水中), 待TEOS完全水解, 且水解产生的乙醇完全蒸发后, 加入1.3 g 40%(质量分数)HF, 将得到的固体搅拌至凝胶状, 蒸发掉多余的水, 使最终的凝胶中SiO2/Sn/TEAOH/H2O/HF摩尔比为1.0∶0.0067∶0.55∶7.5∶0.55. 将凝胶转移至25 mL聚四氟乙烯内衬的不锈钢反应釜中, 置于140 ℃烘箱中晶化28 d. 得到的固体产物经过滤分离, 用超纯水洗涤至无Cl‒离子, 最后将所得到的样品在80 ℃烘箱中干燥10 h, 然后置于管式炉中, 在600 ℃下焙烧10 h, 最终得到的Sn-样品经ICP元素分析, 其Si/Sn摩尔比为147.
Al-和Sn-物理混合样品的制备. 为了确保和Sn-Al-具有相同的Sn和Al含量, 根据Al-和Sn-的ICP分析结果, 将二者以质量比1∶1.6的比例混合, 研磨30 min, 该物理混合的催化剂记为Sn-/Al-.
采用Na+离子交换法取代Sn-Al-分子筛B酸质子. 按照每克Sn-Al-分子筛与100 mL 1 mol/L NaCl溶液固液比例混合, 于常温下搅拌1 h, 经过滤分离固体样品, 用超纯水洗涤3次, 重复以上操作4次, 最后于100 ℃干燥10 h, 最终得到的催化剂记为Na-Sn-Al-.
1.2.2ICP-OES元素分析在密闭体系中将0.1 g样品溶解于5 mL HNO3(质量分数65%)和2 mL HF(质量分数40%)溶液中, 测定其Si, Al和Sn的含量.
1.2.3葡萄糖催化反应将0.134 g催化剂(Sn-或者Al-的量为0.348 g)、 0.248 g 葡萄糖和10 mL无水甲醇依次加入到50 mL的高压反应釜中, 用氮气置换釜内空气3次, 然后用氮气加压至0.4 MPa. 以5 ℃/min的升温速率升温至160 ℃, 开启磁力搅拌, 转速为800 r/min,反应时间为5 h. 反应结束后, 用冰水浴冷却至室温, 离心分离反应液和催化剂, 将收集到的反应液定容至50 mL, 加入萘作为内标物, 进行GC定量分析测定.
1.2.4TMP和2-13C-丙酮探针分子的吸附在吸附探针分子之前, 先将催化剂在真空系统上进行真空脱水, 脱水程序为: 以 2 ℃/min速率从室温逐渐升温至120 ℃, 保持2 h; 再以2 ℃/min速率从 120 ℃升温至400 ℃, 保持10 h, 最终真空度低于10-3Pa. TMP的吸附: 通过真空系统将过量TMP引入到0.1 g脱水样品中, 室温下保持1 h, 使TMP分子完全扩散, 然后在50 ℃加热条件下脱附过量的TMP分子; 2-13C-丙酮的吸附: 通过真空系统将2-13C-丙酮引入到0.1 g脱水样品中, 控制吸附量为75 μmol/g, 室温下保持1 h, 使其达到平衡. 最后将吸附两种探针分子的样品均在氮气气氛保护的手套袋里装入密封的4 mm ZrO2转子, 进行固体NMR实验.
1.2.5固体NMR实验单脉冲27Al MAS NMR,1H →31P CP/MAS NMR(交叉极化)以及1H →13C CP/MAS NMR实验在配备4 mm探头的Bruker Avance III 500 MHz 固体NMR谱仪上完成,1H核、31P核、13C核、27Al核的Larmor频率分别是500.6, 202.6, 125.9和130.4 MHz, 转速为10 kHz. 单脉冲27Al MAS NMR实验采用小扳转角技术进行采样,/18脉冲宽度为0.32 μs, 采样间隔为1 s, 累加次数为1024,使用 Al(NO3)3定标(Al0);1H →31P CP/MAS NMR实验的采样间隔为2 s, 接触时间为4 ms, 累加次数为1024, 使用磷酸二氢铵定标(P0.81);1H →13C CP/MAS NMR实验的采样间隔为2 s, 接触时间为4 ms, 累加次数为4000, 以金刚烷为定标物质(C38.5). 单脉冲29Si MAS NMR实验在Varian Infinity plus 600 MHz固体NMR谱仪上进行,1H和29Si核的共振频率分别为599.5和120.4 MHz, 转速为4 kHz,/4脉冲宽度为6.8 μs, 采样间隔为60 s, 累加次数为64, 以高岭土为定标物质(Si= -91.5).
1.2.6Hammett指示剂法测定分子筛酸强度将指示剂(对硝基甲苯和对硝基氯苯)溶解在干燥环己烷(质量分数5%)中, 获得指示剂溶液. 在氮气气氛保护的手套带中将0.1 g脱水分子筛样品分散到5 mL干燥环己烷中, 加入2滴指示剂溶液.待混合物2 h达到平衡后, 记录颜色变化.
2 结果与讨论
2.1 催化剂结构的表征
利用XRD对所合成的分子筛催化剂的结构进行了表征, 发现所合成样品均呈现*BEA拓扑结构的衍射峰[图1(A)]. 这说明分子筛脱铝、 引入Sn的过程均不会影响分子筛的晶体结构. UV-Vis常用于研究Sn改性分子筛中Sn原子的配位状态, 为了确定金属Sn物种是否成功引入到分子筛骨架中, 对所制备分子筛的Sn物种进行了固体UV-Vis表征. 在Al-分子筛上观测到220 nm处的骨架四配位Al的特征吸收峰和270 nm处的少量骨架外六配位Al的特征吸收峰[图1(B)谱线]; 在Sn-和Sn-Al-分子筛上仅可观测到220和254 nm处的骨架四配位Sn的特征吸收峰, 并没有出现280 nm处的骨架外SnO物种的信号[图1(B)谱线和][21, 27, 28]. 这说明在所有样品中, Sn都成功进入到分子筛骨架之中, 且主要为骨架四配位Sn物种. Na-Sn-Al-与Sn-Al-具有基本相同的吸收信号[图1(B)谱线], 表明Na+离子交换不会对骨架四配位Sn产生影响.

Fig.1 XRD patterns(A) and UV⁃Vis spectra(B) of the prepared samples H⁃β(a), Al⁃β(b), Sn⁃β(c), Sn⁃A⁃β(d) and Na⁃Sn⁃Al⁃β(e)
为了进一步了解金属Sn物种如何被引入到Al-分子筛骨架中, 利用固体27Al MAS NMR和29Si MAS NMR实验, 研究了H-分子筛在硝酸脱铝以及引入Sn物种后, 其骨架铝和硅原子的变化. 固体27Al MAS NMR实验表明, 原始样品上有着大量的骨架四配位Al物种(Al54)和少量六配位非骨架 Al物种(Al0)[图2(A)谱线]. 经硝酸处理后, 骨架四配位Al和非骨架Al物种明显减少[图2(A)谱 线]. 同时在固体29Si MAS NMR谱图中, 化学位移在-102处的Si(3Si, 1OH)信号峰面积百分比由10.0%增加到13.5%, 而化学位移在-105处的Q3位点[Si(3Si, 1Al)]信号峰面积百分比由24.3%降低至12.7%[图2(B)谱线]. 上述现象说明硝酸脱铝步骤能在分子筛上生成更多Si—OH缺陷位. 在Sn-Al-分子筛中, 由于合成过程中发生了轻微的脱铝, 导致Al54的信号略有降低,Al0的信号略微增加[图2(A)谱线], 并且在固体29Si MAS NMR谱图中发现-102处的Si(3Si, 1OH)信号峰面积百分比降至11.9%[图2(B)谱线], 同时-105处的Q3位点信号峰面积百分比增加到17.4%. 这说明在 Sn-Al-合成过程中, 首先硝酸脱铝处理产生了 Si—OH缺陷位, 引入Sn后, 分子筛发生重结晶过程, Sn与缺陷位处的Si—OH结合, 形成四配位Sn, 从而使Sn进入分子筛骨架.

Fig.2 27Al MAS NMR(A) and 29Si MAS NMR(B) spectra of the prepared samples H⁃β(a), Al⁃β(b) and Sn⁃Al⁃β(c)
Peak integral(percentage) are indicated in parentheses.
2.2 催化剂的酸性
TMP是一种可以区分B酸位和L酸位类型的固体NMR探针分子, TMP可被B酸质子化形成TMPH+, 其31P的化学位移为P-2~P-6,与L酸位相互作用后, 其31P的化学位移通常出现在P-20~P-50[29~31]. 图3为TMP吸附到不同分子筛上的1H →31P CP/MAS NMR谱图. Sn-在L酸特征区域可观测到P-20的信号(图3谱线), 其L酸性来源于骨架四配位Sn,另外, 还可观测到一个微弱的P-5的B酸位特征信号, 由于该样品上不存在Al原子, 因此, 所观测的酸性位应该是由“Open” Sn(Sn—OH)与邻近的Si—OH基团(Sn—OH···OH—Si)相互作用产生的[14], 在P-60处的信号可以归属为分子筛上物理吸附的TMP分子. 由于Al-样品不含Sn原子, 因此只表现出很强的B酸位的特征峰(图3谱 线), 来源于骨架上的Si-OH-Al桥式羟基. 在Sn-/Al-(图3谱线)和Sn-Al-(图3谱线)上都观测到来自B酸位和L酸位的信号, 表明它们都是同时具有B酸位和L酸位的催化剂. 对于Na-Sn-Al-样品(图3谱线), 在31P NMR图谱上除了L酸位以外, 仍可观测到较弱的P-5信号, 说明存在少量未被Na+离子交换掉的B酸位. 从以上分析可以看出, 尽管TMP能够有效分辨出催化剂上的B酸位与L酸位, 但不能区分不同样品上B酸位的酸强度.

Fig.3 1H→31P CP/MAS NMR spectra of the prepared samples with adsorbed TMP
. Sn-;.Al-;.Sn-/Al-;.Sn-Al-;.Na-Sn-Al-
为了确定Sn-Al-和Sn-/Al-的B酸位性质是否存在差异, 选择了2-13C-丙酮探针分子做了进一步探究. 丙酮分子可以与B酸位以及L酸位作用. 对于B酸位而言, 其酸性质子与丙酮羰基的氧原子形成氢键, 通过氧原子将吸电子作用传递到2-13C原子上, 在NMR谱图上可观测到2-13C的化学位移向 低场移动, 即B酸位酸性越强,13C的化学位移越大(“超强酸”阈值为C245)[32~34]. 图4为不同样品上吸附2-13C-丙酮后的1H →13C CP/MAS NMR谱图. Al-分子筛上只观测到C223和C236两个酸位信号 [图4(A)], 而在Sn-/Al-样品上由于存在Sn-组分, 增加了一个C229的信号[图4(B)], 此信号可归属为丙酮吸附到骨架四配位Sn上的L酸位信号[35]. 在Sn-Al-分子筛上除了这3个信号外, 还观测到一个C241的强酸信号和一个C213的丙酮分子吸附到非酸性的Si—OH的信号[36][图4(C)]. 为了确定C241,C236和C223信号对应的酸性种类, 对Na-Sn-Al-进行了表征, 从图4(D)可以看到,C223和C241的信号完全消失, 因此, Sn-Al-分子筛上的这两个信号均可归属为吸附到B酸位上的丙酮分子, 而C236的微弱信号来源于未被Na+离子交换掉的残余B酸位, 这与TMP探针分子表征的结果一致. 新出现的C217的信号为过量吸附的丙酮分子.

Fig.4 1H→13C CP/MAS NMR spectra of the prepared samples with adsorbed 2⁃13C⁃acetone
(A) Al-; (B) Sn-/Al-; (C) Sn-Al-; (D) Na-Sn-Al-
上述结果清晰地表明, Al-中存在两种强度的B酸位, 这与文献[37]报道一致.C223的信号可归属于吸附到孤立的桥式羟基(Si—OH—Al)的丙酮分子[图5(A)],C236的信号可归属于吸附到缺陷位(Si—OH)附近桥式羟基上的丙酮分子[图5(B)], 由于桥式羟基与Si—OH的氧原子存在氢键作用, 导致B酸位强度有所增加, 从而导致吸附的2-13C-丙酮分子化学位移增大. Sn-与Al-分子筛简单物理混合不会改变Al-上B酸位的性质, 然而将Sn与Al双金属同时引入分子筛骨架上, 在Sn-Al-催化剂上产生了一种强度接近“超强酸”的B酸位(C241), 这可能是由于空间临近的B酸位(Si—OH—Al)和L酸(Sn)位能发生协同作用, B酸位的酸性增强[图5(C)], 这与过渡金属(Zn, Ga)改性分子筛上产生的协同活性位类似[38,39].

Fig.5 Schematic diagram of 2⁃13C⁃acetone adsorption at different Brønsted acid sites
为了进一步确认强B酸位的存在, 采用Hammett指示剂法对分子筛B酸强度进行了检测[18,40]. 选择对硝基甲苯(0=‒11.4)和对硝基氯苯(0=‒12.7)作为指示剂, 二者碱型色均为无色, 酸型色为黄色. 结果如表1所示, 可以看到Sn-Al-催化剂可以使对硝基甲苯变色, 但不能使对硝基氯苯变色, 表明其B酸位的酸强度为‒12.7<0≤‒11.4, 接近“超强酸”强度(阈值为‒11.9). 而Al-和Sn-/Al-两种催化剂均不能使上述两种指示剂变色, 这说明它们的B酸强度低于0=‒11.4. 上述结果与丙酮NMR探针分子的实验结果相吻合.
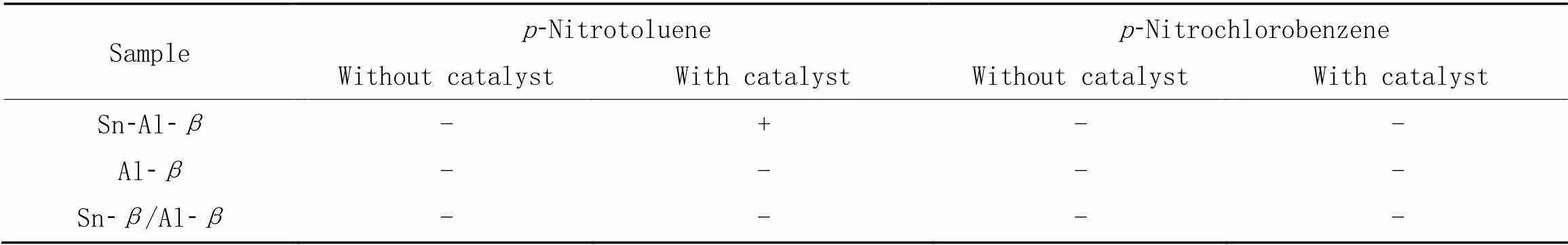
Table 1 Acidic strength analysis of zeolites by Hammett indicators*
* + represent changed color of indicator; - represent unchanged color of indicator.
除了上述酸种类和强度分析外, 还利用吡啶吸附的红外实验对所制备催化剂上的B酸位和L酸位的含量进行定量分析, 结果如图6所示. 1546和1454 cm‒1处的谱峰分别代表吡啶吸附到B酸位和L酸位上的特征吸收峰, 1490 cm‒1处为B酸位和L酸位共同贡献的吸收峰, 1447 cm‒1是吡啶以氢键形式吸附在分子筛(Py—H)上的特征峰. 采用1.67和2.22 cm/μmol分别作为计算B酸位和L酸位的摩尔消光系数[41], 结合1546和1454 cm‒1处红外吸收峰的积分面积, 可定量分析出催化剂上B酸位和L酸位的含量, 结果如表2所示. Al-和Sn-Al-上的总B酸位量基本一致, 约为150 μmol/g. 即Sn-/Al-混合样品和Sn-Al-催化剂上具有近似量的B酸位.

Table 2 Concentration of B and L acid sites on zeolites determined by pyridine⁃probed FTIR

Fig.6 IR spectra of Sn⁃β(a), Al⁃β(b) and Sn⁃Al⁃β(c) after pyridine adsorption at 298 K for 30 min and desorption at 423 K
2.3 催化反应活性
葡萄糖在不同类型酸性中心的催化作用下具有不同的转化反应途径(Scheme 1). 当只有L酸位催化时, 葡萄糖先异构化为果糖, 随后发生逆羟醛缩合生成二羟基丙酮(DHA)和它的同分异构体甘油醛(GA), 然后经过脱水和重排反应生成丙酮醛(PAL), 最后与甲醇反应生成乳酸甲酯(MLA)[42]. 相同条件下B酸中心无法催化上述过程, 然而当L酸位和B酸位同时存在时, 葡萄糖被L酸位异构化为果糖后, B酸位可先将果糖脱水为HMF, 然后将其醇解为MLE[43]. 因此, 该反应能够很好地区分催化剂B酸位和L酸位性质, 可以用来探究所制备的分子筛催化剂酸性质与反应性能的关系. 葡萄糖转化反应结果如图7所示, Sn-分子筛上主要体现L酸性, 因此, 反应产物主要为MLA(收率37.3%), 而MLE的收率非常低(2.4%), 在Al-样品上由于缺乏使葡萄糖异构化的L酸位, 反应难以进行, 其MLE和MLA收率分别仅为5.9%和1.8%. 相比较而言, Sn-/Al-和Sn-Al-上, B酸位和L酸位的共同作用能明显提升MLE收率, 分别为23.9%与43%, 其MLA收率分别为11.0%和6.1%. Sn-Al-上的B酸质子被Na+离子交换后的Na-Sn-Al-样品, 表现出类似于Sn-的催化反应性能.
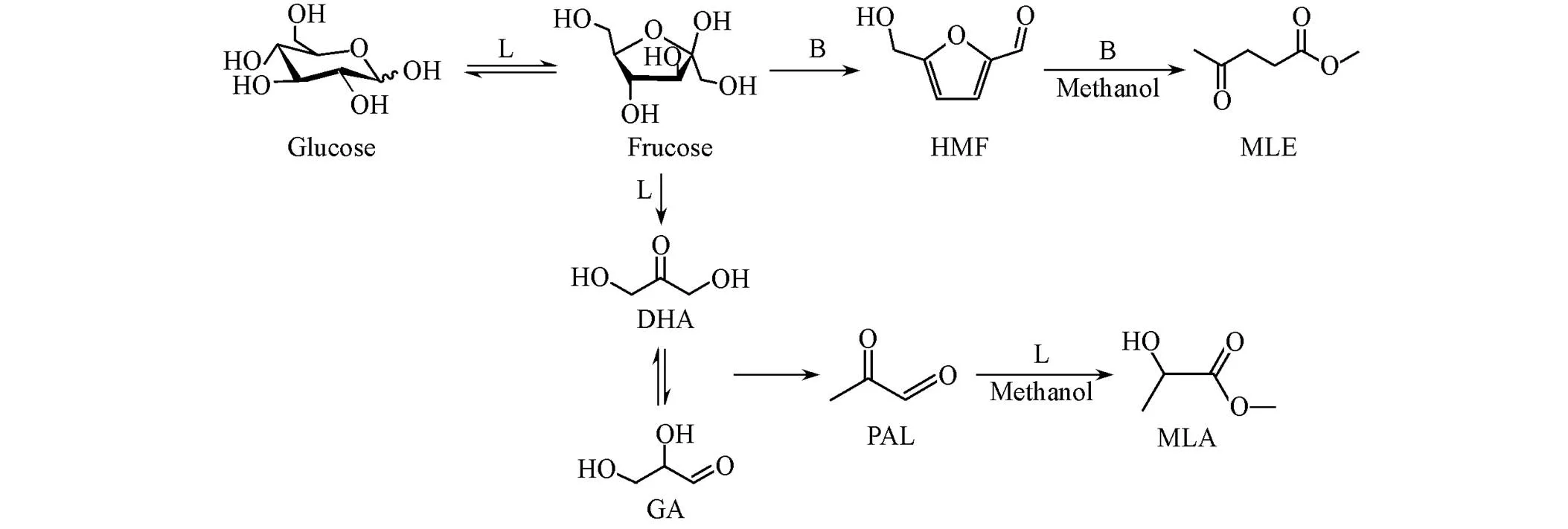
Scheme 1 Reaction scheme of glucose catalyzed by different acid sites in methanol
a. Sn⁃; b. Al⁃; c. Sn⁃/Al⁃; d.Sn⁃Al⁃; e.Na⁃Sn⁃Al⁃
从上述催化反应结果可以看到, Sn-Al-在葡 萄糖转化为MLE的反应中, 表现出很高的催化活 性和MLE选择性, 尽管Sn-/Al-催化剂上具有跟Sn-Al-近似B酸位含量且同时含有锡L酸位, 但由于缺少类似于Sn-Al-的强B酸位, 这可能是导致其催化活性和产物选择性均较差的原因. 这表明在该反应中, 催化剂的B酸位强度是催化性能的决定因素. 主要原因是, B酸催化的果糖脱水生成HMF的过程是葡萄糖转化为MLE反应的决速步骤, 其反应速率受B酸强度的影响[18, 25]. 另外, 在葡萄糖转化反应中, MLE与MLA的选择性受B酸位与L酸位的竞争控制. 更强的B酸强度可提高果糖脱水生成HMF的反应速率, 这增加了对生成MLE反应途径的竞争优势, 同时抑制了生成MLA的反应途径, 从而导致了Sn-Al-分子筛催化剂能够获得更高的MLE选择性.
3 结 论
采用固体NMR探针分子技术对Sn改性分子筛催化剂进行了酸性表征, 并研究了其在葡萄糖转化为MLE的反应中酸位性质与反应性能间的关系. 研究发现, 在Sn-Al-分子筛骨架中引入Sn与Al原子可以分别产生Lewis酸位和Brønsted酸位: Lewis酸位源于骨架四配位Sn原子, Brønsted酸来源于骨架Si—OH—Al桥式羟基. 由于Si—OH—Al桥式羟基在分子筛骨架中的位置不同导致产生3种不同 B酸酸强度, 其中较弱的Brønsted酸位源于孤立的桥式羟基, 中等强度的Brønsted酸位源于与骨架上 Si—OH存在氢键作用的桥式羟基, 而最强的Brønsted酸位与骨架Sn的引入有关, 可能是由于Brønsted酸位和Lewis酸位之间存在协同作用导致的. 通过与只有Brønsted酸位的Al-、 只有Lewis酸位的Sn-以及两者的物理混合样品Sn-/Al-相比, Sn-Al-催化剂上的Brønsted酸位和Lewis酸位之间协同作用产生的强Brønsted酸位, 使其在葡萄糖转化为MLE的反应中表现出最好的催化活性和MLE选择性. 研究结果为高性能生物质转化催化剂的可控构筑提供了指导.
[1] Kubička D., Kubičková I., Čejka J.,, 2013,(1), 1—78
[2] Besson M., Gallezot P., Pinel C.,,2014,(3), 1827—1870
[3] Ennaert T., Van Aelst J., Dijkmans J., De Clercq R., Schutyser W., Dusselier M., Verboekend D., Sels B. F.,,2016,(3), 584—611
[4] Dapsens P. Y., Mondelli C., Pérez⁃Ramírez J.,,2015,(20), 7025—7043
[5] Shamzhy M., Opanasenko M., Concepción P., Martínez A.,,2019,(4), 1095—1149
[6] Ye X. D., Qi G. D., Xu J., Deng F.,,2020,(5), 960—966(叶晓栋, 齐国栋, 徐君, 邓风. 高等学校化学学报,2020,(5), 960—966)
[7] Vispute T. P., Zhang H., Sanna A., Xiao R., Huber G. W.,,2010,(6008), 1222—1227
[8] Taarning E., Osmundsen C. M., Yang X., Voss B., Andersen S. I., Christensen C. H.,,2011,(3), 793—804
[9] Lin L., Sheveleva A. M., da Silva I., Parlett C. M. A., Tang Z., Liu Y., Fan M., Han X., Carter J. H., Tuna F., McInnes E. J. L., Cheng Y., Daemen L. L., Rudic S., Ramirez-Cuesta A. J., Tang C. C., Yang S.,,2020,(1), 86—93
[10] Qi G. D., Ye X. D., Xu J., Deng F.,,2021,(1), 148—164(齐国栋, 叶晓栋, 徐君, 邓风. 高等学校化学学报,2021,(1), 148—164)
[11] Corma A., Nemeth L. T., Renz M., Valencia S.,,2001,(6845), 423—425
[12] Corma A., Domine M. E., Nemeth L., Valencia S.,,2002,(13), 3194—3195
[13] Román-Leshkov Y., Moliner M., Labinger J. A., Davis M. E.,,2010,(47), 8954—8957
[14] Sushkevich V. L., Ivanova I. I., Yakimov A. V.,,2017,(21), 11437—11447
[15] Kuster B. F. M.,, 1990,(8), 314—321
[16] Nikolla E., Román-Leshkov Y., Moliner M., Davis M. E.,, 2011,(4), 408—410
[17] Lew C. M., Rajabbeigi N., Tsapatsis M.,,2012,(14), 5364—5366
[18] Jiang L. Y., Zhou L. P., Chao J. Y., Zhao H. T., Lu T. L., Su Y. L., Yang X. M., Xu J.,,2018,, 589—596
[19] Dijkmans J., Dusselier M., Gabriëls D., Houthoofd K., Magusin P. C. M. M., Huang S., Pontikes Y., Trekels M., Vantomme A., Giebeler L., Oswald S., Sels B. F.,, 2015,(2), 928—940
[20] Li L., Ding J., Jiang J. G., Zhu Z., Wu P.,, 2015,(6), 820—828
[21] Antunes M. M., Lima S., Neves P., Magalhães A. L., Fazio E., Fernandes A., Neri F., Silva C. M., Rocha S. M., Ribeiro M. F., Pillinger M., Urakawa A., Valente A. A.,,2015,, 522—537
[22] Winoto H. P., Ahn B. S., Jae J.,,2016,, 62—71
[23] Yang X., Yang J., Gao B., Lu T., Zhou L.,, 2019,, 105783
[24] Baranowski C. J., Roger M., Bahmanpour A. M., Kröcher O.,,2019,(19), 4421—4431
[25] Sun Z., Xue L., Wang S., Wang X., Shi J.,,2016,(3), 742—752
[26] Zhu Z., Xu H., Jiang J., Wu H., Wu P.,,2017,(93), 12516—12519
[27] Pârvulescu V. I., Coman S. M., Candu N., El Haskouri J., Beltrán D., Amorós P.,,2009,(24), 6693—6700
[28] Qi G., Wang Q., Xu J., Wu Q., Wang C., Zhao X., Meng X., Xiao F., Deng F.,,2018,(1),
[29] Lunsford J. H., Rothwell W. P., Shen W.,,1985,(6), 1540—1547
[30] Guan J., Li X., Yang G., Zhang W., Liu X., Han X., Bao X.,,2009,(1/2), 113—120
[31] Zheng A., Liu S. B., Deng F.,,2017,(19), 12475—12531
[32] Beck L. W., Haw J. F.,,1995,(4), 1076—1079
[33] Fang H., Zheng A., Chu Y., Deng F.,,2010,(29), 12711—12718
[34] Li S., Pourpoint F., Trébosc J., Zhou L., Lafon O., Shen M., Zheng A., Wang Q., Amoureux J. P., Deng F.,,2014,(17), 3068—3072
[35] Qi G., Chu Y., Wang Q., Wang X., Li Y., Trébosc J., Lafon O., Xu J., Deng F.,,2020,(44), 19532—19538
[36] Dai W., Lei Q., Wu G., Guan N., Hunger M., Li L.,,2020,(23), 14135—14146
[37] Pazè C., Zecchina A., Spera S., Cosma A., Merlo E., Spanò G., Girotti G.,,1999,(10), 2627—2629
[38] Zhao X. L., Qi G. D., Wang Q., Chu Y. Y., Gao W., Li S. H., Xu J., Deng F.,,2020,(12), 2681—2689(赵星岭, 齐国栋, 王强, 褚月英, 高伟, 李申慧, 徐君, 邓风. 高等学校化学学报,2020,(12), 2681—2689)
[39] Xu J., Wang Q., Deng F.,,2019,(8), 2179—2189
[40] Arata K., Hino M., Yamagata N.,,1990,(1), 244—246
[41] Emeis C. A.,,1993,, 347—354
[42] Holm M. S., Saravanamurugan S., Taarning E.,, 2010,(5978), 602—605
[43] Takagaki A., Ohara M., Nishimura S., Ebitani K.,,2009, (41), 6276—6278
Role of Catalyst Acidity in Glucose Conversion over Sn-Al-Zeolite as Studied by Solid-state NMR
LIZhiguang1,2, QIGuodong1, XUJun1*, DENGFeng1
(,,,,,430071,;,100049,)
A series ofzeolite catalysts with different acidic properties were prepared. The acidity of these catalysts was characterized by solid-state nuclear magnetic resonance(NMR) probe molecule technique. These catalysts were tested for the conversion of glucose to methyl levulinate.31P NMR of trimethyl phosphine adsorbed on Sn-Al-zeolite showed that the introduction of framework Sn and Al atoms resulted in both Brønsted and Lewis acidity. Three Brønsted acid sites with different acidic strength were distinguished by13C NMR of 2-13C-acetone probe molecule, with one being close to “super acid”, which is most likely generated by the synergistic effect between the spatially adjacent Brønsted and Lewis acid sites. The catalytic reaction of glucose to methyl levulinate showed that Sn-Al-was superior in catalytic activity and selectivity to methyl levulinate as compared to Sn-containing only Lewis acid sites, Al-containing only Brønsted acid sites and the mixed sample of Sn-and Al-. This can be accounted by the synergy of Brønsted and Lewis acid sites and stronger Brønsted acidity of Sn-Al-.
Zeolite; Probe molecule; Acidity; Solid-state nuclear magnetic resonance(NMR); Glucose conversion
O657
A
10.7503/cjcu20220138
2022-03-03
2022-04-17.
徐 君, 男, 博士, 研究员, 主要从事固体核磁共振与多相催化方面的研究. E-mail: xujun@wipm.ac.cn
国家自然科学基金(批准号: 21872170, U1932218, 21733013, 22061130202)和湖北省自然科学基金(批准号: 2021CFA021, 2020CFB552)资助.
Supported by the National Natural Science Foundation of China(Nos. 21872170, U1932218, 21733013, 22061130202) and the Natural Science Foundation of Hubei Province, China(Nos. 2021CFA021, 2020CFB552).
(Ed.: V, K, S)

