一种作为锂离子电池负极材料的不含溶剂分子的镉配位聚合物
陈晓娟 戎红仁 于丽丽 程美令 孙光池 刘 琦
(常州大学石油化工学院,江苏省精细石油化工重点实验室,常州 213164)
0 引 言
锂离子电池(LIB)具有体积小、重量轻、环境友好和无“记忆效应”等优点,是一种具有长循环寿命和高储存容量的储能体系,在便携式电子设备中具有广泛的应用。石墨是LIB最常用的商业化负极材料,其理论容量为372 mAh·g-1,已经无法满足LIB不断增长的能量存储的需求[1-4]。目前,高能量密度的金属或金属氧化物用作LIB的负极材料已被广泛研究。然而,在锂离子的嵌入和脱出过程中,这些材料伴随着巨大的体积变化和滞后电压,导致容量的快速衰减。因此,人们付出了巨大的努力来开发新的负极材料,以提高锂的存储容量[6-8]。
配位聚合物(CPs)是一类由金属离子或金属簇与有机配体通过配位作用而构筑的具有一维、二维或三维结构的化合物,其中的二维或三维的多孔CPs又常称为金属有机骨架(MOFs)。MOFs在光电、催化、气体分离和存储以及能量储存等领域具有广泛的应用前景[9-13]。理论上,多孔CPs可以作为LIB的电极材料,因为它不仅能提供具有氧化-还原活性的金属离子和有机配体,还可以提供有利于电解质离子移动和存储的孔道。CPs作为LIB电极材料可以分为2种途径,一种途径是利用CPs作为前驱体,通过煅烧它们来获得金属氧化物、金属氧化物和碳的复合物或多孔碳[14-16];另外一种途径是直接利用CPs作为电极材料[17-53]。2006年,人们首先选择了MOF-177(Zn4O[1,3,5-benzenetribenzoate]2)作为LIB负极材料[20]。2007年,人们首次考察了MIL-53(Fe)(FeⅢ(OH)0.8F0.2[O2C-C6H4-CO2])作为LIB的正极材料的可能性[21]。随后,人们又制备了许多种作为LIB电极材料的三维和二维结构的CPs(MOFs),如[Zn3(HCOO)6]和[Mn(tfbdc)(4,4′-bpy)(H2O)2][23,26]。与一维有机聚合物聚蒽醌类似[54],一维的CPs同样可以作为LIB的电极材料。最近,Cheng等和我们课题组先后报道了几种基于一维CPs的LIB的负极材料,如[Co1.5L(H2O)4]n(H3L=4-hydroxypyridine-2,6-dicarboxylic acid)[37]、[M(C5O5)(H2O)3]n(M=Cd、Co)[51]、[Zn(H2mpca)2(tfbdc)(H2O)](Zn-ODCP)和[Mn(tfbdc)(Im)4][40,52]。但到目前为止,有关一维CPs作为LIB负极材料的报道还不多。此外,作为LIB负极材料的CPs,大多数都含有溶剂分子或配位溶剂分子;这些溶剂分子通常能与锂发生反应,这是该类电极产生大的初始不可逆容量衰减的原因之一[37,40]。为了减少这种效应,以含有溶剂分子的CPs作为电极材料之前,通常先要采用加热的方法将溶剂分子从CPs中除去[43]。据我们所知,到目前为止,不含溶剂分子/配位溶剂分子的CPs作为LIB的电极材料的报道只有2例:[Co2(OH)2(bdc)]和[Mn(tfbdc)(Im)4][27,52]。因此,开发新的不含溶剂分子的CPs基电极材料,对于推进该类材料在LIB领域的应用是一项有意义的工作。
考虑到基于四氟对苯二甲酸(H2tfbdc)和咪唑类的CPs已经被人们用作LIB的电极材料,如[Cd(tfbdc)(4,4′-bpy)(H2O)2][41]和 Zn(IM)1.5(abIM)0.5[31],我们利用CdCl2、咪唑(Im)和H2tfbdc反应,成功地合成了一种不含溶剂分子的镉基一维CP:[Cd(tfbdc)(Im)4](Cd-TBI)。Cd-TBI作为LIB的负极材料具有良好的循环稳定性和倍率性能,在电流密度50 mA·g-1下,它的初始库仑效率为75.2%,循环50次后还能保持154 mAh·g-1的放电容量。我们的研究工作再次证实一维CPs可以用作LIB的负极材料。
1 实验部分
1.1 试剂
水合氯化镉和Im均购于上海化学试剂公司。所有试剂均为分析纯,使用前不需进一步纯化。H2tfbdc参考文献方法制备[14]。碳酸二甲酯和碳酸乙烯酯产自山东利兴化工有限公司。
1.2 [Cd(tfbdc)(Im)4](Cd-TBI)的合成
将 CdCl2·2.5H2O(0.022 8 g,0.1 mmol)、H2tfbdc(0.047 6 g,0.2 mmol)和 Im(0.068 1 g,0.1 mmol)溶于含有3 mL甲醇、3 mL去离子水和3 mLN,N-二甲基甲酰胺的混合溶剂中,室温搅拌2 h后过滤,得到无色溶液。将所得无色溶液于室温下静置,约一个月后,溶液中出现无色透明的块状晶体,收集晶体。元素分析按C20H16CdF4N8O4计算的理论值(%):C 38.69,H 2.60,N 18.05;实验值(%):C 38.53,H 2.54,N 18.15。红外光谱数据(KBr压片,cm-1):3 145(s),3 059(s),2 950(s),2 858(s),2 727(m),2 629(m),1 605(s),1 539(m),1 457(s),1 364(s),1 321(m),1 249(w),1 170(w),1 141(w),1 069(s),983(s),938(m),887(m),836(m),758(m),731(s),655(m),621(m),462(m)。
1.3 单晶衍射数据的收集和结构解析
从所合成的单晶中,选出大小为0.30 mm×0.20 mm×0.10 mm的单晶,在Bruker Smart Apex CCD单晶衍射仪上采用经石墨单色器单色化的MoKα射线(λ=0.071 073 nm),在2.32°<θ<25.0°范围,于296(2)K下运用φ-ω扫描方式收集Cd-TBI的衍射数据,数据经过Lp因子和经验吸收校正。采用SHELXS-97程序直接法解出晶体结构,部分非氢原子坐标是经多次差值傅里叶合成得到。所有非氢原子的坐标及各向异性热参数用SHELXL-97程序,并以全矩阵最小二乘法对结构进行精修。Cd-TBI中的氢原子采用理论加氢,利用全矩阵最小二乘法对其各向同性热参数进行修正。Cd-TBI的晶体学数据列于表1中。
1.4 表征
利用Nicolet 460型红外光谱仪和溴化钾压片法测试合成的Cd-TBI的FT-IR光谱。利用X射线衍射仪(D/max 2500 PC,Rigaku)收集Cd-TBI样品的粉末X射线衍射(PXRD)数据,仪器的扫描范围2θ=10°~80°,管电流和管电压分别为300 mA和60 kV,采用CuKα辐射(λ=0.154 06 nm)。采用 ESCALABMK Ⅱ型X射线光电子能谱仪对样品进行X射线光电子能谱(XPS)的测定。采用透射电子显微镜(TEM,JEM-2100,加速电压200 kV)和场发射扫描电子显微镜(FESEM,日立S-4800,加速电压20 kV)研究样品的形貌和微观结构。在液氮温度为77 K的条件下,使用表面孔径吸附仪(ASAP2010C)测定Cd-TBI样品的N2吸附-脱附等温线,利用Brunauer-Emmett-Teller(BET)方法计算样品的比表面积,采用Barrett-Joyner-Halenda(BJH)方法计算样品的孔径大小和孔体积。在氮气气氛下,在TG 209 F3热分析仪上测试Cd-TBI样品的热重曲线,测试的升温速率为10℃·min-1,温度范围为室温至800℃。
1.5 电化学测定
Cd-TBI工作电极的制备程序如下:将Cd-TBI(活性物质)、乙炔黑(导电剂)以及聚偏氟乙烯(黏结剂)按6∶3∶1的质量比放入研钵中进行混合,并研磨至均匀,然后加入适量的N-甲基吡咯烷酮,继续混合成胶状物。将所得胶状物均匀涂覆在铜箔上,在80℃下真空干燥12 h,然后将铜箔裁剪成半径为10 mm的电极片,并在压片机上压实。每个电极片上活性物质的质量约为0.84 mg。组装成CR2032型纽扣式电池进行电化学性能测试。纽扣式电池的组装程序如下:在充满氩气的Etelux敞开型手套箱LAB2000中,将Celgard2400隔膜置于纯锂片(对电极)和Cd-TBI工作电极之间,然后以含有1 mol·L-1LiPF6的碳酸乙烯酯(EC)、碳酸二甲酯(DMC)和碳酸二乙酯(DEC)混合溶液(体积比为1∶1∶1)作电解质溶液。电化学测试之前,需将组装好的纽扣式电池搁置10 h。在0.01~3.0 V的扫描电压范围和0.1 mV·s-1的扫描速度下,利用电化学工作站(CHI600E,北京华科)测试循环伏安(CV)曲线。在振幅为5 mV和频率范围为0.1~105Hz条件下,采用CHI600E电化学工作站检测交流阻抗谱图。使用电池性能测试系统(CT-3008W-5V10mA-S4,深圳新威尔)测试纽扣式电池的充放电性能和倍率性能,电压范围为0.01~3.0 V。电池的比容量根据Cd-TBI的质量计算,比容量单位为mAh·g-1。
2 结果与讨论
2.1 Cd-TBI的晶体结构
Cd-TBI的不对称单元包括一个Cd(Ⅱ)离子、半个tfbdc2-阴离子和2个Im分子。从图1a可以看出,Cd(Ⅱ)离子与来自2个tfbdc2-的2个氧原子和来自4个Im的4个氮原子配位,形成了一个八面体构型。八面体的轴向位置由O1和O1A原子占据,赤道平面的位置由4个N原子占据。如表2所示,Cd1—O(0.228 53 nm)和 Cd1—N(0.226 16~0.226 69 nm)键长接近文献报道的Cd(Ⅱ)配合物中的键长值[41],键角N1A—Cd1—N1、O1—Cd1—O1A 和 N3—Cd1—O1分别为 180.00(8)°、180.00(5)°和 87.86(5)°。如图1b所示,每个tfbdc2-通过单齿连接相邻的Cd(Ⅱ)离子,形成一维链结构。从表S1(Supporting information)中可以看出,在Cd-TBI晶体中存在4种氢键(N—H…O、O—H…O、C—H…O和C—H…F)。上述的一维链通过这几种氢键相互连接,产生一个沿b轴具有一维通道的三维超分子结构(图1c)。

表2 配合物Cd-TBI中的主要键长(nm)和键角(°)Table 2 Selected bond lengths(nm)and bond angles(°)for Cd-TBI
2.2 表 征
Cd-TBI的红外光谱如图2a所示。3 264 cm-1处的强峰归属于νs(N—H),来自Im分子;来自tfbdc2-的νas(OCO)和νs(OCO)的伸缩振动峰分别出现在1 604和1 369 cm-1;位于1 539和762 cm-1处的峰应属于C—N键伸缩振动和δ(OCO)的弯曲振动[41];Cd—O键伸缩振动峰出现在463 cm-1。这些结果表明Cd(Ⅱ)离子与tfbdc2-之间形成了配位键[41]。Cd-TBI的PXRD图与基于Cd-TBI单晶衍射数据的模拟图一致(图2b),这表明它具有纯的固体相。Cd-TBI的热重曲线如图S1所示。Cd-TBI在182℃之前相当稳定,但Cd-TBI的快速分解发生在182~230℃之间;之后,剩余的物质逐渐分解。
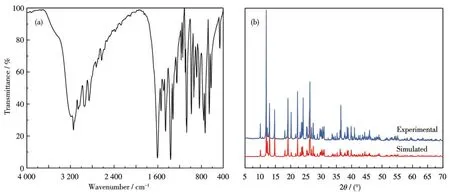
图2 Cd-TBI的(a)红外光谱和(b)XRD图Fig.2 (a)IR spectrum and(b)XRD patterns of Cd-TBI
2.3 电化学性能
采用恒电流循环试验研究了Cd-TBI电极的电化学性能。从图3a的Cd-TBI电极的充放电曲线中,我们可以发现在50 mA·g-1的电流密度下,Cd-TBI电极的初始充放电容量分别为121和161 mAh·g-1,对应于75.2%的库仑效率。初始库仑效率较低主要与电解质分解和固体电解质界面(SEI)的产生有关,起源于锂离子在Cd-TBI中的不可逆插入[23,26]。由于Cd-TBI中没有溶剂分子,其初始库仑效率高于许多其他CPs(表S2)。在50 mA·g-1电流密度下,考察了Cd-TBI电极的循环性能。如图3b所示,由于副反应的消失和SEI的形成,库仑效率在第3次循环中增加到91%,并且在第50次循环中仍然保持为99.2%,这表明Cd-TBI电极材料具有良好的循环稳定性。令人印象深刻的是,经过50次循环后,Cd-TBI电极放电容量还保持为154 mAh·g-1,容量保持率高达95.7%。为了了解不同电流密度下电极的放电容量和循环稳定性,我们测试了Cd-TBI电极的倍率性能。图3c展示了在不同电流密度下(50~1 000 mA·g-1)Cd-TBI电极的充放电容量。当电流密度为50、100、300、500和1 000 mA·g-1时,Cd-TBI电极的平均放电容量分别为147、145、128、110和97 mAh·g-1。更引人注目的是,随着电流密度恢复到50 mA·g-1,其放电容量达176 mAh·g-1,这表明Cd-TBI不仅具有良好的倍率性能,而且在倍率测试的循环过程中电极性能被进一步激活。

图3 Cd-TBI电极的电化学性能:(a)在50 mA·g-1下,电压范围0.01~3.0 V内的充放电曲线;(b)循环性能;(c)不同电流密度下的倍率性能;(d)EIS谱图Fig.3 Electrochemical performance of the Cd-TBI electrode:(a)charge-discharge curves in a range of 0.01-3.0 V at 50 mA·g-1;(b)cycling performance at 50 mA·g-1;(c)rate performance at different current densities;(d)EIS spectra
为了进一步探索Cd-TBI电极的电化学反应动力学,我们测量了其电化学阻抗谱(EIS)。图3d显示了Cd-TBI电极在第1次和第50次循环后的EIS谱图。从图3d可以看出,每条EIS曲线都是由一个位于高频区的半椭圆和一条位于低频区的斜线组成。根据2条曲线跟横坐标相交的点几乎相同,可以得出1次循环后和50次循环后的电解质溶液电阻也是相同的(约为5 Ω),这说明Cd-TBI具有优良的稳定性。50次循环后的电荷转移电阻值约为118 Ω,要小于1次循环后的电荷转移电阻值(约为152 Ω),这可能要归因于50次循环后Cd-TBI电极具有更好的浸润性和连接性。较小的电荷转移电阻值证实了Li+脱嵌过程中的快速电子传输[14]。此外,2条EIS曲线相位角都大于45°,这表明离子迁移性良好。
采用CV法进一步评估Cd-TBI电极的电化学性能。根据图4a所示Cd-TBI电极的CV曲线,我们可以观察到在第1次循环的负向扫描过程中,2个还原峰分别出现在0.69和0.1 V左右,这可能要归属于SEI膜的形成、Cd2+离子还原成Cd以及Li+离子嵌入Cd-TBI中,这表明[Cd(Ⅱ)(tfbdc)(Im)4]变成了[Cd(0)Lin+2(tfbdc)(Im)4]。在第1次循环的正向扫描过程中,0.76 V附近处出现了1个氧化峰。这是因为Cd被氧化为Cd2+离子,与Li+离子发生脱嵌。但在第2次循环时,还原峰的位置从0.69 V附近迁移到0.9 V附近。在第3次循环之后,CV曲线几乎重叠,这表明Cd-TBI电极的稳定性优越。我们推测Cd-TBI电极经历的可逆反应可能如式1和2所示:

图4 Cd-TBI电极的CV曲线Fig.4 CV curves of the Cd-TBI electrode

已经报道的一些过渡金属CPs基电极材料,如Mn-TBI[52]和Zn-ODCP[40],也经历了类似的反应过程。Li+离子可能是通过与来自tfbdc2-的羧酸根上的氧原子以及苯环上的碳原子作用而嵌入Cd-TBI中[52]。此外,Cd-TBI电极的放电容量除了来自上述电极反应的贡献外,可能还有一部分来自电容贡献,正如[Mn(tfbdc)(4,4′-bpy)(H2O)2]电极那样[26]。
3 结 论
我们成功地合成了一个一维CP([Cd(tfbdc)(Im)4],Cd-TBI)。当利用Cd-TBI作为LIB的负极材料时,在50 mA·g-1电流密度下循环50次后,Cd-TBI电极的放电容量保持率为95.7%,显示了其良好的循环稳定性。Cd(Ⅱ)离子和Cd-TBI中的有机配体tfbdc2-可能都参与了容量贡献。本研究再次证实一维CPs与二维/三维多孔CPs类似,可以作为LIB的负极材料。值得一提的是,一维的不含溶剂的镉CP作为LIB的负极材料,是首次被报道。与其他CPs电极材料相比,尽管Cd-TBI电极的放电容量不高,但通过研究Cd-TBI的电化学性能与其结构和组成的关系,将为今后设计与合成新的高性能CPs基负极材料提供参考,相关的研究工作正在我们实验室开展。
Supporting information is available at http://www.wjhxxb.cn

