乳块散结颗粒制备工艺研究
周维利,孙铜,王坤
(山东省食品药品检验研究院,山东 济南 250101)
乳块散结颗粒由丹参、川楝子、皂角刺、柴胡(醋制)、赤芍、醋香附、夏枯草、鳖甲(醋制)、橘叶、昆布、王不留行和淫羊藿组成,功能活血化瘀,疏肝理气,软坚散结。临床上用于肝气瘀滞,痰瘀互结所致的乳腺增生。本试验以丹参素含量为指标,对其提取和制备工艺进行了研究,现报道如下。
1 仪器与材料
1.1 仪器 HS-337电子分析天平(邢台慧思科技有限公司);ESJ203-S电子分析天平(洛阳美优实验设备有限公司);KQ3200DE型数控超声波清洗器(昆山市超声仪器有限公司);岛津LC-20高效液相色谱仪(岛津);Shimpack VP-ODS(C18柱,4.6 mm×250 mm,5 μm);LC-RE-5000旋转蒸发仪(上海力辰仪器科技有限公司);101-1AB电热恒温干燥箱(金坛市水北科普实验仪器厂)。提取设备、离心机。
1.2 试剂 丹参、川楝子、皂角刺、柴胡(醋制)等药材饮片(济南漱玉平民大药房有限公司)、丹参素对照品(110855-201614,20 mg/支,标示含量98.1%,中国食品药品检定研究院);乳块散结颗粒(自制);阴性对样品(自制);乙腈、甲醇和冰醋酸为色谱纯,水为重蒸去离子水,草酸为分析纯。
2 方法与结果
2.1 丹参素含量测定方法
2.1.1 色谱条件与系统适应性试验[1-6]以十八烷基硅烷键合硅胶为填充剂;以乙腈-甲醇-水-冰醋酸(0.5∶8∶92∶1)为流动相;检测波长为280 nm。理论板数按丹参素峰计算不得低于3 500。
2.1.2 对照品溶液 取丹参素钠对照品适量,精密称定,加50%甲醇溶液制成每1 mL含50 μg的溶液(相当于每1含丹参素45 μg),即得[7]。
2.1.3 供试品溶液 ①取乳块散结颗粒适量,研细,取约1.0 g,精密称定,置离心管中,加水2 mL及中性氧化铝(100~200目)1.5 g,搅拌均匀,用水洗涤3次,每次10 mL,离心(3 000 r·min-1)弃去水洗液,再用5%草酸溶液搅拌提取3次,每次8 mL,离心,合并5%草酸溶液,置25 mL量瓶中,加5%草酸溶液至刻度,摇匀,滤过,取续滤液,即得[7];②取工艺研究试验得清膏2 mL,置离心管中,中性氧化铝(100~200目)1.5 g,搅拌均匀,同①操作,即得。
2.1.4 阴性溶液 制备不含丹参的乳块散结颗粒,按“2.1.3”项下操作,即得阴性样品。
2.1.5 专属性 分别取乳块散结颗粒供试品、丹参素对照品以及阴性对照3种溶液,按“2.1.1”项下色谱条件进样、测定,不含丹参的阴性对照在丹参素峰处无干扰,见图1~3。
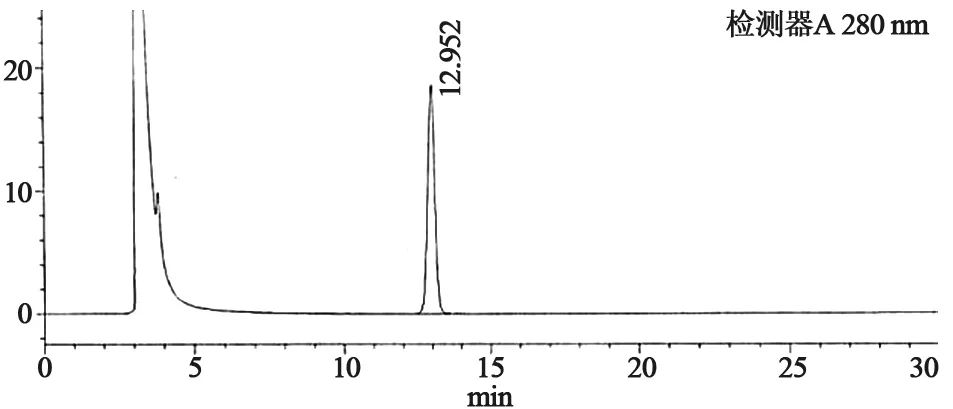
图1 丹参素对照品HPLC图
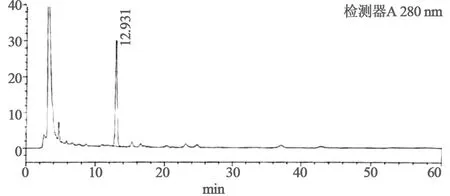
图2 乳块散结颗粒HPLC图
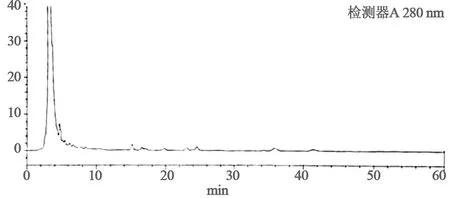
图3 不含丹参阴性HPLC图
2.1.6 线性与范围 取丹参素钠对照品适量,精密称定,加5%草酸溶液溶解并稀释至刻度,作为丹参素钠对照品贮备液(相当于含丹参素264.55 g·mL-1);分别精密量取1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0 mL贮备液置25 mL量瓶中,用5%草酸溶液稀释至刻度,摇匀,作为丹参素对照品溶液。分别吸取上述对照品溶液,按“2.1.1”项下条件进样、测定,以浓度C和峰面积A计算,得回归方程为A=78 937C+928.57,R2=0.999 3;丹参素在10.58~84.65 μg·mL-1范围内,峰面积与浓度呈良好线性关系。
2.1.7 精密度试验 取丹参素对照品溶液(42.33 μg·mL-1)按“2.1.1”项下色谱条件进样、测定,连续进样6次,峰面积RSD为1.21%。
2.1.8 重复性试验 取20200502批乳块散结颗粒(1.02 mg·g-1)样品6份,按“2.1.3”项下制备,按“2.1.1”项下色谱条件进样、测定,重复测定6次,丹参素含量的RSD为0.996%。
2.1.9 稳定性试验 取20200502批乳块散结颗粒供试品溶液分别于0、2、4、6、8和12 h进样测定,丹参素峰面积RSD为0.867%,供试品溶液在室温条件下在12 h内稳定。
2.1.10 回收率试验 取20200502批乳块散结颗粒适量,研细,取约0.5 g,精密称定,取6份,照“2.1.3”项下方法处理,并分别加入丹参素对照品溶液(52.91 μg·mL-1)10.0 mL,混匀,按“2.1.1”项下色谱条件进样、测定,丹参素平均回收率为97.45%,RSD为1.56%。
2.2 工艺研究
2.2.1 提取工艺研究 通过预试验及参考相关文献,经预试验后以水为提取溶剂。分别称取丹参200 g、川楝子40 g、皂角刺64 g、柴胡(醋制)48 g、赤芍56 g、醋香附40 g、夏枯草40 g、鳖甲(醋制)40 g、王不留行64 g、橘叶64 g、昆布64 g、淫羊藿80 g,共9份,每份计800 g,按表1进行试验,以丹参素含量为评价指标进行试验,因素水平见表1~3。

表1 水提因素水平表
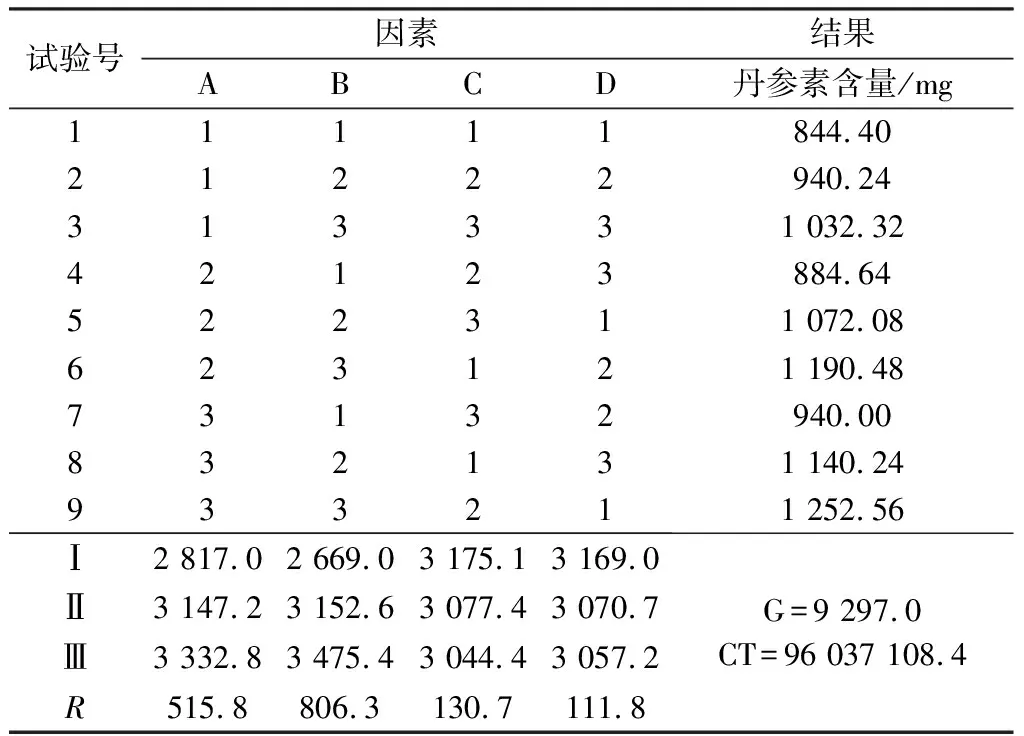
表2 L9(34)正交试验设计与结果
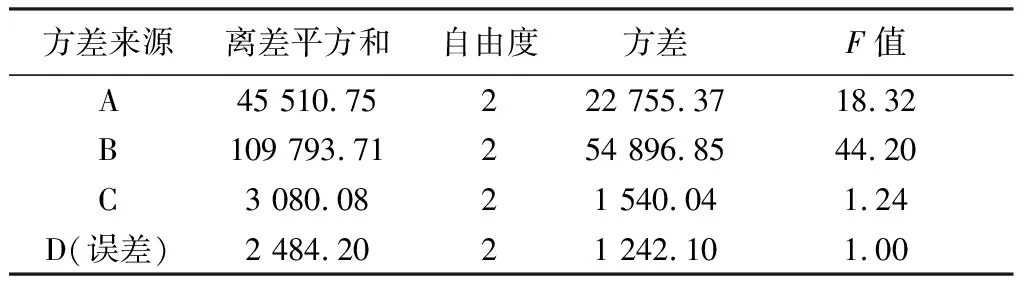
表3 水提方差分析
由直观分析可知,各因素影响依次为B>A>C,最佳为A3B3C2(药材加8倍量水提取3次,每次3 h);考虑到生产成本、效率和人工等因素,综合考虑选择A2B2C1(药材加8倍量水提取2次,每次2 h)。
2.2.2 提取工艺验证 称取乳块散结颗粒处方中各药材饮片6份,每份800 g,分别按A3B3C1和A2B2C1各提取3次,浓缩为1.26(80 ℃)的清膏,测定丹参素含量,结果见表4。
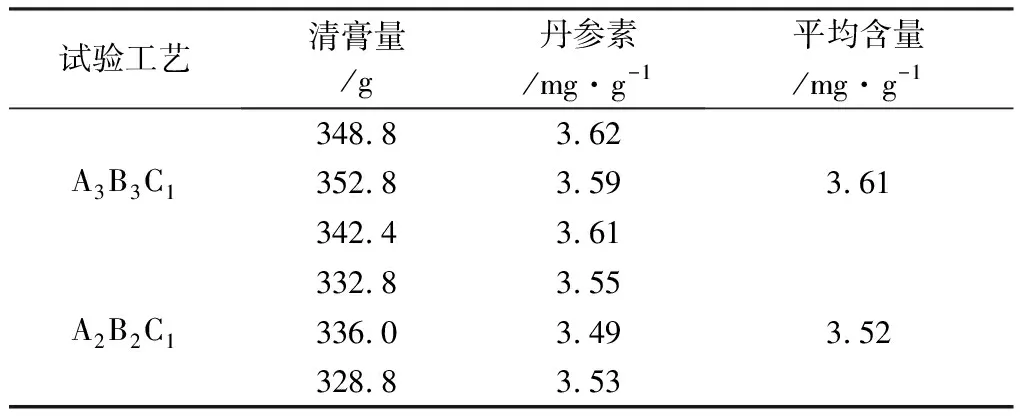
表4 提取工艺验证试验结果表
按A3B3C1与A2B2C1工艺各提取3次,工艺A2B2C1与工艺A3B3C1相比,丹参素含量基本无差别,故选择按A2B2C1进行提取。
2.2.3 醇沉工艺研究
2.2.3.1 醇沉浓度试验 称取乳块散结颗粒处方中各药材饮片4份,每份800 g,按A2B2C1提取,提取液滤过,滤液合并浓缩至1.27(80 ℃)的清膏,分成4份,以不同含醇量进行醇沉,搅匀,静置48 h,滤取上清液,回收乙醇,浓缩为稠膏,测定丹参素含量与稠膏率,结果见表5。
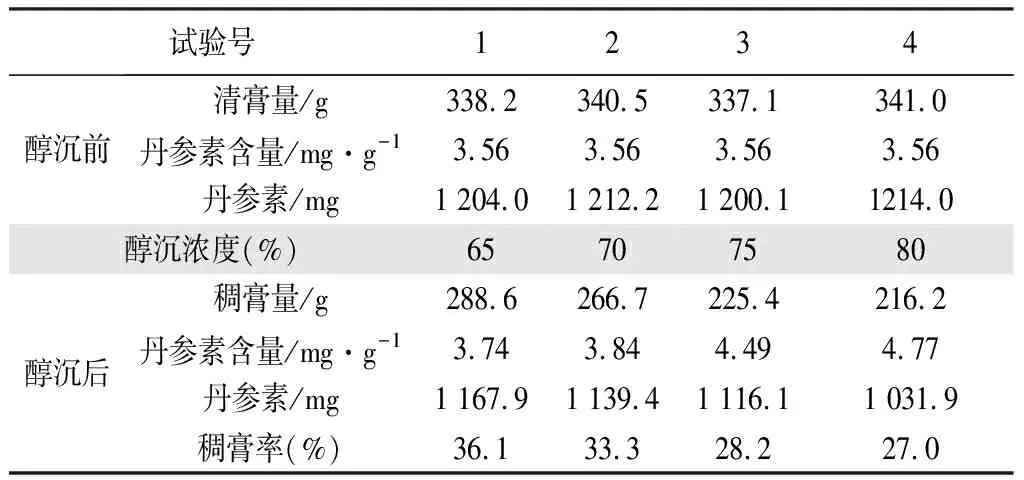
表5 醇沉浓度试验结果表
乙醇浓度为75%进行醇沉时丹参素含量与出稠膏均合适,故选择醇沉浓度为75%。
2.2.3.2 静置时间试验 按“2.2.3.1”项下方法制备清膏,测定含量,分成4份,加乙醇进行醇沉,静置不同时间,滤取上清液,回收乙醇,浓缩为稠膏,测定丹参素含量与稠膏率,结果见表6。

表6 醇沉后静置时间试验结果表
药液静置48 h,分层明显,容易过滤,故选择静置时间为48 h。
2.2.4 成型工艺研究 取丹参200 g、川楝子40 g、皂角刺64 g、柴胡(醋制)48 g、赤芍56 g、醋香附40 g、夏枯草40 g、鳖甲(醋制)40 g、王不留行64 g、橘叶64 g、昆布64 g、淫羊藿80 g,每份计800 g,4份,按“2.2.3.1”项下方法制备清膏,使乙醇浓度达75%,醇沉,静置,滤过,回收乙醇,浓缩为稠膏,分成4份,加入不赋形剂制软材,以14目尼龙网筛制粒,75 ℃干燥,16目筛整粒。
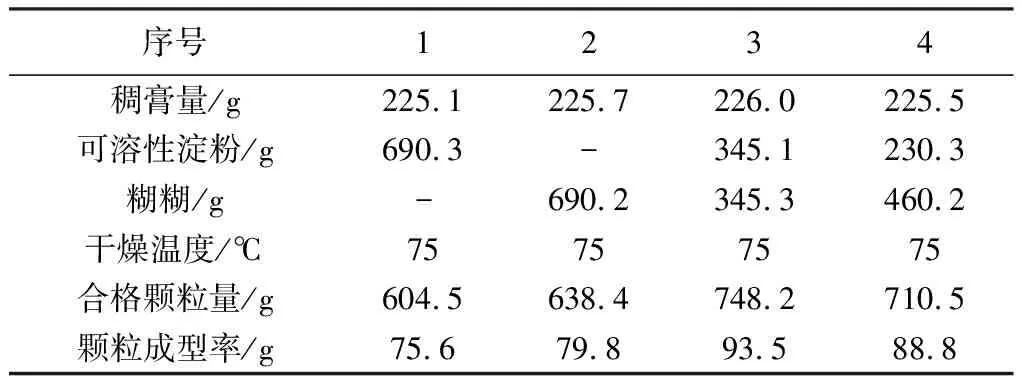
表7 赋形剂试验结果表
结果:在成型试验中,以可溶性淀粉与糊精(1∶1)赋形剂时易制粒,颗粒成型率最佳。
3 讨论
3.1 处方中药材饮片的各主要药理成分均溶于水,以水溶性成分丹参素含量为指标,经预试验后以水为溶剂进行了正交优选,对乳块散结颗粒的最佳直观工艺和综合考虑后提取工艺各进行3批验证试验,最终选定提取工艺为药材饮片加8倍量水提取2次,每次2 h。为最大可能保留有效成分,易于成型,减少颗粒装量,便于患者服用,水提液浓缩至相对密度为1.25~1.30(80 ℃)时进行了醇沉,减少出膏量。
3.2 可溶性淀粉为白色细腻粉末,是可溶颗粒的良好稀释剂,并有矫味及黏合作用;糊精为白色或微带黄色的细腻粉末,不溶于醇,微溶于水,能溶于沸水成黏胶状溶液,黏性强,并呈弱酸性[8]。在颗粒的成型试验中,醇沉后上清液浓缩成稠膏,加入可溶性淀粉与糊精(1∶1)为赋形剂制粒,在赋形剂与稠膏比大于3时易于制粒,颗粒成型性好,简化了清膏干燥、粉碎的工序,可节约资源与人工,提高生产效率。

