固定化酵母对金属离子吸附性能的研究
孟君,丁慧娇,陈鑫,张峻松,韩永辉,郑炬萍
郑州轻工业学院食品与生物工程学院(郑州 450002)
随着生活水平的提高,含重金属的污染物通过各种途径进入生活的各个方面,造成严重的环境污染。其中,空气、土壤和水中的有毒重金属对环境的严重威胁正逐渐成为全球性问题,因此与环境相关的有毒重金属离子的有效去除与分离技术就成为一项富于挑战性的工作[1]。常用重金属废水处理方法有化学沉淀法、离子交换法、电化学法、膜过滤等[2]。与这几种处理方法相比,生物吸附法作为新兴的水体重金属污染处理方式具有效率高、成本低、价格低廉、吸附迅速、废弃物便于储存与分离等特点受到广泛关注[3-4]。国内外研究现状,自从20世纪70年代生物吸附引起关注以来,生物吸附的研究变得非常活跃[5]。近年来的大量研究表明,一些微生物如细菌、真菌藻类对重金属有很强的吸附作用[6]。其中,酿酒厂的废菌体啤酒酵母(Saccharomyces cerevisiae)是具有实用潜力的生物吸附剂[7]。以啤酒酵母吸附法处理重金属废水的优点:价格低廉,制备方法简单,吸附效果好,具有良好的稳定性,天然、无毒、不造成生态系统的二次污染。因此,啤酒酵母将在重金属废水处理中具有良好的应用前景。游离的和悬浮的微生物生物量的缺点是颗粒小、机械强度低,处理后的生物量与出水难以分开,采用固定化细胞可以克服这些缺点[8]。
试验选择酿酒酵母,采用海藻酸钠包埋的方法进行固定化,探讨固定化酵母对重金属离子的吸附性能以及吸附条件对吸附率的影响,具有一定现实意义。
1 材料与方法
1.1 材料与试剂
安琪酿酒高活性干酵母(白酒专用耐高温型);浓硝酸(优级纯,烟台市双双化工有限公司);盐酸(优级纯,烟台市双双化工有限公司);氢氧化钠(分析纯,天津市德恩化学试剂有限公司);CuCl2·2H2O(分析纯,广东汕头市西陇化工厂);MnCl2·4H2O(分析纯,广东-汕头市西陇化工厂);铅、铜、锌、镉,锰单元素标准溶液(GB,1 000 μg/mL,国家标准物质研究中心);无水葡萄糖(分析纯,天津市科密欧化学试剂有限公司);无水氯化钙(分析纯,天津百伦斯生物技术有限公司);海藻酸钠(食品级,河南三化生物科技有限公司);试验用水均为去离子水。
1.2 仪器与设备
电子天平(上海浦春计量仪器有限公司);恒温培养摇床(THZ-100,上海一恒科技仪器有限公司);pH计(pHS-2C实验室pH计,上海仪电科学仪器股份有限公司);原子吸收光谱仪(AA240FS,美国瓦里安公司);元素空心阴极灯(美国瓦里安公司);容量瓶,试管,烧杯,玻璃棒,移液管等。所有试验玻璃仪器用前均用10% HNO3浸泡过夜,并用去离子水洗干净。
1.3 方法
1.3.1 固定化酵母的制备
称取4 g酿酒活性干酵母放置于50 mL烧杯中,加入10 mL 2%葡萄糖溶液进行活化,活化至出气泡(时间约10 min)。加入100 g海藻酸钠水溶液(质量分数2.5%),将其混合均匀。将混合液吸入针筒中,滴入约含300 mL氯化钙溶液(质量分数10%)的500 mL烧杯中,注意滴出的速度和下落高度,使凝胶颗粒保持均匀一致。滴完后使其在氯化钙溶液中浸泡60 min,得到海藻酸钠固定化酵母球形颗粒,用蒸馏水冲洗3次,放入冰箱里备用。
1.3.2 试验方法
配制5种重金属水溶液,加入一定量固定化酿酒酵母吸附剂,采用火焰原子吸收分光光度法,测定不同条件下吸附前后水溶液中相应离子浓度,计算吸附剂对离子的吸附率和吸附量,每个条件下的试验重复3次,结果取平均值,并与空白吸附试验对照。
1.3.2.1 标准工作系列及工作方程的建立
标准曲线的制作:准确吸取各重金属元素标准贮备液,用去离子水配制成各元素浓度范围的标准系列Mn:0.5,1.0,1.5,2.0,2.5 mg/L,Pb:1.0,2.0,3.0,4.0,5.0 mg/L,Cu:1.0,2.0,3.0,5.0,7.0,9.0 mg/L,Zn:0.2,0.4,0.6,0.8,1.0 mg/L,Cd:0.4,0.6,0.8,1.0,1.2 mg/L。在各元素测定的最佳条件下,上机测定各元素相应的标准系列溶液得Mn、Pb、Cu、Zn、Cd相应的回归方程分别为:A=0.240 03C+0.004 48,A=0.050 27C+0.026 08,相关系数为0.999 6,Cu:A=0.100 34C+0.038 49,Zn:A=0.559 64C+0.003 45,Cd:A=0.106 34C+0.324 72,相关系数依次为0.998 9,0.999 6,0.991 4,0.999 0,0.993 2。
1.3.2.2 样品测定
在5种重金属元素标准系列溶液测定的最佳条件下,依次测定不同条件下的样品溶液中对应元素吸光度,由制订的各元素的标准曲线方程,得样品溶液中待测离子含量。
2 结果与分析
2.1 固定化酿酒酵母对5种重金属离子的吸附效率
分别配制50 mg/L的5种重金属离子的溶液,使离子溶液pH范围为2~3,分别吸取3 mL该质量浓度的溶液到试管中,依次加入1.3.1中制备的固定化后酵母吸附剂1.0 g,在30 ℃、转速180 r/min条件下,在恒温振荡摇床中振荡吸附1 h后,从对应试管中各吸取1 mL,用0.45 μm的微孔滤膜过滤,稀释50倍后,用原子吸收光谱仪,测定加入吸附剂前后溶液中相应离子浓度,计算固定化酵母吸附剂对5种重金属的吸附效率。吸附效果见图1。
从图1中可以看出,相同条件下,该吸附剂对5种重金属离子的去除效率依次Cu2+>Mn2+>Pb2+>Zn2+>Cd2+,固定化酿酒酵母对Cu2+、Mn2+的吸附率较高,因此,试验选择Cu2+、Mn2+作为研究对象。

图1 固定化酿酒酵母对5种重金属离子的吸附效率
2.2 影响固定化酵母吸附性能的因素
为使生物吸附剂达到使用的理想状态,对影响生物吸附剂吸附性能的因素进行考察研究,从而确立最佳吸附条件[9]。
2.2.1 重金属离子初始质量浓度对吸附效率的影响
配制Cu2+、Mn2+系列质量浓度为10,20,30,40和50 mg/L,取3 mL不同浓度系列Cu2+、Mn2+的溶液于40 mL试管中,分别加入1.3.1制备的固定化酵母各1.0 g,混合后,用1%的HCl和0.1 mol/L的NaOH将溶液调至pH 2.0~3.0,在30 ℃、转速180 r/min条件下,在恒温振荡摇床中振荡,吸附1 h。从各自对应试管中吸取1 mL,稀释50倍,用火焰原子吸收光谱仪,测定加入吸附剂前后溶液所含待测重金属离子的质量浓度,每个条件做3个平行样,结果取平均值,根据测定结果,计算固定化酿酒酵母吸附剂对两种离子的吸附率,结果见图2。
从图2可以看出,Mn2+初始质量浓度在10~40 mg/L,固定化酿酒酵母对锰离子的吸附效率不断增大,40~50 mg/L之间吸附效率呈下降趋势,锰离子的最佳吸附质量浓度为40 mg/L;而Cu2+初始质量浓度在10~50 mg/L之间呈上升趋势,50 mg/L的吸附率达53.15%,为进一步考察吸附剂对Cu2+吸附的最佳质量浓度,将Cu2+初始质量浓度设定为100,150,200,250和300 mg/L。

图2 Mn2+、Cu2+的初始质量浓度对吸附效率的影响
由图2可以看出,在Cu2+初始质量浓度为100~300 mg/L时,随着溶液中重金属离子初始质量浓度增加,吸附效率先升高再降低。Cu2+初始质量浓度为250 mg/L时,固定化酵母具有较好的吸附效果,但较50 mg/L时的低。因此,固定化酵母吸附Cu2+的浓度最佳质量浓度选取50 mg/L。
2.2.2 吸附剂投放量对重金属吸附效率的影响
分别将0.5,1.0,1.5,2.0和2.5 g的固定化酿酒酵母吸附剂,依次加入有3 mL 40 mg/L Mn2+、50 mg/L Cu2+的溶液试管中,混合均匀,吸附1 h,从对应试管中各取1 mL,稀释50倍,测定溶液加入吸附剂前后相应离子浓度,根据测定结果,比较不同投放量的固定化酿酒酵母吸附剂对Mn2+、Cu2+离子的吸附效果,根据吸附率选出吸附剂最佳的投放量,试验结果见图3和图4所示。
从图3可以看出,Mn2+、Cu2+吸附率随着吸附剂投放量增加呈上升趋势,且上升趋势比较明显,固定化酿酒酵母对锰离子的吸附呈现缓慢上升趋势。

图3 不同吸附剂投放量对Mn2+、 Cu2+的吸附效率的影响
从图4可以看出,单位吸附剂投放量1.5 g时,Cu2+吸附效率最大,单位吸附剂投放量2 g时,Mn2+吸附效率在最大。这主要是因为固定化酿酒酵母的投加量增加,为重金属离子提供了更多的吸附位点,而溶液中Cu2+和 Mn2+的量是一定的,因而有更多的重金属离子被吸附,去除率升高。总体来说,Mn2+、Cu2+单位吸附剂投放量吸附效率随着固定化酿酒酵母投加量的增加而减少,这是因为固定化酿酒酵母的投加量增加,而溶液中重金属离子总量一定,导致吸附剂上大量吸附位点没有被利用,单位吸附剂吸附的重金属离子的量减少。考虑运行成本,选择吸附剂最佳投放量为1.5 g固定化酿酒酵母用于吸附Cu2+,2 g固定化酿酒酵母吸附用于吸附Mn2+。

图4 单位吸附剂投放量Mn2+、 Cu2+的吸附效率
2.2.3 吸附时间对吸附效率的影响
吸附时间是表征吸附剂对重金属离子吸附过程的重要参数。以Mn2+40 mg/L、Cu2+50 mg/L,固定化酿酒酵母吸附剂2.0 g和1.5 g,混合后振荡吸附,每隔1 h取1次样,考察1,2,3,4和5 h吸附时间对吸附性能的影响,试验结果见图5和图6所示。

图5 Mn2+、Cu2+的不同吸附时间变化对吸附效率的影响
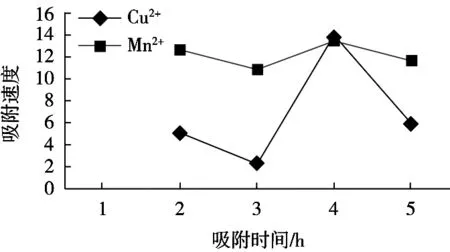
图6 不同吸附时间变化对Mn2+、 Cu2+的吸附速度的影响
从图5可以看出,随着吸附时间的增加,Mn2+、Cu2+吸附率呈上升趋势,铜离子在3~4 h之间上升趋势比较明显,4~5 h之间上升趋势略弱,Mn2+呈直线上升趋势。
从图6可以看出,在4 h时,Mn2+、Cu2+的吸附率差值最大,即4 h是二者的吸附速度都最大,所以,从经济效率及成本考虑,Mn2+、Cu2+的最佳吸附时间选择4 h。
2.2.4 吸附温度对吸附效率的影响
固定其他吸附条件不变,依次改变吸附温度为20,25,30,35和40 ℃。吸附4 h后,从对应试管中吸取1 mL,取出的样品稀释50倍,用火焰原子吸收光谱仪测定溶液加入吸附剂前后所含待测重金属浓度,测定结果如图7所示。
从图7可以看出,Mn2+在20~40 ℃温度范围内,改变吸附温度,固定化酵母对Mn2+的吸附几乎没有影响。Cu2+随着温度的变化吸附率大小变化也不大,考虑到升高温度会使溶液薄膜厚度减薄,密度和黏度降低,离子的扩散速度增加,适当升高温度有利于固定化酿酒酵母对重金属离子的吸附。为此,在试验过程中,选择吸附温度为30 ℃。
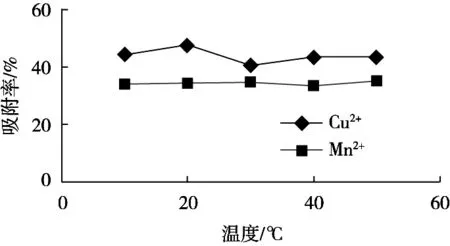
图7 Mn2+、Cu2+的不同吸附温度变化对吸附效率的影响
2.2.5 pH对重金属吸附效率的影响
其他吸附条件不变,用1%的HCl或0.1 mol/L的NaOH调节溶液的酸碱度,使溶液的pH依次为1,2,3,4和5,考察溶液pH对吸附效果的影响,试验结果如图8所示。在溶液pH 1~2时Mn2+吸附率呈上升趋势,pH 2~5时呈下降趋势,在pH 2时,固定化酿酒酵母对Mn2+的吸附率最高,所以固定化酿酒酵母对Mn2+的最佳吸附pH为2。固定化酿酒酵母对Cu2+的吸附效率在pH 1~4时呈上升趋势,pH 4~5时呈下降趋势,在pH 4时固定化酿酒酵母对Cu2+的吸附率最高,所以固定化酿酒酵母对Cu2+的最佳吸附pH为4。
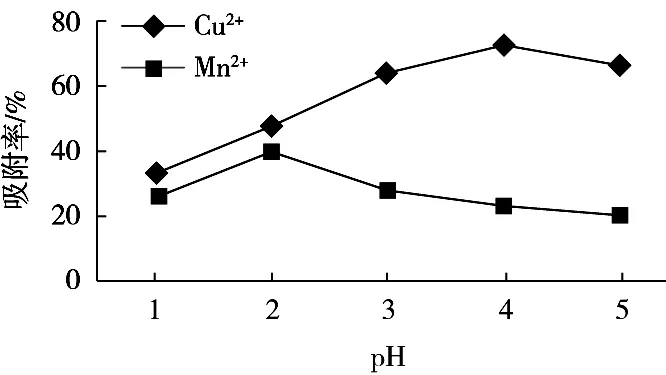
图8 Mn2+、Cu2+的不同pH对吸附效率的影响
2.3 同存离子的竞相吸附
配制Mn2+、Cu2+100 mg/L单元素离子液及Cu2+、Mn2+100 mg/L的混合储备液调节溶液pH 3,依次吸取3 mL的相应溶液到试管中,分别加入固定化酿酒酵母吸附剂1.0 g,混合后,在30 ℃,转速为180 r/min的条件下,在恒温振荡摇床中振荡吸附4 h。吸附时间结束后,稀释测定,每1个条件有3个平行样,结果取平均值。比较2种重金属的竞相吸附效率,相同条件下,单组份 Cu2+和Mn2+的吸附率分别为56.99%和21.20%。双组分的吸附率分别为67.24%和29.05%。
由此可以看出,Mn2+、Cu2+共存时,单位吸附剂吸附Mn2+、Cu2+吸附率较单独离子存在时的吸附率高,这可能是因为Mn2+、Cu2+与固定化酿酒酵母之间发生共同吸附,形成Mn2+、Cu2+金属络合物。
3 结论
试验以海藻酸钠为包埋剂,采用包埋的方法固定化酿酒酵母,用固定化酵母作为吸附剂,研究其对5种重金属离子Cu2+、Mn2+、Cd2+、Pb2+、Zn2+吸附性能。结果表明,固定化酿酒酵母对5种离子的吸附效率依次Cu2+>Mn2+>Pb2+>Zn2+>Cd2+,其中吸附效果最好的2种重金属是Cu2+、Mn2+。
以吸附效果较好的2种重金属离子Cu2+、Mn2+为研究对象,改变重金属离子的初始质量浓度、吸附剂投放量、吸附温度、吸附时间、pH,考察对吸附效率的影响,得出固定化酿酒酵母对Cu2+、Mn2+最佳的吸附条件。Cu2+的最佳吸附条件:初始质量浓度50 mg/L,吸附剂投放量1.5 g,时间4 h,温度30 ℃,pH 4。Mn2+的最佳吸附条件:初始质量浓度40 mg/L,吸附剂投放量2 g,时间4 h,温度30 ℃,pH 2。
Cu2+、Mn2+2种重金属离子的竞相吸附试验表明,在2种离子共存的条件下,固定化酵母对2种离子吸附效率比单个金属离子的吸附率都有明显提高,说明两种离子的存在能相互促进吸附。
生物吸附法是一种经济有效的处理大规模低浓度重金属废水的生物技术,其中酵母是具有实用潜力的生物吸附剂。研究开发新的生物吸附剂及其固定化技术,研究增强生物吸附剂吸附性质的化学或生物试剂在将来有更广泛的应用[10]。试验结果为利用价廉易得的废弃酵母作为吸附材料去除废水中的重金属、解决重金属污染的净化处理问题提供一定参考。但由于试验是在实验室条件下的模拟重金属离子水溶液的试验,对于多种基质存在条件下的复杂环境中实际样品的吸附,还需要更进一步的研究和论证,固定化酿酒酵母作为吸附剂吸附废重金属离子的吸附机理,固定化酿酒酵母吸附重金属离子后的后续处理等有待进一步研究探讨。

