苯羧酸一级电离Gibbs自由能的密度泛函研究
位艳宾,何伟平,孙婷婷,刘 焕,李 想
(1.徐州工业职业技术学院化学工程学院,江苏 徐州 221140;2.江苏省化工新材料工程技术研究开发中心,江苏 徐州 221140)
苯羧酸作为一类重要的化工原料和化工中间体,在合成纤维、增塑剂、医药、农药、工程塑料及染料中间体等领域有着广泛的应用。目前,苯羧酸的主要工业来源是通过相应的芳烃催化氧化制取。随着石油资源的日益紧张,以芳烃为原料制取苯羧酸的工艺受到限制,以煤及其衍生物为原料,通过氧化降解制取苯羧酸,是一项很有发展前景的研究课题[1-2]。通过煤及其衍生物的氧化解聚,可获得高产率的苯羧酸,但混合物的成分复杂,苯羧酸的物化性质相似,导致产物的分离很困难[3]。因此,如何实现苯羧酸的精细分离,是有效利用煤及其衍生物的氧化解聚产物的一大难题。例如以褐煤为原料,通过碱氧化法制取苯羧酸,已取得一定进展,但是得到的苯羧酸却是以钾盐混合物的形式存在。吴桐采用抗溶剂法分离苯羧酸的模型混合物,测试了丁酮-正己烷、丁酮-石油醚、乙醇-水、丙酮-石油醚、丁酮-环己烷等抗溶剂体系,研究结果表明,丁酮-石油醚(60~90℃沸程)、丁酮-正己烷等抗溶剂体系对分离苯多羧酸混合物具有一定的效果。鉴于苯羧酸在工业应用中的重要性,以煤及其衍生物为原料氧化解聚制取苯羧酸,在产物分离的过程中会涉及苯羧酸/苯羧酸盐的相关性质,因此本文利用密度泛函理论,对苯羧酸一级电离Gibbs自由能进行理论研究,以期解释它们在水溶液中的有关性质。
1 计算方法
本文采用密度泛函方法B3LYP/6-311G(d)并考虑色散校正[4],优化得到苯羧酸分子及其一级电离产物的几何结构。通过振动频率分析,证实所有结构均为稳定构型,并获得了气相状态下各物种的Gibbs自由能。为获得较高精度的溶解自由能,根据文献[5],本文采用uESE (universal Easy Solvation Energy Evaluation)溶剂模型,在B3LYP/def2TZVP[6]级别计算了各物种的几何结构和波函数,在此基础上获得了CM5原子电荷。再利用uESE程序,根据CM5原子电荷,计算溶解自由能[7-10]。最后,通过式(1)计算了水溶液中各物种的Gibbs自由能:
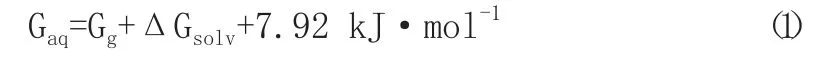
其中,Gg为B3LYP/6-311G(d)计算级别下,经色散校正得到的某物种Gibbs自由能(气相标准态);ΔGsolv为B3LYP/def2TZVP水平下计算某物种的CM5原子电荷,再利用uESE程序计算得到的溶解自由能(溶解前后均为1mol·L-1);7.92 kJ·mol-1为校正项,是气体摩尔体积从气相标准态(298.15K,1atm)压缩为溶液标准态(1mol·L-1)的自由能变化值。
根据Newton等人的研究[11],相比HO+,HO+394能更好地代表水合质子,故使用式(2)来计算苯羧酸一级电离反应的Gibbs自由能。
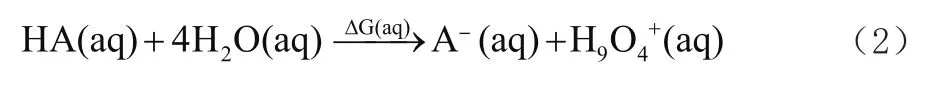
2 结果及讨论
2.1 几何结构
本文采用B3LYP/6-311G(d)计算级别并采用色散校正,获得了苯羧酸及其一级解离产物的几何结构,优化结果见图1。在相同计算级别下进行振动频率分析,发现所有物种的结构均无虚频,证实所得结构为稳定构型。
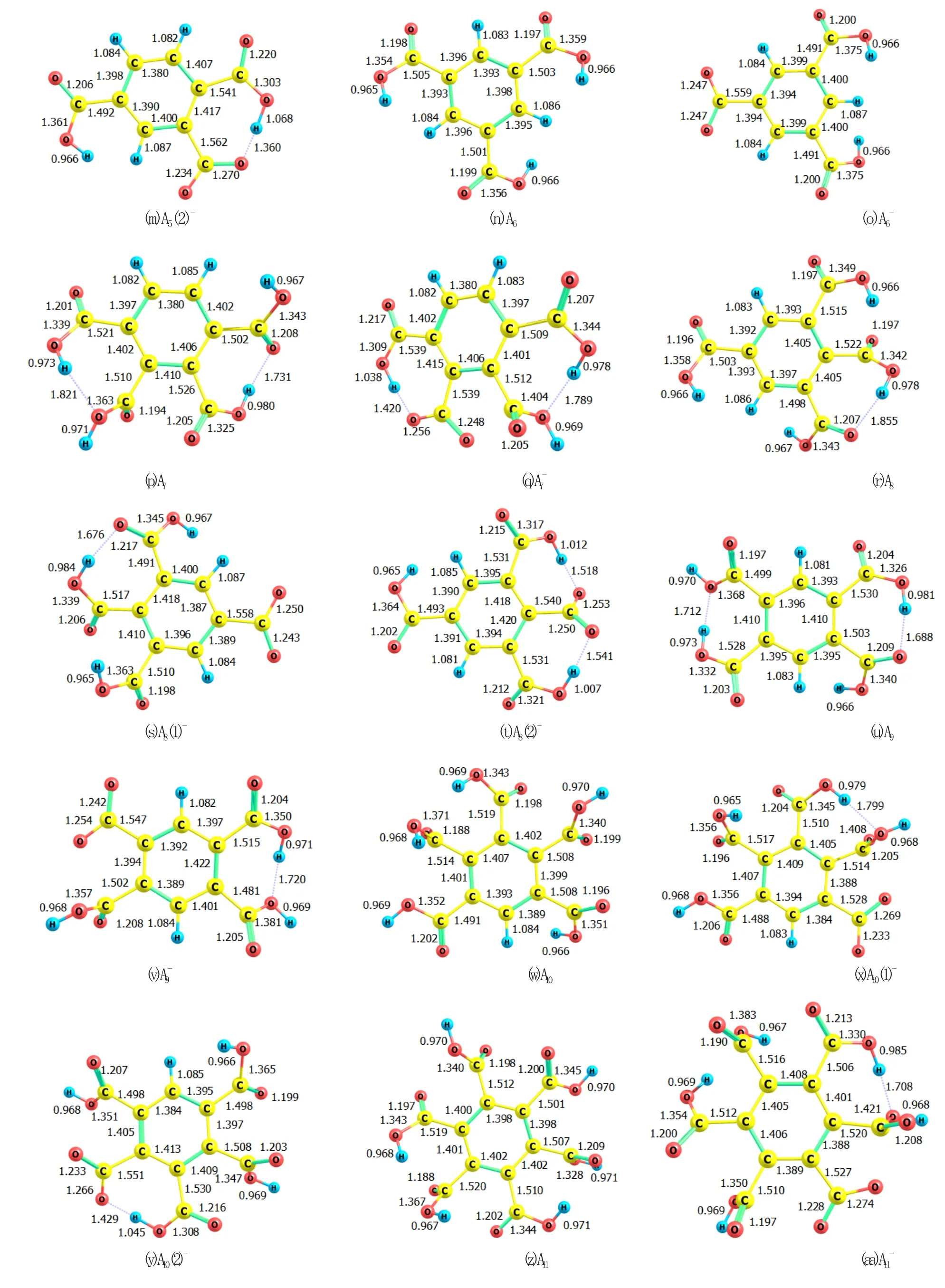
图1 苯羧酸及其一级电离产物的结构Fig.1 Structure of benzene carboxylic acids and its primary ionization products
2.2 一级电离Gibbs自由能
采用B3LYP/6-311G(d)计算级别及色散校正,计算得到各物种在气相标准态的Gibbs自由能Gg。根据B3LYP/def2TZVP方法计算得到CM5原子电荷,利用uESE及Multiwfn程序[12-15],根据CM5原子电荷计算溶解自由能ΔGsolv,所得结果如表1所示。

表1 各物种的Gibbs自由能计算结果Table 1 Calculation results of Gibbs free energy of each species
根据式(2),可得苯羧酸的一级电离Gibbs自由能ΔG如表2所示。

表2 苯羧酸的一级电离Gibbs自由能Table 2 Gibbs free energy of primary ionization of benzene carboxylic acids
由表2可见,苯羧酸电离反应的邻位效应非常明显。如苯二甲酸~苯五甲酸的一级电离反应[式(2)、(5)、(7)、(11)、(14)]的Gibbs自由能,分别为 -46.921、-63.857、-70.397、-88.071、-67.227 kJ·mol-1,比它们异构酸的一级电离反应Gibbs自由能低20~60 kJ·mol-1,这是因为邻位电离反应的产物均形成了分子内氢键(图1) ,使得结构更加稳定,从而降低了产物的Gibbs自由能。由此可以预见,邻位苯羧酸的溶解度及酸性,应大于不含邻位羧基的异构酸,事实上,邻苯二甲酸的溶解度大大超过其他异构酸,如间苯二甲酸和对苯二甲酸[16]。
均苯四甲酸A9由于存在分子内氢键,形成电离产物时需要破坏氢键,因此反应的Gibbs自由能较高。苯五甲酸、苯六甲酸一级电离反应的Gibbs自由能也较高。尽管A10(1)-形成了分子内氢键,但由于2个羧基之间形成了分子内氢键,相较于图1中其他情形下的电离产物,形成的氢键较弱,不足以明显降低反应产物的Gibbs自由能。
苯六甲酸的一级电离Gibbs自由能为-6.949 kJ·mol-1,仅从一级电离来看,并不利于产物在溶液中以离子状态存在,但实际上,苯多酸会发生多级电离,故其电离情况还应考虑其他级别的电离。例如苯六甲酸的二级电离产物依次为邻位、间位、对位羧基电离,其计算结果如图2所示。
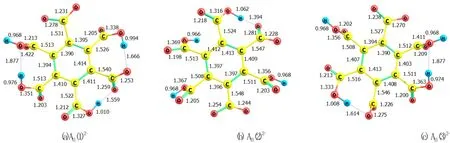
图2 苯六甲酸的二级电离产物结构Fig.2 Structure of secondary ionization products of benzene hexacarboxylic acid
苯六甲酸二级电离产物的Gibbs自由能计算结果见表3。由表3可知,苯六甲酸的二级电离Gibbs自由能,明显大于一级电离Gibbs自由能,由此可知,苯六甲酸的二级电离常数应大于其一级电离常数。根据文献[17],苯六甲酸的一级电离常数pKa1=1.1~1.4,二级电离常数pKa2=1.69~3.19,亦证实了上述分析结果。

表3 苯六甲酸二级电离产物的Gibbs自由能及电离Gibbs自由能Table 3 Gibbs free energy and ionization Gibbs free energy of secondary ionization products of benzene hexacarboxylic acid
3 结论
利用密度泛函方法B3LYP/6-311G(d)和色散校正,对苯羧酸分子及其一级电离产物进行了几何结构优化和振动频率计算,获得了苯羧酸分子及其一级电离产物的几何结构和Gibbs自由能。根据B3LYP/def2TZVP水平得到CM5原子电荷,利用uESE程序计算了各物种的溶解自由能。在此基础上,进行了羧酸一级电离Gibbs自由能的密度泛函分析。研究结果表明:
1)苯二甲酸~苯五甲酸的一级电离反应的邻位效应非常明显,可见与其异构酸相比,具有邻位羧基的苯羧酸其酸性应当较强,电离产物也较稳定,原因在于其电离产物形成了分子内氢键,增强了产物的稳定性。
2)电离产物形成的分子内氢键有利于电离反应,但电离反应的Gibbs自由能是否足够低,还与苯羧酸自身的稳定性及产物的分子内氢键的形成位置有关。例如,均苯四甲酸A9、苯五甲酸、苯六甲酸的一级电离产物虽然也存在分子内氢键,但其反应的Gibbs自由能却不一定低。
3)苯多羧酸可以发生多级电离,故其实际电离情况除一级电离外,还应考虑高级电离情况。例如,苯六甲酸二级电离的Gibbs自由能显著大于一级电离的Gibbs自由能,导致它的二级电离常数明显大于一级电离常数。
——以高中化学“氢键”的教学为例

