以蛋白质为基础物质的姜黄素传递体系研究进展
舒 心,郭 擎,高彦祥
(中国农业大学食品科学与营养工程学院 中国轻工业健康饮品重点实验室 北京 100083)
自21世纪以来,心血管疾病、癌症、糖尿病等慢性疾病的发病率一直居高不下[1],对人类健康造成严重的威胁。研究发现,食品中的功能性成分能通过调节机体代谢过程来预防慢性疾病的发生[2]。随着人们健康认识的不断提高,功能食品开始受到广泛关注,消费者们对功能因子在食品领域的开发与应用提出更高的要求。享有“固体黄金”美誉的姜黄素(Curcumin,CUR)是从姜科植物姜黄(Curcuma longa L.) 中提取的一种小分子多酚类物质[3]。大量研究表明姜黄素有抗氧化[4]、抗炎症[5]、抗癌[6]、预防老年痴呆[7]等功效。然而,姜黄素水溶性较差[8],在光热条件下容易发生分解[9],在体内的生物利用率较低[10]。这些特点使其作为功能因子在食品中的应用受到很大限制。采用生物大分子物质对姜黄素进行包埋递送,其水溶性、稳定性和生物利用率得到显著提升。以蛋白质为基础物质构建传递体系,更是具有无毒、可降解、生物相容性好等突出优点。目前,人们虽已围绕姜黄素传递体系开展了大量研究,但仍缺乏对以蛋白质为基础物质的传递体系,从原料选择到构建方法再到物质间作用机理的系统总结与探讨。本文结合近年来国内外研究现状,介绍姜黄素的理化性质,传递体系构建的基础蛋白质原料、制备方法以及物质间相互作用类型。在此基础上,总结归纳常见的以蛋白质为基础物质的姜黄素传递体系类型及其应用,旨在为新型姜黄素传递体系的构建与应用提供理论基础和依据。
1 姜黄素的结构与性质
从草本植物姜黄根茎中提取的姜黄色素(Curcuminoids)在常温下为橙黄色结晶粉末,略具生姜辛辣味,主要作为天然色素和调味品应用于食品工业中[11]。商业上使用的姜黄色素主要组成为:姜黄素(77%)、脱甲氧基姜黄素(Demethoxycurcumin,17%) 和双脱甲氧基姜黄素(Bisdemethoxycurcumin,6%)[12]。其中,姜黄素(3-甲氧基-4-羟基-苯基-1,6-庚二烯-3,5-二酮)分子式为C21H20O6,相对分子质量为368.39,是姜黄色素最主要的活性成分,属于β-二酮功能基团的多酚化合物[13]。
姜黄素溶于乙醇、丙二醇,易溶于碱和冰醋酸溶液,不溶于水和乙醚[14]。姜黄素熔点高达183℃,具有较高的晶格能[15]。相比于无定形态,结晶态下的姜黄素在水中的溶解度更低[16]。在酸性和中性水溶液中,姜黄素主要以酮构型存在,溶解度较低(11 ng/mL pH 5.0)[16]。而在碱性环境中(pH >12),姜黄素的构型主要为烯醇式,羟基易发生去质子化,水溶性有所提高[17-18]。姜黄素的酮式与烯醇式结构见图1。
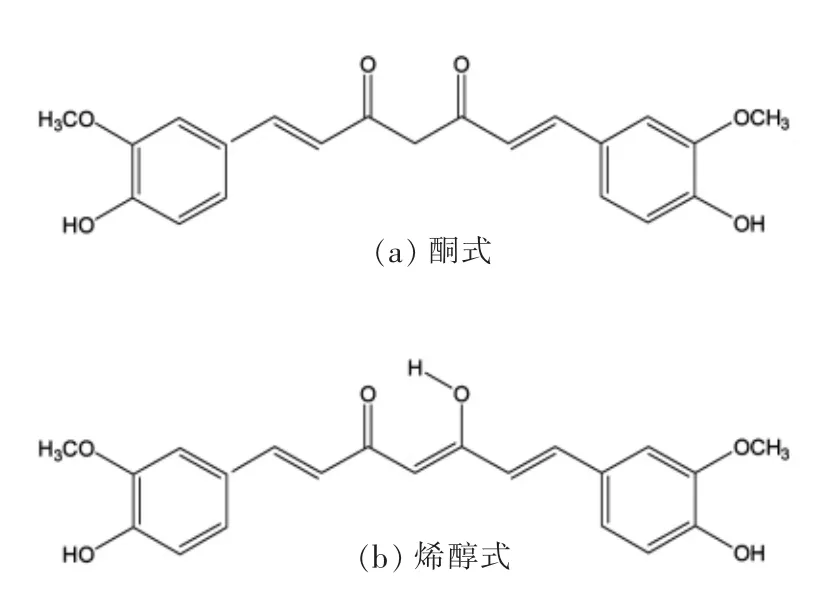
图1 姜黄素的酮式与烯醇式结构Fig.1 Keto and enol structure of curcumin
姜黄素的稳定性受许多环境因素的影响。例如,姜黄素在酸性环境下较为稳定,在中性和碱性条件下可快速分解生成阿魏酸和阿魏酰甲烷等降解产物,然而在强碱性条件下(pH>11.7)其稳定性又有所提高[19-20]。Tønnesen 等[21]研究发现,在紫外或可见光照射下,姜黄素会发生快速光解并产生一系列降解产物。在热处理过程中,姜黄素的降解速率随着温度的升高而加快[22],这可能与其不稳定的二酮结构有关[23]。有研究表明,姜黄素在水缓冲溶液(pH 7.2)中发生的分解是一种自氧化反应,降解的主产物是二环戊二酮衍生物[24],这说明姜黄素自氧化机制主要是通过酚羟基脱氢形成自由基,自由基离域至共轭烯酮链,进而引发姜黄素降解的链式反应,最终形成环氧化合物[25]。抗氧化剂如抗坏血酸、没食子酸、特丁基对苯二酚等的加入能使姜黄素的降解速率显著放缓[26]。一些金属(如铜、铁、锌等)能与姜黄素螯合,对姜黄素的稳定性以及生物活性产生影响[27-28]。
目前,人们已围绕着姜黄素的分离纯化、理化性质、生理功效等方面展开了大量研究。如何实现姜黄素的稳态化递送,使其达到期望的生物学效应,是突破其在功能食品中的应用局限性所亟需解决的问题。大量研究证明,蛋白质能与姜黄素相互作用形成复合物,姜黄素的水溶性、稳定性与生物利用率显著提高[29-30]。选择合适的蛋白原料及制备方法对获得具有理想功能特性的姜黄素传递体系而言尤为关键。
2 蛋白质种类
许多来源于食品的蛋白质都可以作为传递体系的基础物质,例如酪蛋白、乳清蛋白、明胶、大豆蛋白、玉米醇溶蛋白等(表1)。不同来源蛋白质的氨基酸种类、数量、排列顺序不同,造成蛋白质分子质量、分子构象、带电性、亲疏水性、物质间相互作用、化学反应活性的差异。根据蛋白质的来源,可以将其分为动物源蛋白质与植物源蛋白质两大类。

表1 常用于构建传递体系的蛋白质分子主要性质Table 1 Main properties of protein molecules commonly used to construct delivery systems
2.1 动物源蛋白
2.1.1 酪蛋白 酪蛋白(Casein)约占牛奶中总蛋白含量的80%,由αS1-、αS2-、β-和κ-酪蛋白4 种蛋白单体组成[39]。酪蛋白构型较为灵活且无序,会根据环境条件的变化调整其结构[40]。此外,由于酪蛋白二级或三级结构的缺乏,其对热处理的敏感性较低[41]。酪蛋白是两亲性蛋白质,在水溶液中,酪蛋白和胶体磷酸钙发生自组装形成稳定的胶体聚集物,称为酪蛋白胶束,直径在50~300 nm 范围[42]。这些胶束能够在其内部溶解疏水性成分如姜黄素、类胡萝卜素、油溶性维生素等,可以作为疏水性物质的传递体系。酪蛋白酸盐(Caseinate)是酸沉法获得的酪蛋白胶束经中和、干燥后获得的产物[43],具有良好的水溶性、乳化性、发泡性和包封性能,目前已得到了广泛地应用[44]。
2.1.2 乳清蛋白 乳清蛋白(Whey protein)是从牛奶中分离出的一大类球蛋白的总称,其含量约占牛奶总蛋白的20%,主要由β-乳球蛋白 (β-Lactoglobulin)、α-乳清蛋白(α-Lactalbumin)、免疫球蛋白 (Immunoglobulins) 和血清白蛋白(Serum albumin)组成[45]。当将乳清蛋白加热到变性温度(Td)以上后,球蛋白结构趋于舒展,原先位于蛋白内部的活性氨基酸侧链和非极性基团暴露,进而能促进蛋白与疏水活性物质的结合。同时,蛋白之间的适度交联聚集能形成一定的网状结构,可用于姜黄素的包埋传递[46],或用于提高特定结构的稳定性[47-48]。需要注意的是,蛋白变性聚集的程度受环境条件(pH 值、加热温度、离子强度)以及蛋白浓度的影响,过度的聚集可能会导致其稳定性下降[49]。
2.1.3 明胶 明胶(Gelatin)是从动物(例如猪、牛或鱼)胶原蛋白中提取的、应用最广泛的蛋白质之一[50]。由于制备方法的不同,明胶可以分为A、B 两种类型。A 型明胶由胶原蛋白酸水解获得(pI 7~9),B 型明胶由胶原蛋白经碱处理获得 (pI 4.7~5.5)[51]。从结构上看,明胶分子含有重复的Gly-XY 三联序列,其中X 和Y 主要为脯氨酸和羟脯氨酸[52]。明胶在相对较高的温度下以一种灵活的无序(随机螺旋)状态存在。当温度降低至临界温度以下时,明胶分子构型转变为螺旋态。当浓度高于临界交叠浓度时,明胶分子还能形成具有三重螺旋结构的热可逆型凝胶[53]。除可在食品中用作增稠剂、稳定剂、乳化剂外,明胶分子还可通过疏水相互作用、静电相互作用、氢键等非共价相互作用与疏水性小分子物质结合[54],形成具有一定功能特性的结构(如凝胶、涂层等),用于营养物质的包埋与传递[52,55]。
2.2 植物源蛋白
2.2.1 玉米醇溶蛋白 玉米醇溶蛋白(Zein)是一种从玉米中提取的天然混合蛋白,由α-(含量70%~85%)、β-(含量1%~5%)、γ-(含量10%~20%)和δ-(含量1%~5%)型玉米醇溶蛋白组成[56]。玉米醇溶蛋白是一种疏水性蛋白,其中含有大量的非极性氨基酸(亮氨酸、丙氨酸和脯氨酸),约占玉米醇溶蛋白中氨基酸总含量的50%[57]。玉米醇溶蛋白虽在水中溶解性较差,但可溶于乙醇-水、丙酮-水或碱性(pH>11.5)水溶液中[58]。研究表明,通过改变溶剂的成分与极性,可诱导玉米醇溶蛋白发生从α-螺旋到β-折叠的构象转变,疏水相互作用将驱动玉米醇溶蛋白分子以反平行的β-折叠形式排列形成长条带状,长条带状的玉米醇溶蛋白卷曲成环或线圈状并不断堆积、环绕、生长,形成玉米醇溶蛋白颗粒(图2)[59]。玉米醇溶蛋白的自主装能使其形成具有不同功能特性的结构,例如薄膜、纳米颗粒、纤维和胶束等。试验证明,一些疏水性活性物质,如姜黄素、槲皮素等包埋在玉米醇溶蛋白胶体颗粒中,可以提高活性物质的稳定性及生物利用率[60]。

图2 玉米醇溶蛋白自组装机理[59]Fig.2 Mechanism for zein self-assembly[59]
2.2.2 大豆分离蛋白 大豆分离蛋白(Soy protein isolate,SPI) 是由脱脂大豆粉去除大部分非蛋白质成分、脂肪和碳水化合物而获得的纯化大豆蛋白,其蛋白质含量在90%以上[61]。根据沉降系数的不同,SPI 又可分为2S、7S、11S 和15S 4 类[62]。在这4 种蛋白中,7S 球蛋白(β-Conglycinin)和11S球蛋白(Glycinin)占SPI 总含量的80%以上[63]。SPI除具有成本低、来源广和营养价值高等优势外,还表现出许多良好的功能特性。例如,在热或酸诱导下,球蛋白构象发生变化,表面疏水性增加,进而表现出高度的聚集性和良好的胶凝性[38,64]。经改性处理后的SPI 具有良好的乳化性能[38,65-66]。SPI 颗粒还能与白藜芦醇[67]、姜黄素[68]、β-胡萝卜素[69]等疏水性功能因子复合,以提高其在水中的溶解度、稳定性以及生物利用率。
3 传递体系的构建方法
3.1 自上而下法
工业中广泛应用的自上而下法是通过研磨、粉碎、均质等方式来减小大颗粒(固体或液体)尺寸的一系列制备方法的总称。这些方法主要依靠设备对物质以及物质和物质间的强烈剪切、撞击、挤压作用使颗粒破碎。常见的自上而下法包括高压均质、微射流、研磨法、超声法等(图3)[70]。

图3 传递体系制备常用方法(自上而下)[70]Fig.3 Comnon methods for preparation of delivery systems (top-down)[70]
3.1.1 高压均质法 高压均质是制备乳液时常用的一种方法。均质过程中,物料在高压下通过均质阀并以极高流速喷出,撞击碰撞环。高压产生的强烈剪切、撞击、空穴作用使物料达到细化和均质的效果。Silva 等[71]以乳清分离蛋白为乳化剂,中链甘油三酯(Medium chain triglycerides,MCT)作为溶解姜黄素的油相,采用高压均质法制备了包埋有姜黄素的O/W 型纳米乳液。与游离姜黄素相比,纳米乳液传递体系中姜黄素在Caco-2 细胞中的抗氧化活性提高了8.5 倍。高压均质后获得的液滴性质受均质条件(均质压力、均质次数)、油水界面张力、乳化剂类型、浓度等因素的影响。Ma 等[72]采用高压均质法,以不同油相(MCT、菜籽油和亚麻籽油)和不同乳化剂(吐温-80、卵磷脂、乳清分离蛋白和阿拉伯胶)制备负载姜黄素的纳米乳液,探究乳化剂类型、乳化剂浓度、油相类型、姜黄素溶解方法(加热、超声、微波处理)对乳液理化性质(姜黄素含量、粒径、电位、物理稳定性)和贮存稳定性的影响。结果表明,经超声处理后姜黄素在MCT 中溶解度最高,采用MCT 和吐温-80 制备的姜黄素纳米乳液稳定性最好。
3.1.2 微射流法 微射流法是指将预形成的粗乳液经高压装置泵入均质器的两个狭窄通道中,两股流体以高速相互碰撞,产生强烈的湍流、应力、剪切、空穴作用,形成细化乳液的均质方法。采用微射流技术可以制备出粒径小、稳定性好的颗粒,在姜黄素传递体系应用中有巨大的潜力。Wei 等[73]以玉米醇溶蛋白(Zein)和海藻酸丙二醇酯(PGA)为基础物质,采用热处理-高压微射流-溶剂蒸发法制备了负载有姜黄素的二元复合物颗粒。经热(75 ℃,30 min)与微射流(100 MPa,循环2 次)处理后获得的颗粒在不同环境应力(pH 值、离子强度、光和热)和储存条件(37 ℃和55 ℃)下表现出最佳的稳定效果。同样,采用微射流法获得的颗粒的理化性质及其稳定性也受均质条件(压力、循环次数)、乳化剂类型、浓度的影响。Raviadaran 等[74]以棕榈油为油相溶解姜黄素,以吐温-80 为乳化剂,采用微射流法成功制备了O/W 型纳米乳液,并采用响应面法对微射流参数(压力、循环次数和乳化剂浓度)进行优化。试验结果表明,在乳化剂质量分数为1%,微射流参数350 bar,循环5 次的条件下,获得的姜黄素微乳液稳定性最好。
目前,自上而下法已广泛应用于乳液的研究与加工中。对于水溶性差的姜黄素而言,乳液传递体系有巨大的应用潜力:一是因为姜黄素在油相中有较好的分散性;二是因为蛋白质分子具有两亲性,可以单独地或者与其它分子相互作用后作为乳化剂来稳定乳液。然而,自上而下法的能耗较大,设备运行维护成本较高,制备精度较低,其在工业中的应用仍具有一定的局限性。
3.2 自下而上法
自下而上法是在环境因子如pH 值、离子强度或温度等的诱导下,分子间实现自组装或共组装,进而形成传递体系的一系列方法的统称。姜黄素传递体系构建时常用的自下而上技术有反溶剂沉淀法、pH 驱动法、复凝聚法、喷雾干燥法等。
3.2.1 反溶剂沉淀法 使用反溶剂沉淀法构建传递体系主要依赖于溶剂-反溶剂比例的变化[75]。在此过程中,大分子蛋白和姜黄素首先需要在合适的溶剂中充分溶解混合,然后通过改变溶剂条件形成反溶剂,使蛋白和姜黄素的溶解度降低,诱导组分间自发地结合[76]。反溶剂沉淀法操作较为简单,成本较低,可用于大规模生产[76]。通过反溶剂沉淀法制备传递体系需要保证形成的复合物单体之间有足够强的斥力,防止其发生聚集。在某些情况下,可以通过加入聚合物或表面活性剂使其吸附至颗粒表面,以提高体系的稳定性。Hasankhan等[77]采用两步反溶剂沉淀制备了玉米醇溶蛋白-姜黄素-乙基纤维素复合纳米颗粒。当玉米醇溶蛋白-姜黄素-乙基纤维素体积分数分别为0.16%,0.01%,0.045%且乙醇-水-乙酸乙酯溶剂用量分别为31.25%,62.5%,6.25%时获得的复合颗粒物理稳定性最佳。与单独用玉米醇溶蛋白负载姜黄素相比,乙基纤维素的加入使复合颗粒展现出更好的pH 稳定性,姜黄素的抗氧化活性显著提高。
3.2.2 复凝聚法 采用复凝聚法构建传递体系的驱动力是反应介质中带电生物大分子之间的静电相互作用[78]。除此之外,范德华力、疏水相互作用以及分子间氢键也在凝聚过程中起到重要作用[79]。在食品传递体系中,复凝聚法所采用的原料多为蛋白、多糖等天然高分子聚合物,通过两种或多种带相反电荷物质互作进而形成复合物[80]。例如,Huang 等[81]以溶菌酶(Lysozyme,LYS)和κ-卡拉胶(κ-Carrageenan,CRG)为原料,采用复凝聚法在酸性条件下制备了LYS-CRG 复合物,并对姜黄素进行包埋。研究表明,在pH=4.0、mLYS∶mCRG=2∶1、CUR 质量浓度为7.5 mg/L 条件下制备出的LYS-CUR-CRG 复合物中姜黄素的包埋率与负载量分别达到了96.2%和2.31%。傅里叶变换红外光谱(FTIR)结果显示,复合物各组分间存在氢键和静电相互作用。在此传递体中,姜黄素的抗氧化活性与光热稳定性均显著提高。采用复凝聚法构建食品传递体系具有操作简单、成本低、封装效率高等突出优势。然而,复凝聚法形成的复合物尺寸较难控制,对环境条件变化敏感,易发生团簇聚集等局限仍有待突破。
3.2.3 pH 驱动法 pH 驱动法(也称为pH 循环法或pH 变化法),是通过将体系的pH 值从中性调节至极酸/极碱条件后再调回中性;或将极酸和极碱性溶液混合后最终调节体系达到中性,在pH值变化的过程中诱导分子结构的变化以及分子间发生相互作用的一种方法。姜黄素在水溶液中的溶解性有较高的pH 值依赖性,短时间内强碱性处理可使姜黄素可发生去质子化,溶解度显著增加[82]。当蛋白质暴露在极碱性条件下时,其构象舒展并仍保持相对完整。因此,通过调整环境pH值,能促进姜黄素与蛋白质的结合。当pH 值重新调整为中性时,最初形成的姜黄素蛋白复合物可能会发生结构重排,形成更紧凑的结构[83]。采用pH 循环法制备复合物的方法简单、能耗低、无有机试剂污染风险,有广泛的应用前景。Guo 等[84]以豌豆分离蛋白(PPI)和3 种带电性不同的乳化剂【鼠李糖脂(Rha)、茶皂素(TS)、月桂酰精氨酸乙酯盐酸盐(ELA)】为原料,采用pH 驱动法制备了负载姜黄素(Cur)的纳米复合物。疏水相互作用、氢键以及静电相互作用在复合物的形成过程中起到了重要的作用。PPI 与Rha 在质量比为1∶3 下获得的复合物PPI-Cur-Rha1:3 对姜黄素的包埋率达93.69%,复合物对姜黄素展现出了最佳的光热保护和缓释效果。
3.2.4 喷雾干燥法 喷雾干燥是一种成本低、易获取、能够实现连续加工进行大批量生产的微胶囊技术[85]。如图4所示,含有生物活性物质的悬浮液经喷嘴雾化形成细小液滴。在干燥室内,雾化液滴中的溶剂被连续流动的干燥热气带走并迅速蒸发,形成的微球颗粒从气流中分离收集在容器中[86]。通过喷雾干燥得到的颗粒直径在10~50 μm之间,颗粒性质可通过控制流速、溶质浓度、温度、压力、雾化方式等参数来进行调整[87-88]。Chen 等[89]通过喷雾干燥法制备了姜黄素-大豆分离蛋白微胶囊颗粒。X-射线衍射结果表明,复合物微胶囊中姜黄素呈非结晶态。与游离姜黄素相比,复合颗粒中姜黄素具有更强的抗人肝癌HepG2 细胞增殖效果和抗氧化活性。类似的,Yang 等[90]采用喷雾干燥技术成功构建了乳铁蛋白(LF)-燕麦葡聚糖(OG)-姜黄素(Cur)三元复合物。通过喷雾干燥技术,姜黄素可负载到乳铁蛋白(LF)-燕麦葡聚糖(OG)中形成非晶态的三元复合物。与自主装法相比,喷雾干燥法可以强化LF、OG 和Cur 之间的相互作用,形成的复合物粒径更小、浊度更低、乳化性更强。
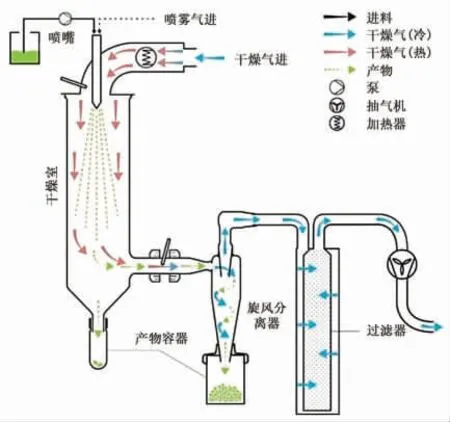
图4 喷雾干燥示意图[86]Fig.4 Schematic diagram of spray drying[86]
4 物质间的作用类型
传递体系中的各组分间(蛋白质分子、姜黄素及其它分子)存在各种形式的相互作用,以保证体系结构的完整、稳定。而物质间相互作用的大小、强弱又会受环境条件如pH 值、离子强度、温度和溶剂类型的影响。为提高包埋效率和传递体系的稳定性,需要对体系中各组分间的相互作用特性及其影响因素有一定的了解。
4.1 非共价相互作用
4.1.1 疏水相互作用 传递体系中主要涉及的非共价相互作用有疏水相互作用、静电相互作用、氢键等。其中,疏水相互作用是一种中等范围的、相对较强的作用力类型[91]。在以蛋白质为基础物质构建的姜黄素传递体系中,疏水相互作用在决定蛋白分子构象、物质间相互作用等方面起着重要作用。在水溶液中,疏水相互作用表现为非极性基团之间的相互吸引。因此,疏水相互作用能使许多蛋白折叠成紧凑的球状结构,以减少非极性基团与水之间的接触[92],并促进蛋白或多糖等生物大分子物质暴露在水相中的非极性基团间发生聚集[93]。此外,疏水活性物质在熵驱动下会自发地与蛋白质表面的疏水区域结合[83]。大量的试验研究表明,姜黄素和蛋白质之间的结合主要是通过疏水相互作用实现的[94-95]。疏水相互作用的强度取决于水与非极性基团之间的界面张力以及非极性区域暴露于水的表面积,界面张力或暴露表面积越高则疏水相互作用越强。pH 值、离子强度、温度或溶剂的变化会改变接触水的非极性基团的数量,也会通过促进生物大分子物质构象的变化进而对疏水相互作用效果产生影响[96]。
4.1.2 静电相互作用 静电相互作用主要发生在带电荷或部分带电荷的生物聚合物之间。生物大分子的许多官能团在适当的条件能发生电离。对蛋白质而言,当环境pH 值低于蛋白质的等电点(pI)时,由于氨基基团的质子化程度高,羧基的离解程度低,蛋白质带正电;当环境pH 值高于等电点时,羧基的高度解离和氨基基团的低质子化使蛋白质带负电[97]。静电相互作用在姜黄素传递体系的构建和稳定方面起着重要的作用。Mirpoor等[98]以β-乳球蛋白与海藻酸钠为原料,通过两者在酸性条件下的静电吸引,成功制备了包埋有姜黄素的纳米复合物,复合物对姜黄素展现出了良好的保护缓释效果。静电相互作用的强弱受相互作用物质间的电荷特性(如物质带电正负性、电荷密度)以及物质所处环境的性质(如pH 值、离子强度和溶剂极性) 等因素的影响。可以通过调整pH 值、离子组成、溶剂组成等方式,调整传递体系物质间的静电相互作用效果,提高体系的稳定性,对姜黄素起到更好的保护效果。
4.1.3 氢键 氢键是带正电氢原子和带负电原子之间的一种短程、定向的相互作用[99]。氢键在稳定生物大分子物质如蛋白、多糖的分子内结构以及不同分子间形成的氢键中发挥着重要作用[31,100]。研究证明,传递体系中蛋白分子与姜黄素间存在有氢键相互作用[101-102]。氢键效果会受温度、溶剂极性等因素的影响[103-104]。温度升高,系统热能增加,氢键作用减弱[31]。溶剂极性增加,物质间氢键相互作用加强[105]。
4.2 共价相互作用
传递体系的各组分间除了存在非共价相互作用外,共价相互作用也起到了重要作用。共价键的形成可以通过特定的化学、物理或酶处理来实现。例如,蛋白质和多糖在一定条件下(pH 值、相对湿度、温度、时间)能发生美拉德反应生成蛋白质-多糖复合物[106]。一些化学物质(例如京尼平、戊二醛)和酶类(如转谷氨酰胺酶、漆酶)也可以促进生物大分子物质之间产生共价交联[31]。在一定情况下,分子之间交联可提高以蛋白质为基础物质的姜黄素传递体系结构稳定性以及传递体系对姜黄素的保护效果。Feng 等[107]以卵清蛋白和葡聚糖为原料,采用美拉德反应制备蛋白-多糖复合物,并将复合物热处理后形成的纳米凝胶用于姜黄素的负载传递,使其生物利用率显著提高。
5 基于蛋白质的姜黄素传递体系类型
5.1 基于蛋白质的纳米颗粒
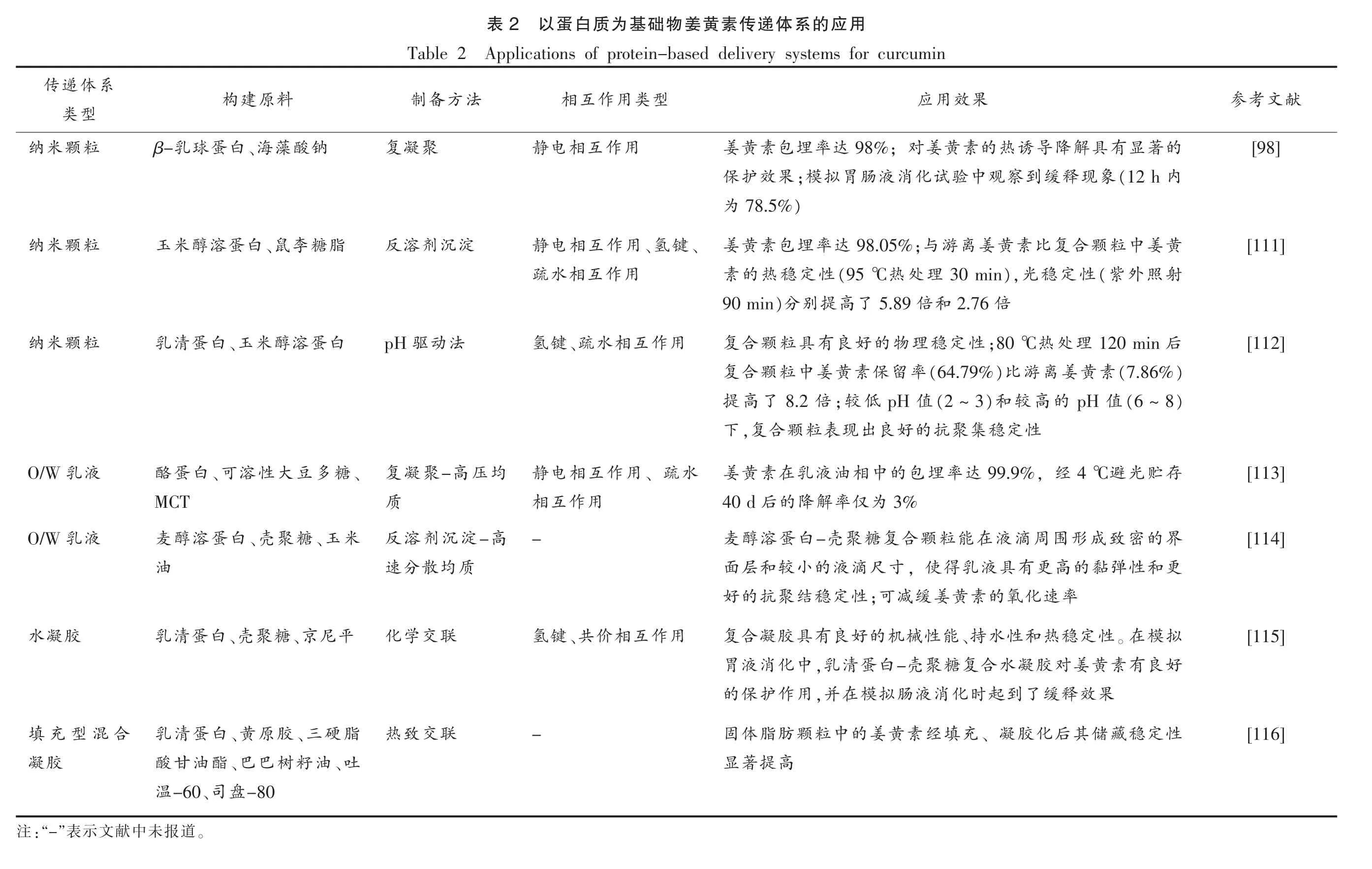
纳米颗粒传递体系是采用食品级原料制备获得的纳米颗粒对生物活性成分进行包埋和递送,从而实现对活性成分控释的传递体系[108]。以蛋白质为原料制备纳米颗粒是姜黄素传递体系中研究最为广泛的类型之一(表2)。Chen 等[109]以经过热处理的大豆分离蛋白为原料制备了姜黄素-大豆分离蛋白复合物。大豆分离蛋白经适当热处理可提高复合物中姜黄素的包埋率和溶解度。并且在25 ℃中性条件下,游离姜黄素在4 h 内降解率为80%,而相同条件下复合颗粒中姜黄素的保留率高达90%。
蛋白质能对姜黄素起到包埋保护的效果。然而,单独采用蛋白荷载功能因子时,其稳定性受pH 值、温度、离子强度等影响较大。因此,人们通常会用多糖、乳化剂等物质来稳定蛋白,同时提高传递体系对姜黄素的保护效果(表2)。例如,Guo等[110]通过钙离子(Ca2+)的诱导,制备了负载姜黄素的豌豆分离蛋白-高甲氧基果胶复合物 (PPI-CUR-HMP-Ca2+),并探究了不同浓度的Ca2+对复合物性质和形成机理的影响。Zeta 电位和FTIR表明,静电相互作用是Ca2+桥形成的主要作用力。Ca2+浓度对纳米复合物的粒径和形貌均有影响。当钙离子浓度达24 mmol/L 时,复合物中CUR 包埋率最高为97.33%,CUR 对紫外光和热胁迫的稳定性也明显提高。然而,过高浓度的Ca2+会导致姜黄素从复合物中解离并处于结晶状态使其稳定性降低。PPI-CUR-HMP-Ca2+复合物能延缓CUR 在胃肠道中的释放,提高其生物利用率。
5.2 基于蛋白质的乳状液
除纳米颗粒外,乳液体系也常被用于荷载姜黄素(表2)。乳液由两种及以上不混溶的液体(通常是油和水)组成[117]。传统乳液中通常会加入乳化剂,其吸附在油水界面上可降低不相溶液体间的界面张力,进而使得乳液在一定时间内保持动力学稳定,防止储存过程中液滴的聚集。食品工业中常用的乳化剂有天然和人工表面活性剂、蛋白质、磷脂和多糖等[82]。Kharat 等[118]分别用酪蛋白酸钠、吐温-80、皂树皂苷、阿拉伯胶4 种乳化剂制备了姜黄素在油相中的O/W 乳液。贮藏试验结果显示,不同类型乳化剂的乳液中姜黄素的降解程度依次为:皂甙>>阿拉伯胶≈酪蛋白酸钠≈吐温-80。蛋白型乳化剂酪蛋白酸钠制备出的乳液(中性pH)液滴尺寸更小、物理化学稳定更性好。
献文考[98][111][112][113][114][115][116]参用应的系体递传素黄姜物础基为质白蛋以2表Applications of protein-based delivery systems for curcumin Table 2 果效用应型类用作互相法方备制的著显有具解降导诱热的素黄姜;对98%达率埋包素黄姜用作互相电静聚凝复内(12 h象现释缓到察观中验试化消液肠胃拟;模果效护保)78.5%为黄姜中粒颗合复比素黄姜离游;与98.05%达率埋包素黄姜、键、氢用作互相电静淀沉剂溶反射照外(紫性定稳),光30 min理处热(95 ℃性定稳热的素用作互相水疏倍2.76和倍5.89了高提别)分90 min后120 min理处热;80 ℃性定稳理物的好良有具粒颗合复用作互相水、疏键氢法动驱pH)(7.86%素黄姜离游)比(64.79%率留保素黄姜中粒颗合复)(6 ~ 8值pH的高较)和(2 ~ 3值pH低;较倍8.2了高提性定稳集聚抗的好良出现表粒颗合,复下存贮光避4 ℃,经99.9%达率埋包的中相油液乳在素黄姜水、疏用作互相电静均压高-聚凝复3%为仅率解降的后40 d用作互相质界的密致成形围周滴液在能粒颗合复糖聚壳-白蛋溶醇麦-高-淀沉剂溶反更和性弹黏的高更有具液乳得,使寸尺滴液的小较和层面质均散分速率速化氧的素黄姜缓减;可性定稳结聚抗的好拟模。在性定稳热和性水、持能性械机的好良有具胶凝合复用作互相价、共键氢联交学化好良有素黄姜对胶凝水合复糖聚壳-白蛋清,乳中化消液胃果效释缓了到起时化消液肠拟模在,并用作护保的性定稳藏储其后化胶、凝充填经素黄姜的中粒颗肪脂体固-联交致热高提著显料原建构钠酸藻、海白蛋球乳β-脂糖李、鼠白蛋溶醇米玉白蛋溶醇米、玉白蛋清乳、糖多豆大性溶、可白蛋酪MCT米、玉糖聚、壳白蛋溶醇麦油平尼、京糖聚、壳白蛋清乳脂硬、三胶原、黄白蛋清乳、吐油籽树巴、巴酯油甘酸-80盘-60、司温。道报未中系体递传型类粒颗米纳粒颗米纳粒颗米纳液乳O/W液乳O/W胶凝水合混型充填胶凝献文示”表:“-注
近年来,传统乳液使用小分子表面活性剂(LWSFs) 的安全问题引发了消费者们的关注[119],无LWSFs 的食品乳液将更贴合消费者的需求。除了食品安全问题外,乳液通常对环境变化较为敏感,如加热、冷却、极端pH 值和盐浓度等都可能导致其理化稳定性降低。面对复杂多样的食品体系,传统乳化剂在某些情况下常常难以达到较好的稳定效果。为解决这些问题,以Pickering 乳液为代表的新型乳液的研究不断兴起。Pickering 乳液是一种以颗粒稳定的乳液,通过胶体颗粒在相界面上的吸附作用形成单层或多层膜从而使乳液达到稳定状态[120]。Araiza-Calahorra 等[121]用自上而下法制备了由乳清蛋白纳米凝胶颗粒稳定的Pickering 乳液并作为包埋递呈姜黄素的载体。结果表明,临界质量分数为1.0%的乳清蛋白可在Pickering 乳液液滴表面形成单颗粒层,界面处间隙尺寸极小 (约30 nm),姜黄素能较好保留在Pickering 乳液中而不会扩散释至外层介质中。
5.3 基于蛋白质的微凝胶
利用食品级生物大分子的凝胶特性,通过链间的相互交联构建具有一定三维网络空间结构的微凝胶体系(通常为0.1~1 000 μm)[122],可以起到改善疏水活性成分溶解性,提高理化稳定性和生物利用率的效果。根据三维网络中分散介质的不同,微凝胶可以分为气凝胶、有机凝胶和水凝胶[123]。许多种类的物质和结构都能被纳入微凝胶传递体系当中(图5)。负载生物活性物质微凝胶的制备首先需要使活性成分与生物大分子物质形成复合颗粒,再通过改变溶液或环境条件使复合颗粒交联形成微凝胶[124]。因此在颗粒形成步骤中,疏水性生物活性物质须先溶解在脂滴或其它疏水载体中。Brito-Oliveira 等[125]以棕榈硬脂为脂相,吐温-80 和司盘-80 为表面活性剂,制备了负载姜黄素的固体脂质颗粒,并将其填充在大豆分离蛋白-黄原胶-CaCl2复合物中,获得了乳液填充凝胶。姜黄素在最初的15 d 内有很高的稳定性,而在之后的储存过程中逐渐降解。姜黄素的降解可能与凝胶结构的溃解,硬度和持水性下降有关。Alavi等[126]用负载有姜黄素的乳清蛋白聚集体与κ-卡拉胶制备出冷固型混合水凝胶。凝胶具有很高的姜黄素负载能力,还能减缓姜黄素在上消化道的释放和降解速率,适用于生物活性物质的结肠定位输送。

图5 可被纳入微凝胶体系中的多种物质[124]Fig.5 Various kinds of substances that can be incorporated into microgel[124]
6 总结与展望
目前,姜黄素主要是作为天然色素和调味品应用于食品工业中。随着人们对健康的重视度越来越高,功能性食品越来越受市场青睐,消费者对“固体黄金”姜黄素在食品领域的应用提出了更高的要求。我国作为全球姜黄素的主要供应国之一,资源丰富,价格低廉,有着明显的优势。然而姜黄素存在的水溶性差、光热易分解、生物利用率低等问题限制了其作为食品中功能活性物质的开发利用。蛋白质作为一种人体所需的营养物质来源广泛,且具有可分解、无毒害的特点。以蛋白为活性物质载体对姜黄素进行包埋保护、稳定、缓释大大拓宽了其应用范围。
目前,传递体系在食品工业中的应用还处于初期探索阶段。寻找新型材料及制备方法,构建具有新型或改进功能特性的蛋白基传递体系仍将是该研究领域的重点。此外,每种传递体系的组成、结构、理化功能性质各有不同,传递体系与食品基质中其它组分之间的关系、对活性物质在体内代谢和生理效应的影响还有待阐明。应根据实际情况选择合适的传递体系,以保证其在食品加工、储存或使用过程的稳定性,使活性物质的功能实现最大化。相信未来在经济、环保、营养、多功能型食品发展趋势推动下,食品领域中以蛋白质为基础物质构建的传递体系会有更多的研究与应用。

