镍基CH4-CO2重整催化剂研究综述
张云飞,张晓娣,王 影,李国强,张国杰
(太原理工大学 省部共建煤基能源清洁高效利用国家重点实验室,山西 太原 030024 )
0 引 言
随着世界经济的快速增长和人口的增加,能源消耗急剧增加。但化石能源仍是目前最主要的能源。石油、天然气和煤炭等化石燃料燃烧产生大量CO2温室气体并排放到大气中,由此引起一系列环境和气候问题[1-3]。近年来,全球CO2排放量居高不下,2021年全球与能源相关的CO2排放量达363亿t[4]。除CO2外,CH4是另一种主要的温室气体。尽管与CO2相比,大气中CH4浓度较低,但其对全球变暖的贡献约为20%。因此,CH4和CO2排放的减少和转化利用对缓解温室效应尤为重要[5-6]。为了减少大气中CH4和CO2含量,研究者进行了广泛研究,以寻找将CH4和CO2转化为其他有价值产品的有效方法。由于成本低且技术相对成熟,将CO2和CH4转化为合成气是最常见的选择。其中,CH4-CO2重整(DRM)反应不仅可以同时将CH4和CO2两种温室气体转化为合成气,且产生的合成气可直接作为F-T反应的原料生产醋酸、二甲醚、长链碳氢化合物等高附加值值的化学品[7-8];同时DRM反应也可以用来储能[9],引起广泛关注。
催化剂有助于改变和提高反应速率,可最大限度地提高DRM反应中合成气的产量。 催化剂的工作原理是提供一种降低活化能的替代机制,从而减少达到过渡态所需的能量。尽管 DRM反应是强吸热反应,需要高温操作条件,但催化剂的存在可显著降低反应温度。催化剂成本与其各自的活性、选择性和稳定性之间的权衡是干重整生产合成气面临的主要挑战。目前,DRM催化系统研究主要集中于昂贵的贵金属(Ru、Pt、Rh、Ir、Pd)或可用的非贵金属(主要是Ni或Co基复合材料)两大类[10]。贵金属在高温DRM工艺条件下表现出高催化活性和稳定性;然而,高成本限制了其应用[11-12]。非贵金属Ni是目前应用于甲烷干重整(DRM)以替代贵金属廉价且丰富的催化剂活性组分,但Ni基催化剂烧结和重整条件下表面碳沉积而导致加速失活成为重大挑战[13-14]。为克服碳沉积和镍催化剂烧结的挑战,研究人员研究了各种因素来减少或消除其影响[15-17],包括改变载体、添加特定功能的助剂、改变制备路线、调控焙烧温度和改变活性金属负载量等[15],进而调控催化剂活性组分的分散性、载体与活性组分的相互作用和催化剂表面酸碱性,最终实现对Ni基催化剂催化活性、抗烧结能力以及抗积碳能力的调控[16]。为更全面了解DRM反应及近年来Ni基干重整催化剂的研究情况,笔者首先对CH4-CO2重整反应的热力学、反应机理和动力学进行综述;进一步对影响Ni基催化剂性能的载体、助剂、制备方法和焙烧温度等主要因素进行分析,介绍新型结构的Ni基干重整催化剂研究进展;最后,对Ni基DRM催化剂未来的研究方向进行展望。
1 DRM反应热力学
DRM热力学研究对确定反应温度、工作压力和最优进料比以获得高产率的合成气具有重要意义。由于DRM是一种高度吸热的可逆反应,因此需要高温条件才能将CH4和CO2转化为合成气,但催化剂的存在可显著降低反应温度、提高反应速率,同时也可以防止其他不利的副反应发生[18-19]。DRM反应是一个复杂的过程,主要反应见表1(H为反应焓变;G为吉布斯自由能)[20]。
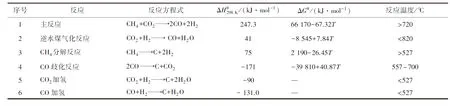
表1 DRM过程中发生的主要反应
由表1可知,DRM主反应(1)为强吸热反应,在热力学温度超过640 ℃才可能发生反应;反应为体积增大的反应,因此在低压下有利于反应向正方向进行;反应后理论生成的H2/CO体积比为1。但通常CH4-CO2重整过程中伴随着逆水煤气变换反应(RWGS)(2)发生,导致DRM反应后生成的H2/CO体积比小于1。尽管产生的H2/CO体积比小于1对重整反应不太理想,但其可用于F-T合成以生产高级烃。由热力学计算可知,RWGS反应发生的温度在527~820 ℃,在此范围以外其影响可以忽略不计;另外,在较低反应温度且CH4/CO2体积比大于1时,RWGS反应不发生;但当反应温度高于700 ℃,且CH4/CO2体积比小于1时,RWGS反应强烈,结果导致产品气中H2产率不断减小,CO产率不断增加;此外,高压也有利于RWGS反应发生。研究发现,副反应与原料气的CH4/CO2体积比(进料比)、反应温度和反应压力等因素都有一定关系[21]。积碳的产生往往不利于反应进行,因为其会覆盖在催化剂活性位点表面或堵塞孔结构导致催化剂失活。积碳通常被认为是由CH4分解反应(3)和CO歧化反应(Boudouard reaction)(4)产生;有研究者认为反应(5)和(6)也会产生积碳[22]。当CH4/CO2体积比大于1时,CH4分解反应(3)是积碳产生的主反应;当CH4/CO2体积比小于1时,CO歧化反应(4)、CO2的加氢反应(5)和CO的加氢反应(6)是积碳产生的主反应。尽管高温有利于DRM反应的进行,然而研究表明即使在高温条件下,较高的压力会抑制反应进行。高压不利于CH4的裂解反应(3)和CO歧化反应(4)进行,不仅导致CH4和CO2的转化率降低,也会增加催化剂积碳量[23]。SHAMSI等[24]通过热力学研究发现,CH4裂解产生的积碳随反应压力的增加而减小,CO歧化反应产生的积碳随压力的增加而增加,高压下积碳主要由CO歧化反应产生,尤其是CH4/CO2体积比小于1时更为显著。另外,在催化剂表面上形成的积碳很大程度上取决于温度,在典型的DRM反应条件下(800 ℃),积碳主要由CH4裂解产生;而在600~700 ℃时,积碳主要由Boudouard反应产生[25]。研究者发现[20],CH4在557 ℃以上才能发生分解,Boudouard反应在700 ℃以下才会发生,RWGS在低于820 ℃下发生反应;在557~700 ℃主要发生CH4裂解和Boudouard反应而产生积碳。因此,DRM反应应该控制在850 ℃以上。较高的温度会抑制其他副反应发生,从而促进DRM反应进行;DRM反应的最佳温度在870~1 040 ℃,其中原料气的CO2/CH4最佳体积比为1∶1。
进一步,KAREMORE等[26]研究了反应空速、反应温度、CH4/CO2体积比对Ni/MgO-Al2O3和Ni-Pt/Al2O3干重整催化剂催化性能的影响,研究发现2种催化剂虽然CH4/CO2进料比为1,但由于逆水煤气反应的发生,产物H2/CO体积比均小于1;当进料中CO2/CH4体积比低于1时,CH4转化率低于CO2转化率;反而当CO2/CH4体积比大于1时,CO2转化率低于CH4转化率。CH4和CO2转化率以及H2和CO收率随反应空速的增加而减小,CH4和CO2转化率随反应温度的增加而增加。CAO等[27]考查了DRM反应温度、压力、CH4/CO2体积比对CH4和CO2转化率、H2和CO产率以及碳产率的影响,发现较低的CH4/CO2物质的量比有利于提高CH4转化率和CO选择性,但会阻碍CO2转化率和H2选择性;增加压力会降低CH4转化率、CO2转化率、H2选择性和CO选择性。进一步研究还发现,当DRM操作温度提高到700 ℃以上时,在常压和CH4/CO2物质的量比不大于1条件下,获得的H2/CO物质的量比适合直接用于烯烃、重质烃和含氧化合物的合成。
综上所述,高温低压有利于DRM反应进行。根据热力学优化的DRM反应最佳操作条件为:重整反应温度870~1 040 ℃、常压、CH4/CO2体积比为1时,在此条件下反应具有较高的CH4和CO2转化率、H2选择性和CO选择性、合理的H2/CO体积比(约为1),且反应产生的积碳量最少。
2 DRM反应动力学和机理研究
DRM反应是一个复杂的过程,根据反应中间体形成的难易程度,DRM在不同的催化剂体系和反应条件下的机理差异显著[28]。众多研究表明,DRM的关键步骤是CH4在催化剂表面的吸附和解离。在低温下,CH4解离逐渐进行,在高温下解离迅速进行。通常DRM反应被认为有2种反应机理,在第1种反应机理(单功能机理)中,CO2和CH4在同一金属位点被活化[29]。这种反应机理认为,CH4被吸附在活性金属表面上解离生成H2和碳氢化合物,CO2在金属表面上解离产生吸附的CO和O;吸附的O和吸附的CHx在金属位点上反应生成CO和H;同时,氧和吸附的H反应生成羟基,羟基移动到载体上或与H结合形成水分子,具体的反应机理主要步骤见表2[30]。在第2种反应机理(双功能机理)中,CH4在金属活性位上被活化,而CO2在载体上被活化。在金属表面上,CH4被直接解离或间接解离。在反应过程中,会形成次甲基或甲酰基中间体,其中氧来自载体。具体的反应机理主要步骤见表3[31]。
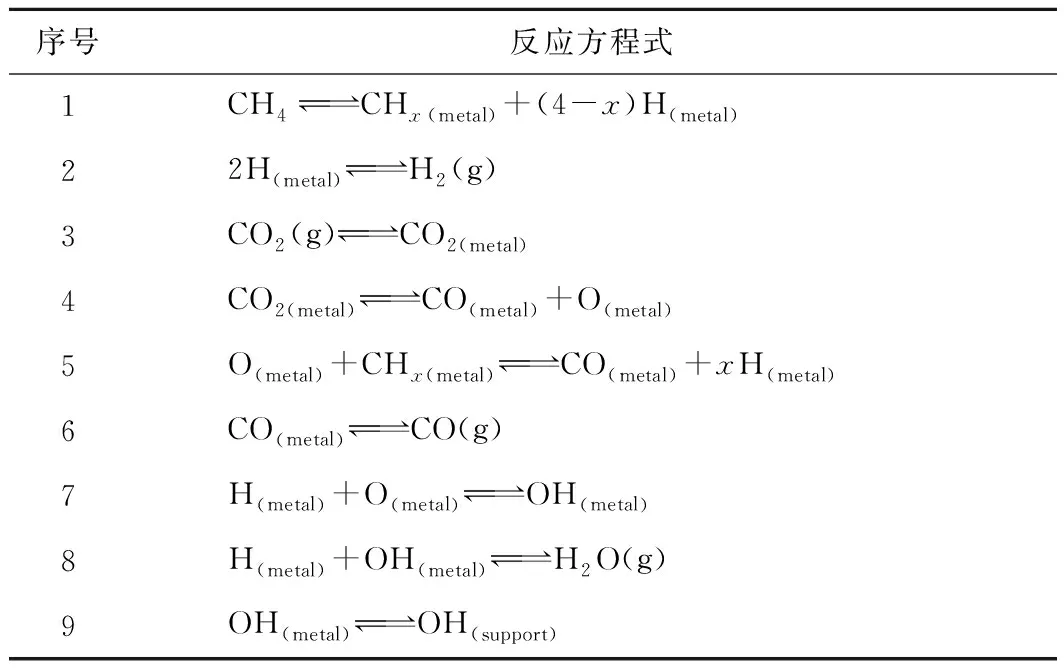
表2 单功能机理反应步骤
ZHANG等[32]通过原位DRIFTS手段证明DRM在NixAl1O2-δ催化剂上反应符合上述第1种反应机理,即CH4和CO2在NixAl1O2-δ表面上吸附和活化,CH4在金属表面的活性位点上分解形成被吸附的CHx和H物种。在H物种的协助下,碳酸盐和甲酸盐吸附在金属镍活性位点和载体之间的界面上,引起CO2活化。其反应机理和模型如图1(a)所示,具体的反应机理方程式如式(1)~(11)所示。

(1)

(2)

(3)

(4)

(5)

(6)

(7)

(8)

(9)

(10)

(11)
其中,*为催化剂表面的吸附位点;Ov为NiAl2O4上的氧空位。
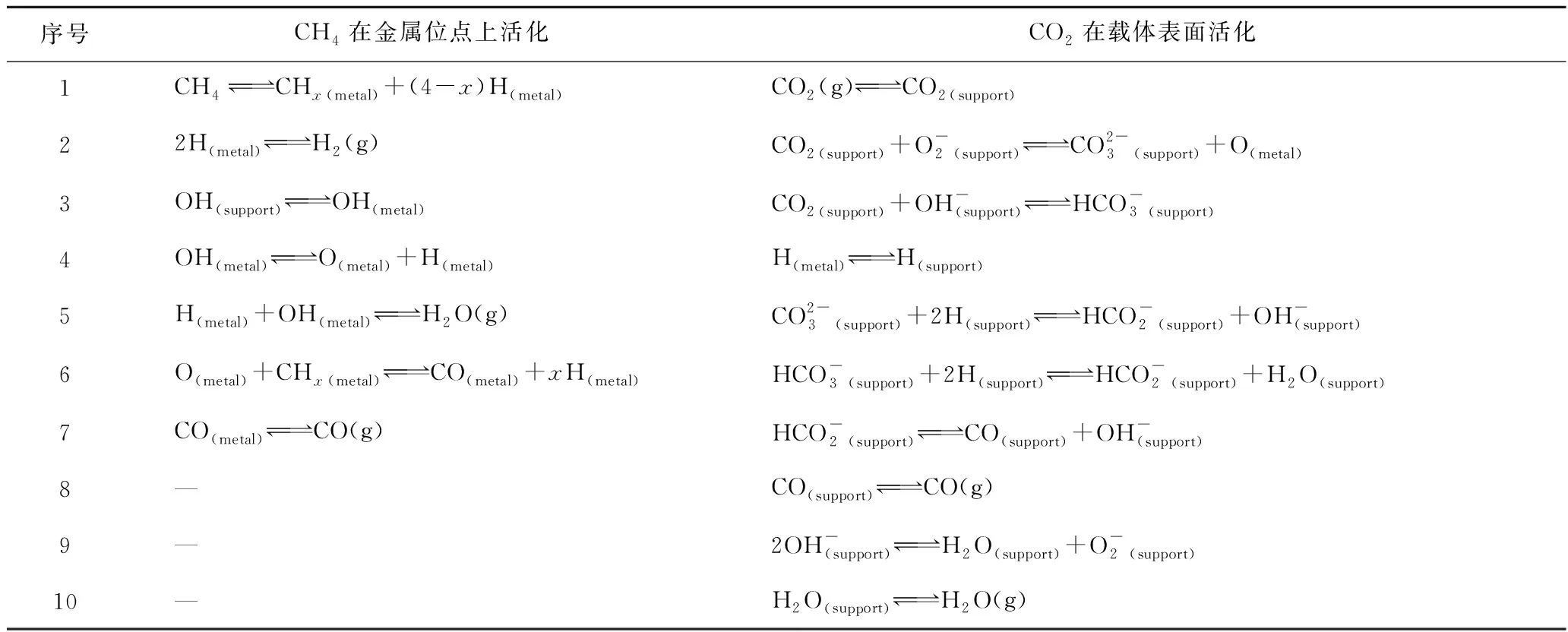
表3 双功能机理反应步骤
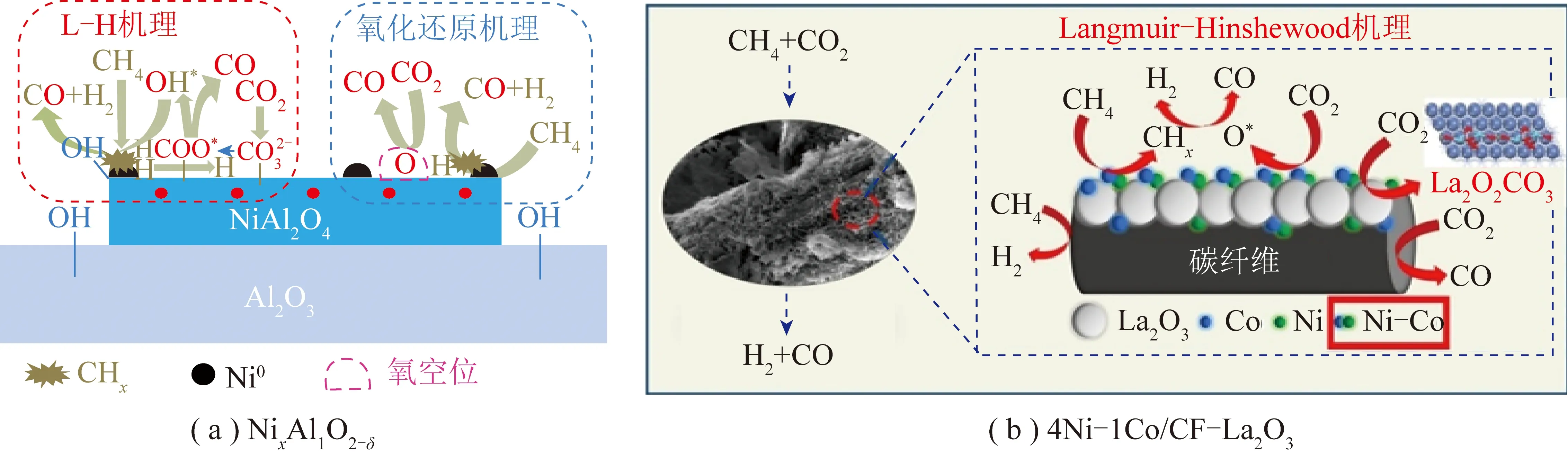
图1 催化剂上DRM反应的反应机理示意Fig.1 Schematic diagram of reaction mechanism of DRM reactions of catalysts
JANGAM等[33]研究了2种不同形貌Ni/La2O3催化剂的DRM反应机理,其假设模型和机理如图2所示。CH4在Ni表面发生活化和解离,形成H2和活性中间物质;CO2被吸附在La2O3上形成La2O2CO3,然后与相邻的活性碳质中间物反应生成CO,并完成La2O2CO3和La2O3之间的循环。需要注意的是,反应过程中形成的La2O2CO3只能与附近Ni颗粒与载体界面上的积碳发生反应。因此,活性金属的分散性越好,La2O2CO3就会及时参与消碳;金属分散性差,La2O2CO3会产生积累。因此,La2O2CO3可以作为反应活性金属在La2O3载体上分散程度的评价指标。
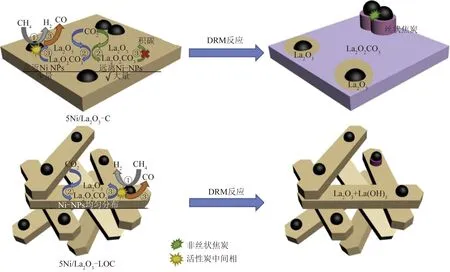
图2 不同 Ni/La2O3 形貌的反应机理示意 Fig.2 Schematic of reaction mechanism on difffferent Ni/La2O3 morphologies
研究者[34]对Ni/CeO2和Ni/6MnOx-CeO2催化DRM反应机理进行了分析,提出了2种反应路径。路径I中,甲烷在镍活性位点上快速裂解为CHx和Hx,然后CO2吸附到金属表面与产生的Hx反应生成碳酸氢盐;同时,CHx在金属表面进一步分解为C和H2(g)或Hx。生成的碳酸氢盐进一步与Hx反应生成CO和H2O,活性位点上的碳与可流动氧发生氧化反应。路径Ⅱ中,甲烷直接与流动氧反应产生羰基类的中间物质;吸附的羰基中间体与Hx反应分解成CHx和OH,或解吸生成CO,Hx也可以解吸生成H2。此外,CHx可以分解为C和H2或Hx;形成的碳通过路径 I 再次与可流动氧发生氧化反应。WEI等[35]通过DFT计算对4Ni-1Co/CF-La2O3催化DRM反应进行了动力学和反应机理研究,其假设模型和机理如图1(b)所示。研究发现,4Ni-1Co/CF-La2O3上发生的DRM反应过程基本符合LH机理:其中部分CO2在碳纤维和活性金属上分解生成CO*和O*,另一部分CO2与La2O3反应形成La2O2CO3中间产物,在催化剂表面上与碳纤维反应再生成La2O3和CO。与CO2解离相似,在碳纤维和活性金属上面CH4直接裂解生成CHx和H2。生成的O*和CO*活性基团,进一步与CH4裂解生成的中间产物生成CO和H2。
动力学研究通常采用经验或理论反应速率模型拟合的试验结果,并描述反应速率、定义化学过程。此外,通过动力学研究结果可进一步优化催化剂和反应器设计,从而改善DRM反应的效率。常用的动力学模型有3种:幂律模型、Eley-Rideal (ER) 模型和 Langmuir-Hinshelwood-Hougen-Watson (LHHW)模型。早期,幂律模型因参数应用和估计方法简单而被广泛使用。尽管该模型有助于进行初步估计并获得有效信息,但并不能合理解释各种催化剂上的反应动力学,特别是解释发生在催化剂表面反应机制中各步骤方面存在局限性。LHHW模型由于提出的大多数机理步骤与表征结果相一致,因此被广泛用于DRM反应研究。在LHHW模型中,假设一个反应步骤缓慢并且由速率决定,其他反应步骤处于热力学平衡[36]。根据该模型,FOO等[37]提出了双金属Co-Ni/Al2O3催化剂催化DRM反应机理,如式(12)~(20)所示:

(12)

(13)

(14)

(15)

(16)

(17)

(18)
H-X1+O-X2→OH-X2+X1,
(19)
H-X1+OH-X2→H2O+X2+X1,
(20)
式中,X1和X2为2个不同的位点。
根据LH模型,方程(16)为速控步骤,则CH4反应速率可表示为:
-r(CH4)=
(21)
K(rxn)=Aexp(-Ea/RT),
(22)
(23)
(24)
式中,K(rxn)为反应的速率常数;P(CH4)为CH4分压;P(CO2)为CO2分压;K(CH4)为CH4吸附常数;K(CO2)为CO2吸附常数;A为指前因子;Ea为反应活化能;△S(CH4)ads为CH4的吸附熵;△H(CH4)ads为CH4的吸附焓;△S(CO2)ads为CO2的吸附熵;△H(CO2)ads为CO2的吸附焓。
同样,根据上述模型,SHAH等[38]提出Ni/La-Al2O3催化干重整反应机理如式(25)~(28)所示:
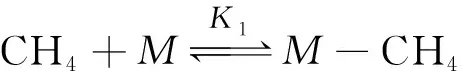
(25)
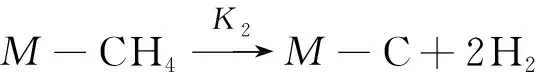
(26)
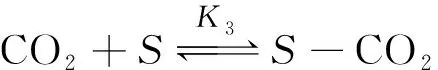
(27)
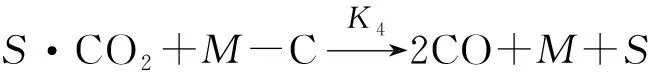
(28)
式中,M为活性金属位点;S为载体表面位点。
同时,提出了重整反应过程中的副反应RWGS反应机理,如式(29)~(31)所示:

(29)

(30)

(31)
同样,根据上述模型,Ni活性位点上CH4的裂解反应为速控步骤,CH4反应速率表示为
(32)
式中,K1和K3分别为式(25)和式(27)反应步骤的吸附常数;K2和K4分别为式(26)和式(28)反应的速率常数。
CH4-CO2重整反应过程主要与表面氧原子、氢原子和催化剂表面活性位点有关。虽然,傅里叶变换漫反射红外、同位素瞬态动力学和产物瞬态分析等技术已经被用来研究DRM反应的动力学和反应机理。但是,至今没有统一的反应机理适用于所有催化剂。不同的催化剂有不同的反应机理和不同的速控步骤,动力学结果也不尽相同。但对DRM反应的动力学和机理进一步研究可优化催化剂,从而提高CH4-CO2重整催化剂的催化性能。
3 Ni基催化剂性能的影响因素
3.1 载体的影响
载体是催化剂的重要组成部分,载体在反应中虽然本身不具有活性,但可以从整体上改变催化剂性能。载体结构对催化剂活性金属的物理化学性质、微晶尺寸、酸度、碱度、氧迁移率和表面积都会产生影响。载体与活性金属的相互作用可促进金属分散、抑制活性组分烧结,加速催化剂还原、减少或消除积碳[39]。DRM反应Ni基催化剂常用的载体有Al2O3、MgO、ZrO2、SiO2等。其中,Al2O3具有容易获得、成本较低、比表面积大和金属分散性好等优点,因而常被用来做载体。TALKHONCHEH等[40]考察了不同载体对镍基催化剂的影响,发现Ni/CeO2催化剂的活性组分分散最好;而Ni/Al2O3纳米催化剂不仅具有分布均匀的活性金属和良好的镍含量,且具有高比表面积,展现出最佳的催化性能。SUN等[41]制备了负载在纳米片(S)和纳米板(P)γ-Al2O3上的Ni基催化剂,制备的Ni/Al2O3-S和Ni/Al2O3-P的比表面积分别达245.6和48.5 m2/g;高比表面积有助于活性组分分散,致使Ni 具有较小的尺寸,从而提高了Ni/Al2O3-S金属-载体的相互作用,提高了催化剂的稳定性。进一步,AQANS等[42]采用铝罐粉末合成的氧化铝为载体制备了Ni/Al2O3催化剂,研究发现铝罐粉末中含有的Mg、Mn、Fe和K等元素与活性金属相互作用提高了催化剂的催化性能。
氧化镁由于具有良好的热稳定性和较好的碱度,也常被用来做DRM催化剂的载体。USMAN等[43]采用微乳液法合成了比表面积为153.22 m2/g的Ni/MgO催化剂,形成的Ni-MgO固溶体使活性组分具有很好的分散性,具有很高的催化活性和稳定性。PARK等[44]研究发现,向Ni/Al2O3催化剂中添加MgO可以改善MgAl2O4尖晶石结构和碱度,有助于CH4和CO2分子的活化;进一步研究还发现,载体MgO∶Al2O3的比例不仅会影响催化剂的碱度,还会影响催化剂的分散性和催化剂表面的还原性;MgO过多时会形成NiO-MgO固溶体导致催化剂还原温度升高、分散度减小;优化得到的MgO∶Al2O3=3∶7时,催化剂的催化性能最好。HUANG等[45]以介孔MgO-ZrO2为载体制备了Ni基催化剂,发现当制备载体的孔径为10 nm时有助于活性组分的分散,同时具有较好的还原性;当Ni负载量为10%时,制备催化剂的分散度最好,活性最高。
ZrO2因其具有良好的表面酸碱性和热稳定性而被广泛用作DRM催化剂的载体。IBRAHIM等[46]研究了不同原料制备的ZrO2载体(RC-100、Z-3215、MKnano和ELTN)对催化剂性能的影响,结果发现不同原料制备的ZrO2载体对催化剂性能具有显著影响。5Ni-RC-100催化剂活性组分分散性最好,平均粒径为3.35 nm,且其具有最高的碱度;同样反应条件下,5Ni-RC-100催化剂的CH4转化率比5Ni-ELTN高44%,而且反应后产生的积碳量最少。ZHANG等[47]研究了焙烧氛围对制备Ni/ZrO2催化剂性能的影响,发现O2气氛下焙烧出的催化剂Ni分散度最好,且N2和O2气氛下焙烧出活性组分Ni能够掺入到稳定亚稳态四方ZrO2结构中,具有更多的氧空位和更高的氧迁移率。ZHANG等[48]对比了Ni/SBA-15和Ni/ZrO2的抗积碳性能,发现Ni/SBA-15更易产生积碳而失活,而由于ZrO2表面氧物质可以与生成的积碳反应消碳,使催化剂表现出更高的催化活性和稳定性。
CeO2因具有很强的储氧能力和氧迁移率,能提高催化剂的活性和抗积碳性能,也经常被用作催化剂的载体。WANG等[49]研究了CeO2材料的形貌和晶面对Ni/CeO2在甲烷干重整中催化性能的影响,研究发现Ni可以掺入晶格中,并占据CeO2纳米材料中的空位来诱导氧空位的增加,使Ni与CeO2纳米棒的相互作用更强,从而有助于锚定Ni纳米颗粒;同时氧空位和晶格氧的迁移率有助于消除积碳。LIU等[50]研究发现,Ni/CeO2对DRM反应非常活跃,金属和载体之间的强金属相互作用增强了Ni对CH4解离的反应活性,并有效防止积碳的生成。TURAP等[51]制备了Ni-Co/CeO2双金属催化剂用于重整反应,研究发现载体CeO2的强储氧能力和Co的强亲氧能力有助于消除积碳;当Co/Ni比为0.8时,催化剂的活性和稳定性最好。KHAJENOORI等[52]制备了不同Ni/Ce的催化剂,当CeO2质量分数为7%时,发现Ni负载量小于10%时,CH4和CO2转化率随Ni含量的增加而增加;Ni负载量超过10%时,Ni微晶尺寸增大,分散性下降,导致催化性能下降。
SiO2因具有比表面积大和金属分散性好等优点,常被用作催化剂的载体[53]。SiO2的多孔性和大比表面积可有效促进活性组分的分散及抑制活性组分的团聚,提高催化剂的稳定性。万吉纯等[54]采用氨辅助浸渍法制备了Ni/SiO2催化剂,研究发现浸渍过程加入氨水显著改善了活性组分的分散度,焙烧后生成的镍硅酸盐物种促进了载体与活性组分的相互作用力,提高了催化剂的抗烧结能力。KWEON等[55]通过Ni-MWW沸石转化合成了具有3D大孔结构的Ni/BEA催化剂,研究发现BEA三维大孔体系有利于Ni的高度分散,使制备的Ni/BEA催化剂显示出更高的催化活性和稳定性。WANG等[56]以不同孔结构的介孔载体用于负载LaNiO3钙钛矿制备了系列催化剂(LaNiO3/SBA-15、LaNiO3/MCM-41和LaNiO3/SiO2)用于DRM,反应后催化剂的TEM图像和金属颗粒粒径如图3所示。由图3可知,反应后LaNiO3/SBA-15活性粒子粒径最小,且反应后介孔结构仍保持完整,这主要是因为LaNiO3/SBA-15规则的介孔结构限制了Ni物种的团聚;LaNiO3/MCM-41的介孔结构在反应过程中被破坏,导致金属颗粒发生聚集;而LaNiO3/SiO2稳定性最差,且反应后产生大量积碳。
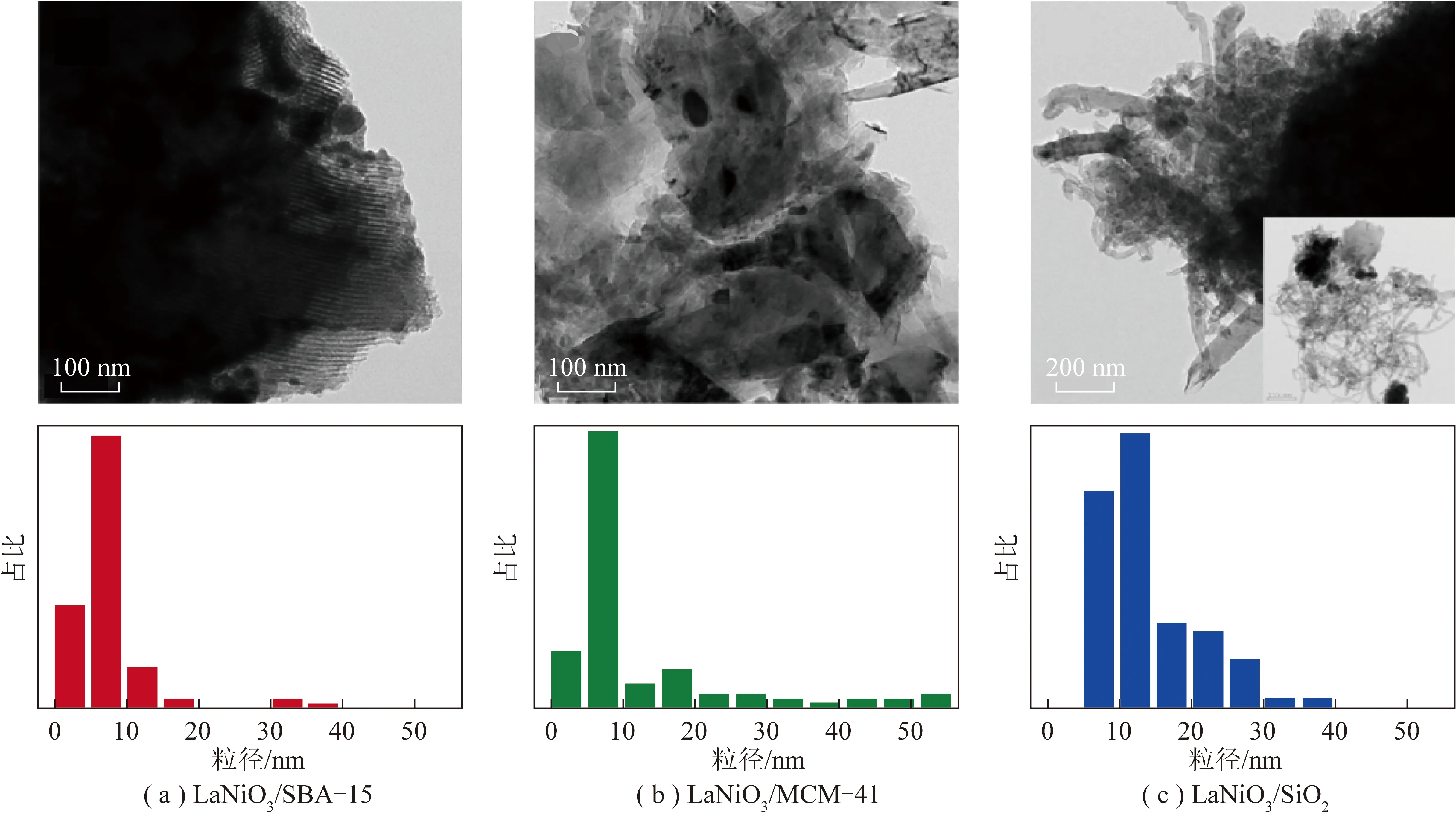
图3 用过的样品的 TEM图像和镍粒度分布Fig.3 TEM images and Ni particle size distribution of used samples
碳材料,如活性炭、碳纳米管、碳纳米纤维等,因其成本低、比表面积大、稳定性强、化学惰性好和表面化学性质易被改性而被用作Ni基催化剂载体。FIDALGO等[57]考察了活性炭载体的表面氧化、干燥方法、还原温度对Ni/AC重整催化剂性能的影响,研究表明活性炭载体的氧化有利于提高Ni组分与载体的相互作用力从而提高活性组分分散性,还原温度对粒径大小也有很大影响,微波干燥大大缩短了干燥时间且获得的Ni颗粒更小、催化活性更好。WANG等[58]以活性炭为载体制备了Ni/AC干重整催化剂用于等离子体辅助DRM反应,研究发现与无等离子体相比,等离子体的催化剂比表面积更高、金属与载体的相互作用(SMSI)更强,因此DRM催化性能更优越。LI等[59]以椰子壳活性炭为载体制备了双金属Ni-Co/AC干重整催化剂,研究发现部分金属颗粒分布在活性炭孔结构中有效抑制了团聚,Ni∶Co质量比为2∶1时催化剂金属粒径最小为4.4 nm,此外催化剂表面含有丰富的含氧官能团显著提高了催化性能,900 ℃、12 h稳定性评价后催化剂无积碳产生。AFANDI等[60]以水热浸渍法制备了Ni-Ce/CNT催化剂,研究发现水热法制备的催化剂活性金属均匀地分散在载体表面,与载体有较强的相互作用力,同时催化剂表面存在大量含氧基团,800 ℃反应30 h后催化剂未明显失活,积碳量为2%。YOUSEFPOR等[61]以介孔碳CMK-3为载体,Sm为助剂制备了Ni-Sm/CMK-3干重整催化剂,发现添加Sm显著增强催化剂活性组分分散,减小了活性组分的粒径,从而提高了催化剂的活性和稳定性。YU等[62]制备了一系列Ni/Al2O3-ACF催化剂,研究发现Al2O3与ACF的最佳比例为1∶1,在Ni/γ-Al2O3中添加ACF有利于提高DRM反应催化活性,这是因为ACF上的Ni和Al2O3涂层抑制了ACF与CO2反应,ACF表面的大量碱性位点有利于CO2吸附和活化,加速了积碳的消除,同时Ni和Al2O3形成的固溶体增强了Ni组分分散。笔者课题组[63]以有序介孔二氧化硅-碳(MSC)为载体制备了一系列Ni基甲烷干重整催化剂,研究发现以强碱性NaOH为沉淀剂,采用沉淀法制备的催化剂前驱体中形成了Ni3Si2O5(OH)4纳米薄片,其与载体的结合更加紧密,从而使Ni分散度更高,催化活性更高。此外,Ni3Si2O5(OH)4物种与载体之间的强相互作用也有利于抑制烧结和积碳生成。不同载体所负载Ni催化剂甲烷干重整性能见表4。
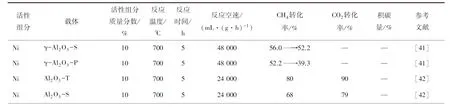
表4 不同载体Ni基催化剂催化性能
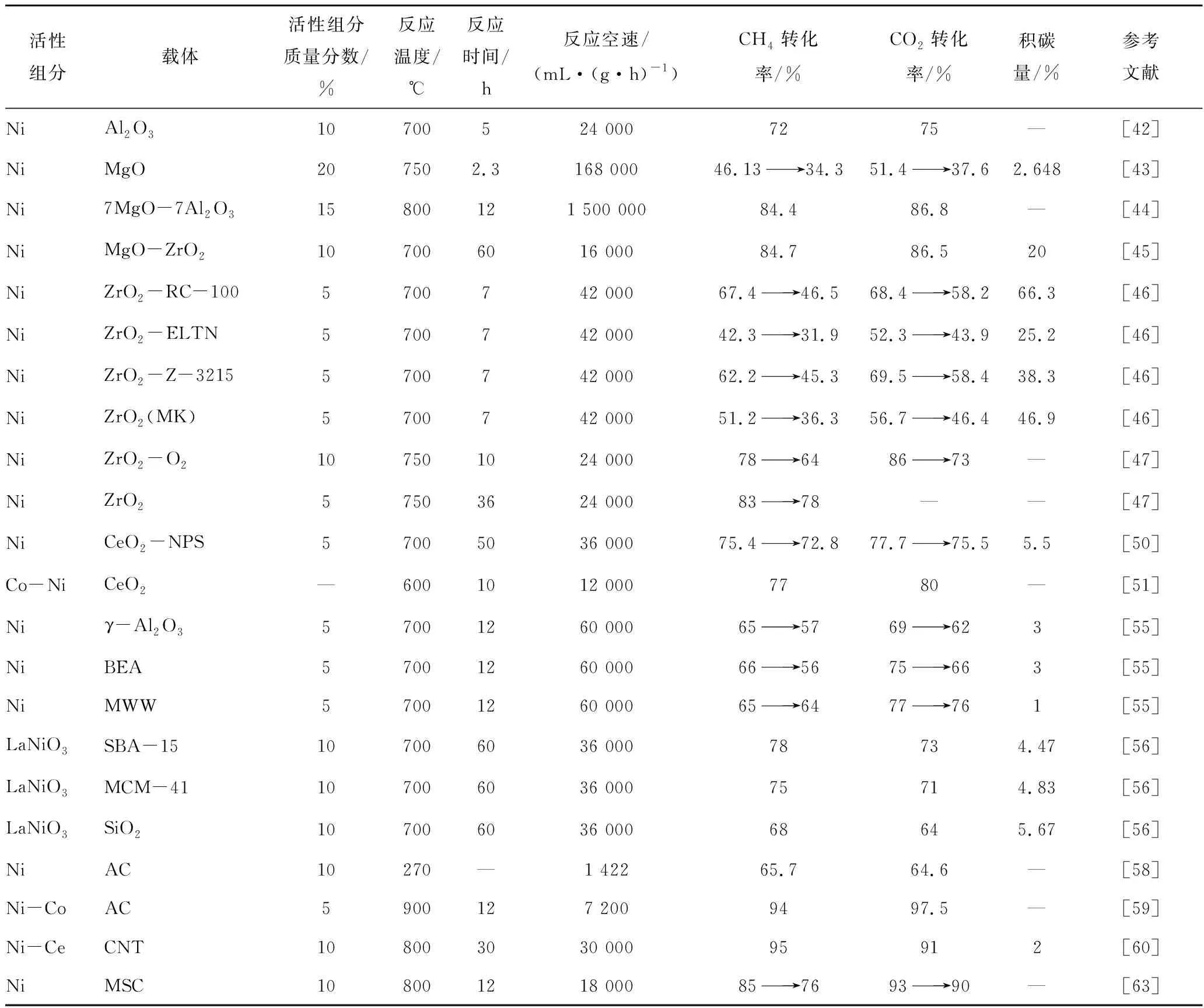
续表
综上所述,不同载体的催化剂,催化性能和稳定性明显不同,载体的比表面积、孔隙结构、与活性金属组分间的相互作用、表面酸碱性和活性金属的分散性对催化剂的性能影响显著。其中,Al2O3和SiO2具有较大的比表面积,有利于提高金属分散性;表面强碱性的MgO有助于促进对CO2的吸附和活化;ZrO2的电子效应能与活性组分形成强相互作用力,促进活性组分的分散,有助于提高催化剂的抗积碳性能;CeO2具有很强的氧吸附和解离能力,能显著提高催化剂的抗积碳性能。介孔SiO2规整的孔结构能均匀分散活性金属,有效抑制活性组分的烧结,从而提高催化剂的抗烧结和抗积碳能力。碳材料具有发达的孔结构和大比表面积,有利于活性组分的分散和CO2的吸附,通过对其表面化学性质进行改性可有效提高催化剂的催化性能。
3.2 助剂的影响
在催化剂中加入助剂不仅可以改善催化剂表面的酸碱度和金属与载体的相互作用,且可以调节活性金属相的电子密度,从而改善金属分散性。助剂还有助于CH4和CO2的吸附、解离和活化,从而提高催化剂的反应效率和抗积碳能力。碱金属(Na和K)、碱土金属(Mg和Ca)的氧化物、稀土金属(Ce和La)氧化物及其混合物都是常用助剂。AZANCOT等[64]研究了不同含量助剂K对Ni/MgAl2O4甲烷干重整催化剂抗积碳能力的影响,发现添加的助剂钾会在载体上产生强烈的Mg-O-K碱性位点,从而形成具有较好热稳定性的碳酸盐物质,促进积碳气化反应,提高催化剂的抗积碳性能。催化剂反应15 h后的热重曲线如图4(a)所示,对比发现,加入K有助于减少积碳;当K添加质量分数高于3%时,添加的助剂K降低了CH4裂解C*物质的成核率,有效加速了积碳的气化,从而显著降低催化剂反应后产生的积碳量,提高催化剂的稳定性。JIN等[65]采用浸渍法将不同数量MgO负载在Ni/Al2O3催化剂上,催化剂的CO2-TPD曲线如图4(b)所示。由图4(b)可知,CO2吸附量随MgO添加量的增加而增加,表明MgO助剂的添加提高了催化剂表面的碱量和碱强度,这有助于CO2的吸附和活化;同时加入MgO助剂与活性金属形成NiO-MgO固溶体,在还原后仍有一部分Ni2+残留在MgO晶格中形成缺陷,与MgO形成强相互作用,进而抑制Ni的烧结;并为CO2活化提供足够的金属-载体界面,提高了副反应产生表面碳的氧化速率,因此不仅提高了重整速率,且抑制了积碳的形成。AL-FATESH[66]将不同含量的助剂Ce添加于MCM-41负载的镍催化剂用于甲烷DRM反应,发现添加Ce助剂后催化剂表面碱性位点增加,有助于CO2的吸附;同时添加的助剂增强了活性组分与载体间的相互作用力,促进了CH4的分解;而且外表面的二氧化铈薄层含有丰富的表面氧物种,有助于积碳的氧化,从而使催化剂表现出优秀的催化性能。但当Ce负载量超过0.5%时,过量的二氧化铈层会掩盖活性Ni位点,从而导致碱性位点数量减少,催化性能变差。RODRIGUEZ-GOMEZ 等[67]研究发现,助剂Ce的添加有效改善了活性组分Ni在SBA-15载体中孔内的分散,从而有效抑制了积碳的产生。SUN等[68]研究了助剂CaO的添加对Ni/HMS催化剂干重整性能的影响,发现助剂CaO的加入不仅显著增强了金属与载体的相互作用,而且促进了CO2的吸附、活化,加速了积碳消除,降低了积碳的石墨化程度;当Ni/Ca的质量比为3∶2时,催化剂表现出最好的稳定性。
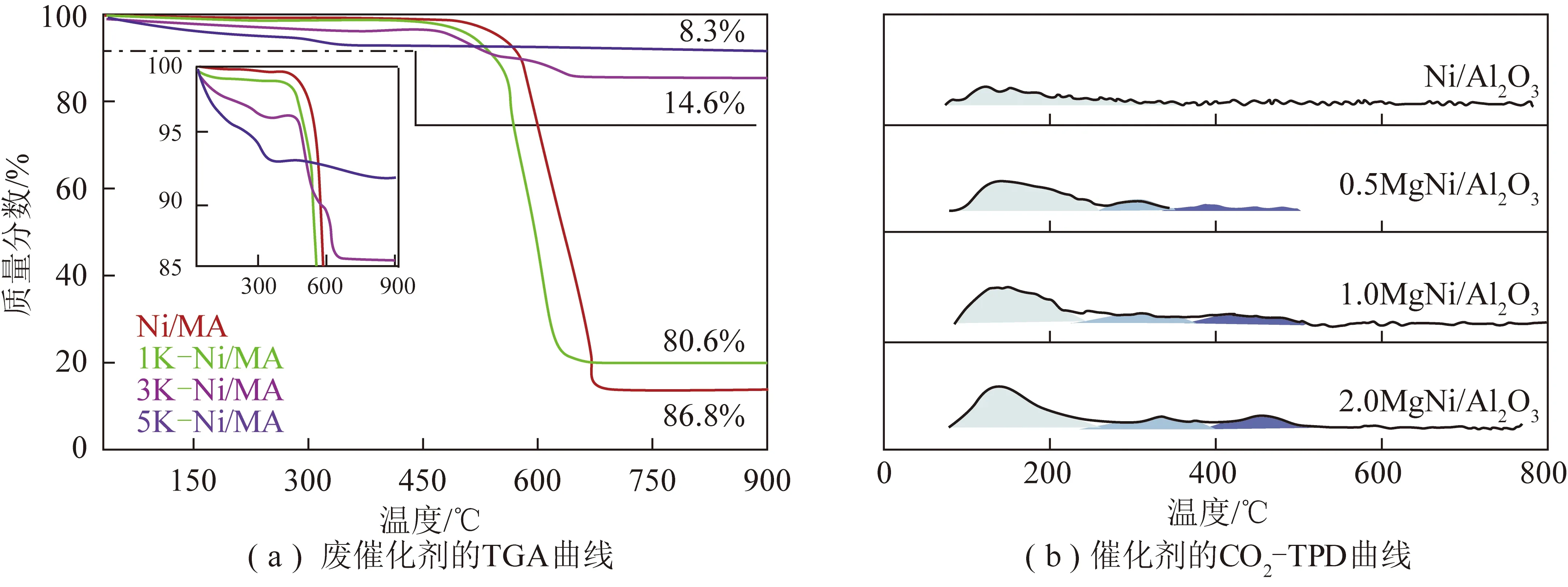
图4 甲烷干重整后废催化剂的TGA 曲线及CO2-TPD曲线[63-64]Fig.4 TGA curves and CO2-TPD curves of all spent catalysts after methane dry reforming[63-64]
研究发现,在Ni基催化剂中添加第2种金属也可以改善催化剂的性能,增加活性组分的分散性,提高催化剂的稳定性和抗积碳能力。LUISETTO等[69]研究了在催化剂Ni/Me-DC上添加不同掺杂剂对CH4干重整催化性能的作用,发现掺杂不同金属后催化剂载体表面氧缺陷的数量明显变化,其顺序为La-DC≈Sm-DC > Zr-DC > CeO2;较多的氧缺陷可有效提高催化剂的抗积碳能力,800 ℃反应50 h后,Ni/Sm-DC和Ni/La-DC积碳最少。ABDULLAH等[70]考察了不同Zr添加量对Ni/SBA-15催化CH4干重整催化性能的影响,发现Zr物种的添加不仅有效促进了Ni活性位点在催化剂表面上的分散,且提高了氧原子迁移率,促进CO2分子的活化和还原;当Zr负载量为1%时,催化剂性能最好。AL-FATESH等[71]研究了助剂钪的添加对Ni/MCM-41 催化剂活性的影响,结果发现Sc的加入不仅加强了Ni与载体的相互作用,也增加了催化剂的碱度,进而提高了对CO2的吸附能力,抑制了积碳的形成,提高了催化剂的稳定性。LI等[72]考察了镧系金属及其氧化物的添加对Ni基催化剂催化甲烷干重整性能的影响,发现添加不同镧系金属对活性金属Ni的粒径具有明显影响,其中添加La和Ce催化剂的Ni纳米颗粒尺寸相对较小,为4 nm;而添加Sm和Gd的晶粒较大,约8 nm。进一步研究发现,添加的镧系元素氧化物对CH4解离和CO2解离、活化也有显著影响,与Ni/SiO2相比,添加的Sm和Gd会抑制CO2解离,而添加的Ce和La可有效促进CO2解离,从而提高催化活性和稳定性。LI等[73]考察了双金属Ni-Co/Al2O3催化剂干重整的催化性能,发现添加的金属Co与活性金属Ni形成了Ni-Co合金,提高了CH4解离的活化能,抑制了CH4裂解的活性;同时添加的Co提高了催化剂的亲氧能力,有助于消碳,提高了催化剂的抗积碳能力。HAN等[74]考察了Cu添加对Ni/SiO2催化性能的影响,研究发现Cu的加入显著提高了催化剂的活性和稳定性,这主要是因为形成的Ni-Cu合金有效提高了活性组分的分散性,同时促进了CO2的活化。GARCIA-DIEGUEZ等[75]制备了双金属Ni-Pt/Al2O3催化剂用于干重整反应,发现添加的Pt与Ni形成了Pt-Ni合金,生成合金,不仅减小了活性金属的粒径,且提高了催化剂活性和稳定性,减少了积碳的生成。添加不同助剂的Ni基催化剂甲烷干重整性能见表5。
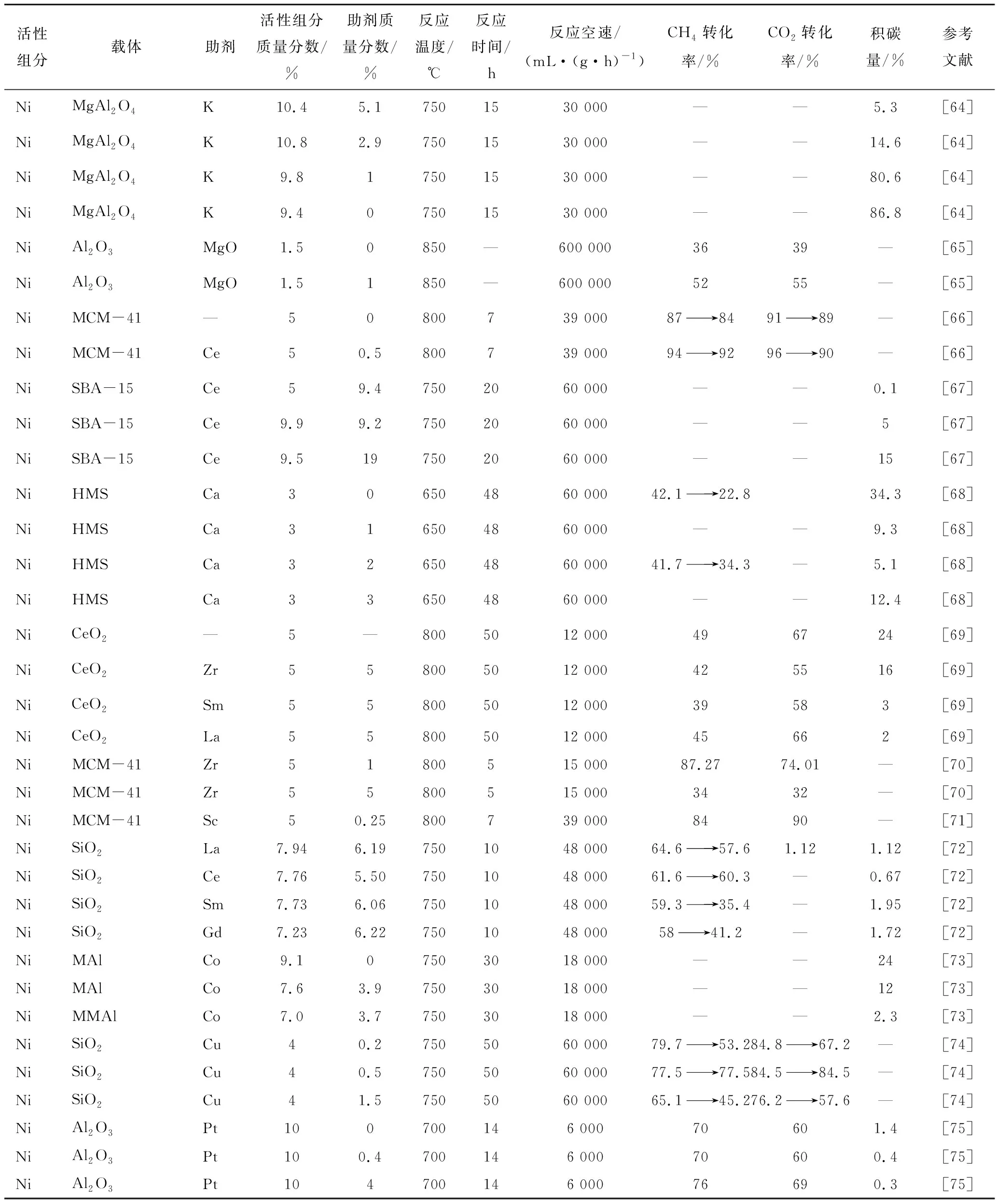
表5 不同助剂Ni基干重整催化剂催化性能
综上,添加助剂不仅可以调节催化剂表面的酸碱度、增强载体与活性组分的相互作用力、提高活性金属粒子的分散性,且能提高对CH4和CO2的吸附、活化和解离能力,从而改善催化剂的催化活性,提高催化剂的抗积碳性能。其中,碱金属和碱土金属及其氧化物的添加可以增加催化剂表面碱性度,从而提高对CO2的吸附能力,降低CH4脱氢的活性,提高催化剂的稳定性和抗积碳性能。而镧系金属及其氧化物的添加可以影响CH4解离和CO2解离的活化能,改变催化剂的活性和稳定性。添加的第二金属可以协同提高载体与活性组分的相互作用力和提高金属的分散度,进而提高催化剂的稳定性和抗积碳能力。
3.3 制备方法的影响
不同催化剂的制备方法对催化剂的性能,催化剂的组成、结构、尺寸和活性金属的分散度产生不同影响,进而影响催化剂的活性、稳定性、抗积碳能力和抗烧结能力。张堉彬等[76]采用4种不同的制备方式制备了不同的Ni-Co/MgO催化剂,发现采用沉积沉淀法,在制备过程中可以为活性组分Ni2+和Co2+的完全水解沉淀提供好的碱性环境,不仅使得粒子的成核和生长速率较快,而且避免了局部过饱和现象,制备的催化剂活性组分粒径较小,分散度更高,从而表现出较好的催化活性和强抗积碳性能。AHMAD等[77]考察了溶液燃烧法、溶胶-凝胶法、均相沉淀法、溶剂热法和改性油胺-辅助合成法5种不同制备方法对合成Ni/La2O3-X催化剂干重整性能的影响,发现通过溶液燃烧法制备的Ni/La-SC催化剂具有最小的Ni晶粒尺寸、高Ni0/Ni2+比值、大比表面积,高活性组分分散性,从而表现出最好的催化活性、稳定性和抗积碳性。SUN等[78]考察了湿法浸渍、柠檬酸辅助浸渍和氨蒸发3种不同制备方法对合成Ni/SBA-16催化剂干重整性能的影响,发现氨蒸发法制备的催化剂Ni/SBA-16-AE催化性能最佳,这主要是由于氨蒸发制备过程中形成了Ni-层状硅酸盐,导致载体与活性组分的强相互作用,提高活性组分分散性;而且在碱性环境下,增加了催化剂的碱性位,从而提高其抗积碳性能。GAI等[14]采用氨回流浸渍法和普通浸渍法制备了Ni-Co/SiO2干重整催化剂,XRD表征结果发现采用氨回流浸渍制备的催化剂均未出现NiO的特征峰,表明氨回流浸渍提高了Ni颗粒的分散性、减小了粒径;研究还发现,氨回流不仅可以降低载体的酸度从而增加CO2的吸附,同时形成硅酸镍,增强了活性金属与载体的相互作用,有效抑制了高温活性组分粒子的烧结。ABDULLAH等[79]通过浸渍法和旋转蒸发仪、振动筛和超声波制备了4种Ni/SBA-15甲烷干重整催化剂,发现采用超声波制备的Ni/SBA-15(US)催化剂活性最好,这是因为超声辐射提供的空化效应能破坏Ni颗粒的软团聚,提高Ni—O—Si相互作用,从而实现活性金属的更好分散。LYU等[80]采用干式浸渍、强静电吸附、共沉淀和燃烧合成法制备了一系列Ni/Ce0.83Zr0.17O2催化剂,研究发现采用CP和CS两种方法制备的催化剂中的Ni可以结合到载体CZ晶格中,提高了CZ的还原性和活性表面氧,从而提高了催化剂的活性和稳定性。REN等[81]分别使用柠檬酸和甘氨酸作为络合剂采用复合浸渍法制备了Ni-C/SiO2和Ni-G/SiO2催化剂,催化剂的TEM如图5所示。由图5可知,与Ni/SiO2相比,Ni-C/SiO2和Ni-G/SiO2催化剂的Ni活性组分分散性明显提高,且粒径较小。TPR表征结果表明,与Ni/SiO2相比,Ni-C/SiO2和Ni-G/SiO2催化剂的载体和活性组分的相互作用力也更强,表明制备方法对活性金属Ni的粒径和分布以及Ni与载体之间的相互作用具有显著影响。

图5 还原催化剂的 TEM 图像Fig.5 TEM images of the reduced catalysts
ERGAZIEVA等[82]采用毛细管浸渍法和溶液燃烧法制备了双金属Ni-Co/γ-Al2O3催化剂,研究发现采用SC法制备的催化剂形成了NiCo2O4固溶体,还原后活性组分均匀分布在载体表面,因而催化剂催化活性高。DEKKAR等[83]通过浸渍法和微乳液法(ME)制备了Ni-Al2O3催化剂,其主要结构特性见表6,可知通过微乳液制备的催化剂活性组分粒径更小、分散性和催化活性更好;且载体与组分相互作用力也更强,使催化剂具有良好的抗积碳性能和稳定性。郭芳等[84]采用等离子体强化制备了Ni/γ-Al2O3催化剂,研究发现与常规焙烧催化剂相比,在H2还原过程前引入N2等离子体处理催化剂能有效提高催化剂的低温反应活性,N2等离子体处理能使前驱体中的硝酸盐在温和条件下分解,不仅使催化剂具有较强的还原能力和较大的比表面积,且显著提高了催化剂活性组分分散度,此外也显著减少了反应产生的积碳。RAHEMI等[85]采用辉光放电处理了Ni/Al2O3-ZrO2催化剂,发现等离子体可以诱导活性金属的重新分散,Ni粒子平均粒径从35.5 nm减小到18.5 nm。HUA等[86]制备了一种介质阻挡放电等离子处理的Ni/MgO干重整催化剂,发现等离子体制备的Ni/MgO催化剂具有比常规还原的催化剂更小的粒径、更强的Ni粒子分散性和更高的比表面积,在700 ℃、96 000 mL/(g·h)空速下,CH4和CO2的转化率比传统催化剂高20%以上。DAI等[87]通过介电阻挡放电(DBD)等离子体分解法制备了Ni/CeO2-ZrO2催化剂,发现等离子体分解催化剂具有较小的Ni纳米颗粒、更高的还原性、更多的碱性位点和氧空位,因此等离子体分解催化剂活性更好,且反应生成的积碳活性好、易消除。HUANG等[88]通过冷等离子体辅助法制备了Ni/Al2O3-MgO催化剂,发现氢等离子体(PH)和氮等离子体(PN)处理的样品催化活性更好,而氢氮等离子体(PNH)处理后的催化剂活性和抗积碳性能较差。
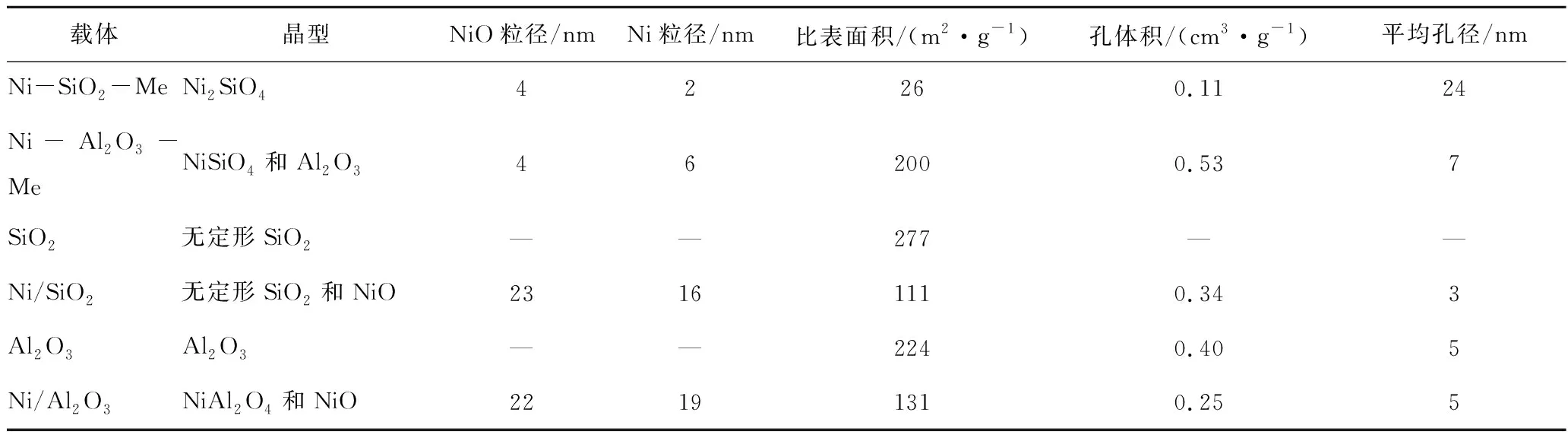
表6 催化剂的结构性质
不同制备方法获得的载体,其催化活性和稳定性也有显著差异。PARK等[89]采用两步法对SBA-15进行了预处理,然后采用浸渍法制备了Ni/SBA-15催化剂。预处理制备的催化剂与未处理制备的催化剂反应前后的TEM图及反应后粒径统计如图6所示。
由图6可知,反应前后NP(1.5)/SBA-15催化剂的活性组分均匀分布于SBA-15介孔孔道内;而NP/SBA-15(N)催化剂的活性组分在孔道外表面也有大量Ni粒子分布,且在反应后粒径变大;反应后未处理催化剂的Ni粒径显著大于处理的催化剂。这是因为预处理过的载体在浸渍过程中活性组分可以优先进入载体有序介孔中,充分利用了孔道的限域效应,有效抑制活性组分的烧结,从而提高了催化剂的稳定性。
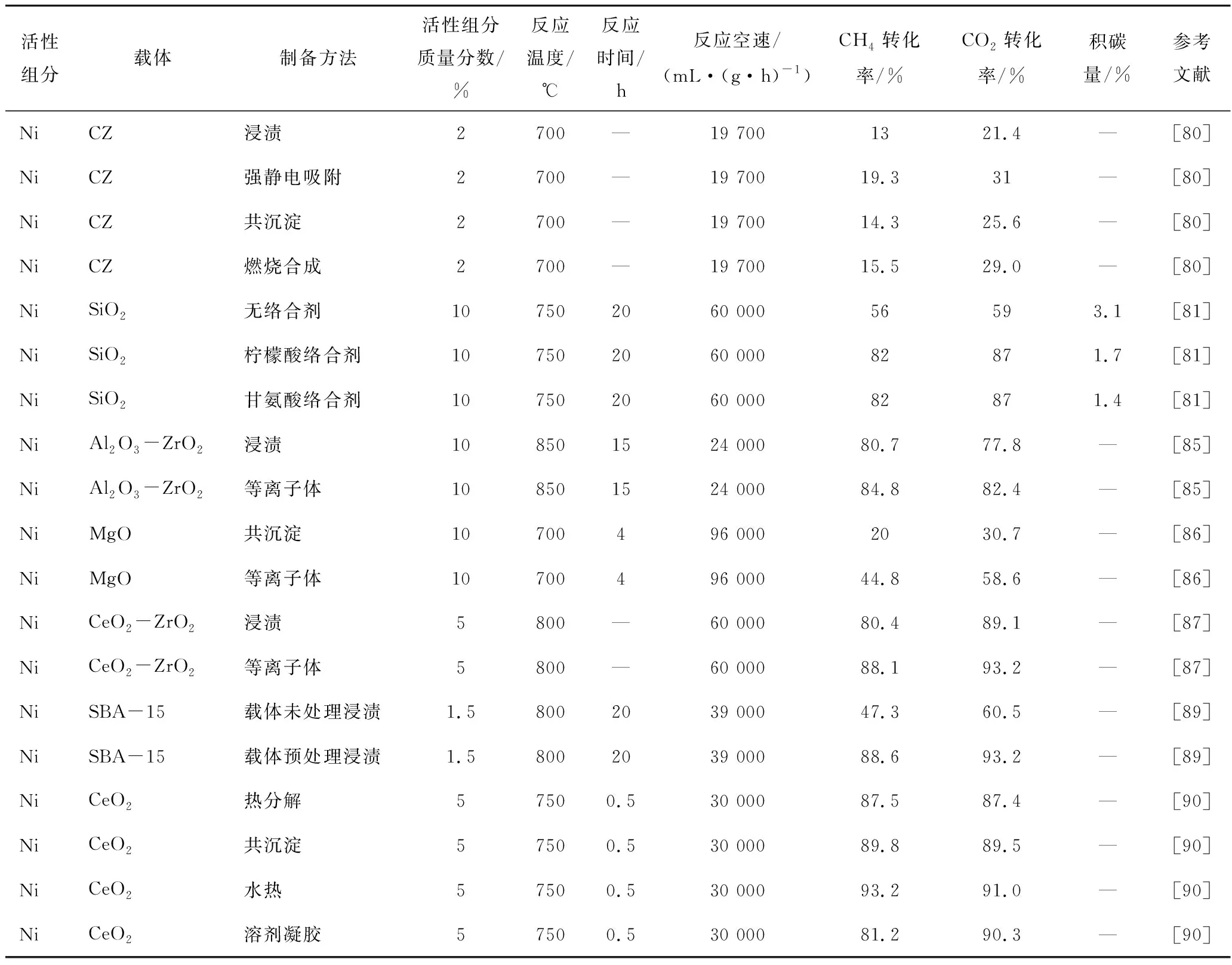
DAMASKINOS等[90]考察了4种不同载体CeO2合成方法对所制备催化剂性能的影响,研究发现4种方法制备的催化剂形态和结构、金属分散度和粒径明显不同,导致催化剂的活性和稳定性各有差异;其中,沉淀法制备的催化剂Ni/CeO2-PT抗积碳性最强,其次为溶胶-凝胶法制备的Ni/CeO2-SG催化剂,而水热法制备的Ni/CeO2-HT催化剂抗积碳性能最差。不同制备方法制备的Ni基催化剂甲烷干重整性能见表7。
综上,催化剂的制备方法对催化剂的催化性能有显著影响,且不同制备方法制备的载体对催化剂的催化性能也不同。浸渍法、溶胶凝胶法和共沉淀法是Ni基催化剂制备最常用的方法。浸渍法制备催化剂操作最简单,但催化剂重现性差;溶剂-凝胶法制备的催化剂活性组分比较均匀,但制备过程较复杂,制备时间较长;共沉淀法制备过程简单、反应条件易控制,且合成所需时间相对较短,但制备的催化剂活性成分分布不均匀。等离子体辅助法具有操作简便、工艺流程短、催化剂活性组分分散度好、催化剂活性高、稳定性好和清洁无污染等优点,应用前景较广。近年来,一些新型的制备方法(如溶液燃烧法、微乳液法等)已被用于制备DRM催化剂,且表现出较好的催化性能,但合成技术不太成熟,仍需改进,以实现大规模制备高性能的催化剂。

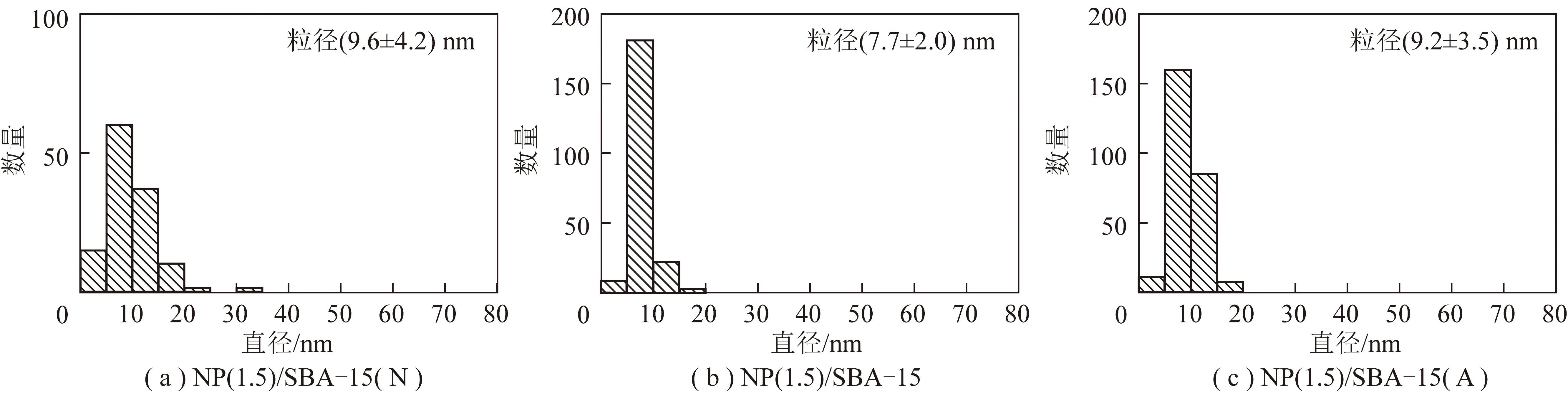
图6 新鲜和使用过的催化剂TEM及粒度分布Fig.6 High resolution TEM images of fresh and used catalysts and particle size distributions after DRM reaction
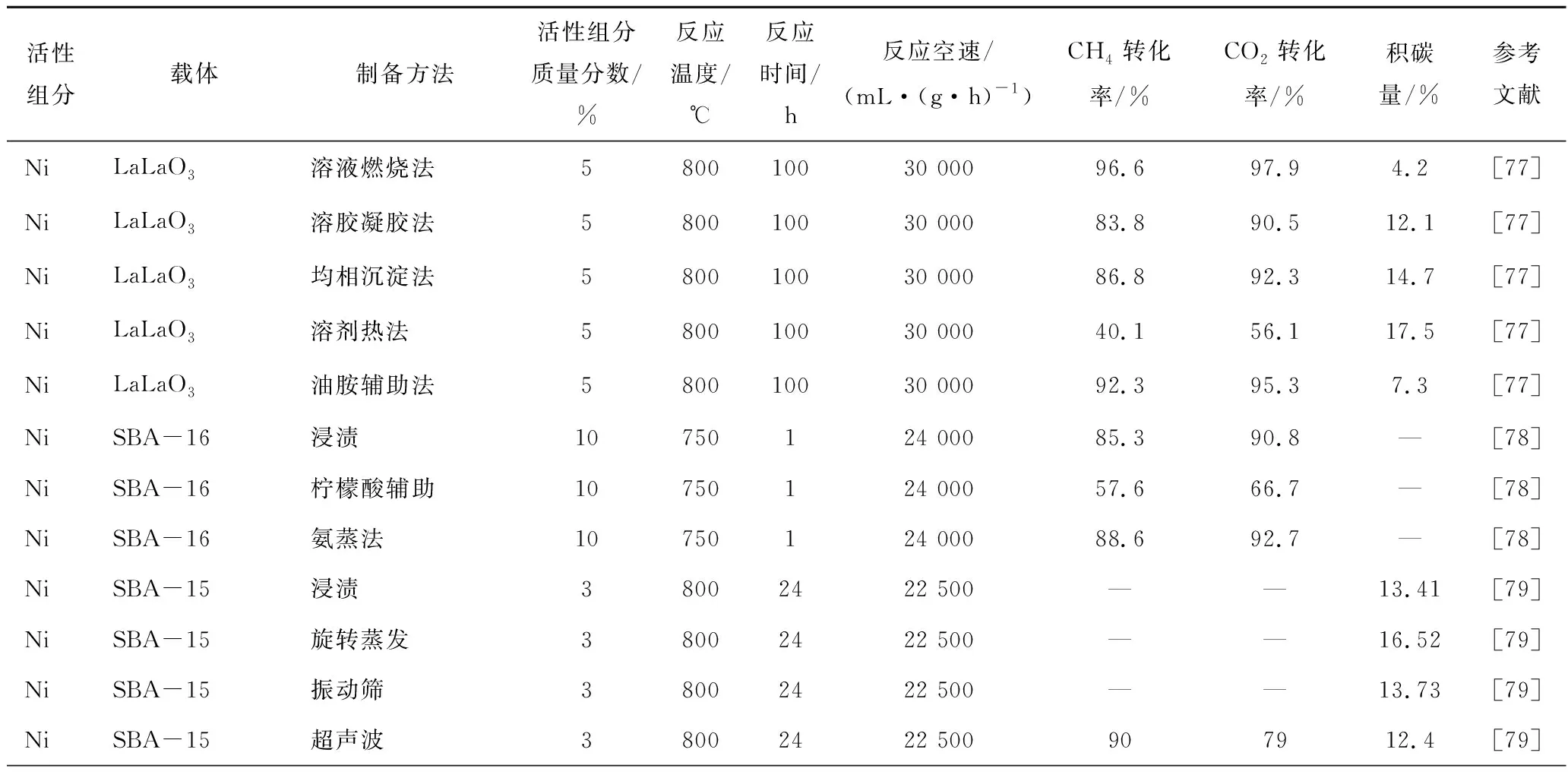
表7 不同制备方法Ni基干重整催化剂催化性能
续表
3.4 焙烧温度的影响
焙烧是催化剂制备过程中的重要环节,焙烧温度对催化剂活性组分的分散及其与载体的相互作用有一定影响,进而影响催化剂的催化性能。BIAN等[91]考察了煅烧温度对 Ni/M-Al2O3催化剂性能的影响,研究发现活性组分Ni的颗粒尺寸随焙烧温度的升高而降低;在700 ℃焙烧,载体与活性金属形成NiAl2O4尖晶石结构,有助于活性金属Ni的分散和催化剂催化性能的提高;但焙烧温度超过700 ℃时,催化剂比表面积降低,不利于气体传质,导致催化剂活性降低。HAN等[5]考察了不同煅烧温度对Ni@SiO2催化剂干重整性能的影响,发现随焙烧温度升高,Ni纳米颗粒从3.2 nm增加到8.3 nm,活性组分Ni的分散度则先增加后减小,750 ℃焙烧制备的催化剂具有较好的Ni尺寸、较好的活性组分分散性以及较强的活性组分与载体的相互作用,表现出最优的催化性能。HE等[92]研究了不同焙烧温度对Ni/Al2O3催化剂性能的影响,不同焙烧温度的XRD图谱如图7所示。
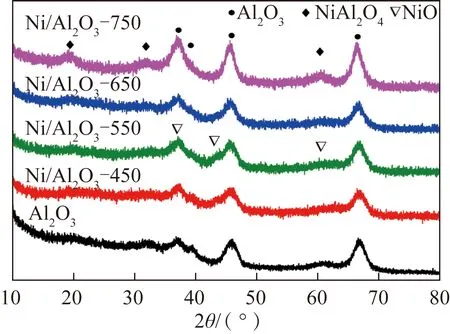
图7 在不同温度下煅烧的Al2O3载体和Ni/Al2O3样品的 XRD 图谱Fig.7 XRD patterns of the Al2O3 support and Ni/Al2O3 samples calcined at different temperatures
由图7可知,随着焙烧温度升高,载体与活性金属形成的NiAl2O4的结晶度增大,活性组分与载体的相互作用力增加,还原后活性组分分散性提高,催化剂表现出优异的催化活性和抗积碳能力。USMAN等[93]研究了不同焙烧温度对Ni/MgO催化性能,结果表明随焙烧温度提高,金属与载体的相互作用力增强,催化剂抗积碳能力提高;焙烧温度为750 ℃时,催化活性最好。SCHAFFNER等[94]研究了煅烧温度对Ni/Al2O3催化性能的影响,发现随焙烧温度的增加催化剂酸度不断降低;不同焙烧温度对催化剂的比表面积、孔体积等都有影响,进而影响催化剂的活性。LI等[95]分析考察了不同焙烧温度对Ni/MoCeZr/MgAl2O4-MgO催化性能和抗积碳性能的影响,发现随焙烧温度的增加,MgAl2O4结晶度变大、催化剂孔径增大、比表面积和孔体积减小,700 ℃焙烧时催化剂稳定性最好。
不同焙烧温度的Ni基催化剂甲烷干重整性能见表8。
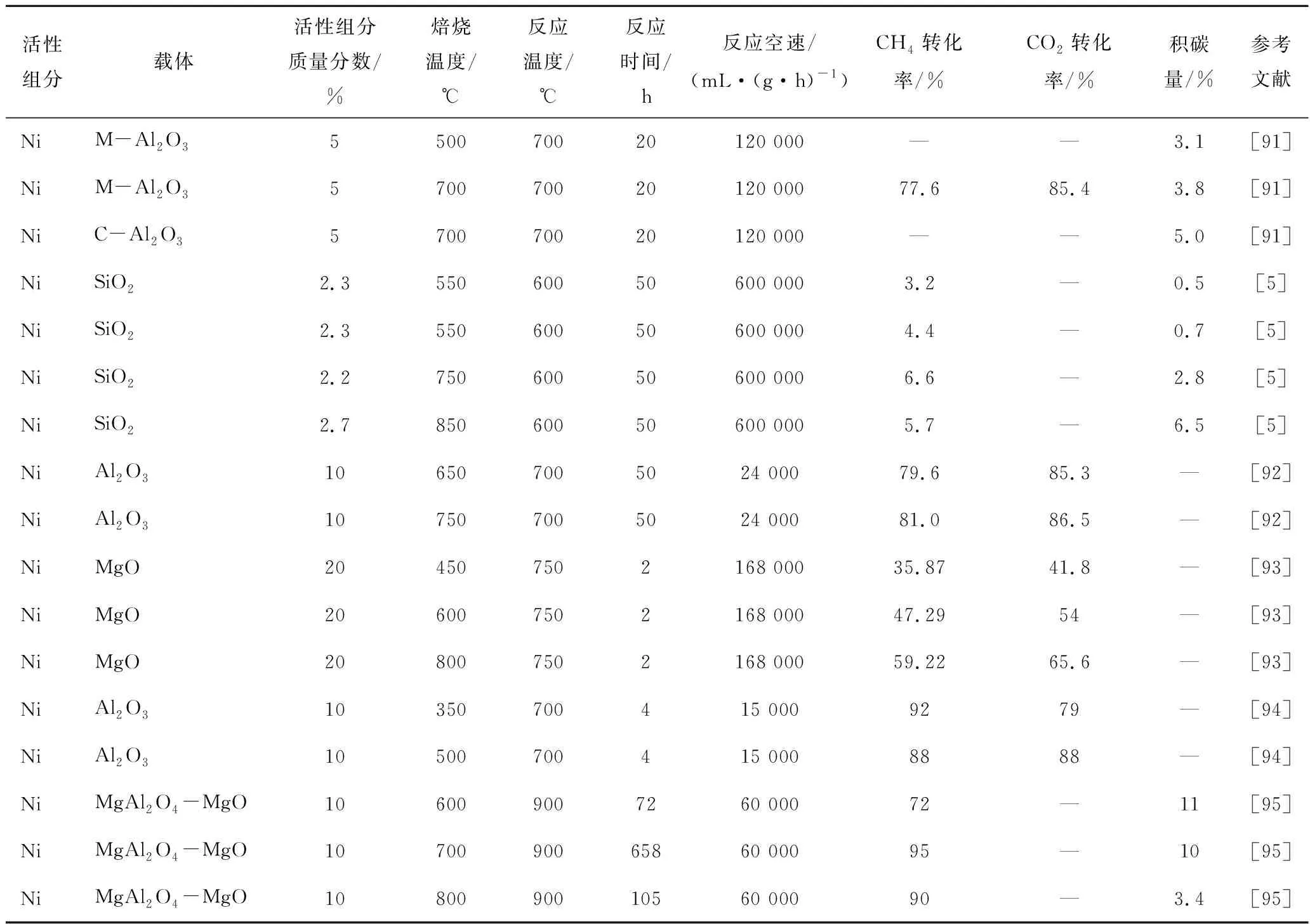
表8 不同焙烧温度的Ni基催化剂甲烷干重整性能
综上,焙烧温度对催化剂Ni活性组分的粒径、还原程度、活性金属与载体的相互作用以及表面Ni活性物种的含量都有显著影响,进而影响催化剂的催化活性和稳定性。但过高的焙烧温度会使催化剂结构发生变化,孔结构破坏,比表面积和孔径降低,表面碱性位降低,活性组分烧结;而过低的焙烧温度会导致前驱体分解不彻底或晶型转化不成功,不利于活性位的生成与暴露。
4 新型催化材料结构对Ni基干重整催化剂性能的影响
随着现代研究表征手段的发展,研究发现催化剂结构在提高催化剂性能方面也起重要作用。如前文载体影响研究中所述,由于介孔SiO2分子筛规整的介孔结构能限制活性组分的分布而不至烧结被广泛用作催化剂载体。另外,一些特定结构的材料,如尖晶石、钙钛矿、水滑石和固溶体等被用作无载体催化剂,其在还原过程中使活性金属迁移到表面。由于金属Ni与材料中其他元素之间的强相互作用,这些结构有效阻止了Ni 催化剂因烧结而失活。周则龄等[96]制备了一系列MTiO3(M=Mg、Ca、Sr、Ba)钙钛矿型氧化物负载的Ni催化剂,研究发现,与其他催化剂相比,制备的Ni/CaTiO3催化剂上金属载体之间的相互作用较强,结构最好,还原后暴露的活性组分Ni最多,晶格氧流动性也最高,因此该催化剂具有很好的催化活性和稳定性。ZHANG等[31]采用柠檬酸溶胶凝胶法合成了介孔NixAl1O2-δ尖晶石催化剂用于DRM反应,研究表明煅烧后的NixAl1O2-δ催化剂Ni2+物种以NiAl2O4尖晶石形式存在,在高温还原条件下NiAl2O4被还原形成与载体相互作用强、分散性好的活性Ni0粒子,使催化剂活性较好;此外,由于NiAl2O4中的Ni2+粒子不能被完全还原,催化剂以Ni0-NiAl2O4/Al2O3形式存在,从而使催化剂表现出优越的稳定性,在36 000 mL/(g·h)空速、600 ℃条件下反应100 h,CH4和CO2表现出良好的稳定性。SHAMSUDDIN等[97]制备了系列NiO/TALC甲烷干重整催化剂,发现催化剂类滑石结构形成的Mg2Ni相在还原过程中与H2反应形成稳定高活性的Mg2NiH4,有助于促进CH4的分解和CO2的吸附解离;制备的催化剂NiO/TALC在活性金属表面可以产生更多的氧原子,有效抑制了积碳的形成,催化剂显示出良好的催化性能;10% NiO/TALC的催化剂,在700 ℃时,CH4转化率达98%。
核壳结构也是一种独特的结构,其可渗透的多孔外壳可保护金属粒子避免烧结和聚集;同时,其丰富的纳米多孔道允许反应物快速扩散进出。因此,即使在苛刻的反应条件下,核壳结构的催化剂显示出优秀的催化活性和稳定性。LU等[98]设计制备了一种Ni纳米粒子高度分散在空心二氧化硅球的新型蛋黄壳型 Ni@HSS催化剂,考察了其甲烷干重整(DRM)性能,研究发现制备的催化剂不仅Ni颗粒尺寸小,且多孔二氧化硅壳载体与金属的相互作用强,以及良好的空间限域效应使催化剂展现出高催化活性和稳定性;在空速为144 000 mL/(h·g)条件下,CH4和CO2转化率都稳定在95%,反应55 h后无积碳产生。LU等[99]制备了系列Nix-V@HSS催化剂,研究发现Ni与氧化钒之间的强相互作用形成了Ni-VOx结构,其有效抑制了Ni颗粒的烧结;钒的加入改变了镍的电子云密度,增强了其电子供应能力;同时,由于VOx物种的存在产生了大量氧空位,有助于消除积碳,提高了催化剂的稳定性。FUJITSUKA等[100]合成了Ni@Silicalite-1催化剂用于DRM反应,发现催化剂的核壳结构空间效应有效阻止了Ni颗粒的团聚和积碳的形成,提高了稳定性;在600 ℃、1 080 000 mL/(h·g)空速条件下,反应24 h后无积碳产生。HAN等[101]通过在Ni@SiO2表面涂覆CeO2合成了Ni@SiO2@CeO2催化剂,2种催化剂还原后的TEM和尺寸分布如图8所示。由图8可知,SiO2壳和Ni核结构清晰可见,涂覆的CeO2成功包覆在SiO2表面;涂覆CeO2前后2种催化剂的活性组分Ni颗粒相差不大;但由于涂覆的CeO2具有高氧迁移率,与Ni@SiO2催化剂相比,Ni@SiO2@CeO2催化剂表面氧增多,从而有效抑制了积碳的沉积,使甲烷干重整活性提高了1.5倍,积碳降低60%。
5 结语与展望
DRM反应可将2种温室气体转化为有价值的化学原料,是实现碳达峰、碳中和目标的有效手段之一。然而,DRM反应是催化剂结构敏感的反应,现有机理认为CH4脱氢和随后含碳物质的转化发生在活性金属中心,由于缺少高质量的催化剂导致至今尚未工业化。其中,催化剂烧结和积碳是急需解决的核心问题。笔者对DRM反应的热力学、反应机理和动力学,影响Ni基催化剂性能的载体、助剂、制备方法和焙烧温度的因素以及新型结构的Ni基催化剂进行综述,为设计开发高活性和高稳定性催化剂提供借鉴。热力学研究发现,高温低压有利于DRM反应进行。不同的催化剂反应机理不同,然而现有反应机理普遍认为CH4的裂解发生在活性金属表面,且深度裂解会导致积碳产生,但催化剂的表面氧可气化消碳。金属与载体的强相互作用有助于降低活性金属的粒径和活性组分的团聚,从而提高催化剂的稳定性。强碱性、大比表面积的载体有利于CO2的吸附和活化,载体的有序介孔结构也可以提高活性组分分散度,抑制活性组分的团聚,从而提高催化剂的稳定性。助剂研究表明,强输氧能力助剂的添加有助于提高催化剂的抗积碳能力。优化的催化剂制备过程和焙烧温度可以改善载体与活性组分的相互作用和活性金属的分散性,从而改善催化剂的稳定性和抗积碳性。新型结构催化剂利用其空间限域效应可有效抑制活性组分的团聚和烧结,从而使催化剂表现出优异的抗烧结和抗积碳能力。上述研究表明知,仅通过单一参数的调整很难获得理想的抗积碳和抗烧结催化剂。因此,未来在设计稳健高效的DRM催化剂时,必须考虑各种参数的协同关联:
1)利用更加先进的表征手段对催化剂的反应机理和积碳机理进行研究,深层次地明晰金属催化剂的催化反应和抗积碳机理,以理论和实践相结合的方式,设计和开发高性能干重整催化剂。
2)尝试通过2种或多种活性金属、载体和/或促进剂的组合协同发挥各种载体和活性金属的作用,为催化剂提供更多的活性位点,抑制金属烧结、减小金属颗粒尺寸,减少积碳生成,提高催化剂的催化活性和抗积碳性。
3)构建不同新型种类的DRM催化剂,如利用限域效应限制催化剂活性组分粒径的长大和烧结,加大对新型结构催化剂的研究力度,以提高非贵金属Ni基催化剂的抗烧结和抗积碳性能。
——会偷偷侵蚀你的发动机!

