高脂高热量饮食对中国健康受试者口服氟康唑片药动学的影响
郭彩会,李颖,孙雪,刘亚丽,宋浩静,王祁民,董占军
(1.河北省人民医院药学部,石家庄 050051;2.石家庄四药有限公司,石家庄 052100)
氟康唑是一种新型三唑类抗真菌药物,具有广谱抗真菌作用、吸收快且完全、耐受性好、不良反应少等特点,在体内通过抑制真菌细胞色素P450(CYP)介导的14α-甾醇的去甲基作用,从而抑制麦角甾醇的合成,导致真菌细胞膜合成不足。广泛用于各种深部真菌感染性疾病及浅表、黏膜真菌感染的治疗[1]。国内外研究氟康唑人体药动学和生物等效性的相关文献报道较多[2-3],但笔者未见饮食对中国健康人体内的氟康唑药动学参数影响的相关报道,本研究以中国健康成年人为研究对象,采用液相色谱-串联质谱联用(liquid chromatography-tandem mass spectrometry,LC-MS/MS) 法测定血浆氟康唑浓度,在空腹和餐后给药条件下,研究氟康唑片在健康人群中吸收程度和速度的差异,评价高脂高热量饮食对单次口服氟康唑片药动学的影响,同时评价空腹和餐后条件下氟康唑片的安全性,旨在为临床用药安全提供科学依据。
1 材料、对象与方法
1.1材料
1.1.1药品 氟康唑片(辉瑞制药有限责任公司,批号:H79933,规格:每片150 mg);待测物信息:氟康唑对照品(中国食品药品检定研究院,批号:100314-201605,含量:99.7%) 、内标:氟康唑-d4对照品(TLC Pharmaceutical Standards公司,批号:1132-051A1,含量:98.7%)。空白人血浆来自健康受试者。
1.1.2仪器 LC-30AD 型 UPLC 系统(日本 Shimadzu 公司,配有 LC-30AD 型二元高压梯度泵、CTO-20A 型柱温箱、SIL-30AC 型自动进样器);LCMS-8050质谱仪(日本 Shimadzu 公司)。BP211D 型分析天平(北京赛多利斯仪器系统有限公司,感量:0.1/0.01 mg);Elmasonic S150 实验室应用型超声波清洗器(德国 Elma公司);Sorvall ST16R 型高速冷冻离心机(美国 Thermo Scientific 公司);MIULAB MIX-25P 型涡旋仪(杭州米欧仪器有限公司)。
1.2受试者选择 本文研究高脂高热量饮食对氟康唑片药动学影响,数据来源是研究项目“氟康唑片(150 mg)在健康受试者中随机、开放、两制剂、单次给药、双周期、交叉空腹/餐后状态下的生物等效性试验”的统计分析报告,本文仅对原试验方案中参比药物氟康唑片结果进行二次统计分析,试验方案经河北省人民医院伦理委员会批准。共入组健康成年受试者45例,所有受试者均知晓本试验的目的和要求,并签署知情同意书。其中24例完成空腹试验,男15例(62.5%),女9例(37.5%),年龄(30.2±6.09)岁,体质量(64.29±8.52) kg,身高(168.50±9.10) cm,体质量指数(BMI)(22.59±1.85) kg·(m2)-1;21例完成高脂餐后试验,男12例(57.1%),女9例(42.9%),年龄(29.0±7.76)岁,体质量(62.33±8.56) kg,身高(166.48±6.78) cm,BMI为(22.42±1.96) kg·(m2)-1。两组年龄、身高、体质量、BMI、男女比例等一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2.1入选标准 ①年龄为≥18岁的男性和女性受试者;②男性体质量≥50.0 kg,女性体质量≥45.0 kg,BMI 19.0~26.0 kg·(m2)-1;③无心、肝、肾、消化道、神经系统、精神异常及代谢异常等病史;④生命体征、体格检查、临床实验室检查、12导联心电图、胸部X线片,结果显示正常或异常无临床意义者;⑤受试者自筛选之日起未来6个月内无妊娠计划且自愿采取有效避孕措施。
1.2.2排除标准 ①过敏体质,或有食物、药物过敏史者,对氟康唑或对其他吡咯类药物(如酮康唑、伊曲康唑等)过敏者;易发生皮疹、荨麻疹等过敏症状体质者;②筛选前6个月内有药物滥用史或筛选前3个月内使用过毒品;③筛选前3个月内献血包括成分血或大量失血(>400 mL),接受输血或使用血制品者;④体格检查及血液分析、尿液分析、血生化、胸部X线片、心电图检查异常且具有临床意义者。
1.3方法 本研究共开展空腹、餐后2个试验。空腹试验筛选60例,合格24例,随机入组24例;餐后试验筛选64例,合格21例,随机入组21例(餐后试验受试者筛选困难,合格21例,虽未满足方案规定的24例,但病例数符合相关法规要求,故以21例受试者开展餐后试验)。两组资料见表1。分别服用氟康唑片150 mg,比较空腹条件下和高脂餐后氟康唑药动学参数的变化。
根据《以药动学参数为终点评价指标的化学药物仿制药人体生物等效性研究技术指导原则》[4]推荐餐后生物等效性研究采用高脂(提供食物中约50%的热量)高热量餐(3352~4190 kJ)(1 cal=4.19 J)。其中蛋白质提供热量约628.5 kJ,碳水化合物提供热量约1047.5 kJ,脂肪提供热量2095~2514 kJ。试验中提供的食物可由含类似量的蛋白质、碳水化合物、脂肪的食物替代。高脂高热量餐如未吃完,需称重,保证吃掉的食物热量>3352 kJ。
空腹试验24例受试者空腹过夜 >10 h,口服氟康唑片150 mg,温水240 mL送服,给药前1 h以及给药后0.25,0.50,1.00,1.50,2.00,2.50,3.00,6.00,12.00,24.00,36.00,48.00,72.00,96.00,120.00 h采集前臂静脉血4 mL,至EDTA-K2真空采血管中,轻柔颠倒混匀。餐后试验于第 2 天早上服药前 30 min 开始进食高脂(提供食物中的热量约50%)高热量餐(3352~4190 kJ)(高脂餐成分见表2)( 30 min 内结束进餐),进食高脂餐后30 min时服用氟康唑片150 mg,温水 240 mL送服,在高脂餐后至给药前以及给药后0.25,0.50,1.00,1.50,2.00,2.50,3.00,6.00,12.00,24.00,36.00,48.00,72.00,96.00,120.00 h时采集前臂静脉血4 mL至EDTA-K2真空采血管中,轻柔颠倒混匀。
空腹组和餐后组所采集的血样在1 h内4 ℃条件下离心(1700×g,10 min),所有离心后血浆样品将被分成2份,2 h内存放于-60 ℃以下冰箱中,以供药动学分析。
1.4测定方法
1.4.1色谱条件 色谱柱:GL Sciences Inc.,InertSustain C18(2.1 mm×50 mm,3 μm);流动相A:0.1%甲酸,流动相B:100%乙腈,梯度洗脱,0.50~1.30 min,15.0%→50.0%B;>1.30~1.60 min,50.0%→95.0%B ;>1.60~2.50 min,95.0%B;>2.50~2.60 min,95.0%→15.0%B;>2.60~3.50 min,15.0%B,流速:0.400 mL·min-1;柱温:40 ℃;分析时间为3.5 min;进样量:5 μL。
1.4.2质谱条件 离子源:大气压化学电离(APCI)源,正离子模式;监测方式:MRM 模式;接口温度:300 ℃;脱溶剂管温度:250 ℃;加热块温度:400 ℃;雾化器流量:3.00 L·min-1;加热器流量:10.00 L·min-1;干燥器流量:10.00 L·min-1。氟康唑定量离子对为m/z307.10→220.10,驻留时间为100 ms,预四级杆偏转电压偏差Q1 Pre偏差-15.0 V,碰撞能量(CE)为17.0 eV,预四级杆偏转电压偏差Q3 Pre偏差-23.0 V;氟康唑-d4离子对为m/z311.10→223.10,驻留时间为 100 ms,Q1 Pre偏差-16.0 V,CE为18.0 eV,Q3 Pre偏差为-23.0 V。
1.4.3血浆样品处理 样品室温下融化后,涡旋混匀;吸取样品(校正标样、质控样品或测试样品)30.0 μL至96孔板中,对于双空白样品或QC0样品,加入空白基质30.0 μL;加入内标溶液30.0 μL,对于双空白样品加入50%乙腈溶液30.0 μL;加入100%乙腈溶液180.0 μL,然后涡旋约10 min,在约4 ℃条件下1700×g离心10 min;转移上清液30.0 μL至已加入30%乙腈溶液270.0 μL的96孔板中,涡旋5 min,待进样。
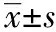
表1 空腹试验与餐后试验健康受试者一般资料比较
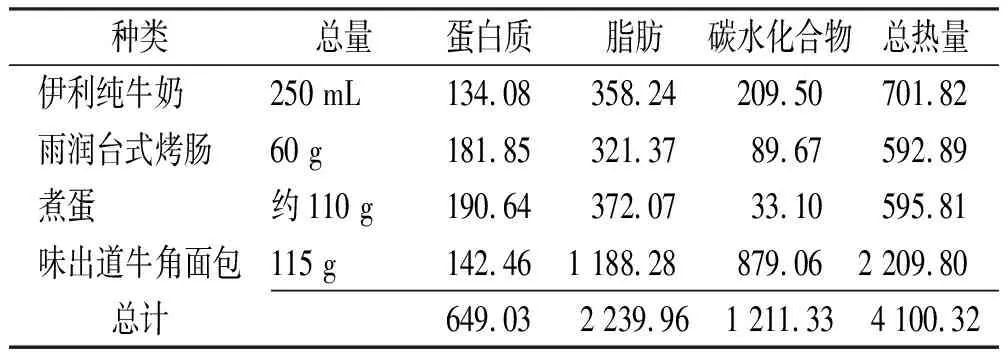
表2 高脂餐成分
1.5统计学方法 用Phoenix WinNonlin 7.0版软件的非房室分析方法计算空腹和高脂饮食后单次服用氟康唑片150 mg后药动学参数,并对其做描述性统计分析。采用独立样本t检验和非参数检验比较空腹组和高脂餐组之间药动学参数。
2 结果
2.1方法学考察 LC-MS/MS的方法学验证由苏州国辰生物科技股份有限公司的质量保证部门根据实验室标准化操作规程对方案、原始数据及报告进行监督及审核,并且检查或者审核实验的实施与相应的标准化操作规程的符合性。
血浆中内源性物质不干扰氟康唑的测定。氟康唑的标准曲线线性范围为 10~5000 ng·mL-1,氟康唑线性关系好,准确度及精密度结果见表3。血浆样品中氟康唑提取回收率为95.0%~99.9%,内标氟康唑-d4 的回收率为 91.7%。氟康唑在 3750~25 000 ng·mL-1浓度范围内,稀释因子为 1:10时具有良好的稀释可靠性。血浆样本在-20 ℃条件下储存28 d的稳定性良好,-60 ℃条件下储存28,90 d的稳定性良好;血浆样本在-60 ℃条件下经历5次冷冻-解冻循环的稳定性良好;全血样本于冰浴白光下放置2 h的稳定性良好;基质效应( 包括溶血基质效应与高脂基质效应) 、残留均不影响血浆中氟康唑的准确定量。方法学验证结果表明本方法可用于临床试验血浆样品的分析。
2.2血药浓度-时间曲线 健康受试者空腹和高脂饮食后口服氟康唑片150 mg后的平均血药浓度-时间曲线,见图1。
2.3药动学参数 空腹和高脂饮食后氟康唑片150 mg后主要药动学参数见表4。
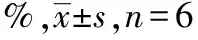
表3 血浆中氟康唑的精密度和准确度
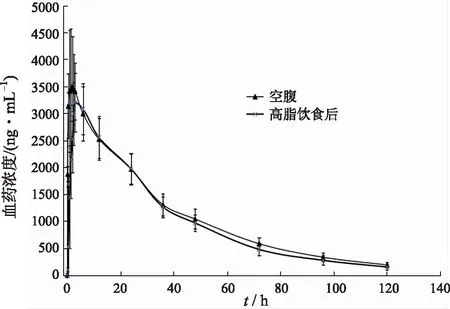
图1 空腹或高脂饮食后健康受试者口服氟康唑后药-时曲线图
2.4饮食影响分析 空腹与高脂饮食后药物动力学见表3。与空腹给药比较,高脂饮食后氟康唑平均最大血药浓度Cmax降低16.77%(P<0.01),tmax推迟约2 h(P<0.01),但AUC并未明显改变(P>0.05)。说明食物对氟康唑的吸收速度有显著影响,对吸收程度无影响。
2.6安全性评价 本研究45例受试者在空腹或高脂饮食条件下口服氟康唑片150 mg后,空腹组3例受试者发生不良事件3例次,其中尿上皮细胞增高1例次,转归为消失,上呼吸道感染1例次,转归为缓解,转氨酶升高1例次,转归为稳定。 餐后组2例受试者发生不良事件2例次,丙氨酸氨基转移酶升高1例,转归为消失,尿白细胞阳性1例,转归为消失,所有不良事件严重程度均为1级,均未发生严重不良事件和导致退出试验的不良事件。氟康唑可能对患者的肝功能有影响,服用药物时需定期检查肝功能。
表4 空腹和高脂饮食口服氟康唑片后药动学参数
3 讨论
LC-MS/MS适用于复杂基质中微量药物及代谢物的定量分析,在灵敏度、选择性以及对药物分析的适用性等方面有突出的优势,具有很高的精密度和准确性,是非常成熟的生物分析技术[5]。本研究采用 LC-MS/MS 方法对氟康唑血药浓度进行定量分析,可实现氟康唑血浆分析的重现性和高灵敏度[6]。
氟康唑相关的常见不良事件为胃肠道症状包括恶心、腹痛、腹泻,其次为皮疹、肝肾功能异常[7],本研究出现的不良反应均为轻度,与文献[8]报道一致,安全性较好。
食物可能改变药物的生物利用度,FDA认为应采用高热量、高脂肪的食物作为标准餐来考查饮食对药动学的作用,以使食物的影响达到最大[9]。目前笔者未见国内食物对氟康唑药动学影响的相关报道,本研究分析显示高脂高热量饮食会使氟康唑的吸收延迟,峰浓度降低,但不影响药物的吸收程度,分析原因可能是进食后,食物降低胃排空速率,使药物到达小肠的时间延长,因此导致tmax延长,Cmax降低。此外,本研究与国外报道的氟康唑在高脂饮食后的药动学参数变化稍有不同,国外报道餐后给药与空腹给药相比,Cmax、 AUC0-t和 AUC0-∞差别不大[10-11],可能与种族差异有关;另外,本研究因是二次分析,非交叉设计,也可能是与国外报道数据有差异的原因之一。
氟康唑属于吡咯类药物,根据抗菌药物药动学/药效学(PK/PD)特点其为时间依赖型长抗菌后效应药物,评估其PK/PD指数主要是AUC0~24/最低抑菌浓度(minimum inhibitory concentration MIC),高脂高热量饮食后其体内药物暴露量并未改变,但吸收延迟,峰浓度降低,因此建议中国人群空腹服用氟康唑片。本研究结果可为氟康唑片在中国人群的安全合理用药提供重要参考依据。

