依托泊苷方案对儿童急性髓系白血病的疗效及预后影响因素分析
胡海辉
急性髓系白血病(AML)是一种来源于骨髓的恶性异质性白血病,其恶性程度较高,病死率为70%~80%,且病情尽快发展极快[1-2]。如不能及时治疗,其生存时间不足半年。AML可发生与任何年龄,无性别差异,其中儿童病患较常见。AML患儿在初诊时体内一般会有20%以上的白血病细胞,经有效治疗后,机体内的白血病细胞减少到5% 以下,无浸润性骨髓现象,血象也基本恢复正常[3-5]。目前治疗AML方案和药物较多,依托泊苷方案较常用。目前依托泊苷方案中主要以米托蒽醌、依托泊苷、阿糖胞苷药物为主,其临床获得认可,有利于预后。但AML患儿治疗预后与诸多因素有关,不仅仅包括治疗方案,还有其他因素如免疫力、年龄等。分析影响AML患儿预后显著尤为重要。本文对医院2017年6月~2019年6月诊治的AML患儿作为依托泊苷方案治疗对象,分析其治疗效果和预后因素,现报告如下。
1 资料与方法
1.1 一般资料
选择医院2017年6月~2019年6月诊治的AML患儿69例作为研究对象。纳入标准:①符合《儿科学》中关于AML诊断标准;②7~15岁患儿;③病案信息完整;④沟通能力正常;⑤家属和患儿配合。排除标准:①急性早幼粒细胞患儿;②自体干细胞或异体干细胞移植患儿;③骨髓癌患儿;④对治疗药物过敏的患儿;⑤自闭症患儿;⑥病理性黄疸患儿。根据治疗方案不同分为对照组和治疗组,分别为33例和36例。对照组男性18例,女性17例,年龄7~15岁,平均(11.97±1.05)岁。治疗组,男性19例,女性17例,年龄8~14岁,平均(11.91±1.04)岁。两组患儿年龄和性别差异比较无统计学意义(P>0.05),具有可比性。
1.2 方法
治疗方法:对照组患儿接受姑息治疗,羟基脲、输血等治疗,连续治疗14 d。治疗组患儿接受依托泊苷方案治疗,米托蒽醌针5 mg(m2·d),连续治疗3 d;依托泊苷针1000 mg(m2·d),连续治疗5 d;阿糖胞苷针1000 mg·m2·d,连续治疗14 d。
基础信息:使用问卷调查方法调查患儿的性别、染色体核型、CD34细胞表达情况、白细胞(WBC)水平、病因、Charlson合并症指数(charlson complication index,CCI)评分、血小板计数(PLT)水平、乳酸脱氢酶(LDH)值、骨髓原始细胞比例、治疗方案。
染色体核型参考荧光原位杂交(FISH)法检测,分为低危核型、标危核型和高危核型。在治疗前抽取患儿肘静脉血8 ml,离心处理后使用全自动生化分析仪检测WBC、PLT、LDH。使用免疫组化法检CD34细胞表达情况。使用定量RT-PCR法检测骨髓原始细胞比例。采用Charlson合并症指数(charlson complication index,CCI)对患儿合并症进行评价。
临床疗效:参考《血液学诊断与疗效》标准对患儿治疗效果进行评定,主要评价指标是完全缓解。随访1年统计两组患儿生存时间,作为评价临床疗效的指标之一。
1.3 评价指标
比较两组患儿临床疗效,分析影响患儿预后的单因素和多因素。
1.4 统计学方法

2 结果
2.1 两组患儿临床疗效比较
治疗组(36例)患儿中完全缓解30例(83.33%)。对照组(33例)患儿中完全缓解23例(69.70%)。治疗组患儿生存时间(10.57±0.29)个月,对照组患儿(8.95±0.23)个月。治疗组患儿完全缓解率和生存时间均大于对照组(P<0.05),见图1。

图1 生存曲线图
2.2 影响AML患儿预后单因素分析
经2.1结果可知,完全缓解53例,未完全缓解16例。经单因素分析发现,CCI评分、WBC、染色体核型、治疗方案差异比较有统计学意义(P<0.05),而性别、年龄、CD34细胞表达情况、病因、PLT水平、LDH值、骨髓原始细胞比例情况差异比较无统计学意义(P>0.05),见表1。
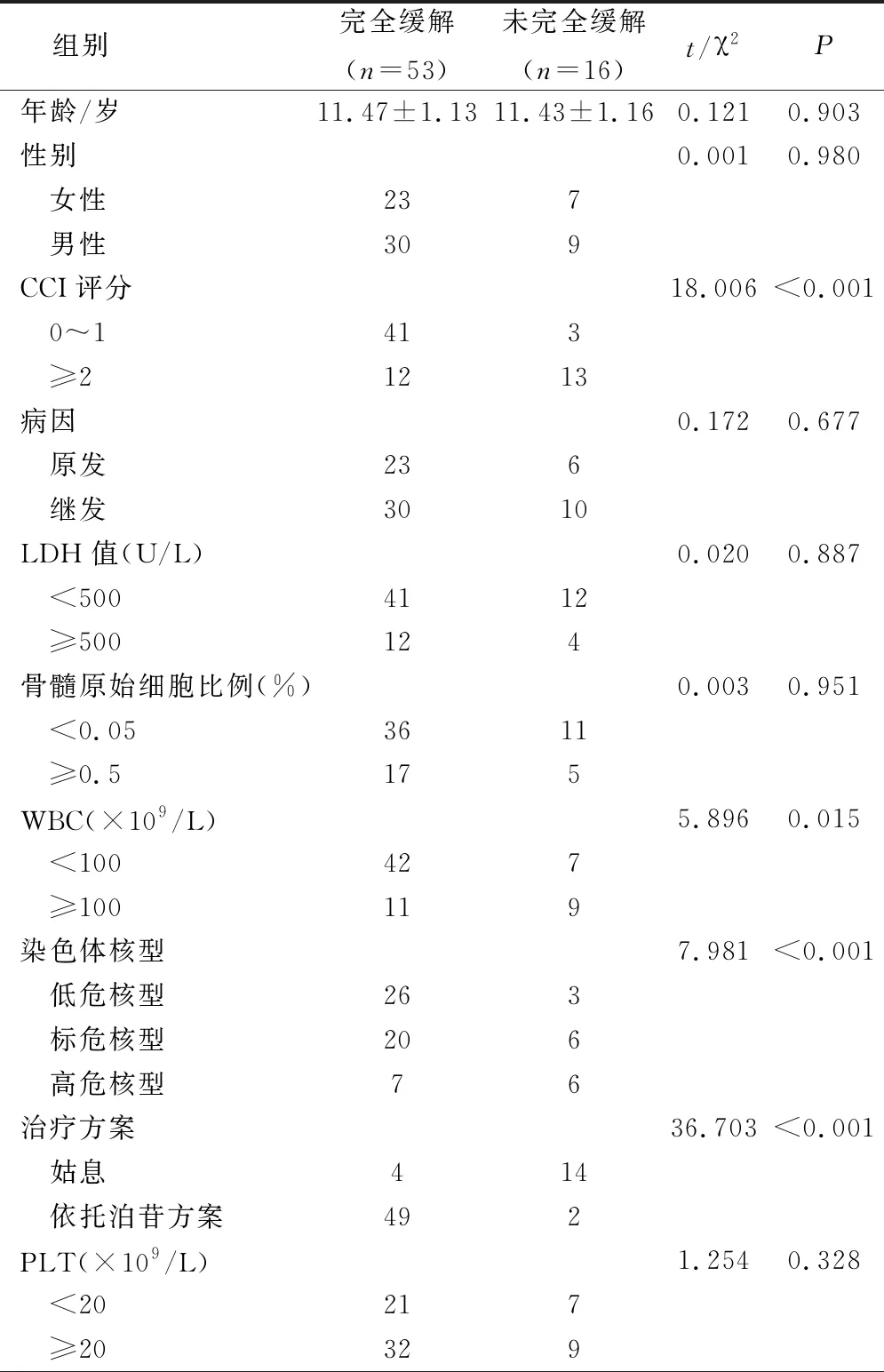
表1 影响AML患儿预后单因素分析/例
2.3 影响AML患儿预后因素Logistic分析
将表1中有统计学意义的因素“CCI评分、WBC、染色体核型、治疗方案”进行赋值并作为自变量(X)(表2),将其纳入Logistic中,因变量(y)为是否完全缓解,结果显示CCI评分≥2分(OR=2.125,95%CI=1.382~3.678)、WBC≥100×109/L(OR=2.270, 95%CI=1.409~4.118)、高危核型染色体核型(OR=6.317,95%CI=1.762~20.127)是影响AML患儿预后的独立危险因素(P<0.05),见表3。

表2 赋值表

表3 影响AML患儿预后因素Logistic分析
3 讨论
米托蒽醌、依托泊苷、阿糖胞苷药物共同组成了依托泊苷治疗方案。依托泊苷是一种氨基醌类药物,是细胞周期非特异性广谱抗肿瘤药物,现已广泛用于实体瘤和复发难治性白血病的治疗,与米托蒽醌、阿糖胞苷药物无较差性耐药[6-7]。米托蒽醌嵌插型抗癌药物,可用于治疗恶性肿瘤。阿糖胞苷是治疗白血病常用药物之一。三药联合使用可用过代谢产生自由基,杀伤肿瘤细胞,且能协同起到抗肿瘤的疗效。白血病是一种异质性恶性克隆疾病,是造血干细胞突变引起的造血系统的恶性肿瘤。临床主要表现为异常细胞在骨髓及其他造血组织中恶性增殖[8-10]。随着疾病发展,恶性细胞会浸润导其他组织,导致骨髓中正常造血功能受到抑制。AML是白血病中常见恶性肿瘤,是一种分化受阻于髓系干细胞的一种异质性白血病,其特点较明确,是恶性克隆性白血病干细胞无显著增殖并且显著损伤免疫细胞[11-12]。AML临床主要表现为白细胞和血小板增多或减少。AML生存期较短,生存率较低,60岁以上 的患者治愈率不足20%,小于60岁的患者其治愈率为35%~40%。最近几年随着治疗方法发展,新技术和新药的出现,其治疗效果获得较大提升。以往研究认为[13],AML疗效和很多因素有关,且影响预后的因素相互关联、相互影响,包括临床特点、形态学和免疫学等等。预后因素之间的相互影响是指预后好的指标与其他预后不好的因素结合也会导致预后因素不好[14]。最近几年大量关于预后指标出现,使得AML治疗越来越根据预后危险因素进行分层治疗,有利于患者康复。
本文研究结果显示,接受依托泊苷治疗方案治疗的治疗组患儿的完全缓解率和生存时间较单纯接受姑息治疗的对照组患儿优佳。依托泊苷治疗方案具有广谱抗肿瘤作用,能阻止细胞进入分裂期,作用于S1和S2期细胞,从而保证患儿安全度过骨髓抑制期,进而提升了完全缓解率,延长了患儿生存时间。CCI评分≥2分、WBC≥100×109/L、高危核型染色体核型是影响AML患儿预后的独立危险因素。CCI评分主要是对合并症进行评定,2分及以上预示死亡风险大。CCI评分≥2分是影响AML预后独立危险因素很可能与患儿常合并心、肝、肺等重要器官功能障碍有关。严重性的合并症会导致机体对药物清除力降低的同时影响机体抵抗力。WBC是评价机体炎症反应重要指标,WBC≥100×109/L说明出诊时患儿机体外周血白细胞水平显著升高。WBC≥100×109/L时可能会出现高白细胞综合征,增加血液粘度,导致血栓形成,进而促使患儿出现呼吸困难和缺氧等状态,极容易诱导患者在治疗期间出现颅内出血和肺功能障碍,进而影响治疗预后,促使患儿早期死亡[15]。染色体核型是与AML预后的相关重要因素,约有60%的患者伴有染色体核型异常。染色体核型在AML预后中起到非常重要意义。细胞遗传学通过染色体核型分析将AML患儿分为低危核型、标危核型、高危核型例数分别是26例、20例和7例。预后相同的核型的患儿在分子生物水平和治疗过程中具有高度异质性。高危核型恶性化程度严重,患儿在接受治疗中很难获益。
综上所述,依托泊苷方案治疗儿童急性髓系白血病能明显延长患儿生存时间,提升预后。临床在治疗前要重视观察CCI评分≥2分、WBC≥100×109/L、高危核型染色体核型患儿,制定个性化治疗方案,以提升预后。

