吗啡缓释片与羟考酮缓释片在中重度癌性疼痛中的应用效果
刘 曼 吴 珊 赵 森 徐保利
大连大学附属中山医院药剂科,辽宁大连 116000
随着医学技术改进和治疗水平提升,多种疾病均得到有效治疗和控制。但肿瘤发病率仍然逐年攀升,疾病治疗进展慢。有65%~85%的癌症患者存在程度不同的疼痛[1],特别是中晚期患者,此为临床急需解决的问题之一。目前WHO 组织推荐治疗癌性疼痛的核心药物则为阿片类药物[2],其镇痛效果理想,患者耐受性高。但我国人均消耗阿片类药物量比西方国家低,其原因为医护人员缺乏对癌性疼痛的认知、顾虑阿片类药物存在较大毒副作用等。近年逐步有学者尝试将阿片类药物用于中重度癌性疼痛患者中[2],进而了解到了药物的作用特征。本研究共选取大连大学附属中山医院收治的100 例中重度癌性疼痛患者进行分组对照研究,探讨吗啡缓释片、羟考酮缓释片的镇痛效果。
1 资料及方法
1.1 一般资料
选取2019年4月至2021年2月大连大学附属中山医院收治的100 例中重度癌性疼痛患者作为研究对象,采用随机数字表法将其分为对照组和观察组,各50 例。对照组中,年龄35~75 岁,平均(56.32±1.25)岁;女21 例,男29 例;肿瘤类型:肝癌10 例,食管癌8 例,乳腺癌5 例,肺癌12 例,大肠癌8 例,鼻咽癌3 例,胰腺癌4 例。观察组中,年龄34~74 岁,平均(56.35±1.26)岁;女22 例,男性28 例;肿瘤类型:肝癌11 例,食管癌7 例,乳腺癌6 例,肺癌13 例,大肠癌7 例,鼻咽癌4 例,胰腺癌2 例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。纳入标准:①各患者均满足《成人癌症疼痛诊疗规范(2018年版)》[3]中癌性疼痛诊治指南;②各患者疼痛程度数字评估量表(numerical rating scale,NRS)[4]评分范围为4~10 分;③病历记录完整。排除标准:①无法正常与医护人员沟通、交流、配合者;②哺乳或妊娠者;③对本研究使用药物禁忌或过敏者;④合并支气管哮喘、慢性阻塞性肺疾病、严重呼吸抑制者;⑤放化疗治疗者;⑥MRI 或CT 等检查显示存在神经破坏或压迫者;⑦预估生存时间<3 个月者。本研究经医院医学伦理委员会批准后实施,所有患者均签署知情同意书。
1.2 方法
对照组服用吗啡缓释片(西南药业股份有限公司,国药准字H10930001,生产批号:20180212),开始剂量为每12 h 服用10 mg,用药量保持在20~60 mg/日。观察组口服羟考酮缓释片(BARD PHARMACEUTICALS LIMITED,注册证号:H20120518,生产批号:20170521),NRS 评分4~6 分,开始剂量为每12 h 服用5 mg;NRS 评分7~10 分,开始剂量为每12 小时服用10 mg,每日用药量保持在10~40 mg 即可。
两组患者均持续治疗1 个月。
1.3 观察指标及评价标准
观察治疗前后患者疼痛状况、给药后药效见效时间、不良反应等指标。
①镇痛效果:用数字评价量表(numerical rating scale,NRS)[4]判定其用药后镇痛效果。无痛:0 分;轻度疼痛:1~3 分;中度疼痛:4~6 分;重度疼痛:7~10 分。②药效见效时间:记录药物起效时间,即给药后至疼痛得到缓解的时间。③不良反应:记录口干、皮疹和瘙痒、睡眠或失眠、恶心呕吐、精神异常等发生率。
1.4 统计学方法
采用SPSS 22.0 统计学软件进行数据分析,计量资料用均数±标准差(±s)表示,两组间比较采用t检验;计数资料采用率表示,组间比较采用χ2检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者治疗前后镇痛效果的比较
两组患者治疗前NRS 评分的比较,差异无统计学意义(P>0.05);治疗后,两组患者的NRS 评分均低于治疗前,且观察组NRS 评分低于对照组,差异有统计学意义(P<0.05)(表1)。
表1 两组患者治疗前后镇痛效果的比较(分,±s)

表1 两组患者治疗前后镇痛效果的比较(分,±s)
组别例数治疗前治疗后t 值P 值观察组对照组t 值P 值50 50 7.21±0.21 7.08±0.54 1.587 0.116 4.21±0.24 6.33±0.21 47.007<0.001 66.519 9.153<0.001<0.001
2.2 两组患者药效见效时间的比较
观察组药效见效时间为(0.52±0.02)h,对照组为(1.36±0.05)h,观察组药效见效时间短于对照组,差异有统计学意义(t=110.297,P<0.001)。
2.3 两组患者不良反应总发生率的比较
观察组不良反应总发生率低于对照组,差异有统计学意义(P<0.05)(表2)。
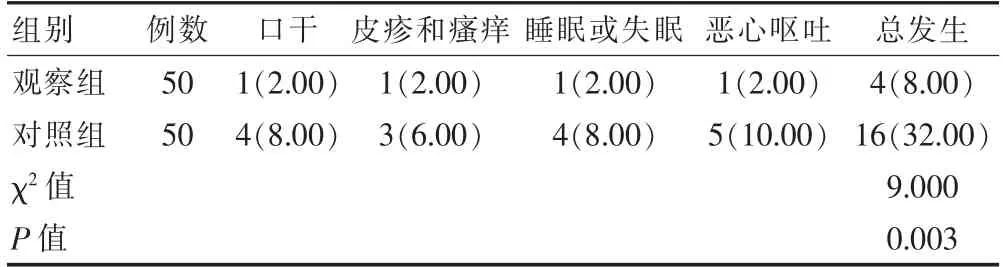
表2 两组患者不良反应总发生率的比较[n(%)]
3 讨论
目前及此后长时间内,癌症仍为医学界所关注和攻克的重点问题。癌症疾病死亡率高[5],大部分中晚期癌症患者均需承受疾病带来的心理和生理痛苦,而控制疼痛则为姑息治疗的主要内容[6-7]。因此,如何选择止痛药物以及药物疗效和安全性成为患者和医护人员关注的共同问题。吗啡缓释片属于治疗癌性疼痛的典型药物,其临床认可度较高[8-10]。此药物主要对人体μ受体产生作用,用于治疗躯体疼痛的效果较好,人体服用后,大约1.5~2 h 则可见效,药效可持续12 h,生物利用度可达65%[12-13]。而盐酸羟考酮属于新型研制药物,相较于阿片受体亚型,其作用更为全面,可对人体κ 受体和μ 受体产生作用[14-15],用于非癌性疼痛和癌性疼痛镇痛中,均可发挥其疗效,但用于治疗内脏疼痛的效果比吗啡缓释片效果更理想。人体口服后,1 h 内则可见效,药效持续12 h,生物利用度达87%,现已成为临床主要麻醉药物之一[16-18]。
本研究结果显示,观察组治疗后NRS 评分低于对照组,差异有统计学意义(P<0.05),提示本研究中吗啡缓释片与羟考酮缓释片在中重度癌性疼痛中的镇痛效果基本相当。观察组药效见效时间短于对照组,差异有统计学意义(P<0.05),提示羟考酮缓释片的见效速度快,这点也与上述药物机制中见效速度快的优势相符。羟考酮缓释片主要成分为提取的生物碱蒂巴因[19],可达到双相释放,结合不同部位阿片受体,抑制释放感觉神经末梢兴奋性递质,控制疼痛感觉信号传导至中枢神经,快速发挥镇痛效果[20-22]。观察组不良反应发生率(8%)低于对照组(32%),差异有统计学意义(P<0.05),提示羟考酮缓释片的用药安全性更高,其原因可能与药物主要成分有关。金冉等[23]在报告中分析了60 例胰腺癌(晚期)患者。结果显示,研究组给药时间[(2.86±0.89)d]短于对照组[(4.20±1.15)d],疼痛控制效果优于对照组,且血浆P 物质(substance P,SP)、组胺(histamine,HIS)、5-羟色胺(5-hydroxytryptamine,5-HT)等指标低于对照组,差异有统计学意义(P<0.05),两组患者不良反应比较,差异无统计学意义(P>0.05)(30%vs13.33%),证实了吗啡缓释片与羟考酮缓释片两者比较,后者的见效速度、镇痛效果理想,安全性高。本研究与其相比,见效速度相符,但在镇痛效果上存在一定差异,可能因选取的样本差异等因素导致。本研究所研讨样本,覆盖多种病例,加之药物药理机制等因素影响,可能导致结果差异[23]。条件成熟后,可进一步深入分析和探讨。
综上所述,吗啡缓释片与羟考酮缓释片治疗中重度癌性疼痛的效果基本相当,但羟考酮缓释片见效速度更快,不良反应少,临床可根据实际状况选择给药。

