自发性卵巢过度刺激综合征合并卵巢蒂扭转1例
刘艳玲,肖子文,陈慧*
(1.贵州医科大学,贵阳 550004;2.贵州医科大学附属医院,贵阳 550004)
一、病例资料
患者,女,31岁,因“停经11+3周,右下腹痛5+h”于2020年6月9日入住贵州医科大学附属医院。
患者G3P1A1,自然受孕,末次月经2020年3月21日。就诊前5+h,患者出现无明显诱因、持续性、剧烈的右下腹疼痛,无阴道流血、流液。查体:生命体征平稳,身高158 cm,体重51 kg,体质量指数(BMI)20.4 kg/m2。辅助检查:入院B超提示双侧附件区均可见囊实性回声团块,左、右卵巢大小分别为9.61 cm×6.71 cm×5.81 cm(图1A)和11.64 cm×7.37 cm×5.65 cm(图1B),未见明显血流信号;β-HCG为230 541 U/L;雌二醇>11 010 pmol/L;糖链抗原125(CA125)61.72 U/ml;抗苗勒管激素(AMH)5.26 ng/ml;阑尾及泌尿系统B超均未见明显异常。妇科检查:子宫增大如孕3+月大小、质软,压痛明显,双侧附件区可扪及大小约9 cm×7 cm×6 cm和11 cm×8 cm×6 cm包块,边界清楚,活动度可,双侧附件区均有压痛及反跳痛,以右侧为甚。入院诊断:(1)腹痛原因:卵巢囊肿蒂扭转?OHSS?;(2)G3P1孕11+3周;(3)双绒毛膜双羊膜囊双胎妊娠。
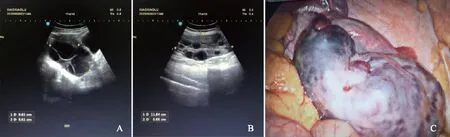
A:左侧卵巢B超图像;B:右侧卵巢B超图像;C:术中见右侧卵巢囊肿蒂扭转。图1 双侧卵巢B超及术中腹腔镜下图像
由于患者腹痛难忍,故考虑卵巢囊肿蒂扭转,行急诊腹腔镜探查。术中见子宫增大如孕3+月,左右卵巢增大,大小约9 cm×6 cm×5 cm和10 cm×8 cm×6 cm,卵巢表面有多个囊泡突出,呈多囊样改变;右侧卵巢囊肿蒂扭转2圈,呈蓝紫色(图1C),表面可见黄体样组织。将右卵巢复位后,行双侧卵巢穿刺抽液术。术后予头孢呋辛钠预防感染、硫酸镁抑制宫缩、地屈孕酮保胎治疗。检测DIC全套:D-二聚体检测1.18 μg/ml、纤维蛋白原降解物3.80 μg/ml。予低分子肝素钠抗凝治疗。术后第4天病情平稳出院。术后42 d复查B超示双侧附件未见异常。定期产检无异常,孕36+6周剖宫产一活男婴和一活女婴,均体健。
二、讨论
自发性卵巢过度刺激综合征(sOHSS)在临床较少见,发生时卵巢并未受到刺激,可能与自发排卵周期有关[1]。据报道,12%~20%的sOHSS女性发生卵巢蒂扭转[2],而右侧附件较左侧更常见[1],但也有发生双侧附件扭转的报道[3]。调查显示,发生sOHSS的常见危险因素包括年龄<35岁、BMI偏低、多囊卵巢综合征、血清雌二醇水平迅速升高、既往发生过sOHSS史[4]。本病例中患者年龄(31岁)<35岁、BMI(20.4 kg/m2)偏低及雌二醇水平(>11 010 pmol/L)升高是sOHSS明确的危险因素。
目前sOHSS的发病机制尚不明确,可能是由于HCG对突变的卵泡刺激素受体(FSHR)异常敏感或具有相同β亚单位的糖蛋白激素过多分泌造成的[4]。也有研究指出HCG浓度的增高,可引发FSHR突变,促进下游激素的级联反应,从而导致sOHSS的发生[5]。最近的研究表明,所有FSHR基因突变均与sOHSS相关[6]。FSHR的基因突变会导致FSHR特异性配体与受体结合减少,从而增强HCG的反应性,最终导致sOHSS[2,7]。也有学者认为卵巢内的肾素-血管紧张素系统在OHSS的发病过程中起重要作用[8-9]。
研究者根据临床表现和FSHR突变情况将sOHSS分为4种亚型[10]。(1)Ⅰ型:与FSHR的突变相关,即使HCG、促甲状腺激素(TSH)及FSH水平正常,FSHR突变也可以被FSH、LH、HCG及具有相同β亚基的TSH激活[11],从而促进FSHR对自然妊娠的影响。这类sOHSS具有家族性及复发性的特点[12];(2)Ⅱ型:是继发于高水平HCG,在葡萄胎和多胎妊娠中较常见。多胎妊娠和妊娠滋养细胞疾病可使内源性HCG水平升高[3,13],较高的HCG生物活性可导致卵巢颗粒细胞内FSHR受到过度刺激[2,11],从而引发sOHSS;(3)Ⅲ型:与TSH高水平的甲状腺功能减退有关。甲状腺功能减退引起促性腺激素释放过多导致sOHSS的发生,但经甲状腺激素替代治疗后病情好转[14];(4)Ⅳ型:与分泌FSH或LH的促性腺激素腺瘤有关。本例患者入院时的HCG水平显著高于其他自然受孕的宫内妊娠者,其中双胎妊娠的HCG显著高于单胎妊娠。较高水平的HCG可促进卵巢肾素原的分泌,激活肾素-血管紧张素系统,使毛细血管通透性增加,从而引起卵巢过度刺激,故认为其发病因素与高水平HCG有关。因此,妊娠期HCG水平升高激活肾素血管紧张素系统可能是sOHSS的发病机制。由于环境和资源的限制,该患者未进行FSH受体基因检测及甲状腺功能评估,根据现有临床资料考虑该病例的sOHSS分型为Ⅱ型。
sOHSS的临床症状及影像学检查可反映该疾病的严重性及预后。临床症状包括腹胀腹痛、恶心呕吐和呼吸困难;影像学检查主要表现为卵巢增大、胸水、腹水及心包积液。文献报道sOHSS患者的血液生化检查显示血液浓缩、红细胞压积增大,白蛋白浓度下降,血清离子紊乱,HCG、FSH、LH等血清激素及CA125水平同时出现不同程度升高[15]。在严重的情况下,血液高凝状态可能导致血栓栓塞、肝肾衰竭、急性呼吸窘迫,甚至死亡[16]。对于存在腹水、CA125升高、卵巢增大的sOHSS患者,应与卵巢恶性肿瘤相鉴别。有学者指出,由于妊娠、腹膜刺激和OHSS等共同作用也可使CA125升高,临床上sOHSS容易被误诊为卵巢恶性肿瘤,因此需要综合分析[17]。本例患者年龄在35岁以下、BMI偏低,发病时间约在妊娠11周左右,临床表现以腹痛为主,无多囊卵巢综合征病史,未使用促排卵药物及保胎药物,HCG>200 000 U/L、E2>11 010 pmol/L、CA125显著升高,影像学和手术检查发现双侧卵巢呈多囊样改变,可确诊为sOHSS。
目前sOHSS缺乏有效的预防措施,因此早期诊断和治疗sOHSS,对预防并发症有重要意义。sOHSS以轻中度为主,病程呈自限性。对于sOHSS治疗的总体原则是:对症支持治疗,推荐继续妊娠,尽量避免手术操作[18]。治疗上以增加胶体渗透压扩容为主,同时纠正电解质絮乱、预防血栓形成以及其他对症治疗。Nwafor等[19]研究认为若患者胸腹水较多伴呼吸困难则需行胸腔穿刺或腹腔穿刺放液缓解症状。Ahmed Kamel[20]报道了1例自然妊娠合并重度sHOSS,经保守治疗后反应良好,足月顺利分娩。
对于不适合对症治疗的患者,特别是卵巢蒂扭转、卵巢囊肿破裂出血或妊娠合并卵巢恶性肿瘤时,应及时进行手术治疗,腹腔镜检查可作为诊断和辅助治疗的重要手段。当sOHSS并发急腹症时,需及时手术治疗,腹腔镜手术创伤性小、恢复期短,因此临床上首选腹腔镜手术[21]。本文中患者自然妊娠,无多囊卵巢综合征病史,无促排卵药物使用史,超声检查双侧卵巢明显增大,CA125进行性升高,主要症状为腹痛、无明显腹胀及腹水等症状,但仍不排除卵巢恶性肿瘤蒂扭转的可能性,因此急诊行腹腔镜探查。Munshi等[3]报道1例单胎妊娠sOHSS合并双侧卵巢扭转病例,腹腔镜下行双侧卵巢穿刺和卵巢固定术,术后效果改善明显。胡晓燕等[22]报道了1例自然妊娠并发sOHSS病例,经腹腔镜下行卵巢复位和卵巢穿刺放液术后,继续妊娠至足月分娩。雷瑞霖等[23]也报道了1例妊娠合并重度sOHSS可疑腹腔内出血病例,经腹腔镜下取卵巢囊肿活检及抽吸腹水后,成功保胎至足月分娩。
当血液浓缩或凝血因子异常时,可以进行预防性肝素治疗;伴有血栓性疾病的患者应积极进行抗凝和溶栓治疗[24]。对于保留卵巢的患者,术后需监测凝血功能,若血液处于高凝状态,D-二聚体升高,应适当给予肝素治疗,避免深部血栓形成。
总之,充分认识sOHSS的同时还需警惕卵巢恶性肿瘤的发生,及早诊断,及时治疗,以免出现严重并发症而延误患者病情甚至危及生命。

