新型优化心脏康复模式干预对急性冠脉综合征PCI术后患者心功能、血管内皮功能及心外膜脂肪厚度的影响
饶培玲 张琳 王昭君
郑州大学第一附属医院心血管内科,河南省郑州市 450000
经皮冠状动脉介入(Percutaneous Coronary Intervention,PCI)术可以改善急性冠脉综合征(Acute Coronary Syndrome,ACS)患者的冠状动脉血流灌注,缓解患者的心肌缺血,但同时会引起局部冠脉炎性反应,导致冠脉再狭窄,因此术后患者除需继续进行药物治疗之外还需进行必要的心脏康复干预以避免冠脉发生再狭窄[1]。对PCI术后ACS患者采用传统心脏康复模式进行干预,可逐渐增加患者的运动量,降低冠脉发生再狭窄的风险,但由于患者锻炼强度较弱,心功能恢复效果不够理想[2]。新型优化心脏康复模式通过采用科学规律的运动方案,可对PCI术后ACS患者进行科学规律的运动训练,有利于开放患者冠状动脉侧支循环,提高心肌细胞活力,改善心功能。为探讨新型优化心脏康复模式干预对PCI术后ACS患者心功能、血管内皮功能及心外膜脂肪(EAT)厚度的影响,本研究选取100例患者进行了干预观察,现将结果报告如下。
1 资料与方法
1.1 一般资料 选取2017年10月至2020年10月在我院行PCI术治疗的ACS患者100例为研究对象。纳入标准:(1)ACS确诊患者,首次成功进行了PCI治疗;(2)患者及其家属签署干预研究知情同意书。排除标准:(1)存在严重脑血管病后遗症;(2)罹患外周神经系统疾病;(3)精神异常或有精神疾病史。采用随机数字法将纳入研究的患者分为对照组和观察组,每组50例。对照组患者男27例、女23例;年龄56~77岁,平均(62.18±4.42)岁;其中急性非ST段抬高性心肌梗死(NSTEMI)患者16例、不稳定型心绞痛(UA)患者21例、急性ST段抬高性心肌梗死(STEMI)患者13例。观察组患者男26例、女24例;年龄54~76岁,平均(61.84±5.31)岁;其中NSTEMI患者17例、UA患者20例、STEMI患者13例。两组患者的性别、年龄等一般资料比较,差异无统计学意义(P>0.05)。本研究经我院医学伦理委员会批准。
1.2 方法
1.2.1 对照组 在常规药物治疗的基础上,采用传统心脏康复模式进行干预:术后第1天指导患者自主进食,协助其站立;术后第2天指导患者下床站立,在房间走动;术后第3天在家属监护下慢行100 m,以后每天逐渐增加步行距离以及活动时间。持续训练3个月。
1.2.2 观察组 在常规药物治疗的基础上,采用新型优化心脏康复模式进行干预:(1)术后第1天,进行间歇运动锻炼,要求能量消耗控制在2代谢当量(METs),自觉疲劳程度量表(PRE)评分<10分,靶心率<30%症状限制心率;(2)术后第2天,进行循环阻力和单一阻力交替的训练,要求能量消耗为2METs,阻力强度<50%一次最大重量,靶心率为30%~50%症状限制心率,PRE评分10~11分;(3)术后第3天,继续进行第2天的运动项目,但要增加训练时间,要求能量消耗2~3 METs,靶心率为40%~55%症状限制心率,PRE评分11~12分;(4)术后第4~7天,利用设备进行动态运动训练,要求能量消耗3~5 METS,靶心率为65%症状限制心率,PRE评分12~14分;(5)术后第8~14天,继续利用设备进行动态运动训练,要求能量消耗5~6 METs,靶心率为65%~85%症状限制心率,PRE评分14~16分。持续训练3个月。
1.3 观察指标
1.3.1 心功能 分别于干预前、干预3个月后,采用超声心动仪(GEV7)检测比较两组患者的左心室收缩末期容积(LVESV)、左室射血分数(LVEF)、室壁运动积分指数(WMSI)以及左心室舒张末期容积(LVEDV)。
1.3.2 血清因子水平 分别于干预前、干预3个月后,采两组患者外周空腹静脉血,采用全自动生化分析仪(BK-280)检测比较血清一氧化氮(NO)、可溶性血管细胞黏附分子-1(sVCAM-1)以及内皮素-1(ET-1)水平。
1.3.3 体脂参数和EAT厚度 分别于干预前、干预3个月后,采用智能身高体重测量仪(HW-700Z)检测比较两组患者的体质量、腰围、体质量指数(BMI);采用CT扫描仪(3D-1020S)检测比较两组患者的心外膜脂肪(EAT)厚度。
1.4 统计学处理 采用SPSS 22.0统计学软件进行数据分析。计量资料以x±s表示,两组间均数比较采用独立样本t检验,同组干预前后比较采用配对t检验。计数资料以%表示,比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者干预前后的心功能比较 干预前,两组患者的LVESV、LVEF、WMSI和LVEDV比较,差异无统计学意义(P>0.05);干预3个月后,观察组患者的LVESV以及WMSI水平显著低于对照组,LVEF及LVEDV水平显著高于对照组,差异有统计学意义(P<0.05)。见表1。
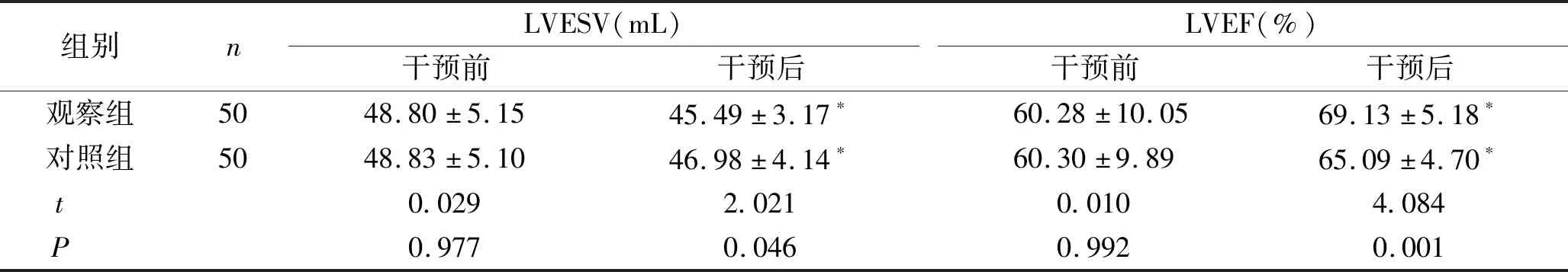
表1 两组患者干预前后的心功能比较 (n,x±s)
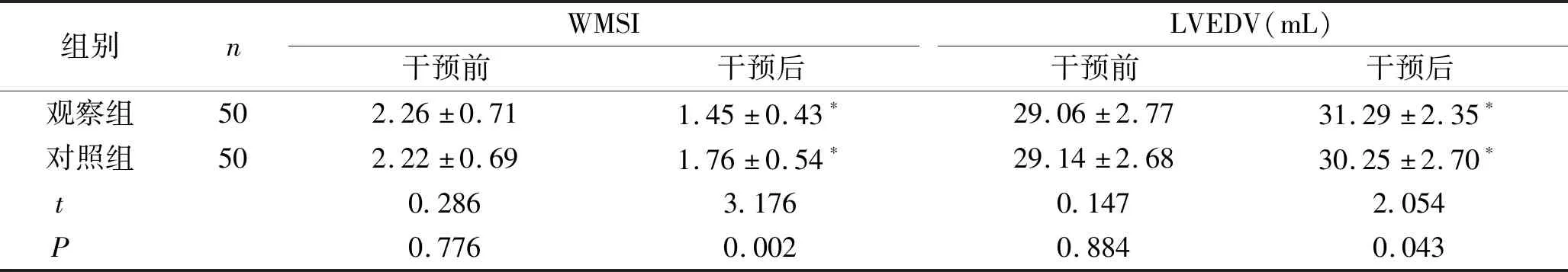
续表1
2.2 两组患者干预前后的血管内皮功能比较 干预前,两组患者的NO、sVCAM-1、ET-1水平比较,差异无统计学意义(P>0.05);干预3个月后,观察组患者的NO水平显著高于对照组,sVCAM-1、ET-1水平显著低于对照组,差异有统计学意义(P<0.05)。见表2。
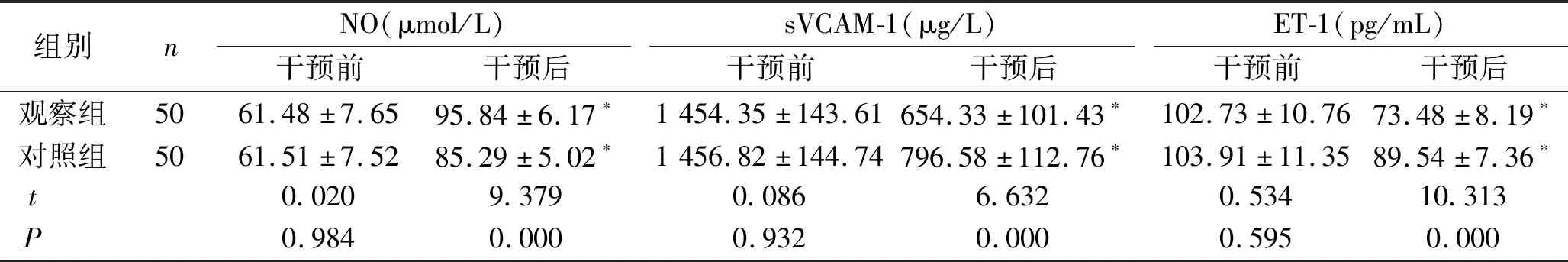
表2 两组患者干预前后的血管内皮功能比较 (n,x±s)
2.3 两组患者干预前后的体脂参数和EAT厚度比较 干预前,两组患者的体脂参数和EAT厚度比较,差异无统计学意义(P>0.05);干预3个月后,观察组患者的EAT厚度显著小于对照组,差异有统计学意义(P<0.05)。见表3。
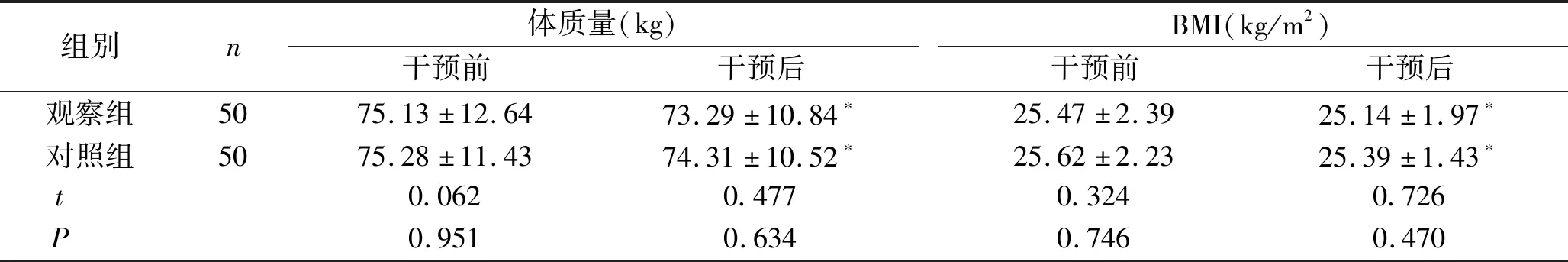
表3 两组患者干预前后的体脂参数和EAT厚度比较 (n,x±s)
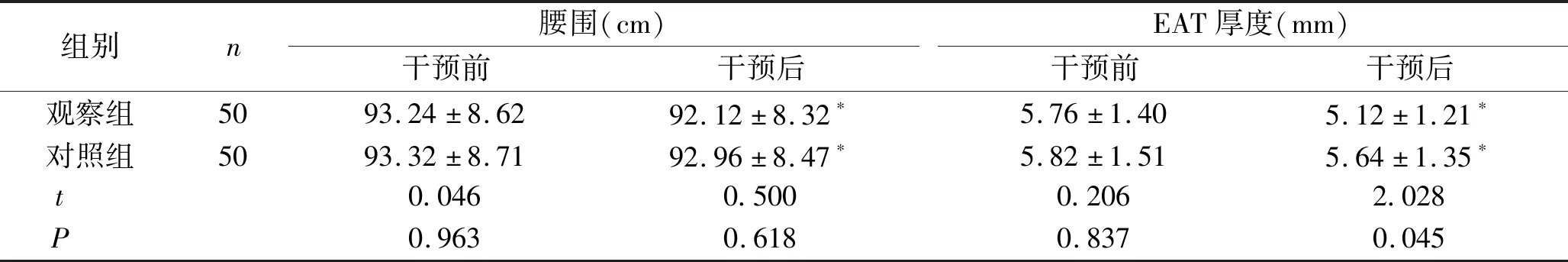
续表3
3 讨 论
PCI是临床治疗ACS患者的有效手段,可迅速开通闭塞动脉,改善心肌缺氧情况,但在一定程度上可能会损伤血管,影响血管内皮功能,甚至增加疾病复发风险[3]。ACS患者行PCI术治疗后容易出现心肌缺血再灌注情况,导致心功能不全。传统心脏康复模式常被用于PCI术后ACS患者的康复,通过活动锻炼改善患者的冠脉血流和心肌血管侧支循环,恢复血管内皮功能,但对患者心功能的改善作用不明显[4]。新型优化心脏康复模式通过采用科学的运动锻炼方案,可扩大PCI术后ACS患者的冠状动脉管径,提高血管弹性,改善心功能。
左心室收缩末期容积(LVESV)越大表示患者的心功能越差;室壁运动积分指数(WMSI)可反映心肌梗死的范围;左室射血分数(LVEF)是指心脏每搏射血量与左心室舒张末期容积的百分比,左心室舒张末期容积(LVEDV)指心室舒张时最大的容积,LVEF和LVEDV水平越高表示患者的心功能越好[5-6]。本研究中,对照组患者采用传统心脏康复模式进行干预,观察组患者采用新型优化心脏康复模式进行干预。结果显示,干预3个月后,观察组患者的LVESV以及WMSI水平显著低于对照组,LVEF以及LVEDV水平显著高于对照组。提示采用新型优化心脏康复模式进行干预可更有效地改善PCI术后ACS患者的心功能。
PCI术中由于使用球囊和金属支架对患者冠脉进行机械性扩张,会导致其血管内膜受损。一氧化氮(NO)是一种内皮衍生性舒张因子,内皮素-1(ET-1)是一种血管收缩因子,NO和ET-1在血管舒缩调节中发挥着关键的作用;可溶性血管细胞黏附分子-1(sVCAM-1)可与白细胞整合素反应,促进动脉粥样硬化发展,可反映出局部炎症反应情况[7-8]。本研究结果显示,干预3个月后,观察组患者的NO水平显著高于对照组,sVCAM-1、ET-1水平显著低于对照组,提示采用新型优化心脏康复模式进行干预可更有效地改善PCI术后ACS患者的血管内皮功能,缓解患者的炎症反应。
体质量、腰围、BMI异常与PCI术后ACS患者的冠脉再狭窄密切相关;心外膜脂肪(EAT)是指心肌与心包膜脏层间的内脏脂肪,EAT厚度和冠脉粥样硬化斑块形成风险呈正相关[9]。本研究结果显示,干预3个月后,两组患者的体质量、腰围以及BMI水平与对照组比较差异无统计学意义(P>0.05),但观察组患者的EAT厚度显著小于对照组,提示采用新型优化心脏康复模式进行干预可显著降低PCI术后ACS患者的EAT厚度,降低其冠脉粥样硬化的发生风险。
综上所述,采用新型优化心脏康复模式进行干预可显著改善急性冠脉综合征PCI术后患者的心功能及血管内皮功能,降低其心外膜脂肪厚度,降低冠脉粥样硬化的发生风险。

