细交链孢菌酮酸及其衍生物的合成与杀虫活性
尤伟晨, 刘小雨, 刘现坤, 柴源卿,王晓菲, 吕 培, 花日茂
(安徽农业大学 资源与环境学院,合肥 230036)
特胺酸 (tetramic acid) 的化学名称为吡咯烷-2,4-二酮,存在烯醇式和酮式两种互变异构体。天然产物中含有特胺酸骨架的化合物主要以烯醇式异构体存在[1],其广泛存在于海绵、蓝藻、细菌和真菌等多类海洋生物和陆地生物的次生代谢物中,具有抗病毒、抗细菌、抗真菌、抗肿瘤及除草等生物活性[2-3]。3-酰基特胺酸是典型的五元杂环次生代谢产物。其生物合成过程为:首先由乙酰辅酶A 在聚酮酶 (PKS) 催化下合成聚酮化合物 (A),进一步在非核糖体蛋白合成酶 (NRPS) 催化下与氨基酸缩合合成聚酮酰胺 (B),最终在细胞质中的完成3-酰基特胺酸骨架的合成[4](图式1)。

图式1 3-酰基特胺酸的生物合成[4]Scheme 1 Biosynthetic route of 3-acylated tetramic acid[4]
细交链孢菌酮酸(tenuazonic acid,以下简称TeA) 是链格孢菌Alternaria alternata(Fr.) Keissler的次生代谢毒素[5],分子式为C10H15NO3,结构式见图式2。研究表明,TeA 对丝光绿蝇Phaenicia sericata的LC50值为120 mg/L[6],并可有效控制紫茎泽兰Eupatorium adenophorum及其生境的主要杂草、农田禾草及多种阔叶杂草[7],同时3-位苯甲酰基、亚乙烯基、酰胺和酰肼取代的TeA 衍生物具有较好的除草[8]、杀虫和杀菌活性[9-13]。
TeA 的生物合成是由异亮氨酸与乙酰基乙酰辅酶A 缩合后得到的中间体经关环形成内酰胺而完成的[4]。在利用狄克曼关环反应进行TeA 的化学合成时,发现在强碱条件下会导致5-位的C 原子发生差向异构化,分别得到TeA 和5R, 6S-TeA异构体(iso-tenuazonic acid) (图式2)[14]。

图式2 TeA (1) 及其5R, 6S-异构体 (2) 的结构Scheme 2 Structures of tenuazonic acid and its 5R,6S-isomer
目前,TeA 及其衍生物的合成多采用双乙烯酮作为乙酰乙酰化试剂[10,15],而双乙烯酮挥发性强,其蒸气易对人眼产生危害,且这些方法仅能合成特胺酸3-位为乙酰基的衍生物。本研究参照特胺酸的生物合成途径,利用不同酰基化米氏酸替代双乙烯酮实现3-位为不同酰基特胺酸骨架化合物以及5-位不同取代衍生物的合成,同时通过测定目标化合物对麦芽虫的杀虫活性筛选出结构新颖的高活性化合物。酰基化米氏酸1a~1e、中间体2a~2s 和3a~3g、目标化合物4a~4s 和5a~5g 的合成路线见图式3,中间体6a 和目标化合物7a、8a 的合成路线见图式4。
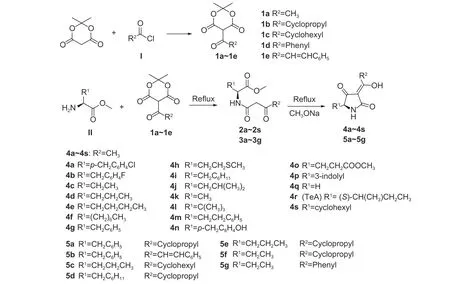
图式3 目标化合物4a~4s 和5a~5g 的合成路线Scheme 3 The synthetic route of the target compounds 4a-4s and 5a-5g

图式4 目标化合物7a 和8a 的合成路线Scheme 4 The synthetic route of the target compounds 7a and 8a
1 材料与方法
1.1 仪器与试剂
MP120 全自动熔点仪,南海能仪器股份有限公司;DD2 600MHz 核磁共振仪,美国Agilent 科技有限公司;人工气候培养箱,合肥达斯卡特科学器材有限公司;DZX-50KBS 立式压力蒸汽灭菌器,上海申安医疗器械厂;Waters ACQUITY UPLC 高效液相色谱 (Chiralpak AD-3R 色谱柱(2.1 mm × 150 mm,3 μm),流动相为V(乙腈) :V(0.1%甲酸水溶液)=50 : 50,流速0.3 mL/min),Waters 公司;XevoTQ-S UPLC/MS-MS 超高效液相色谱串联质谱仪,Waters 公司。
氨基酸甲酯盐酸盐均为L-构型,分析纯;其他试剂均为市售分析纯,未经处理直接使用。对照药剂:98.5%螺虫乙酯 (spirotetramat) 原药,Dr.Ehrenstorfer GmbH 公司产品。
1.2 化合物的合成
1.2.1 化合物1a~1e 的合成 参考文献方法[16]进行。将丙二酸环亚异丙酯 (3.00 g,20.8 mmol) 和吡啶 (3.29 g,41.6 mmol) 溶于25 mL 无水二氯甲烷中,在 -15~-5 ℃下搅拌15 min,缓慢滴加酰氯 Ⅰ (11 mmol) 的二氯甲烷溶液 (5 mL),在25 ℃下反应搅拌3.0 h。加入2 mol/L 的盐酸溶液20 mL,用二氯甲烷萃取,无水硫酸镁干燥有机相,经柱层析 (V(石油醚) :V(乙酸乙酯)=9 : 1) 纯化,得到产物1a~1e。
5-乙酰基-2,2-二甲基-1,3-二噁烷-4,6-二酮 (1a)[16]:棕色固体,产率83%,熔点80~82 ℃;1H NMR (600 MHz, CDCl3),δ: 1.75 (s, 6H), 2.69 (s, 3H), 15.13 (s, 1H). HRMS [ESI-]:C8H9O5[(M-H)-],m/z计算值:185.045 5;测试值:185.045 9.
5-(环丙烷甲酰基)-2,2-二甲基-1,3-二噁烷-4,6-二酮 (1b)[16]:淡黄色固体,产率82%,熔点81~83 ℃;1H NMR (600 MHz,DMSO-d6),δ: 1.30~1.31 (m, 4H),1.67 (s, 6H), 3.31~3.37 (m,1H). HRMS [ESI-]: C10H11O5[(M-H)-],m/z计算值:211.061 2;测试值:211.061 5.
5-(环己烷甲酰基)-2,2-二甲基-1,3-二噁烷-4,6-二酮 (1c)[16]:白色固体,产率85%,熔点79~81 ℃;1H NMR (600 MHz,CDCl3),δ: 1.20~1.27 (m 1H), 1.35~1.42 (m, 2H), 1.47~1.54 (m, 2H), 1.71 (s, 6H), 1.71~1.73 (m, 1H), 1.79~1.84 (m, 4H),3.76~3.80 (m, 1H). HRMS [ESI-]: C13H17O5[(M-H)-],m/z计算值:235.108 1;测试值:235.1083.
5-苯甲酰基-2,2-二甲基-1,3-二噁烷-4,6-二酮 (1d)[16]:黄色固体,产率96%,熔点95~97 ℃;1H NMR (600 MHz,DMSO-d6),δ: 1.76 (s, 6H), 7.46 (dd,J1= 7.8 Hz,J2= 7.2 Hz,2H), 7.57~7.61 (m, 3H). HRMS [ESI-],δ: C13H11O5[(M-H)-],m/z计算值:247.061 2;测试值:247.061 5.
5-肉桂酰基-2,2-二甲基-1,3-二噁烷-4,6-二酮 (1e):黄褐色固体,产率87%,熔点98~100 ℃;1H NMR (600 MHz,DMSO-d6),δ: 1.68 (s, 6H), 6.80 (s, 1H), 6.83 (s, 1H),7.42~7.49 (m, 5H). HRMS [ESI-]: C15H13O5[(M-H)-],m/z计算值:273.076 8;测试值:273.077 0.
1.2.2 化合物2a~2s 和3a~3g 的合成 将氨基酸甲酯盐酸盐(Ⅱ) (10 mmol) 、乙酰化米氏酸(2.09 g,11 mmol) 和三乙胺 (1.01 g,10 mmol) 分别加入到盛有1,4-二氧六环(p-dioxane, 40 mL) 的100 mL 茄形瓶中,加热回流反应4 h,用薄层色谱 (V(石油醚) :V(乙酸乙酯)= 5 : 1) 跟踪直至反应结束。减压浓缩后加入40 mL 乙酸乙酯溶解,分别用40 mL 1 mol/L 的盐酸和40 mL 饱和食盐水洗涤,无水硫酸钠干燥,经柱层析 (V(石油醚) :V(乙酸乙酯)= 5 : 1) 分离得到产物2a~2s 和3a~3g。
(S)-3-(4-氯苯基)-2-(3-氧代丁酰氨基) 丙酸甲酯 (2a):淡黄色油状液体,产率85%;1H NMR (600 MHz, CDCl3),δ: 2.22 (s, 3H), 3.01~3.05 (m, 1H), 3.12~3.15 (m, 1H), 3.38 (s,2H), 3.72 (s, 3H), 4.82~4.86 (m, 1H), 7.07 (d,J= 7.8 Hz, 2H),7.25 (d,J= 7.8 Hz, 2H), 7.28 (d,J= 7.2 Hz, 1H). HRMS[ESI-]: C14H15ClNO4[(M-H)-],m/z计算值:296.069 5;测试值:296.069 7.
(S)-3-(4-氟苯基)-2-(3-氧代丁酰氨基) 丙酸甲酯 (2b):淡黄色油状液体,产率80%;1H NMR (600 MHz, CDCl3),δ: 2.19 (s, 3H), 3.01 (dd,J= 6.6, 14.4 Hz, 1H), 3.11 (dd,J=5.6, 13.8 Hz, 1H), 3.36 (s, 2H), 3.69 (s, 3H), 4.81 (dd,J= 6.6,13.2 Hz, 1H), 6.94~6.96 (m, 2H), 7.07~7.09 (m, 2H), 7.29 (d,J=6.8 Hz, 1H).13C NMR (150 MHz, CDCl3),δ: 30.72, 37.08,49.56, 52.29, 53.38, 115.30, 115.37 (d,2JFC= 21.3 Hz), 130.72(d,3JFC= 8.0 Hz), 131.55 (d,4JFC= 3.3 Hz), 162.99 (d,1JFC=245.5 Hz), 165.23, 171.48, 203.57. HRMS [ESI-]:C14H15FNO4[(M-H)-],m/z计算值:280.099 1;测试值:280.099 4.
(S)-2-(3-氧代丁酰氨基) 丁酸甲酯 (2c):淡黄色油状液体,产率83%;1H NMR (600 MHz, CDCl3),δ: 0.92 (t,J=7.5 Hz, 3H), 1.71~1.78 (m, 1H), 1.85~1.82 (m, 1H), 2.26 (s,3H), 3.44 (s, 2H), 3.73 (s, 3H), 4.53~4.56 (m, 1H), 7.34 (s,1H).13C NMR (150 MHz, CD3OD),δ: 8.97, 24.43, 28.60,47.99, 51.16, 53.88, 167.80, 172.40, 203.00. HRMS [ESI-]:C9H14NO4[(M-H)-],m/z计算值:200.092 8;测试值:200.093 1.
(S)-2-(3-氧代丁酰氨基) 戊酸甲酯 (2d):淡黄色油状液体,产率86%;1H NMR (600 MHz, CDCl3),δ: 0.92 (t,J=7.3 Hz, 3H), 1.31~1.40 (m, 2H), 1.65~1.71 (m, 1H), 1.78~1.84(m, 1H), 2.27 (s, 3H), 3.44 (s, 2H), 3.73 (s, 3H), 4.57~4.60 (m,1H), 7.32 (s, 1H).13C NMR (150 MHz, CDCl3),δ: 13.72,22.18, 27.33, 30.79, 31.84, 49.60, 52.21, 52.28, 165.32,172.62, 203.88. HRMS [ESI-]: C10H16NO4[(M-H)-],m/z计算值:214.108 5;测试值:214.108 7.
(S)-2-(3-氧代丁酰氨基) 己酸甲酯 (2e):淡黄色油状液体,产率89%;1H NMR (600 MHz, CDCl3),δ: 0.87 (t,J=6.9 Hz, 3H), 1.28~.32 (m, 4H), 1.66~1.70 (m, 1H), 1.80~1.83(m, 1H), 2.25 (s, 3H), 3.43 (s, 2H), 3.71 (s, 3H), 4.54-4.57 (m,1H), 7.30 (brs, 1H).13C NMR (150 MHz, CDCl3),δ: 13.72,22.18, 27.33, 30.79, 31.84, 49.60, 52.21, 52.28, 165.32,172.62, 203.88. HRMS [ESI-]: C11H18NO4[(M-H)-],m/z计算值:228.124 1;测试值:228.124 3.
(S)-2-(3-氧代丁酰氨基) 辛酸甲酯 (2f):淡黄色油状液体,产率85%;1H NMR (600 MHz, CDCl3),δ: 0.86 (t,J=6.9 Hz, 3H), 1.25~1.38 (m, 8H), 1.67~1.69 (m, 1H), 1.81~.83(m, 1H), 2.26 (s, 3H), 3.43 (s, 2H), 3.73 (s, 3H), 4.53~4.61 (m,1H), 7.28 (brs, 1H).13C NMR (150 MHz, CDCl3),δ: 13.93,22.45, 25.18, 28.75, 30.85, 31.48, 32.16, 49.54, 52.24, 165.27,172.62, 203.94. HRMS [ESI-]: C13H22NO4[(M-H)-],m/z计算值:256.155 4;测试值:256.155 6.
(S)-3-苯基-2-(3-氧代丁酰氨基)-丙酸甲酯 (2g):淡黄色油状液体,产率78%;1H NMR (600 MHz, CDCl3),δ: 2.19(s, 3H), 3.03~3.07 (m, 1H), 3.13~3.16 (m, 1H), 3.35 (s, 2H),3.70 (s, 3H), 4.83~4.87 (m, 1H), 7.12 (d,J= 7.4 Hz, 2H), 7.23(dd,J= 6.4, 7.2 Hz, 2H), 7.26~7.29 (m, 2H).13C NMR (150 MHz, CDCl3),δ: 30.68, 37.85, 79.69, 52.26, 53.40, 127.10,128.55, 129.19, 135.80, 165.26, 171.63, 203.49. HRMS [ESI-]:C14H16NO4[(M-H)-],m/z计算值:262.108 5;测试值:262.108 7.
(S)-2-(3-氧代丁酰氨基)-4-甲硫基丁酸甲酯 (2h):黄色油状液体,产率80%;1H NMR (600 MHz, CDCl3),δ:1.97~2.03 (m, 1H), 2.08 (s, 3H), 2.15~2.18 (m, 1H), 2.26 (s,3H), 2.51 (t,J= 6.0 Hz, 2H), 3.45 (s, 2H), 3.74 (s, 3H),4.69~4.73 (m, 1H), 7.45 (s, 1H). HRMS [ESI-]: C10H16NO4S[(M-H)-],m/z计算值:246.080 6;测试值:246.081 2.
(S)-3-环己基-2- (3-氧代丁酰氨基) 丙酸甲酯 (2i):黄色油状液体,产率82%;1H NMR (600 MHz, CDCl3),δ:0.84~0.95 (m, 2H), 1.08~1.25 (m, 3H), 1.29~1.32 (m, 1H),1.51~1.56 (m, 1H), 1.60~1.62 (m, 1H), 1.64~1.67 (m, 4H),1.73~1.75 (m, 1H), 2.25 (s, 3H), 3.42 (s, 2H), 3.71 (s, 3H),4.58~4.62 (m, 1H), 7.20 (brs, 1H).13C NMR (150 MHz,CDCl3),δ: 25.93, 26.09, 26.29, 30.79, 32.41, 33.42, 34.11,39.71, 49.60, 50.24, 52.21, 165.33, 173.10, 203.92. HRMS[ESI-]: C14H22NO4[(M-H)-],m/z计算值:268.155 4;测试值:268.155 6.
(S)-4-甲基-2-(3-氧代丁酰氨基)-戊酸甲酯 (2j):黄色油状液体,产率78%,1H NMR (600 MHz, CDCl3),δ: 0.92,0.93 (d,J= 5.4 Hz, 6H), 1.55~1.61 (m, 1H), 1.62~1.69 (m,2H), 2.26 (s, 3H), 3.43 (s, 2H), 3.72 (s, 3H), 4.58~4.62 (m,1H), 7.23 (d,J= 6 Hz, 1H).13C NMR (150 MHz, CDCl3),δ:21.79, 22.72, 24.86, 30.80, 41.22, 49.53, 50.84, 52.18, 165.30,172.98, 203.90. HRMS [ESI-]:C11H18NO4[(M-H)-],m/z计算值:228.124 1;测试值:228.124 4.
(S)-2-(3-氧代丁酰氨基) 丙酸甲酯 (2k):黄色油状液体,产率84%;1H NMR (600 MHz, CDCl3),δ: 1.41 (d,J=7.2 Hz, 3H), 2.26 (s, 3H), 3.43 (s, 2H), 3.73 (s, 3H), 4.51~4.62(m, 1H), 7.38 (s, 1H). HRMS [ESI-]: C8H12NO4[(M-H)-],m/z计算值:186.077 2;测试值:186.077 6.
(S) -3,3-二甲基-2-(3-氧代丁酰氨基) 丁酸甲酯 (2l):淡黄色油状液体,产率88%;1H NMR (600 MHz, CD3OD3),δ: 0.98 (s, 9H), 2.26 (s, 3H), 3.45 (q,J= 12 Hz, 2H), 3.70 (s,3H), 4.40 (d,J= 6.0 Hz, 1H), 7.52 (d,J= 6.0 Hz, 1H).13C NMR (150 MHz, CD3OD),δ: 25.61, 28.77, 33.75, 50.72,60.84, 167.72, 171.38, 203.63. HRMS [ESI-]: C11H18NO4[(M-H)-],m/z计算值:228.124 1;测试值:228.124 3.
(S)-4-苯基-2-(3-氧代丁酰氨基) 丁酸乙酯 (2m):淡黄色油状液体,产率86%;1H NMR (600 MHz, CDCl3),δ: 1.27(t,J= 7.2 Hz, 3H), 1.97~2.06 (m, 1H), 2.17~2.24 (m, 1H),2.27 (s, 2H), 2.60~2.72 (m, 2H), 3.42 (s, 2 H), 4.17 (q,J= 7.2 Hz, 2H), 4.61~4.65 (m, 1H), 7.16~7.20 (m, 3H), 7.23~7.28 (m,2H), 7.35 (d,J= 6.6 Hz, 1H).13C NMR (150 MHz, CDCl3),δ:14.12, 30.85, 31.59, 33.75, 49.62, 52.20, 61.46, 126.13,128.34, 128.44, 140.61, 165.25, 171.76, 203.72. HRMS [ESI-]:C16H20NO4[(M-H)-],m/z计算值:290.139 8;测试值:290.140 1.
(S)-3-(对羟基苯基)-2-(3-氧代丁酰氨基) 丙酸甲酯(2n):淡黄色油状液体,产率81%;1H NMR (600 MHz,CDCl3),δ: 2.20 (s, 3H), 2.95~2.98 (m, 1H), 3.08~3.11 (m,1H), 3.38 (s, 2H), 3.73 (s, 3H), 4.82~4.84 (m, 1H), 6.71 (d,J=8.3 Hz, 2H), 6.98 (d,J= 8.3 Hz, 2H), 7.35 (d, J = 7.5 Hz, 1H).13C NMR (150 MHz, CDCl3),δ: 14.14, 20.99, 30.75, 37.10,49.31, 52.40, 53.62, 60.43, 115.55, 127.06, 130.29, 155.41,165.72, 171.84, 203.95. HRMS [ESI-]: C14H16NO5[(M-H)-],m/z计算值:278.103 4;测试值:278.103 7.
(S)-2-(3-氧代丁酰氨基)-戊二酸二甲酯 (2o):淡黄色油状液体,产率79%;1H NMR (600 MHz, CDCl3),δ:1.98~2.02 (m, 1H), 2.19~2.24 (m, 1H), 2.26 (s, 3H), 2.34~2.44(m, 2H), 3.43 (s, 2H), 3.66 (s, 3H), 3.73 (s, 3H), 4.60~4.64 (m,1H).13C NMR (150 MHz, CDCl3),δ: 27.15, 29.95, 30.75,49.69, 51.68, 5 173, 52.43, 165.53, 171.79, 172.94, 203.50.HRMS [ESI-]: C11H16NO6[(M-H)-],m/z计算值:258.098 3;测试值:258.098 7.
(S)-3-(2-吲哚)-2-(3-氧代丁酰氨基) 丙酸甲酯 (2p):淡黄色油状液体,产率84%;1H NMR (600 MHz, CDCl3),δ:2.12 (s, 3H), 3.26~3.34 (m, 4H), 3.67 (s, 3H), 4.89~4.92 (m,1H), 7.02 (brs, 1H), 7.09 (dd,J= 7.2, 7.8 Hz, 1H), 7.16 (dd,J=7.2, 7.8 Hz, 1H), 7.29~7.32 (m, 2H), 7.51 (d,J= 7.8 Hz, 1H),8.37 (s, 1H). HRMS [ESI-]: C16H17N2O4[(M-H)-],m/z计算值:301.119 4;测试值:301.1197.
(3-氧代丁酰氨基) 乙酸甲酯 (2q):淡黄色油状液体,产率86%;1H NMR (600 MHz, CDCl3),δ: 2.24 (s, 3H), 3.44(s, 2H), 3.71 (s, 3H), 4.02 (d,J= 6 Hz, 2H), 7.46 (brs, 1H).HRMS [ESI-]: C7H10NO4[(M-H)-],m/z计算值:172.061 5;测试值:172.061 9.
(2S,3S)-3-甲基-2- (3-氧代丁酰氨基) 戊酸甲酯 (2r):淡黄色油状液体,产率90%;1H NMR (600 MHz, CDCl3),δ:0.90~0.92 (m, 6H), 1.25~1.28 (m, 2H), 1.40~1.47 (m, 1H),1.88~1.94 (m, 1H), 2.26 (s, 3H), 3.45 (s, 2H), 3.72 (s, 3H),4.56 (dd,J= 5.4, 4.8 Hz, 1H), 7.37 (d,J= 7.2 Hz, 1H). HRMS[ESI-]: C11H18NO4[(M-H)-],m/z计算值:228.124 1;测试值:228.124 3.
1-(3-氧代丁酰氨基) 环己烷-1-甲酸甲酯 (2s):淡黄色油状液体,产率92%;1H NMR (600 MHz, CDCl3),δ:1.21~1.31 (m, 2H), 1.37~1.45 (m, 2H), 1.60~1.65 (m, 3H),1.77~1.82 (m, 2H), 1.97~2.03 (m, 3H), 2.25 (s, 3H), 3.41 (s,2H), 3.66 (s, 3H), 7.38 (s, 1H).13C NMR (150 MHz, CDCl3),δ:21.35, 25.08, 30.90, 32.24, 49.41, 52.19, 58.85, 164.69,174.22, 204.86. HRMS [ESI-]: C12H18NO4[(M-H)-],m/z计算值:240.124 1;测试值:240.124 4.
(S)-3-苯基-2-(3-环丙基-3-氧代丙酰氨基)-丙酸甲酯(3a):淡黄色固体,产率91%,熔点:73~85 ℃;1H NMR(600 MHz, CDCl3),δ: 0.91-0.99 (m, 2H), 1.08~1.10 (m, 2H),1.94~1.97 (m, 1H), 3.04~3.07 (m, 1H), 3.13~3.16 (m, 1H),3.50 (s, 2H), 3.70 (s, 3H), 4.83~4.86 (m, 1H), 7.12 (d,J= 7.3 Hz, 2H), 7.21~7.28 (m, 3H), 7.44 (d,J= 5.4 Hz, 1H). HRMS[ESI-]: C16H18NO4[(M-H)-],m/z计算值:288.124 1;测试值:288.124 4.
(S)-(3-氧代-5-苯基戊-4-顺烯酰氨基) 苯基丙氨酸甲酯(3b):淡黄色固体,产率98%,熔点:82~84 ℃;1H NMR(600 MHz, CDCl3),δ: 3.16~3.25 (m, 2H), 3.75 (s, 3H),5.02~5.05 (m, 1H), 6.09 (brs, 1H), 6.39 (d,J= 15.6 Hz, 1H),7.11 (d,J= 7.2 Hz, 2H), 7.23~7.30 (m, 3H), 7.35~7.36 (m,3H), 7.49 (d,J= 6.0 Hz, 2H), 7.63 (d,J= 15.6 Hz, 1H).13C NMR (150 MHz, DMSO-d6),δ: 42.00, 57.08, 58.95, 124.41,126.54, 131.76, 132.77, 133.46, 134.12, 134.78, 135.38,139.42, 139.88, 142.35, 144.71, 170.13, 172.71, 177.23.HRMS [ESI-]: C21H20NO4[(M-H)-] ,m/z计算值:350.139 8;测试值:350.140 1.
(S) -2-(3-环己基-3-氧代丙酰氨基) 戊酸甲酯 (3c):淡黄色固体,产率93%,熔点:71~73 ℃;1H NMR (600 MHz,CDCl3),δ: 0.90 (t,J= 7.3 Hz, 3H), 1.21~1.38 (m, 7H),1.64~1.69 (m, 2H), 1.75~1.78 (m, 3H), 1.84~1.86 (m, 2H),2.40~2.43 (m, 1H), 3.44 (s, 2H), 3.71 (s, 3H), 4.54~4.57 (m,1H), 7.45 (d,J= 6.6 Hz, 1H).13C NMR (150 MHz, CDCl3),δ:13.56, 18.59, 25.38, 25.65, 28.01, 34.22, 46.79, 51.61, 52.14,165.62, 172.60, 209.50. HRMS [ESI-]: C15H24NO4[(M-H)-] ,m/z计算值:282.171 1;测试值:282.171 3.
(S) -3-环己基-2-(3-环丙基-3-氧代丙酰氨基) 丙酸甲酯(3d):淡黄色固体,产率95%。1H NMR (600 MHz, CDCl3),δ: 0.83~0.92 (m, 2H), 0.94~0.99 (m, 2H), 1.07~1.24 (m, 5H),1.28~1.30 (m, 1H), 1.51~1.56 (m, 1H), 1.59~1.68 (m, 5H),1.74 (d,J= 12.7 Hz, 1H), 1.97~2.02 (m, 1H), 3.55 (s, 2H),3.69 (s, 3H), 4.58~4.62 (m, 1H), 7.46 (d,J= 7.4 Hz, 1H).13C NMR (150 MHz, CDCl3),δ: 11.97, 12.79, 13.53, 13.93,14.02, 18.52, 33.89, 58.54, 62.14, 100.68, 104.32, 175.69,189.47, 193.77, 195.78, 199.73. HRMS [ESI-]: C16H24NO4[(M-H)-] ,m/z计算值:294.171 1;测试值:294.171 3.
(S)-2-(3-环丙基-3-氧代丙酰氨基) 戊酸甲酯 (3e):淡黄色固体,产率92%,熔点:64~66 ℃;1H NMR (600 MHz,CDCl3),δ: 0.89 (t,J= 7.3 Hz, 3H), 0.95~0.99 (m, 2H),1.10~1.11 (m, 2H), 1.29~1.36 (m, 2H), 1.62~1.68 (m, 1H),1.78~1.81 (m, 1H), 1.97~2.01 (m, 1H), 3.55 (s, 2H), 3.70 (s,3H), 4.54~4.58 (m, 1H), 7.57 (d,J= 6.7 Hz, 1H).13C NMR(150 MHz, CDCl3),δ: 11.94, 13.56, 18.57, 21.48, 34.23, 48.88,52.12, 165.52, 172.62, 206.39. HRMS [ESI-]: C12H18NO4[(M-H)-],m/z计算值:240.124 1;测试值:240.124 4.
(S) -2-(3-环丙基-3-氧代丙酰氨基) 丁酸甲酯 (3f):淡黄色固体,产率95%,熔点:59~61 ℃;1H NMR (600 MHz,CDCl3),δ: 0.90 (t,J= 7.5 Hz, 3H), 0.95~0.99 (m, 2H),1.08~1.14 (m, 2H), 1.69~1.76 (m, 1H), 1.83~1.90 (m, 1H),1.97~2.01 (m, 1H), 3.56 (s, 2H), 3.71 (s, 3H), 4.52~4.55 (m,1H), 7.61 (d,J= 5.8 Hz, 1H).13C NMR (150 MHz, CDCl3),δ:9.51, 11.94, 21.49, 25.36, 48.89, 52.19, 53.33, 165.59, 172.39,206.39. HRMS [ESI-]: C11H16NO4[(M-H)-],m/z计算值:226.108 5;测试值:226.108 7.
(S) -2-(3-氧代-3-苯基丙酰氨基) 丁酸甲酯 (3g):淡黄色固体,产率80%,熔点:61~63 ℃;1H NMR (600 MHz,CDCl3),δ: 0.91 (t,J= 7.5 Hz, 3H), 1.72~1.81 (m, 1H),1.86~1.95 (m, 1H), 3.72 (s, 3H), 3.98 (q,J= 16.9 Hz, 2H),4.57~4.61 (m, 1H), 7.47 (dd,J1= 7.4 Hz, J2= 7.6 Hz, 2H),7.59 (d,J= 7.2 Hz, 2H), 7.98 (d,J= 8.1 Hz, 2H).13C NMR(150 MHz, CDCl3),δ: 9.51, 25.43, 45.22, 52.24, 53.49, 125.76,128.52, 128.80, 133.97, 165.60, 172.39, 195.49. HRMS [ESI-]:C14H16NO4[(M-H)-] ,m/z计算值:262.108 5;测试值:262.108 7.
1.2.3 目标化合物4a~4s 和5a~5g 的合成 将化合物2a~2s、3a~3g (10 mmol) 溶解在盛有甲醇(20 mL) 溶液的100 mL 茄形瓶中,搅拌5 min 后,滴加30%甲醇钠溶液 (1.98 g,11 mmol),加热至回流反应0.5 h,用薄层色谱 (V(石油醚) :V(乙酸乙酯)=1 : 5) 跟踪至反应完全。蒸除溶剂后加入12 mL纯水,用1 mol/L 的盐酸调节pH 值至2~3,抽滤,用乙醚萃取,有机相用无水硫酸镁干燥,经柱层析 (V(石油醚) :V(乙酸乙酯)=1 : 5) 分离,得到目标化合物4a~4s 和5a~5g。
(S)-1,5-二氢-5-(4-氯苄基)-3-乙酰基-4-羟基吡咯-2-酮(4a) :白色固体,产率85%,熔点81~83 ℃;1H NMR (600 MHz, CDCl3),δ: 2.45 (s, 3H), 2.67 (dd,J= 14.0, 9.6 Hz, 1H),3.22 (dd,J= 14.0, 3.4 Hz, 1H), 4.00 (dd,J= 9.4, 3.3 Hz, 1H),7.12 (d,J= 8.2 Hz, 2H), 7.27 (d = 8.2 Hz, 2H).13C NMR (150 MHz,CDCl3),δ: 19.62, 37.46, 63.18, 101.34, 128.98, 130.46,133.16, 134.70, 174.79, 185.72, 193.82. HRMS [ESI-]:C13H11ClNO3[(M-H)-],m/z计算值:264.043 3;测试值:264.043 8.
(S)-1,5-二氢-5-(4-氟苄基)-3-乙酰基-4-羟基吡咯-2-酮 (4b):白色固体,产率83%,熔点72~74 ℃;1H NMR(600 MHz, CDCl3),δ: 2.46 (s, 3H), 2.69 (dd,J= 14.0, 9.8 Hz,1H), 3.23 (dd,J= 12.1, 6.0 Hz, 1H), 4.00 (dd,J= 9.5, 3.2 Hz,1H), 7.98~7.02 (m, 2H), 7.15~7.17 (m, 2H).13C NMR (150 MHz,CDCl3),δ: 19.60, 37.30, 63.35, 101.39, 115.71 (d,2JFC=21 Hz), 130.63 (d,3JFC= 7.5 Hz), 131.92 (d,4JFC= 3.0 Hz),162.51 (d,1JFC= 244.5 Hz), 174.76, 185.65, 193.94. HRMS[ESI-]: C13H11FNO3[(M-H)-],m/z计算值:248.072 8;测试值:248.0731.
(S)-1,5-二氢-5-乙基-3-乙酰基-4-羟基吡咯-2-酮 (4c):白色固体,产率88%,熔点75~76 ℃;1H NMR (600 MHz,DMSO-d6),δ: 0.82 (t,J= 7.4 Hz, 3H), 1.45~1.52 (m, 1H),1.63~1.70 (m, 1H), 2.33 (s, 3H), 3.78 (brs, 1H).13C NMR (150 MHz, CDCl3),δ: 9.16, 19.50, 24.87, 63.33, 101.66, 175.22,184.97, 195.38. HRMS [ESI-]: C8H10NO3[(M-H)-],m/z计算值:168.066 6;测试值:168.066 9.
(S)-1,5-二氢-5-丙基-3-乙酰基-4-羟基吡咯-2-酮 (4d):白色固体,产率81%,熔点73~76 ℃;1H NMR (600 MHz,CDCl3),δ: 0.94, 0.96 (t, 3H), 1.37~1.45 (m, 2H), 1.56~1.61(m, 1H), 1.79~1.85 (m, 1H), 2.45, 2.50 (s, 3H), 3.81~3.83,3.97~9.99 (m, 1H), 6.40, 6.65 (brs, 1H).13C NMR (150 MHz,CDCl3),δ: 13.72, 18.52, 19.50, 33.86, 62.20, 101.48, 175.11,185.00, 195.48. HRMS [ESI-]: C9H12NO3[(M-H)-],m/z计算值:182.082 3;测试值:182.082 5.
(S)-1,5-二氢-5-丁基-3-乙酰基-4-羟基吡咯-2-酮 (4e):白色固体,产率83%,熔点78~82 ℃;1H NMR (600 MHz,CDCl3),δ: 0.90 (t,J= 8.0 Hz, 3H), 1.29~1.41 (m, 4H),1.57~1.64 (m, 1H), 1.81~1.87 (m, 1H), 2.45, 2.51 (s, 3H),3.81~3.83, 3.97~3.99 (m, 1H), 6.39, 6.49 (brs, 1H).13C NMR(150 MHz, CDCl3),δ: 13.78, 19.50, 22.38, 27.23, 31.51, 62.36,101.51, 185.00, 195.49. HRMS [ESI-]: C10H14NO3[(M-H)-],m/z计算值:196.097 9;测试值:196.098 1.
(S)-1,5-二氢-5-己基-3-乙酰基-4-羟基吡咯-2-酮 (4f):白色固体,产率78%,熔点138~140 ℃;1H NMR (600 MHz,CDCl3),δ: 0.85 (t,J= 6.2 Hz, 3H), 1.25~1.36 (m, 8H),1.54~1.60 (m, 1H), 1.80~1.84 (m, 1H), 2.43, 2.49 (s, 3H),3.79~3.81, 3.96~3.98 (m, 1H), 6.59, 6.81 (s, 1H).13C NMR(150 MHz, CDCl3),δ: 13.92, 19.48, 22.44, 25.08, 28.90, 31.49,31.81, 62.40, 101.51, 175.14, 184.94, 195.51. HRMS [ESI-]:C12H18NO3[(M-H)-],m/z计算值:224.129 2;测试值:224.129 6.
(S)-1,5-二氢-5-苄基-3-乙酰基-4-羟基吡咯-2-酮 (4g):白色固体,产率80%,熔点102~104 ℃;1H NMR (600 MHz,CD3OD),δ: 2.09 (s, 3H), 2.96~3.00 (m, 1H), 3.14~3.17 (m,1H), 4.70~7.72 (m, 1H), 7.19~7.22 (m, 3H), 7.26~7.28 (m, 2H).13C NMR (150 MHz, CDCl3),δ: 19.61, 38.22, 63.54, 101.41,128.89, 136.43, 174.68, 185.54, 194.11. HRMS [ESI-]:C13H12NO3[(M-H)-],m/z计算值:230.082 3;测试值:230.082 5.
(S)-1,5-二氢-5-(2-(甲硫基)乙基)-3-乙酰基-4-羟基吡咯-2-酮 (4h) :白色固体,产率81%,熔点103~105 ℃;1H NMR (600 MHz, CDCl3),δ: 1.81~1.90 (m, 1H), 2.10 (s, 3H),2.14~2.22 (m, 1H), 2.45, 2.51 (s, 3H), 2.59~2.68 (m, 2H),3.94~3.96, 4.13~4.18 (m, 1H), 6.71, 6.88 (s, 1H).13C NMR(150 MHz, CDCl3),δ: 15.22, 19.62, 30.67, 30.74, 61.67,101.24, 175.00, 185.44, 194.83. HRMS [ESI-]:C9H12NO3S[(M-H)-],m/z计算值:214.054 3;测试值:214.054 7.
(S)-1,5-二氢-5-(环己基甲基)-3-乙酰基-4-羟基吡咯-2-酮 (4i):白色固体,产率89%,熔点96~100 ℃;1H NMR(600 MHz, DMSO-d6),δ: 0.76~0.89 (m, 2H), 1.08~1.27 (m,3H), 1.24~1.27 (m, 1H), 1.46~1.50 (m, 2H), 1.60~1.64 (m,4H), 1.71~1.73 (m, 1H), 2.32 (s, 3H), 3.85~3.86 (m, 1H), 8.98(s, 1H). HRMS [ESI-]: C13H18NO3[(M-H)-],m/z计算值:236.129 2;测试值:236.129 5.
(S)-1,5-二氢-5-异丁基-3-乙酰基-4-羟基吡咯-2-酮(4j):白色固体,产率87%,熔点102~104 ℃;1H NMR(600 MHz, CDCl3),δ: 0.94, 0.95 (s, 6H), 1.39~1.46 (m, 1H),1.66~1.71 (m, 1H), 1.73~1.81 (m, 1H), 2.43, 2.48 (s, 3H),3.82~3.85, 3.99~4.01 (m, 1H), 6.97, 7.31 (s, 1H).13C NMR(150 MHz, CDCl3),δ: 19.50, 21.50, 23.22, 25.27, 60.96,101.27, 175.13, 185.06, 195.80. HRMS [ESI-]: C10H14NO3[(M-H)-],m/z计算值:196.097 9;测试值:196.098 1.
(S)-1,5-二氢-5-甲基-3-乙酰基-4-羟基吡咯-2-酮 (4k):白色固体,产率81%,熔点112~114 ℃;1H NMR (600 MHz, CDCl3),δ: 1.36, 1.39 (d,J= 7.0 Hz, 3H), 2.45, 2.50 (s,3H), 3.87~3.90, 4.03~4.07 (m, 1H), 6.30, 6.43 (s, 1H).13C NMR (150 MHz, CDCl3),δ: 17.44, 19.51, 57.89, 100.87,174.78, 185.38, 195.79. HRMS [ESI-]: C7H8NO3[(M-H)-],m/z计算值:154.051 0;测试值:154.0513.
(S)-1,5-二氢-5-(叔丁基)-3-乙酰基-4-羟基吡咯-2-酮(4l):白色固体,产率88%,熔点107~109 ℃;1H NMR(600 MHz, CD3OD),δ: 1.03 (s, 9H), 2.21 (s, 2H), 4.30 (s, 1H).13C NMR (150 MHz, CD3OD),δ: 25.71, 33.48, 60.74, 97.94,167.60, 172.47, 203.49. HRMS [ESI-]: C10H14NO3[(M-H)-],m/z计算值:196.097 9;测试值:196.0981.
(S)-1,5-二氢-5-苯乙基-3-乙酰基-4-羟基吡咯-2-酮(4m):白色固体,产率81%,熔点80~84 ℃;1H NMR(600 MHz, CDCl3),δ: 1.89~1.96 (m, 1H), 2.17~2.22 (m, 1H),2.44, 2.49 (s, 3H), 2.69~2.76 (m, 2H), 3.80~3.82, 3.96~3.97(m, 1H), 7.18~7.21 (m, 3H), 7.25~7.29 (m, 2H).13C NMR (150 MHz, CDCl3),δ19.56, 31.60, 33.36, 61.75, 101.40, 126.42,128.41, 128.64, 140.23, 175.05, 185.24, 195.13. HRMS [ESI-]:C14H14NO3[(M-H)-],m/z计算值:244.097 9;测试值:244.097 5.
(S)-1,5-二氢-5-(4-羟基苄基)3-乙酰基-4-羟基吡咯-2-酮(4n):白色固体,产率85%,熔点92~95 ℃;1H NMR(600 MHz, CD3OD),δ: 2.33 (s, 3H), 2.84~2.87 (m, 1H),2.97~3.00 (m, 1H), 4.08 (s, 1H), 6.66 (d,J= 8.4 Hz, 2H), 6.97(d,J= 8.4 Hz, 2H). HRMS [ESI-]: C13H12NO4[(M-H)-],m/z计算值:246.077 2;测试值:246.077 4.
(S)-1,5-二氢-5-(甲氧羰基乙基)-3-乙酰基-4-羟基吡咯-2-酮 (4o):白色固体,产率78%,熔点103~104 ℃;1H NMR (600 MHz, DMSO-d6),δ: 1.62~1.70 (m, 1H), 1.90~1.95(m, 1H), 2.33 (s, 3H), 2.38 (t,J= 7.7 Hz, 2H), 3.56 (s, 3H),3.84~3.96 (m, 1H), 8.88 (s,1H). HRMS [ESI-]: C10H12NO5[(M-H)-],m/z计算值:226.072 1;测试值:226.072 3.
(S)-1,5-二氢-5-(3-吲哚-甲基)-3-乙酰基-4-羟基吡咯-2-酮 (4p):棕黄色固体,产率84%,熔点122~124 ℃;1H NMR (600 MHz, CD3OD),δ: 2.25 (s, 3H), 2.98~3.02 (m, 2H),3.07~3.10 (m, 1H), 4.15 (brs, 1H), 6.94 (dd,J1=J2= 7.4 Hz,1H), 7.02 (dd,J1=J2= 7.5 Hz, 1H),7.29 (d,J= 8.1 Hz, 1H),7.50 (d,J= 7.9 Hz, 1H), 8.87 (s, 1H), 10.83 (s, 1H). HRMS[ESI-]: C15H13N2O3[(M-H)-],m/z计算: 269.093 2;测试值:269.093 5.
1,5-二氢-3-乙酰基-4-羟基吡咯-2-酮 (4q):白色固体,产率89%,熔点135~137 ℃;1H NMR (600 MHz, CDCl3),δ: 2.46, 2.51 (s, 3H), 3.80, 3.93 (s, 2H), 6.37, 6.47 (s, 1H).HRMS [ESI-]:C6H6NO3[(M-H)-],m/z计算值:140.035 3;测试值: 140.035 5.
(5S, 6S)-1,5-二氢-5-(仲丁基)-3-乙酰基-4-羟基吡咯-2-酮 (4r):黄色油状液体,产率90%,熔点122~123 ℃;1H NMR (600 MHz, DMSO-d6),δ: 0.78 (t,J= 7.4 Hz, 3H), 0.88(d,J= 7.0 Hz, 3H), 1.07~1.11 (m, 1H), 1.20~1.24 (m, 1H),1.75~1.78 (m, 1H), 2.32 (s, 3H), 3.77 (m, 1H), 8.85 (s, 1H).HRMS [ESI-]: C10H14NO3[(M-H)-],m/z计算值:196.097 9;测试值:196.097 7.
1,5-二氢3-乙酰基-4-羟基-1-氮杂螺环[4.5]癸-3-烯-2-酮 (4s):白色固体,产率95%,熔点134~136 ℃;1H NMR (600 MHz, CDCl3),δ: 1.32~1.56 (m, 5H), 1.70~1.81(m,5H), 2.44, 2.49 (s, 3H), 7.27, 7.77 (s, 1H).13C NMR (150 MHz, CDCl3),δ: 19.48, 21.83, 24.69, 32.97, 66.52, 100.65,174.34, 185.40, 197.87. HRMS [ESI-]: C11H14NO3[(M-H)-],m/z计算值:208.097 9;测试值:208.0977.
(S)-1,5-二氢-5-苄基-3-(环丙烷甲酰基)-4-羟基吡咯-2-酮 (5a):黄色固体,产率87%。1H NMR (600 MHz,DMSO-d6),δ: 1.05~1.07 (m, 4H), 2.83~2.88 (m, 2H),2.96~2.99 (m, 1H), 4.13 (m, 1H), 7.14~7.18 (m, 3H), 7.23 (dd,J1=J2= 7.4 Hz, 2H).13C NMR (150MHz, DMSO-d6),δ:11.32, 11.43, 14.08, 37.11, 126.90, 128.48, 130.03, 136.64,194.90. HRMS [ESI-]: C15H14NO3[(M-H)-],m/z计算值:256.097 9;测试值:256.098 3.
(S)-1,5-二氢-5-苄基-3-肉桂酰基-4-羟基吡咯-2-酮(5b):黄色固体,产率78%。1H NMR (600 MHz, DMSOd6),δ: 2.90~2.94 (dd,J= 13.8, 9.5 Hz, 1H), 3.11 (dd,J= 13.9,4.7 Hz, 1H), 4.55~4.62 (m, 1H), 6.68 (d,J= 18 Hz, 1H),7.16~7.19 (m, 1H), 7.23~7.27 (m, 4H), 7.34~7.39 (m, 4H),7.52 (d,J= 7.4 Hz, 2H), 8.40 (d,J= 7.2 Hz, 1H).13C NMR(150 MHz, DMSO-d6),δ: 37.31, 54.09, 122.14, 126.87,127.98, 128.64, 129.36, 129.50, 129.95, 135.22, 138.03,139.65, 165.31, 173.42. HRMS [ESI-]: C20H16NO3[(M-H)-],m/z计算值:318.113 6;测试值:318.113 2.
(S)-1,5-二氢-5-丙基-3-(环己甲酰基)-4-羟基吡咯-2-酮(5c):白色固体,产率89%。1H NMR (600 MHz, CDCl3),δ:0.94, 0.95 (t,J= 7.2, 3H), 1.18~1.25 (m, 1H), 1.34~1.46 (m,4H), 1.47~1.54 (m, 2H), 1.55~1.60 (m, 1H), 1.69~1.72 (m,1H), 1.75~1.83 (m, 5H), 3.36~3.47 (m, 1H), 3.78~3.80,3.95~3.97 (m, 1H), 6.68, 6.79 (s, 1H).13C NMR (150 MHz,CDCl3),δ: 13.72, 18.48, 25.47, 28.59, 28.61, 33.88, 40.90,62.04, 99.43, 176.05, 192.76, 195.00. HRMS [ESI-]:C14H20NO3[(M-H)-],m/z计算值:250.144 9;测试值:250.145 2.
(S)-1,5-二氢-5-(环己基甲基)-3-(环丙甲酰基)-4-羟基吡咯-2-酮 (5d):白色固体,产率83%。1H NMR (600 MHz,CDCl3),δ: 0.89~1.02 (m, 2H), 1.16~1.23 (m, 5H), 1.34~1.44 (m, 4H), 1.64~1.78 (m, 6H), 2.97~3.02, 3.07~3.12 (m,1H), 3.86~3.88, 4.02~4.04 (m, 1H), 6.67, 7.00 (s, 1H).13C NMR (150 MHz, CDCl3),δ: 11.95, 13.62, 26.30, 32.17, 33.99,34.69, 39.60, 60.29, 100.50, 175.62, 189.46, 196.26. HRMS[ESI-]: C15H20NO3[(M-H)-],m/z计算值:262.144 9;测试值:262.145 2.
(S)-1,5-二氢-5-丙基-3-(环丙烷甲酰基)-4-羟基吡咯-2-酮 (5e):白色固体,产率85%。1H NMR (600 MHz, DMSOd6),δ: 0.85 (t,J= 7.2 Hz, 3H), 1.11~1.14 (m, 4H), 1.29~1.35(m, 2H), 1.41~1.47 (m, 1H), 1.61~1.67 (m, 1H), 2.84 (brs,1H), 3.82 (brs, 1H).13C NMR (150 MHz, CDCl3),δ: 11.98,13.63, 13.74, 18.57, 33.84, 33.93, 62.14, 100.68, 175.69,189.46, 195.77. HRMS [ESI-]: C11H14NO3[(M-H)-],m/z计算值:208.097 9;测试值:208.097 6.
(S)-1,5-二氢- 5-乙基-3-(环丙甲酰基)-4-羟基吡咯-2-酮(5f):白色固体,产率83%。1H NMR (600 MHz, CDCl3),δ:0.96, 0.97 (t,J= 7.2 Hz, 3H), 1.15~1.20 (m, 2H), 1.33~1.36(m, 2H), 1.65~1.70 (m, 1H), 1.86~1.89 (m, 1H), 2.98~3.00,3.04~3.09 (m, 1H), 3.77~3.79, 3.94~3.96 (m, 1H), 6.66, 6.92(s, 1H).13C NMR (150 MHz, CDCl3),δ: 9.27, 11.96, 13.63,24.90, 63.30, 100.88, 175.82, 189.38, 195.65. HRMS [ESI-]:C10H12NO3[(M-H)-],m/z计算值:194.082 3;测试值:194.081 9.
(S)-1,5-二氢-5-乙基-3-苯甲酰基-4-羟基吡咯-2-酮(5g):白色固体,产率87%。1H NMR (600 MHz, CDCl3),δ: 0.99 (t,J= 7.3 Hz, 3H), 1.70~1.75 (m, 1H), 1.90~1.93 (m,1H), 3.82~3.83 (m, 1H), 6.92 (s, 1H), 7.49 (dd,J= 4.8, 7.8 Hz,2H), 7.59 (dd,J= 4.8, 7.8 Hz, 1H), 8.21 (d,J= 7.8 Hz, 2H).13C NMR (150 MHz, CDCl3),δ: 9.15, 25.09, 62.67, 99.70,128.06, 129.60, 131.74, 133.70, 177.44, 180.91, 193.10.HRMS [ESI-]: C13H12NO3[(M-H)-],m/z计算值:230.082 3;测试值:230.082 5.
1.2.4 目标化合物7a 的合成
1.2.4.1 中间体化合物6a 的合成 在 -15~0 ℃下,向14 mL 甲醇中滴加2.8 mL 二氯亚砜,滴加完毕后保持温度搅拌1 h。室温下向混合物中加入1-氨基-1-环己烷羧酸 (1.798 g,12.56 mmol),加热回流反应3 h。冷却至室温后,旋转蒸发除去溶剂甲醇,得到1-氨基-1-环己烷羧酸甲酯 (Ⅲ)。
取化合物 Ⅲ (1.57 g,10 mmol)溶于30 mL 无水二氯甲烷溶液中,分别加入4-二甲氨基吡啶(DMAP) (1.833 g,15 mmol) 和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐 (EDCI) (2.876 g,15 mmol)。在室温下滴加2,4-二氯苯乙酸 (3.075 g,15 mmol) 的5 mL 无水二氯甲烷溶液,在室温下反应16 h。用薄层色谱 (V(石油醚) :V(乙酸乙酯)=2 : 1) 跟踪原料至反应完全。抽滤,有机相分别用5% 碳酸氢钠溶液 (30 mL × 3) 和纯水 (30 mL× 3) 洗涤,无水硫酸钠上干燥,浓缩,经柱层析(V(石油醚) :V(乙酸乙酯)=3 : 1) 分离得到中间产物1-(2-(2,4-二氯苯基)乙酰氨基)环己烷-1-甲酸甲酯 (6a),淡黄色油状液体,产率87%,熔点98~100 ℃。1H NMR (600 MHz, CD3OD),δ:1.27~1.36 (m, 1H), 1.51~1.61 (m, 5H), 1.78~1.83 (m,2H), 1.99~2.01 (m, 2H), 3.63 (s, 3H), 3.69 (s, 2H),7.27 (dd,J= 8.4, 2.4 Hz, 1H), 7.32 (d,J= 8.4 Hz,1H), 7.43 (d,J= 2.4 Hz, 1H), 8.25 (brs, 1H).13C NMR (150 MHz, CD3OD),δ: 21.12, 24.95, 31.95,38.94, 51.16, 58.98, 126.80, 128.51, 132.41, 132.57,133.07, 134.90, 170.32, 174.90.HRMS [ESI-]:C16H18Cl2NO3[(M-H)-],m/z计算值:342.066 9;测试值:342.066 7.
1.2.4.2 目标化合物3-(2,4-二氯苯基)-4-羟基-1-氮杂螺环[4.5]癸-3-烯-2-酮(7a)的合成 取化合物6a (3.44 g,10 mmol) 溶解于20 mL 甲醇中,搅拌5 min 后滴加30%甲醇钠溶液 (1.98 g,11 mmol) ,加热回流反应0.5 h。冷却至室温,蒸发除去溶剂后加入12 mL 纯水,并用1 mol/L 盐酸调节pH至2~3,抽滤,得到目标化合物7a, 白色固体,产率92%,熔点103~105 ℃。1H NMR (600 MHz,DMSO-d6),δ: 1.14~1.21 (m, 1H), 1.33~1.35 (m, 2H),1.54~1.65 (m, 5H), 1.77~1.82 (m, 2H), 7.23 (d,J=8.4 Hz, 1H), 7.36 (dd,J= 1.8 Hz, 8.4 Hz, 1H), 7.56(d,J= 1.8 Hz, 1H), 8.15 (brs, 1H).13C NMR (150 MHz, DMSO-d6),δ: 22.14, 25.00, 33.92, 60.54,101.89, 126.98, 128.78, 130.31, 134.48, 135.54,171.10, 175.22. HRMS [ESI-] for C15H14Cl2NO2[(M-H)-],m/z计算值:310.040 7;测试值:310.040 9.
1.2.5 目标化合物2,2-二甲基丁酸-3-(2,4-二氯苯基)-2-氧-1-氮杂螺环[4.5]癸-3-烯-4-酯(8a)的合成向20 mL 无水二氯甲烷中分别加入2,2-二甲基丁酸 (0.87 g,7.5 mmol) 、DMAP (0.92 g,7.5 mmol) 和 EDCI (1.44 g,7.5 mmol),室温下搅拌30 min 后,滴加化合物7a (1.56 g,5 mmol) 的二氯甲烷溶液。室温反应16 h,薄层色谱 (V(石油醚) :V(乙酸乙酯)=1:3) 跟踪至原料反应完全。反应结束后,过滤,滤液加入20 mL 二氯甲烷稀释,有机相依次用5% 碳酸氢钠溶液 (30 mL × 3) 、1 mol/L 的盐酸溶液 (30 mL × 3) 和纯水 (30 mL ×3) 洗涤,无水硫酸钠干燥,浓缩后通过柱层析(V(石油醚) :V(乙酸乙酯)=1:3) 纯化,得到目标产物8a,白色固体,产率89%,熔点105~107 ℃.1H NMR (600 MHz, CDCl3),δ: 0.71 (t,J= 7.2 Hz,3H), 1.14 (s, 6H), 1.20~1.26 (m, 2H), 1.42~1.49 (m,2H), 1.55 (q,J= 7.2 Hz, 2H), 1.65~1.66 (m, 2H),1.77~1.85 (m, 4H), 7.21 (brs 1H), 7.25~7.28 (m, 2H),7.27 (d,J= 7.8 Hz, 1H), 7.38 (d,J= 1.2 Hz, 1H).13C NMR (150 MHz, CDCl3),δ: 8.94, 22.67, 24.50,24.68, 32.91, 43.34, 61.70, 117.83, 126.98, 127.78,129.10, 132.22, 134.44, 134.73, 167.05, 169.58,172.47. HRMS [ESI-]: C21H24Cl2NO3[(M-H)-],m/z计算值:408.113 9;测试值:408.113 7.
1.3 杀虫活性测定
参考文献中的根部内吸法[17]测定目标化合物在100 μg/mL 下对麦蚜的室内杀虫活性。麦长管蚜Macrosiphum avenae(Fabricius)由安徽农业大学植物保护学院提供,对照药剂为98.5%螺虫乙酯原药。先将目标化合物用N,N-二甲基甲酰胺 (DMF)溶解,再用水稀释成100 mg/L 的待测药液。选择带根的健壮小麦 (3 叶期),将根部洗净、晾干,将植株插入装有药液的烧杯中,置于温度为(25±1) ℃、相对湿度为80%、光照 : 黑暗=16 h : 8 h 的培养箱中。处理24 h 后取出,剪下植株茎部以上的麦苗部分,置于培养皿中,保湿备用。每处理重复4 次,每重复接试虫10~20 头。设置不含药剂的处理作为空白对照并记录初始虫数。分别于处理后24、48 和72 h 调查试虫死亡情况,记录总虫数和死亡虫数,计算校正死亡率。校正死亡率<20%:无活性;校正死亡率<60%:低活性;校正死亡率<85%:中等活性;校正死亡率≥85%:高活性。
1.4 小麦苗中的化合物残留量测定
1.4.1 仪器检测条件 色谱条件:Waters ACQUITY UPLC C BEH C18(2.1 mm × 100 mm,1.7 μm);流速0.3 mL/min;进样量5 μL;柱温40 ℃;流动相为V(0.1%的甲酸水溶液) :V(0.1%的甲酸乙腈溶液) =70 : 30。
质谱条件:正离子喷雾源 (ESI+);多检测反应模式 (MRM);毛细管电压3.6 kV;锥孔反吹气流量150 L/h;脱溶剂气温度400 ℃;脱溶剂气流量500 L/h。质谱分析参数详见表1。

表1 目标化合物的质谱分析参数Table 1 Mass spectrometry parameters of target compounds
1.4.2 样品前处理 将生长到三叶期的小麦根部浸入到100 mg/L 的目标化合物 (4e、5c、7a、8a)溶液中24 h。从距离植株根部2~3 cm 处剪断并置于搅拌机中碾碎。准确称取5.00 g 碾碎的麦苗于50 mL 离心管中,加入5 mL 乙腈和5.00 g 氯化钠,置于涡旋仪上涡旋5 min,以4 000 r/min 离心5 min。取1 mL 上清液过0.22 μm 亲水性滤膜,供超高效液相色谱-串联质谱(UPLC-MS/MS)检测。
1.4.3 基质匹配标准溶液配制 准确称取一定量目标化合物 (4e、5c、7a、8a),用甲醇溶解,配制成 1 000 mg/L 的标准储备液。用空白基质溶液稀释,配制成质量浓度分别为 5、10、25、50、100 和500 mg/L 的系列基质匹配标准溶液。按
1.4.1 节的条件测定,以化合物质量浓度为横坐标、峰面积为纵坐标,绘制标准曲线。
1.4.4 添加回收试验 称取空白麦苗按1.4.2 节方法进行样品前处理。向空白基质中添加4e、5c、7a 和8a 标准溶液,添加水平为10、100 和 500 mg/kg,每个水平重复 5 次,按1.4.1 节条件测定,计算添加回收率及相对标准偏差 (RSD)。
2 结果与分析
2.1 化合物的合成
将米氏酸与不同的酰氯进行亲核取代反应,得到乙酰化米氏酸1a~1e;用L-构型的氨基酸甲酯盐酸盐与1a~1e 进行缩合反应,得到化合物2a~2s 和3a~3e,通过手性色谱柱分析,发现2a~2q 和3a~3e 中酯基α碳原子构型未发生改变;化合物2a~2s、3a~3e 在甲醇钠/甲醇体系中发生Dieckmann 反应,经过盐酸酸化后得到目标产物4a~4s、5a~5e。在强碱条件下,氨基酸甲酯易烯醇化,从而导致氨基酸α位碳原子消旋化。Poncet等研究表明,(2S,3S)-3-甲基-2-(3-氧代丁酰胺基) 戊酸甲酯通过分子内成环反应,可得到(5S,6S)特胺酸与(5R,6S)特胺酸两个差向异构体,且比例随着甲醇钠的量和反应时间的延长而接近相等[14]。通过对反应条件进行优化,发现当甲醇钠为1.1 摩尔当量,反应时间为0.5 h 时能够较好地控制特胺酸C5 位C 的消旋化。化合物4a~4s、5a~5e 具有3 个羰基的次甲基结构,烯醇化可行成4 种可能的烯醇互变异构 (图式5)[18]。Hannes等通过计算NMR 和实验NMR 谱图对比,分析了TeA 在水溶液中的主要互变异构体,利用DFT 计算解释了在气态和不同溶剂中的3-酰基特胺酸主要互变异构体[18]。

图式5 3-酰基特胺酸互变异构[18]Scheme 5 Tautomerism of 3-acylated tetramic acid[18]
1-氨基-环己烷羧酸经过酯化反应、酰胺缩合反应后得到化合物6a。将化合物6a 置于甲醇钠所提供的碱性环境下发生分子内成环反应,形成对应的特胺酸钠盐,经过盐酸酸化后得到目标化合物7a。7a 与2,2-二甲基丁酸发生酯化反应后,得到目标化合物8a。
本研究结果表明,通过乙酰化的米氏酸可以获得多种3-位不同的取代基,由此可以实现具有特胺酸骨架化合物的多官能化,从而获得结构多样性的目标化合物。
2.2 杀虫活性
测定结果(表2)表明,部分目标化合物对于麦蚜均具有较高的杀虫活性,在100 μg/mL 下处理48 h 时,除化合物4a、4b 的校正死亡率分别为7%和17%外,其余化合物对于麦蚜的校正死亡率在24%~100%之间,其中5a、5c、5d、5e、7a 和8a 达88%~100%,而5c、5d、5e、8a 在94%~100%之间,高于TeA (4r) (86%) 和对照药剂螺虫乙酯 (90%)。处理72 h 时,化合物4a、4b、4g、4h、4j、4k、4o 的校正死亡率在50%~82%之间,其余化合物为90%~100%。随着时间的推移,昆虫取食量增加,目标化合物在虫体内的累积量随之增加,杀虫活性增强。
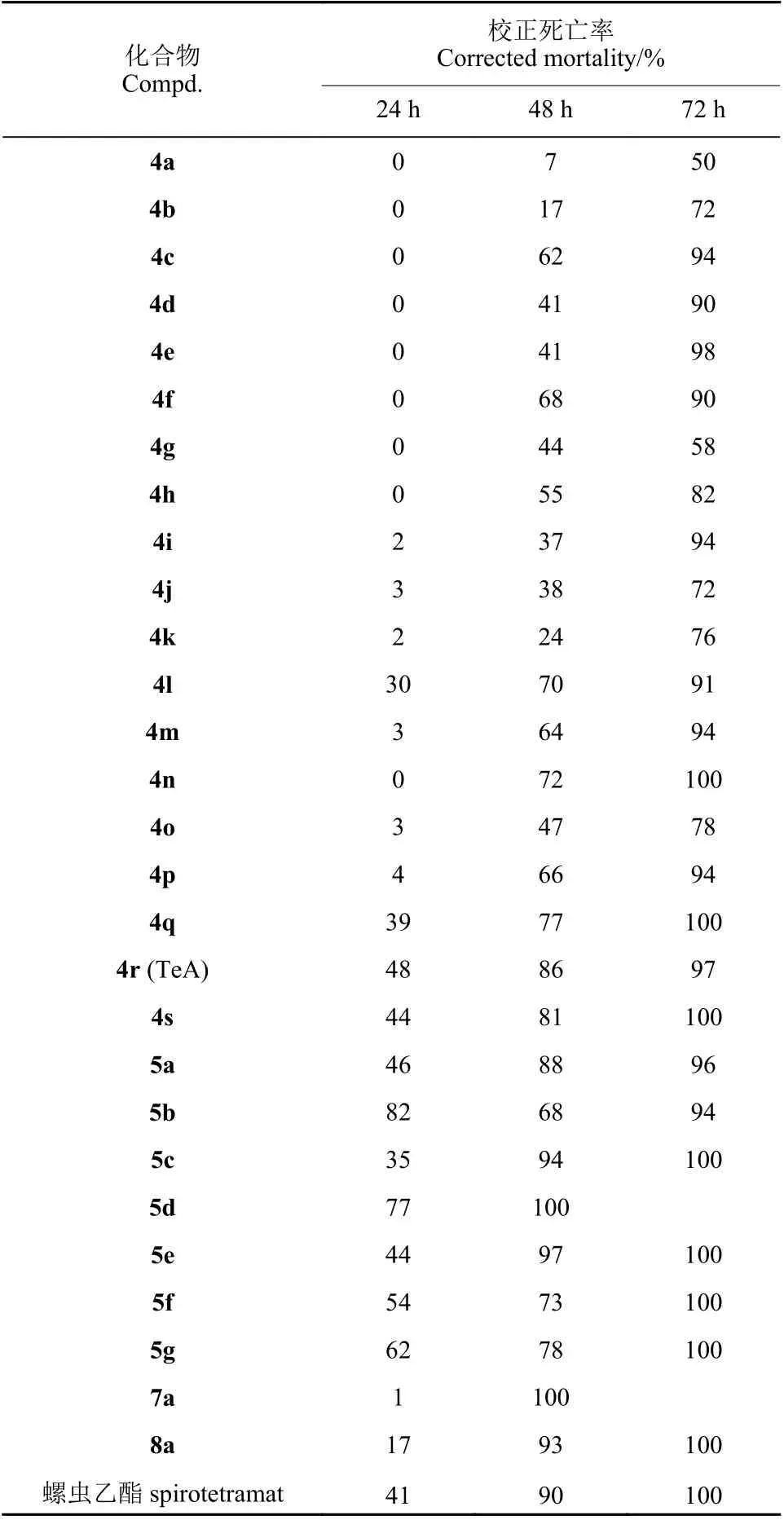
表2 目标化合物在100 μg/mL 下对麦蚜的杀虫活性Table 2 Insecticidal activity of target compounds against wheat aphid under the concentration of 100 μg/mL
初步的构效关系表明,当3-位为环丙酰基时,化合物的活性高于其为乙酰基 (5a>4g, 5e>4d),当5-位为苄基时,有利于增加特胺酸骨架化合物的杀虫活性 (5d>5c, 5d>5e, 5d>5f)。可见,对3-位和5-位进行定向修饰可以提高特胺酸骨架对麦芽的活性。
2.3 目标化合物在麦苗中的残留量
添加回收试验结果表明,在10、100 和 500 mg/kg 3 个添加水平下,化合物4e、5c、7a 和8a在麦苗中的平均回收率在95%~110% 之间,RSD 在0.06%~2.4%之间 (表3)。表明样品的提取和净化方法能够有效地检测植株中4e、5c、7a 和8a 的含量。目标化合物在麦苗中的残留量 (表4)显示,化合物4 个供试化合物均具有一定的内吸性,且其残留量排序为7a<4e<5e<8a。化合物8a 相较于其他3 类化合物更易被植株吸收,可能是由于4 位上酯基的形成使8a 的极性变小,导致其更易被植株吸收。
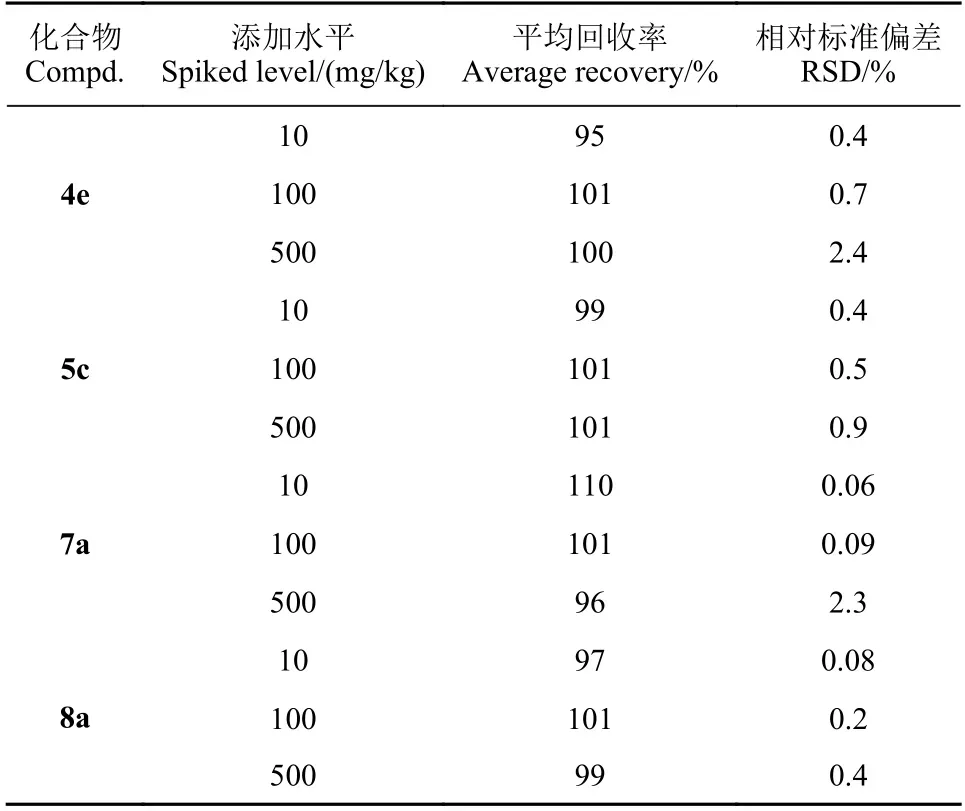
表3 目标化合物在麦苗中的平均添加回收率和相对标准偏差 (RSD) (n = 5)Table 3 The average recoveries and RSD of target compounds in wheat seedlings (n = 5)

表4 目标化合物在麦苗中的残留量Table 4 Residue of target compounds in wheat seedlings
3 结论
本文以天然活性产物细交链孢菌酮酸(TeA)为先导化合物,通过不同结构的氨基酸与酰基化米氏酸进行缩合、分子内成环等反应,合成了TeA 及其一系列具有特胺酸骨架的新化合物。并杀虫活性测定。结果表明,所有目标化合物对麦长管蚜均有较为明显的杀虫活性,并具有内吸性,其中化合物5c、5d、5e、7a 和8a 48 h 的校正死亡率为93%~100%,高于4r (TeA)和阳性对照螺虫乙酯,可以作为先导化合物进一步研究。初步构效关系分析表明,当特胺酸骨架化合物的3-位为环丙酰基或环己酰基,5-位为苄基或者环己亚甲基时,杀虫活性较强。化合物5d 有作为先导化合物的潜力和研究价值。

