载钛半焦活性炭对水中四环素的吸附性能研究
陈楚昭, 王家宏, 梁林青
(陕西科技大学 环境科学与工程学院, 陕西 西安 710021)
0 引言
四环素类抗生素是抗生素中使用量最多、最广泛的一种[1].水环境是抗生素的重要归宿,一半以上的抗生素经多种途径最终进入到水环境当中[2-3],对人类的健康和生态系统造成潜在威胁[4],因此对于水中四环素的处理引起了较大关注.目前去除水中四环素的方法主要有生物降解法、高级氧化法、膜处理法和吸附法等[5],其中吸附法具有效率高、操作简单的优势被广泛用于水中四环素的去除[6].本题组前期研究发现活化半焦活性炭对水中四环素有良好的吸附效果[7],但再生过程中使用NaOH会产生二次污染并且费用高[8,9],因此有必要对半焦活性炭改性,以期得到吸附效率高、再生成本低且再生过程无污染的吸附剂.
前人研究发现,TiO2改性吸附剂可以提升吸附能力,李梦悦等[10]研究表明通过浸渍-水热法合成负载TiO2活性炭吸附RhB,去除效果优于活性炭.同时,TiO2作为常见的光催化材料,具有光催化活性强、对环境友好等特性[11],被广泛应用于光催化再生.刘润田[12]通过超声-煅烧法制备参杂硫脲的TiO2膨化活性炭通过光催化再生后吸附效率达到70%,Xu等[13]用TiO2、聚苯胺等合成复合纤维膜去除刚果红,在光照下再生效率达到60%.因此,在前期研究基础上,将TiO2负载到活化半焦活性炭(TiAC)表面,分析其对水中四环素的吸附性能,探索吸附饱和后光催化再生效果,以期为半焦活性炭的综合利用提供技术参考.
1 实验部分
1.1 实验试剂与仪器
半焦购自于府谷万兴新能源有限公司;氢氧化钾和硫酸钛购自于天津天力化学试剂有限公司.
主要实验设备包括: UV-2600AH紫外-可见分光光度计(生产厂家为尤尼科上海仪器有限公司)、VECTOR-22里叶红外光谱仪(德国布鲁克Bruker公司)、X射线光电子能谱(AXIS SUPRA)、X射线衍射仪(Rigaku D/max220PC).
1.2 载钛半焦活性炭的制备
采用KOH与半焦固相研磨高温活化制备活化半焦活性炭[7],接着将活化半焦活性炭与硫酸钛溶液混合,搅拌24 h离心分离后置于电热鼓风干燥箱内干燥12 h.然后置于管状电阻炉中氮气保护,以10 ℃·min-1升温至300 ℃,保持30 min,再以继续以10 ℃·min-1升温至600 ℃,并保持3 h,冷却至室温,用去离子水洗至不存在硫酸根粒子,烘干制得载钛活性炭,记为x%TiAC,分别制得0.5%TiAC、1%TiAC、2%TiAC、4%TiAC、6%TiAC(x表示TiSO4溶液的质量浓度).
1.3 负载量对吸附影响实验
分别称取活化半焦活性炭、0.5%TiAC、1%TiAC、2%TiAC、4%TiAC和6%TiAC吸附剂50 mg投至棕色反应瓶,再加入50 ml浓度分别为50 mg·L-1至500 mg·L-1的四环素溶液,调节pH为6.0,放恒温振荡箱中振荡12 h.用0.45μm的滤膜过滤,用紫外-可见分光光度计在356 nm波长下测定滤液中四环素含量并计算平衡吸附量.平衡吸附量qe(mg·g-1)计算公式如下:
(1)
式(1)中:qe—平衡吸附量(mg/g);C0—四环素溶液的初始浓度(mg/L);Ce—四环素溶液的平衡浓度(mg/L);V—四环素溶液体积(L);M—吸附剂的质量(g).
为了进一步了解该吸附剂的吸附机理,进行吸附等温线模拟.Langmuir模型理论[14]认为,吸附是在表面进行的单层吸附,描述吸附质在固相吸附剂与液相间的分配关系.方程表示为:
(2)
Freundlich吸附模型[15]通常表达不均匀表面吸附,随着吸附点位变少,吸附结合强度降低.方程表示为:
lgqe=lgKf+1/nlgCe
(3)
式(3)中:qe—平衡吸附量(mg·g-1);qm—理论最大平衡吸附量(mg·g-1);Ce—平衡浓度(mg·L-1);b—亲和系数(L·mg-1),Kf—Freundlich吸附常数(L·mg-1),n—Freundlich经验常数.
1.4 吸附动力学
称取500 mg的2%TiAC于500 mL的三口圆底烧瓶中,加入500 mL初始浓度为150 mg·L-1的四环素溶液,每隔一定时间取样测定并根据公式(1)计算吸附量.为进一步探究2%TiAC吸附四环素的动力学过程,用拟一级动力学方程以及拟二级动力学方程对吸附动力学实验进行拟合.
拟一级动力学方程表示为:
ln(qe-qt)=lnqe-k1t
(4)
拟二级动力学方程表示为:
(5)
式(4)、(5)中:t为吸附时间(min);qe为平衡吸附量(mg·g-1);qt为t时刻的吸附量(mg·g-1);k1为拟一级动力学方程常数(g·mg-1·min-1);k2为拟二级动力学方程常数(g·mg-1·min-1).
1.5 pH值、阳离子和腐殖酸影响实验
称取50 mg的2%TiAC于50 mL初始浓度为400 mg·L-1的四环素溶液中,调节体系的pH值为3~10之间,恒温振荡反应后测吸光度并计算吸附量.取50 mg的2%TiAC,与50 mL浓度为300 mg·L-1的四环素溶液混合,分别调节Na+、K+、Ca2+的浓度为1~10 g·L-1,恒温震荡反应后测其吸光度计算吸附量.取50 mg的2%TiAC,与50 mL浓度为300 mg·L-1的四环素溶液混合,并调节溶液中腐殖酸浓度分别10 mg·L-1、20 mg·L-1、40 mg·L-1、60 mg·L-1、80 mg·L-1、100 mg·L-1,恒温震荡反应后测其吸光度计算吸附量.
1.6 再生实验
分别称取50 mg的活化半焦活性炭和2%TiAC分别置于初始浓度为400 mg·L-1四环素溶液中振荡至吸附平衡,测吸光度并计算平衡吸附量,离心收集吸附剂.取吸附饱和的吸附剂置于300 W的紫外灯下分别照射2 h、4 h、6 h、8 h,离心干燥后再次吸附四环素,测吸光度并计算平衡吸附量.
再生率的计算:
(6)
式(6)中:m1—原始吸附剂的四环素平衡吸附量(mg·g-1);m2—再生后吸附剂的四环素平衡吸附量(mg·g-1)
2 结果和讨论
2.1 TiAC表征
2.1.1 FT-IR分析
图1为载钛前后以及不同浓度载钛催化剂的FT-IR图.图1中3 442 cm-1对应的是TiAC表面O-H的伸缩振动峰,1 637 cm-1对应O-H的弯曲振动峰.1 028 cm-1处为载钛后形成Ti-O-C键引起的吸收峰[16],在450~550 cm-1处出现Ti-O键的振动峰,为锐钛矿型TiO2中Ti-O键的特征振动带[17],说明TiO2成功负载到活化半焦表面.
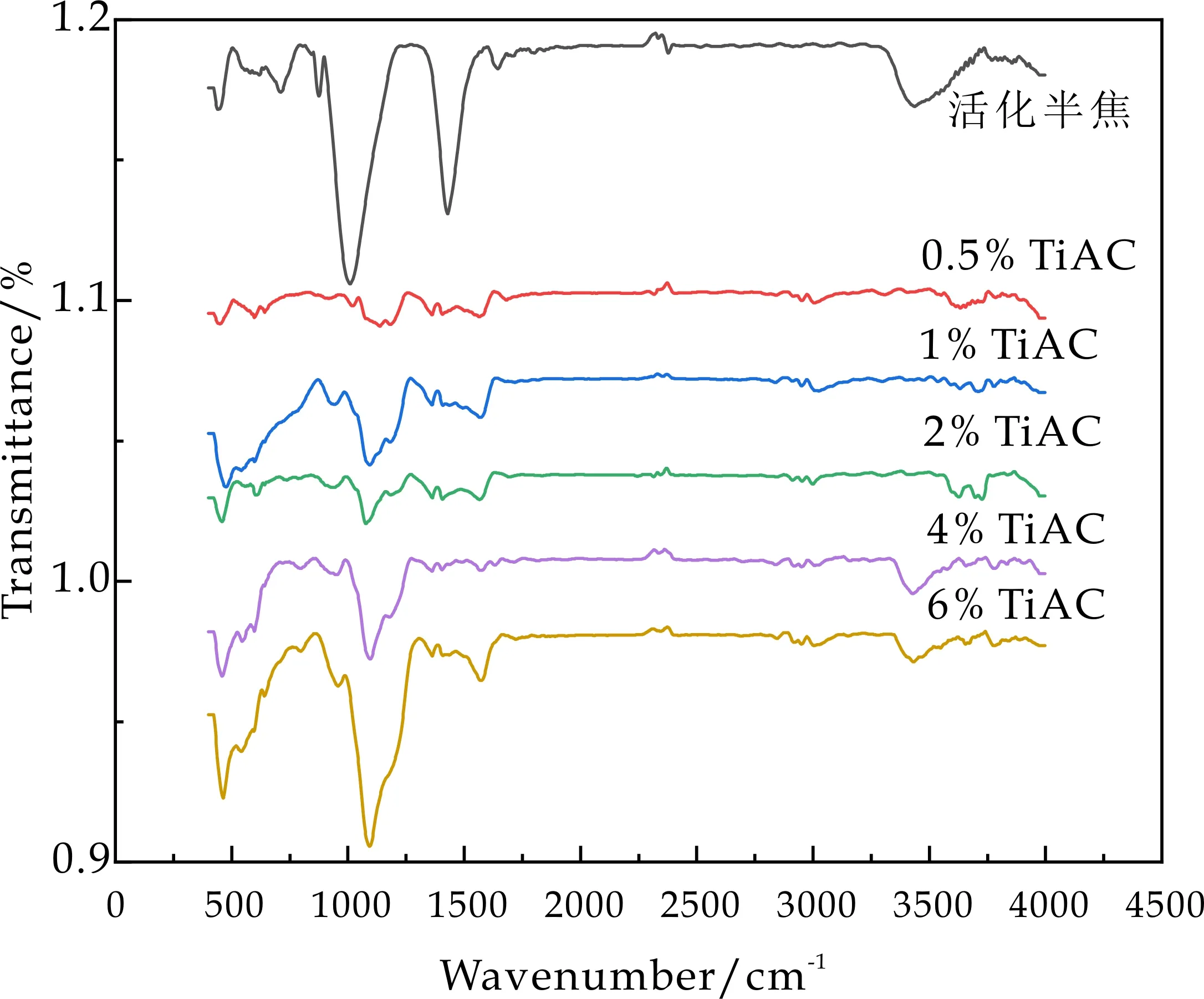
图1 吸附剂的FT-IR图
2.1.2 XRD分析
对半焦活性炭载钛前后进行X-射线衍射分析,结果如图2所示.半焦活性炭是一种以石墨微晶为基础的无定型碳,在2θ约为43.7 °和50.8 °位置附近出现了肩峰,属于石墨微晶晶面.载钛后的吸附剂在2θ为29.6 °处存在锐钛矿相的衍射峰,其晶面特征衍射峰(2θ=29.6 °)与标准卡JCPDS-99-0088一致,说明二氧化钛成功负载到活化半焦活性炭表面.
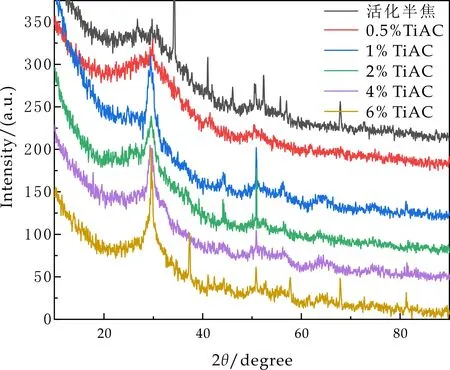
图2 吸附剂的XRD图
2.1.3 XPS分析
图3是2%TiAC吸附四环素前后和光解再生后的XPS图谱.2%TiAC表面出现Ti、C和O三种元素.在Ti2p谱图(如图3(a)所示)中,485.8 eV和464.6 eV处的峰分别归属于Ti4+2p3/2和Ti4+2p1/2,说明TiO2成功负载到半焦活性炭表面;在C1s (如图3(b)所示)中,284.8 eV结合能处是C-C或C-H的特征峰,286.4 eV结合能峰是C-O特征峰,288.9 eV结合能处是C=O的特征峰,均为半焦活性炭C元素特征峰[18],且材料表面富含含氧官能团,有利于提升对四环素的吸附效果[13,19].
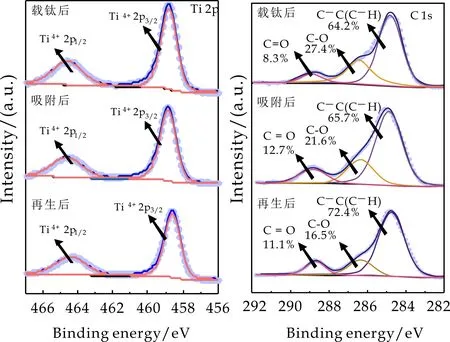
(a)Ti 2p谱图 (b)C 1s谱图图3 2%TiAC吸附四环素前后及再生后的XPS光谱图
2.2 TiAC对四环素的吸附
2.2.1 负载量对吸附效果的影响
图4显示在25 ℃、pH=6.0条件下,活化半焦、0.5%TiAC、1%TiAC、2%TiAC、4%TiAC、6%TiAC对不同初始浓度四环素溶液的最大吸附容量,分别为311.29 mg·g-1、148.53 mg·g-1、190.02 mg·g-1、426.25 mg·g-1、286.55 mg·g-1、228.62 mg·g-1.由此可以看出,当钛投加量为2%(硫酸钛与活化半焦质量比)时,对四环素的吸附效果最好.这可能是由于钛负载量低时,半焦活性炭表面的TiO2可能会堵塞半焦的孔道导致半焦活性炭的活性位点减少,从而导致吸附量降低[20];随着负载的TiO2增加,吸附剂表面TiO2的吸附位点增多,从而引起吸附量增大[21];随着钛负载量进一步增多,TiO2占据部分吸附位点并且堵塞半焦活性炭孔道,从而导致吸附量降低[22].因此,本研究采用吸附量最大的2%TiAC作为后续研究对象.
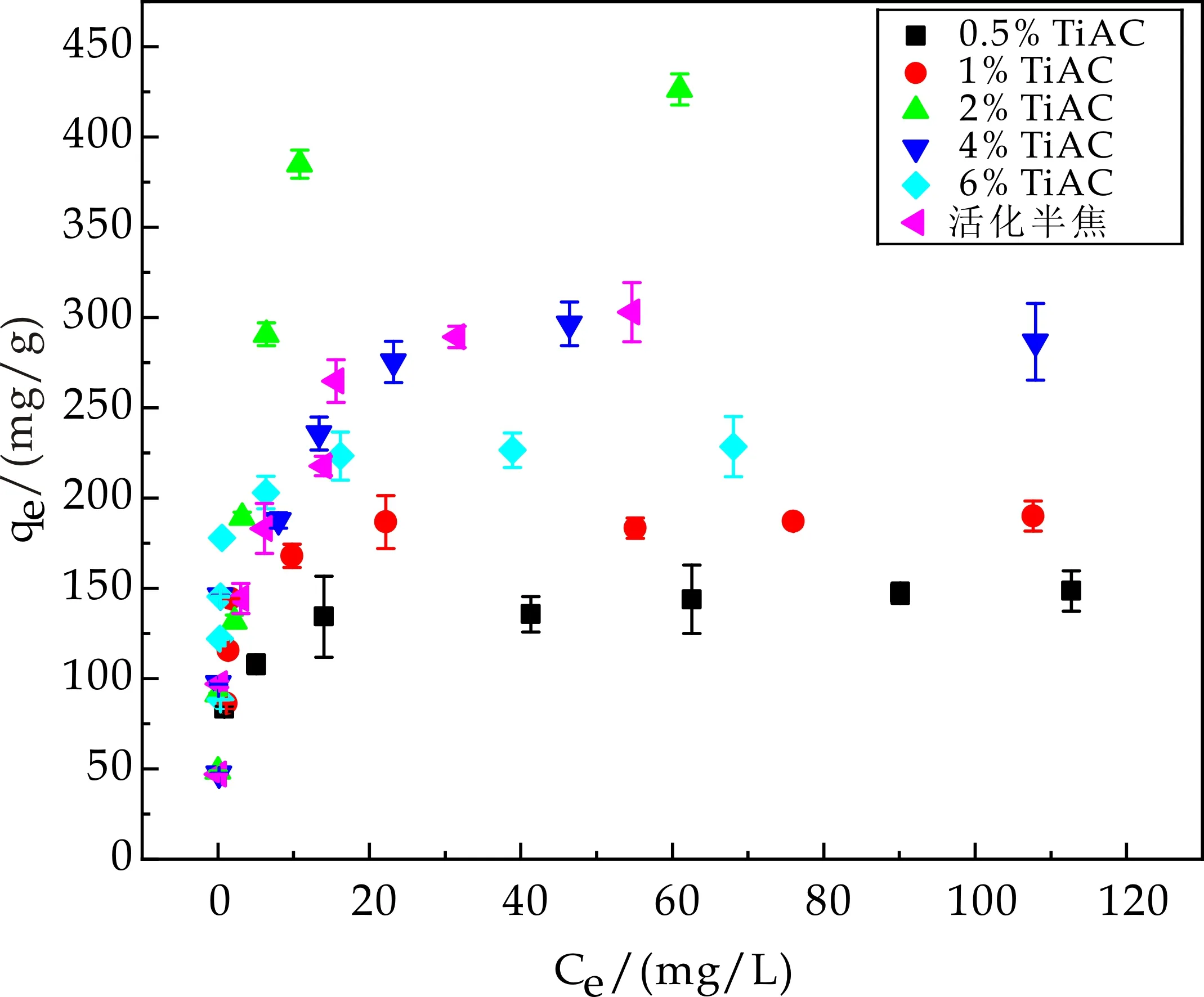
图4 不同负载量对TiAC吸附四环素的影响
为了进一步研究2%TiAC吸附机理,用Langmuir和Freundlich方程对数据进行拟合,拟合结果如表1所示.Langmuir等温吸附模型的相关系数R2高于Freundlich方程,说明吸附过程更符合Langmuir等温吸附模型,表明吸附过程主要在表面单分子层进行[23].

表1 2%TiAC吸附四环素的等温线拟合参数
2.2.2 吸附动力学实验
在25 ℃,2%TiAC对四环素溶液的吸附程度随着反应时间的变化如图5所示.在初始的10 min内,对四环素溶液的吸附速率较快,随后吸附速率减缓,吸附时间为第25 min时,吸附达到平衡,平衡吸附量为126.85 mg·g-1.由图5可知,吸附初期2%TiAC表面有大量吸附点位,因此吸附速率大;随后表面吸附点位被占,可利用吸附位点减少,因此吸附速率下降,在30~50 min趋于吸附平衡.
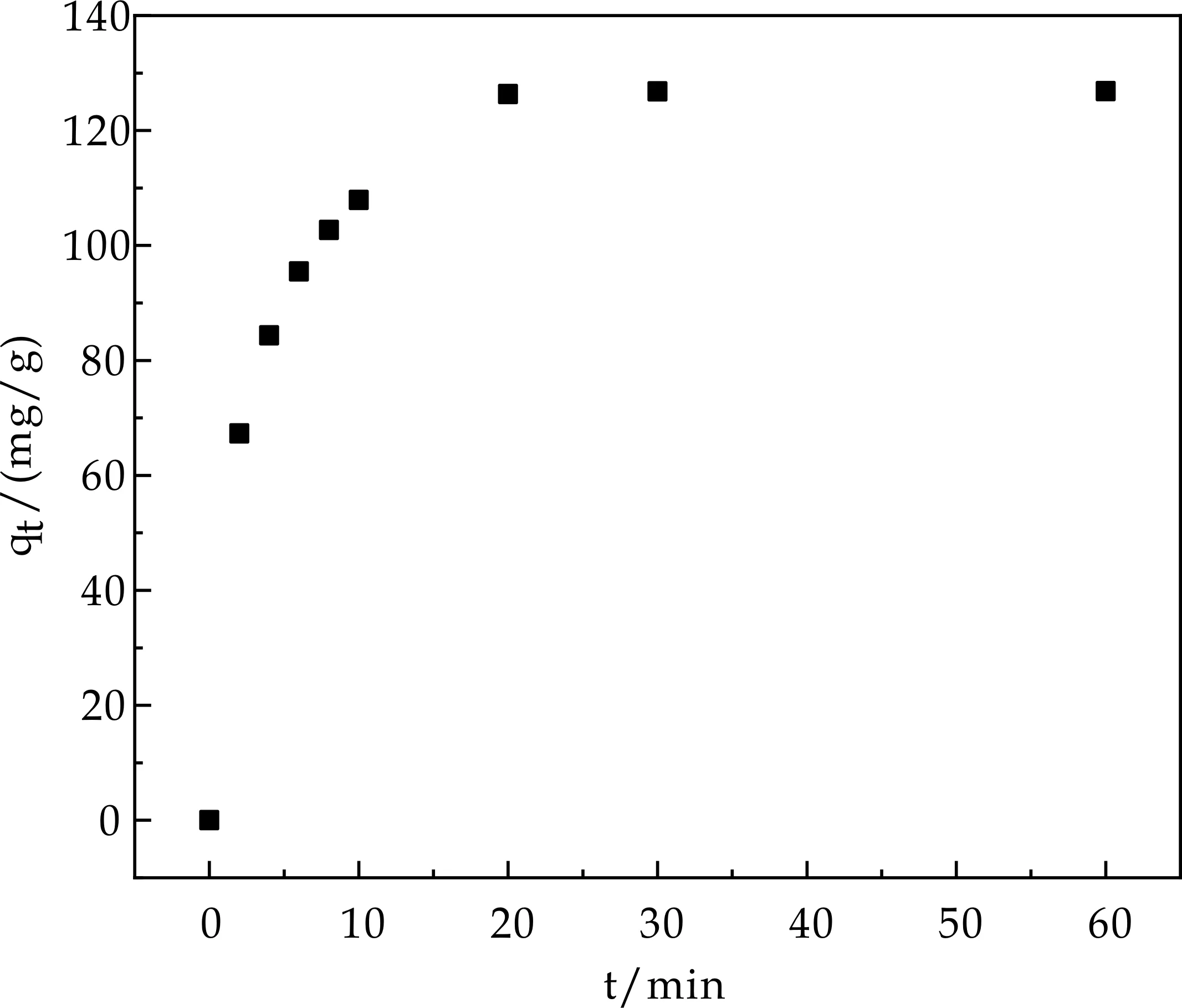
图5 吸附时间对2%TiAC吸附四环素的影响
用动力学模型进行拟合,从表2可以看出,拟二级动力学的拟合相关系数(R2)高于拟一级动力学的拟合相关系数(R2),其相关系数R2=0.999 2,说明对四环素的吸附动力学过程以化学吸附为主[24].

表2 2%TiAC吸附四环素的动力学拟合参数
2.2.3 pH对吸附的影响
pH对2%TiAC吸附水体中的四环素的影响结果如图6所示.pH从2.0上升至7.0的过程中,2%TiAC对水体中四环素的平衡吸附量增大;从7.0到10.0的过程中,2%TiAC对水体中四环素的平衡吸附量呈下降趋势.原因可能是pH值不仅影响吸附剂表面性质,也影响四环素在溶液中的存在形式.四环素分子有多个可电离的官能团,在不同的pH下离子形态不同,pH值小于3.4时,主要以阳离子存在;pH值为3.4~7.6时,主要以两性离子存在;pH值大于7.6时,主要以阴离子的形式[25].而吸附剂负载的TiO2等电位点pH(pHzpc)为6.3,pH值小于6.3时,表面主要是TiOH2+,pH大于6.3时,表面主要是TiO-,并且pH不同,表面电荷数量也不同[26].因此碱性条件下,吸附剂上TiO-和四环素溶液的阴离子存在静电斥力,酸性条件下,TiOH2+和四环素的阳离子存在静电斥力,中性条件下,则通过静电引力进行了吸附.由此可见,静电作用在吸附中有重要影响[27].

图6 pH对2%TiAC吸附四环素的影响
2.2.4 阳离子对吸附的影响
在实际废水体系中常会有多种阳离子与四环素共存,影响吸附剂吸附四环素的效果,因此本实验研究常用阳离子(Na+、K+、Ca2+)对2%TiAC吸附四环素的影响.图7为不同浓度的阳离子对2%TiAC对四环素吸附的影响.由图7可以看出,Na+、K+、Ca2+对吸附基本没有产生影响[28],说明吸附剂2%TiAC的使用范围比较广泛,受盐离子浓度影响较小,可用于高盐废水中四环素的吸附处理.

图7 阳离子对2%TiAC吸附四环素的影响
2.2.5 腐殖酸对吸附的影响
腐殖酸是自然界常见的有机质之一,广泛存在于天然水体和污废水中,其对水中有机物的吸附效果有一定的影响[29],因此本实验探究腐殖酸的存在对2%TiAC吸附四环素的影响.从图8可以看出,随着腐殖酸浓度增大,吸附量逐渐减少,说明腐殖酸的存在会抑制2%TiAC对四环素的吸附,当腐殖酸浓度为100 mg/L时,2%TiAC对四环素的吸附量下降了27.5%.这是因为腐殖酸和四环素竞争2%TiAC表面吸附点位,且腐殖酸属于大分子有机物,可能会堵塞部分表面,因而导致吸附点位减少[30].
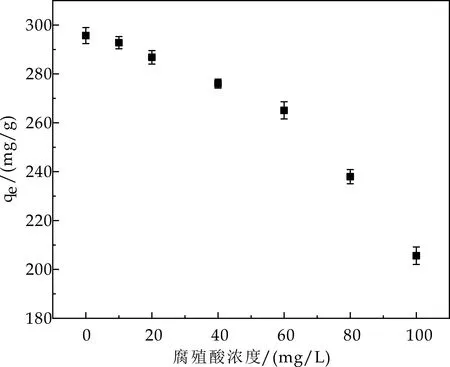
图8 腐殖酸对2%TiAC吸附四环素的影响
2.2.6 吸附剂再生性能研究
吸附四环素饱和的活化半焦和2%TiAC分别进行光解再生结果如图9所示.随着光解时间的增加,再生后吸附剂对四环素的吸附量逐渐增加,2%TiAC光解8 h后对四环素的平衡吸附量为217.25 mg·g-1,再生率达到58.6%;活化半焦光解8 h后对四环素的最大吸附量为36.69 mg·g-1,再生率为11.79%.载钛后光解再生率明显高于活化半焦.对光解再生后的2%TiAC进行XPS光谱分析,从图3(b)中看出,2%TiAC吸附四环素后C=O键含量由8.3%增到12.7%,这是由于四环素含有C=O键.而光解再生后C=O键含量降低为11.1%,证明光解后部分四环素被去除.
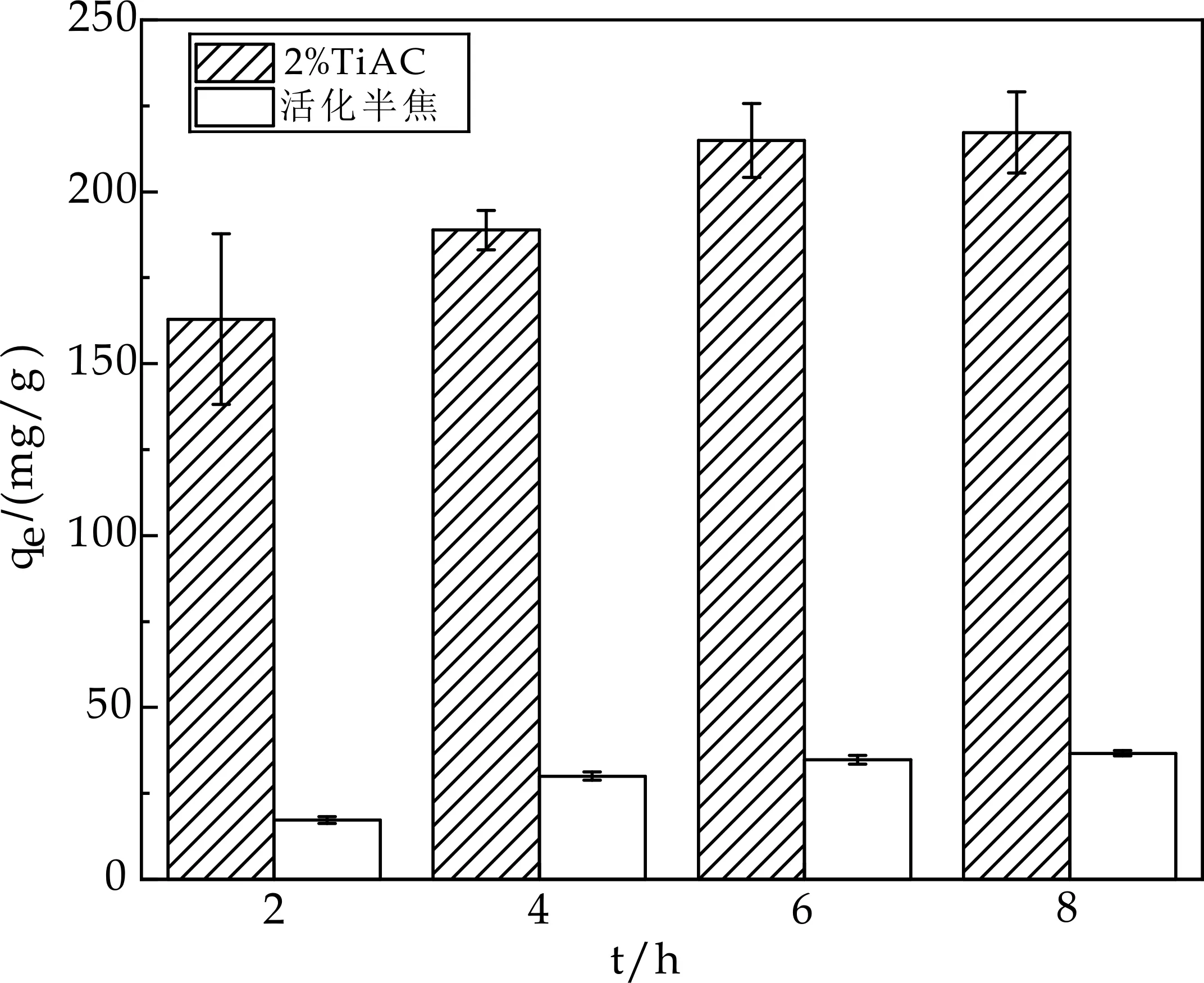
图9 吸附剂光解再生后的吸附量
3 结论
(1)以活化半焦为载体,用浸渍法制备的载钛半焦活性炭能有效吸附水中的四环素,2%TiAC的吸附效果最佳,为426.25 mg·g-1.
(2)2%TiAC吸附四环素的吸附等温线可以用Langmuir方程进行拟合,说明吸附以单层吸附为主,对四环素的吸附更符合准二级动力学模型,说明吸附过程以化学吸附为主.溶液中pH对四环素在2TiAC%上的吸附有较大影响,在25 ℃的条件下,当pH为6~7时,2%TiAC对四环素吸附量最大.水中Na+、K+、Ca2+对吸附量的影响不大.腐殖酸对2%TiAC吸附四环素有抑制作用.
(3)吸附四环素饱和的2%TiAC使用光催化脱附再生率达到58.6%,明显高于活化半焦的再生率,表明2%TiAC吸附水中四环素后可通过光催化再生.

