先天性耳聋儿童分频听性脑干反应检测和多位点耳聋基因筛查
李兴程,张金慧,陈 蓓
郑州大学第一附属医院耳鼻喉医院耳科 郑州 450052
先天性耳聋是最常见的由遗传因素导致的疾病,严重影响患儿的生长发育,是我国产前筛查和遗传预防的重要内容[1]。听性脑干反应(auditory brainstem response,ABR)是检测声刺激诱发的脑干生物电反应,用以评估客观听力及判断病变部位。听力检查目前仍然是诊断耳聋的主要依据,包括短声诱发ABR(Click-ABR)、分频ABR(Chirp-ABR)、多频听觉稳态反应(auditory steady-state response,ASSR)和纯音听阈(pure tone auditory,PTA)等。CE-Chirp是一种专门针对行波延迟设计的刺激声,该声音按低频声-中频声-高频声顺序传导至耳蜗后,整个基底膜同时震动,使更多神经纤维同步放电。研究[2]表明:Chirp音可增大反应幅值,较好反映听力异常儿童的客观听阀,提高低频听力预测准确性。但也有研究[3]提出听力筛查具有较多局限性,易遗漏轻度听力损失、迟发性/渐进性耳聋与敏感性耳聋。国内外多项大宗流行病学调查[4-5]结果显示,单核苷酸多态性(single nucleotide polymorphism,SNP)是先天性耳聋主要的基因变异类型。通过检测外周血微量全基因组DNA序列能够快速、高效、精准判断SNP。本研究对先天性耳聋儿童进行了Chirp-ABR和多位点基因筛查,分析不同基因突变类型患儿听力是否存在差异,为进一步采取合理听力干预措施提供参考。
1 对象与方法
1.1 研究对象选择2019年5月至2021年5月我院确诊的先天性耳聋患儿116例。纳入标准:年龄3~10岁,能够顺利完成各项听力测试,听阈数据可分析。患儿监护人均知情同意。排除复杂性耳聋、耳外伤者,耳内感染性疾病(如中耳炎)者,先天耳部结构或者神经发育异常者。其中男52例,女64例。
1.2 听力检查首先采用电耳镜检查外耳道、鼓膜,去除外耳道耵聍。掩蔽测试选用窄带噪声,使用“平台法”,分别进行掩蔽后进行Chirp-ABR和ASSR测试。Chirp-ABR测试在标准电磁屏蔽室内进行,本底噪声≤35 dB NHL;测试前采用右美托咪定(2 μg/kg)滴鼻麻醉,患儿进入稳定睡眠后开始检测。采用俄罗斯Neuro-Audio听觉诱发电位仪,前额发际放置记录电极,鼻根部放置地电线,两侧乳突部放置参考电极,保证极间电阻≤3 kΩ;采用ER-3A插入式耳机给声,刺激声为Chirp声,刺激类型为交替波,速率为21.1次/s,叠加次数1 024次,记录时间窗20 ms,带通滤波100~3 000 Hz,刺激强度从45 dB NHL开始,每10 dB增减,每个强度至少重复3次;以可重复记录波V的最小声强为波V阈值。Chirp-ABR 波V阈值≤30 dB NHL为正常(0 dB NHL=28.7 dB SPL)。ASSR测试准备和电极安放同Chirp-ABR,骨振器放置耳乳突处,气导较好耳使用ER-3A 插入式耳机进行掩蔽,掩蔽声为白噪声,强度为骨导给声强度上加 30 dB SPL,骨导 ASSR测试载频为 0.5、1.0、2.0和4.0 kHz,调制频率为 77、85、93和101 Hz。系统自动判定各频率阈值。
1.3 耳聋基因突变检测抽取外周静脉血2~3 mL,采用博奥生物集团有限公司的基因组DNA提取和检测试剂盒,应用微阵列芯片法检测4个常见耳聋基因的9个SNP位点,包括GJB2 (35delG、176del16、235delC和299delAT)、GJB3(C538C>T)、SLC26A4(2168A>G和IVS7-2A>G)和线粒体 12S rRNA(1494C>T和1555A>G)。按照说明书操作,依次完成PCR扩增、芯片杂交和结果判读。
1.4 听力受损程度评判标准Chirp-ABR:波V阈值≤30 dB NHL为正常听力,31~50 dB NHL为听力轻度损失,51~70 dB NHL为中度损失,≥71 dB NHL为重度损失。ASSR:≤35 dB NHL为听力正常,36~50 dB NHL为轻度损失,51~70 dB NHL为中度损失,≥71 dB NHL为重度损失。两种检查均满足时为听力某种程度损伤。
1.5 统计学处理采用SPSS 20.0进行数据分析。有和无基因突变组间性别的比较采用χ2检验,听力受损程度的比较采用精确概率法,年龄、Chirp-ABR和ASSR反应阈的比较采用秩和检验;采用Spearman相关分析Chirp-ABR和ASSR反应阈的相关性。单位点突变与双位点突变组、4个单位点突变组间性别、听力受损程度的比较采用χ2检验,年龄、Chirp-ABR和ASSR反应阈的比较采用成组设计资料的t检验或单因素方差分析。检验水准α=0.05。
2 结果
2.1 耳聋基因突变情况116例患儿中共73例(62.9%)检测到耳聋基因突变,其中GJB2基因突变21例(8例35delG、7例176del16、4例235delC、2例299delAT),GJB3突变6例,SLC26A4突变20例(11例2168A>G,9例IVS7-2A>G),线粒体12S rRNA突变15例(10例1494C>T和5例1555A>G),GJB2+SLC26A4双突变7例,GJB3+线粒体12S rRNA双突变4例。
2.2 基因突变组与无基因突变组听力情况的比较见表1。基因突变组听力受损程度重,在0.5、1.0、2.0和4.0 kHz测试频率下Chirp-ABR和ASSR反应阈均高于无基因突变组。Chirp-ABR和ASSR反应阈相关性分析结果见表2,无基因突变组测试频率在4.0 kHz以下时,Chirp-ABR和ASSR反应阈有较好的相关性;基因突变组各测试频率下Chirp-ABR和ASSR反应阈均有较好的相关性。
2.3 单位点突变与双位点突变组听力情况的比较两组性别、年龄、听力受损程度、Chirp-ABR和ASSR反应阈比较,差异均无统计学意义(P>0.05),见表3。
2.4 4个单位点突变组听力情况的比较4组性别、年龄、听力受损程度、Chirp-ABR和ASSR反应阈差异均无统计学意义(P>0.05),见表4。
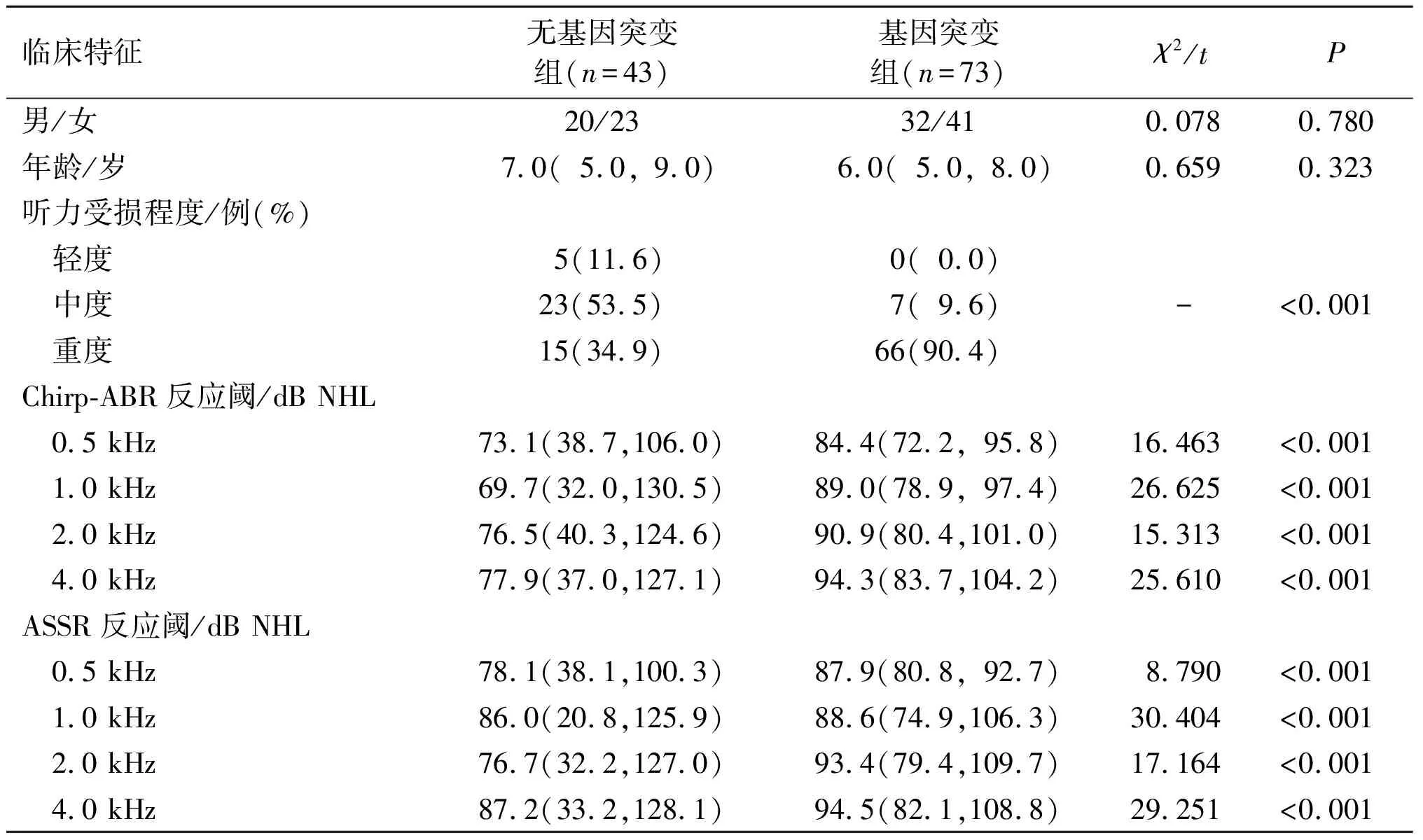
表1 基因突变组与无基因突变组听力情况比较

表2 不同测试频率下Chirp-ABR和ASSR反应阈的Spearman相关系数(P)
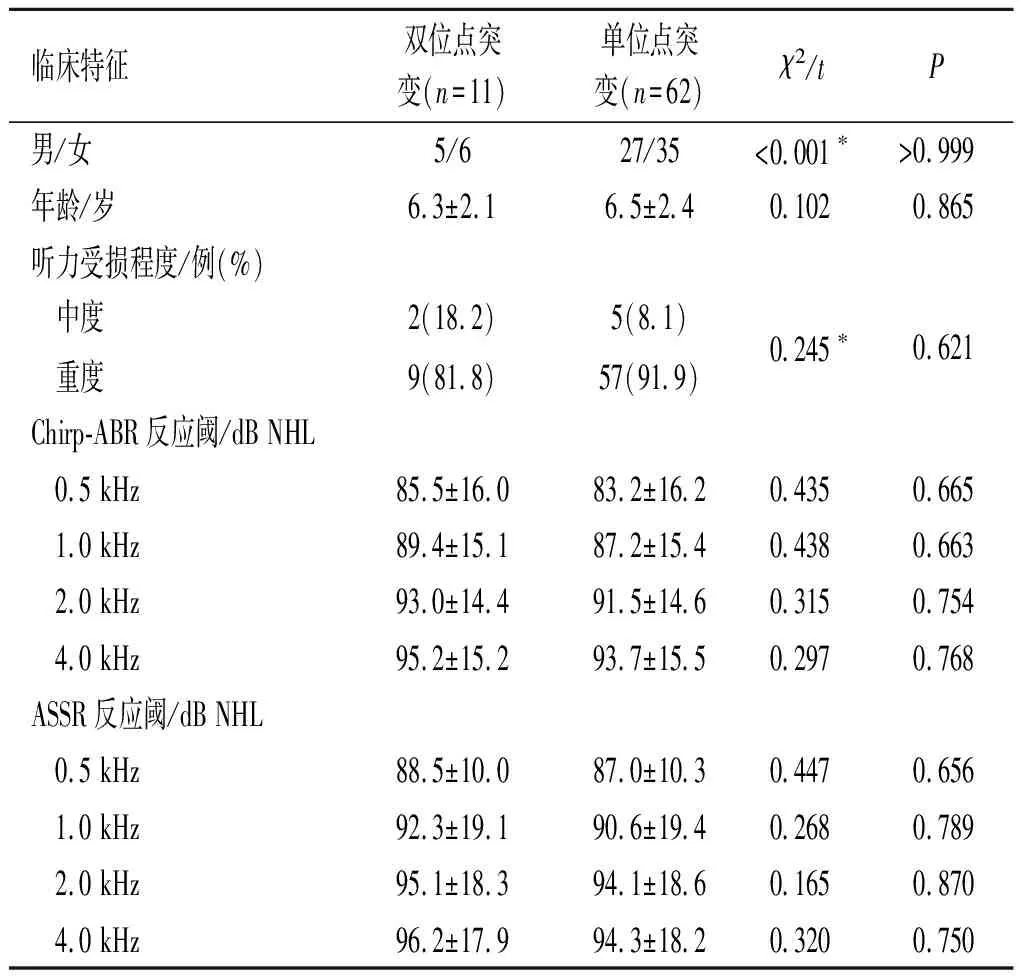
表3 单位点突变与双位点突变组听力情况比较

表4 4个单位点突变组听力情况比较
3 讨论
基因学筛查和多种听力检查是先天性耳聋的必查项目。Chirp-ABR作为目前国际上最新、最先进的ABR设备,在准确性、实用性上优于Click-ABR[2]。楼高忠等[6]指出,骨导Chirp-ABR和ASSR能够反映分频客观听力水平,弥补患者无法配合主观听力测试或主观听力结果不可靠的不足。ASSR频率特异性较好,对人工耳蜗植入候选者残余听力的评估具有重大意义[7-9]。Chirp-ABR与ASSR补充,可充分反映各个频率下的听力受损情况[10-11]。
研究[12]显示,50%~70%先天性耳聋主要由遗传因素所致。韩跃峰等[13]的研究结果显示,江淮地区128例极重度感音神经性聋患儿中,基因突变率为36.72%,其中GJB2基因突变最多见。Wen等[14]2016~2017年对我国多地区新生儿耳聋基因的筛查结果显示,东部地区新生儿耳聋基因筛查比中西部地区更广泛,4个基因(GJB2、GJB3、SLC26A4和线粒体12S rRNA)中9个变体和20个变体的组和检测被广泛使用,GJB2和SLC26A4基因突变最常见。GJB2为常染色体隐性遗传基因,其编码的Cx26 蛋白可与缝隙连接蛋白组成完整的缝隙连接通道,调控细胞间钾离子水平,维持细胞间信号转导[15]。GJB2点突变率较高(全国平均突变率为11.8%),占所有GJB2基因突变的67.7%[16]。SLC26A4 为常染色体隐性遗传基因,编码的Pendrin 蛋白参与多种离子成分的跨膜转运,与大前庭导水管综合征和内耳畸形的发生关系密切[17]。线粒体 12S rRNA为母系遗传基因,对氨基糖苷类抗菌药物有极高的敏感性;该基因突变使蛋白质合成中与氨基糖苷类药物形成结合位点,影响蛋白质的合成[18]。
本研究检测了116例先天性耳聋患儿4个耳聋基因(GJB2、GJB3、SLC26A4和线粒体12S rRNA)9个常见SNP位点,结果显示,耳聋基因突变检出率高达62.9%,其中GJB2、SLC26A4和线粒体12S rRNA突变检出率较高。进一步分析发现,基因突变组听力受损程度大于无基因突变组,在0.5、1.0、2.0和4.0 kHZ测试频率下Chirp-ABR和ASSR反应阈均高于无基因突变组;提示耳聋基因突变的患儿听力受损更严重,单纯助听器助听补偿效果欠佳时,可能需尽早行人工耳蜗植入[19]。本研究还发现,单位点突变与双位点突变患儿比较,4个单位点突变患儿比较,性别、年龄、听力受损程度、各测试频率下Chirp-ABR和ASSR反应阈差异均无统计学意义。本研究结果显示,GJB2突变患儿听力受损程度有增加的趋势,SLC26A4突变患儿低频条件下可有残余听力,线粒体12S rRNA突变患儿可有轻度聋,但这些发现并未表现出统计学意义,可能与样本量较小有关。本研究中SLC26A4突变患儿就诊前已反复多次出现波动性听力下降,在基层医院诊治效果不佳后转诊至我院,残余听力较差;而线粒体12S rRNA突变患儿无法明确是否排除了氨基糖苷类药物接触史;其他耳聋基因也并未检测。
本研究结果显示,基因突变组患儿各频率下Chirp-ABR和ASSR反应阈有较好的相关性。Chirp-ABR可以明确低频下残余听力水平,而ASSR测试的听力可能和实际听力存在一定差距,因此对于部分存在低频残余听力的患儿,尤其是SLC26A4基因突变的大前庭水管综合征患儿,Chirp-ABR检测具有重要的临床意义和必要性。
综上所述,先天性耳聋儿童GJB2、GJB3、SLC26A4和线粒体12S rRNA这4个耳聋基因的突变率较高,以单位点突变为主;有耳聋基因突变的儿童听力受损程度严重,Chirp-ABR可以较准确地反映患儿各频率客观听力。

