使用冻融单一病毒收获液冻干乙脑减毒活疫苗成品质量考察
周卫,郭红,王玖强,廖海棠,杨文杰,李俊明,周超,廖健,刘少祥
(成都生物制品研究所有限责任公司,四川省疫苗工程技术研究中心,四川成都 610023)
流行性乙型脑炎简称乙脑,又称为日本脑炎(Japanese encephalitis,JE),是由嗜神经性病毒乙脑病毒(Japanese encephalitis virus,JEV)引起的中枢神经系统急性炎症[1]。我国每年约6.8万乙脑临床病例,病死率可高达30%,另外高达50%的乙脑幸存者遗留严重的神经系统后遗症[1-3]。目前依然没有治愈乙脑的特效疗法[4],疫苗接种仍是预防乙脑最经济、最有效的手段[5]。
乙脑病毒有5种基因型,分别为G1、G2、G3、G4及G5[1]。疫苗株SA14-14-2在我国广泛使用,并认为对所有基因型均具有较好的保护效果[6-7]。乙型脑炎减毒活疫苗(乙脑活疫苗)是将SA14-14-2乙脑减毒株接种原代SPF地鼠肾细胞,收获病毒液,加入适宜的保护剂,经分装、冻干制成[8]。
有资料表明,乙脑活疫苗的免疫力与病毒滴度高低成正比[9]。目前,成都生物制品研究所有限责任公司(以下简称公司)单一病毒收获液暂存于2~8 ℃冷库,长期储存病毒滴度会逐渐下降[10]。因此滴度结果出来后,需要尽快将单一病毒收获液投入生产使用(单一效期不超过15 d),无法等所有检定结果,从而导致中间品的风险放行。因此,研究将单一病毒收获液-70 ℃冻存,以控制效价损失;待获得单一病毒收获液所有检定结果后,再27 ℃水浴解冻;使用冻融单一病毒收获液冻干成品,统计分析成品的相关质量属性是否会受到影响。
1 材料与方法
1.1 材料与试剂
乙脑活疫苗单一病毒收获液,公司病毒性疫苗一室提供。
糖溶液、明胶溶液、原倍无酚红欧式平衡盐溶液、HCl溶液和20%尿素溶液,公司病毒性疫苗一室提供;人血白蛋白,成都蓉生药业有限责任公司;BHK21细胞、MEM培养液、甲基纤维素覆盖物和质量分数为5%的结晶紫染色液,公司质量检定室。
1.2 仪器与设备
S220型pH计,梅特勒-托利多公司;OM819C型冰点渗透压仪,德国罗泽公司;FLC3120型分装机,德国博世公司;LYO-20型冻干机,上海东富龙科技股份有限公司。
1.3 冻干成品及样品采集
将单一病毒收获液冻存于-70 ℃冰柜,至少储存30 d后,于27 ℃水浴融解。按照公司常规生产方法,使用冻融单一病毒收获液配制半成品,并分装、冻干制得成品,1人份成品批号分别为T-A001~T-A006,5人份成品批号分别为T-C001~T-C006。所有成品进行病毒基础滴度、病毒热稳定性、水分、pH值及渗透压摩尔浓度等项目的检测。
1.4 病毒基础滴度检测
采用《中华人民共和国药典》(2015版)规定的BHK21细胞蚀斑法[11]122-126检测病毒滴度,将待检测液进行10倍系列稀释,至少取3个稀释度的病毒液,分别接种BHK21细胞,用蚀斑法进行滴定。
1.5 病毒热稳定性检测
将样品于37 ℃放置7 d后和病毒基础滴度样品一起进行病毒滴度检测。
1.6 水分检测
采用《中华人民共和国药典》(2015版)规定的费休氏法[11]通则65,根据碘和二氧化硫在吡啶和甲醇溶液中与水定量反应的原理测定水分。
1.7 pH值检测
采用《中华人民共和国药典》(2015版)规定的pH值测定法[11]通则35,使用酸度计进行pH值测定,水溶液的pH通常以玻璃电极为指示电极、饱和甘汞电极和银-氯化银电极为参比电极进行测定。
1.8 渗透压摩尔浓度检测
采用《中华人民共和国药典》(2015版)规定的渗透压摩尔浓度测定法[11]通则36,通常采用测量溶液的冰点下降来间接测定其渗透压摩尔浓度。
1.9 数据统计与分析
使用SPSS 24.0软件处理数据,以常规生产均值为假设中位数和检验值,对检测结果进行单样本Wilcoxon符号秩检验和单样本T检验:P<0.05为差异有统计学意义,P>0.05为差异无统计学意义。
2 结果与分析
2.1 成品病毒基础滴度、热稳定性检定结果分析
2.1.1 1 人份成品
以公司成品滴度历史数据均值6.89 lgPFU/mL为假设中位数,对6批成品滴度进行检验,P=0.463,P>0.05,表明6批成品滴度与常规生产成品滴度均值差异无统计学意义;以成品热稳定性均值6.55 lgPFU/mL为假设中位数,对6批成品热稳定性进行检验,P=0.400>0.05,表明6批成品热稳定性与常规生产成品热稳定性均值差异无统计学意义;以公司成品滴度下降历史数据均值0.34 lgPFU/mL为检验值,对6批成品滴度下降值进行检验,t=0.246,P=0.815>0.05,表明6批成品滴度下降值与常规生产成品滴度下降均值差异无统计学意义。
2.1.2 5 人份成品
以成品滴度均值6.45 lgPFU/mL为假设中位数,对6批成品滴度进行检验,P=0.753,P>0.05,表明6批成品滴度与常规生产成品滴度均值差异无统计学意义;以成品热稳定性均值6.19 lgPFU/mL为假设中位数,对6批成品热稳定性进行检验,P=0.916,P>0.05,表明6批成品热稳定性与常规生产成品热稳定性均值差异无统计学意义;以成品滴度下降均值0.26 lgPFU/mL为检验值,对6批成品滴度下降值进行检验,t=0.937,P=0.392>0.05,表明6批成品滴度下降值与常规生产成品滴度下降均值差异无统计学意义。成品病毒基础滴度、热稳定性检定结果见表1。对公司成品基础滴度和热稳定性及滴度下降值历史数据,使用SPSS 24.0软件进行正态性检验可知,常规生产中,成品基础滴度和热稳定性数据不服从正态分布,滴度下降值服从正态分布。

表1 成品病毒滴度、热稳定性结果
2.2 成品水分、pH值、渗透压摩尔浓度检定结果分析
2.2.1 1 人份成品
以公司成品水分历史数据均值1.07%为检验值,对6批成品水分进行检验,t=0.462,P=0.664(P>0.05),表明6批成品水分值与常规生产水分均值差异无统计学意义;以成品pH=8.29为检验值,对6批成品pH值进行检验,t=-1.030,P=0.350(P>0.05),表明6批成品pH值与常规生产pH均值差异无统计学意义;以成品渗透压摩尔浓度均值734 mOsm/L为检验值,对6批成品渗透压摩尔浓度进行检验,t=-1.496,P=0.195(P>0.05),表明6批成品渗透压摩尔浓度与常规生产渗透压摩尔浓度均值差异无统计学意义。
2.2.2 5 人份成品
以公司成品水分历史数据均值1.08%为检验值,对6批成品水分进行检验,t=1.599,P=0.171(P>0.05),表明6批成品水分值与常规生产水分均值差异无统计学意义;以成品pH=7.96为检验值,对6批成品pH值进行检验,t=0.750,P=0.487(P>0.05),表明6批成品pH值与常规生产pH均值差异无统计学意义;以成品渗透压摩尔浓度均值470 mOsm/L为检验值,对6批成品渗透压摩尔浓度进行检验,t=-0.369,P=0.727(P>0.05),表明6批成品渗透压摩尔浓度与常规生产渗透压摩尔浓度均值差异无统计学意义。成品水分、pH值、渗透压摩尔浓度检定结果,此三项检定结果服从正态分布,见表2。
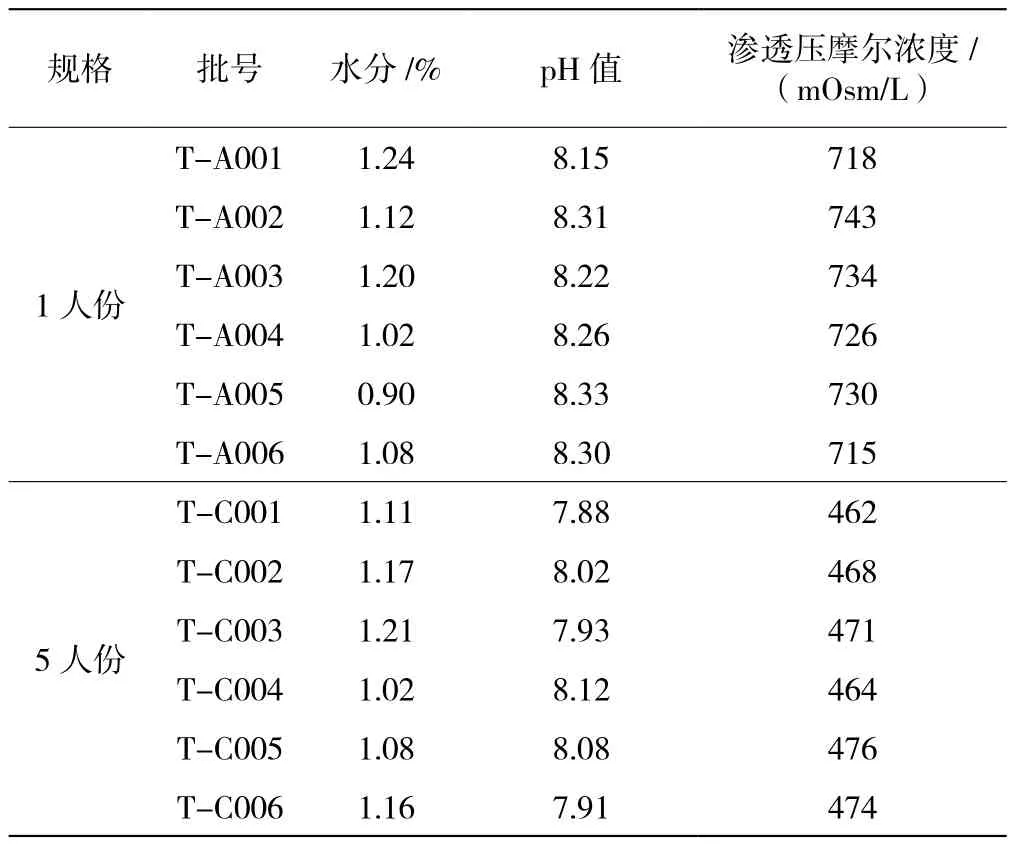
表2 成品水分、pH值、渗透压摩尔浓度结果
3 结论
与公司常规生产工艺相比,冻融生产工艺的优势在于单一病毒收获液冻存在-70 ℃条件下可长期储存,等所有检定项目结束后,再投入下一步使用。该工艺在显著延长储存时间的同时,病毒效价损失也显著减少,且无需进行中间品的风险放行,生产安排更加灵活、可控,大大降低了因生产计划变动而导致的单一病毒收获液废弃的风险。冻存需使用一次性储液袋和超低温设备,这在存储材料和设备方面增加了成本,但是冻存后延长的的存储时间,可以减少浪费以及生产废弃所需要投入的人力、物力、财力成本,综合评估,冻存的方式更有利于公司多方利益。
本文分析数据时使用的参考数据为乙脑减毒活疫苗常规均值,虽然数据差异无统计学意义,但由于试验数据样本量的限制,科室若使用冻融工艺进行生产后,仍需重新收集成品的质量属性数据,并重新制定平均值、警戒限及行动限。
从成本和适用性出发,本试验仅对可能受到冻融工艺影响的部分中间产品、成品质量属性进行了考察,已考察的质量属性数据稳定,表明冻融工艺未影响成品质量。本研究为在生产中使用冻融单一冻干成品提供了试验基础,今后还需对成品所有质量属性,尤其是安全性、长期稳定性等方面进行考察,以确定在常规生产中使用冻融单一病毒收获液冻干成品的可行性。

