预氧化强化混凝工艺处理含锰水实验研究
雷晓玲,秦颖,文永林,魏泽军
(1.重庆交通大学 河海学院,重庆 400074;2.重庆市科学技术研究院,重庆 401120)
锰在水中的存在形式有两种,一种是以Mn2+为主的游离态,无法用过滤去除,另一种是大分子形态的络合态、胶体态,可用过滤等物理手段去除大部分[1]。重庆各区县供水水源均出现不同程度的锰超标问题,且以Mn2+为主要存在形式[2]。锰的去除方法主要以氧化法为主,其除锰机理是氧化剂把Mn2+氧化成MnO2,形成可被过滤工艺有效去除的不溶性物质或胶体物质[3]。本文就氧化剂类型及其投加量、预氧化时间、pH、混凝剂投量、温度等因素对除锰效果进行探讨,以期为预氧化强化混凝工艺提供案例,为工艺参数设置提供借鉴经验。
1 实验部分
1.1 试剂与仪器
硫酸锰、次氯酸钠、高锰酸钾、过氧化氢、盐酸、氢氧化钠、硫酸铝等均为分析纯。
TA-90型可见光分光光度计;TB-2000便携式水质检测仪(浊度检测);sensION+pH1便携式pH计。
1.2 溶液配制
1.2.1 锰标准贮备液(1 g/L) 称取1.69 g硫酸锰,溶于无氨水,1 000 mL容量瓶中摇匀、定容。
1.2.2 1 mg/L Mn2+水 根据山地重庆农村水源特征,配制含锰实验用水,水质CODMn2.1 mg/L,pH 4.5~9.0,浊度<1 NTU。
1.3 实验方法
烧杯中加入水样、氧化剂1.5 mg/L,在室温下以转速200 r/min磁力搅拌10 min。加入50 mg/L的Al2(SO4)3·18H2O混凝剂,以60 r/min搅拌 2 min,再300 r/min快搅2 min,接着60 r/min搅拌10 min,自然沉降20 min。
1.4 分析方法
Mn2+采用水和废水监测分析方法(第四版)——高碘酸钾氧化光度,浊度为便携式浊度计测定,pH为便携式pH计,温度采用温度计测量。
2 结果与讨论
2.1 氧化剂及其投加量对除锰的影响
三种氧化剂及其投加量对除锰的影响,见图1。
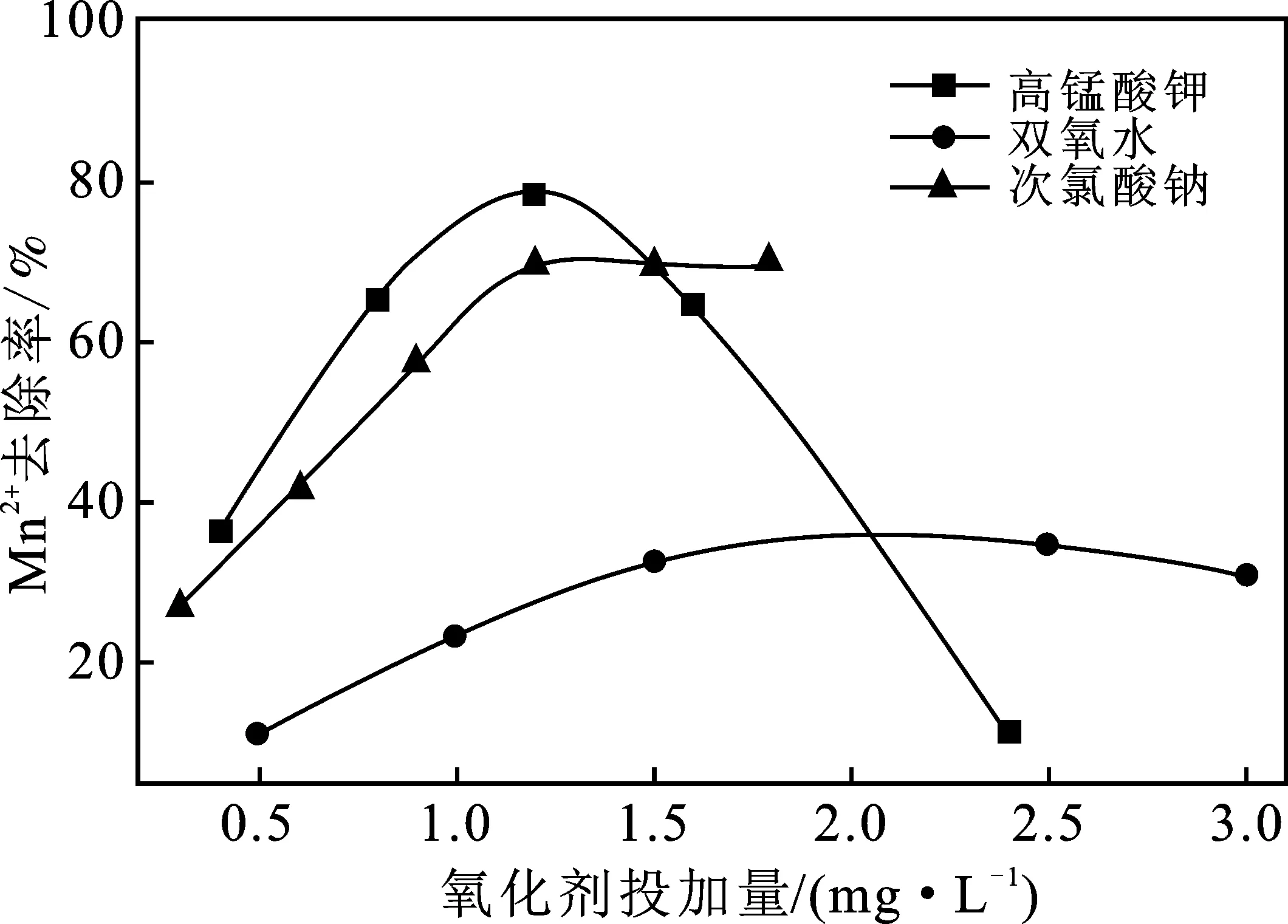
图1 氧化剂投量对Mn2+去除的影响
由图1可知,一定范围内,Mn2+去除率与氧化剂投量成正比,当达到最大去除率后继续添加氧化剂,只有次氯酸钠组基本维持不变,而高锰酸钾组大幅下降,双氧水组小幅度下降。相同条件下,高锰酸钾与次氯酸钠峰值去除率在70%~80%,较双氧水40%效果更为显著,次氯酸钠氧化剂投加量在 1.3 mg/L 时,去除率达到峰值。
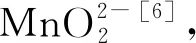
水源中初始Mn2+含量对预氧化工艺后续处理存在较大影响,氧化剂应根据其含量适量添加,以免造成锰含量回升,甚至水源二次污染。鉴于水源地锰含量处于波动状态,不好控制高锰酸钾投加量,其本身也具有管制性、价格昂贵的特点,双氧水氧化性极强、危险系数高,又不易获取,且去除水中锰具有局限性,而次氯酸钠较常见、廉价、效果好。综合考虑经济、效果因素,选择次氯酸钠为工艺的预氧化剂,最佳投加量1.3 mg/L。
2.2 pH对除锰的影响
次氯酸钠投加量1.3 mg/L,调节pH,其他参数不变,考察pH对水中Mn2+去除率的影响,结果见图2。

图2 pH对Mn2+去除的影响
由图2可知,次氯酸钠氧化法除锰时,pH对Mn2+去除率的影响很大,在一定范围内,随溶液pH的增大而增大,当pH>8.65时,去除率基本维持在88.8%左右。生活饮用水卫生标准(GB 5749—2006)Mn2+的限值为0.1 mg/L,由图2可知,pH达到7.68时,Mn2+即可达到标准限值以下,去除率最高的pH值为9.12。
当溶液呈酸性时,去除效果较差,这是因为溶液中较多的H+与OH-结合,使得化学平衡向不利于Mn2+被氧化的方向进行;溶液中OH-的浓度随pH的升高而不断增大,而OH-的存在能使化学反应朝有利方向进行,较多的Mn2+被氧化去除。
2.3 氧化时间对除锰的影响
选用上述实验的最佳条件,其他条件不变,考察氧化时间对水中Mn2+的去除影响,结果见图3。

图3 预氧化时间对Mn2+去除的影响
由图3可知,溶液中Mn2+去除率随着氧化时间的增大先增大后趋于稳定。前10 min内Mn2+去除率变化迅速,尤其氧化5 min时,Mn2+去除率高达79.4%;15 min后去除率达到峰值为89.6%,可见氧化法处理含锰水具有时间短、效率高的优点。增加氧化时间,有助于有机物包裹的Mn2+进一步溶入水中,氧化反应更为充分,继续增加氧化时间,由于生成的水合二氧化锰具有催化作用,增加了氧化剂的均相、非均相分解的时间[7],最终使去除率达到峰值后趋于稳定。选用峰值对应的氧化时间15 min为最佳实验条件进行后续实验。
2.4 预氧化温度对除锰的影响
选用上述实验的最佳条件,其他因素不变,考察预氧化温度对锰去除率的影响,结果见图4。

图4 预氧化温度对Mn2+去除的影响
由图4可知,Mn2+去除率与预氧化温度呈单调递增关系,且温度在20 ℃以下时变化较为明显,达到室温以后变化不大,维持在90%左右。温度对于去除率的影响主要原因是升温加剧了布朗运动,水中原自由能增大,依据相变原理,物质都向趋于自由能减少的方向发展,化学反应会向生成沉淀的方向发展,利于锰的去除;低温时,水的黏度大,不利于布朗运动,也不利于混凝剂水解,絮凝体生成较慢、结构松散,进而影响沉淀生成和去除效果。由于实际工艺中改变温度难度较大,成本较高,而室温条件下的去除效果已经很好,因此,氧化法除锰往往不考虑温度的影响,但在工程研究中,根据当地实际温度来考察水中Mn2+的去除效果影响是有必要的。
2.5 混凝剂投加量对除锰的影响
选用上述最佳实验条件,室温下考察混凝剂投加量对Mn2+的去除影响,结果见图5。

图5 混凝剂投加量对Mn2+去除的影响
由图5可知,锰去除率与混凝剂投加量基本呈正比关系,投加量在60 mg/L以上时,Mn2+的去除率基本稳定在90.8%左右。其原因是混凝过程产生絮凝体直接影响到过滤沉淀的效果,一方面,预氧化产生的沉淀(MnO2)颗粒细小,需要充分混凝后才能形成矾花,进而将其凝聚去除,这也导致化学反应正向移动,反应得更加彻底;另一方面,硫酸铝作为混凝剂,水解后产生Al(OH)3胶体,能吸附小颗粒的MnO2,形成较大的絮凝体,易于过滤去除。考虑到混凝剂投加量较低时,絮凝效果不明显,会影响去除效率;过多,则导致成本增加,回收不好,可能造成水源污染。因此,选用峰值对应的混凝剂投加量 60 mg/L,Mn2+的去除能达到最佳效果。
2.6 正交实验
对4个因素pH、氧化剂投加量、混凝剂投加量和预氧化时间,进行正交实验,分析影响因素主次顺序及工艺最佳工况,因素水平见表1,结果见表2。

表1 因素水平
由表2可知,次氯酸钠预氧化强化混凝工艺除Mn2+主次因素为:pH>氧化剂投加量>混凝剂投加量>预氧化时间,优水平组合为A3B3C2D1,即当原水中Mn2+浓度为1 mg/L时,室温条件下,预氧化强化混凝工艺的最佳参数为:投加1.3 mg/L氧化剂(次氯酸钠),70 mg/L的混凝剂(Al2(SO4)3·18H2O),pH调节为9.12,预氧化时间为15 min。此时Mn2+去除效果最好,去除率92.7%。

表2 正交实验结果
3 结论
(1)预氧化强化混凝工艺去除水中锰,次氯酸钠的除锰效果最好,可优先作为预氧化剂。
(2)影响Mn2+去除的因素,影响程度从大到小依次为:pH>氧化剂投加量>混凝剂投加量>预氧化时间。
(3)在9.12的pH,NaClO 1.3 mg/L,混凝剂 70 mg/L 条件下预氧化15 min,Mn2+浓度从1 mg/L降低到0.1 mg/L以下,去除率达92.7%,符合《生活饮用水卫生标准》(GB 5749—2006)要求。

