半胱氨酸对模拟体系中丙烯酰胺的抑制作用研究
刘浩东,梁文娟,周艳玲,高晴,和劲松
(云南农业大学食品科学技术学院,云南 昆明 650201)
丙烯酰胺是一种小分子水溶性物质,1994年国际癌症研究机构将丙烯酰胺列为2A类致癌物,即“人类可能致癌物”,丙烯酰胺在动物和人体中均可转化为致癌活性产物——环氧丙酰胺[1]。此外,在细胞和动物试验中,丙烯酰胺显示出神经毒性[2]和生殖发育毒性[3]。2002年,STADLER等[4]首次在油炸或焙烤的马铃薯和谷物类食品中发现了丙烯酰胺,这一发现使丙烯酰胺成为食品安全领域的研究热点。食品中丙烯酰胺的产生源自于美拉德反应[5],是由氨基酸和葡萄糖在高温下所发生的一系列复杂的化学反应,有研究通过同位素(15N)示踪证明了丙烯酰胺分子中所有碳原子均来源于天冬酰胺[6],此为目前比较公认的丙烯酰胺形成途径。
目前,国内外对如何抑制食品中丙烯酰胺的生成做了大量研究,主要集中在3个方面:食品原料的选择[7-8]、添加抑制剂[9-11]以及优化加工工艺[12-13]。本课题组前期研究发现,将生马铃薯片进行半胱氨酸(L-cysteine,Cys)和热烫预处理,油炸后,二者对马铃薯片中丙烯酰胺的形成存在协同阻断效应,协同作用下的抑制率与两者单独作用相比显著增加,但目前Cys对丙烯酰胺的抑制机理尚未完全清晰[14]。食品体系中组分复杂,在进行食品中丙烯酰胺的抑制机理研究时,会受到干扰,因此建立有代表性的葡萄糖/天冬酰胺模拟体系对研究Cys抑制丙烯酰胺的作用机制和作用位点等具有现实的意义。
1 材料与方法
1.1 材料与试剂
甲醇(色谱纯):德国Merck KGaA公司;丙烯酰胺标准品(色谱纯):德国Dr.Ehrenstorfer GmbH公司;Cys(分析纯):德国Sigma-Aldrich有限公司;尼龙注射器过滤器(0.22 μm)、水系滤膜、有机系滤膜(0.45 μm):天津津滕实验设备有限公司;3,5-二硝基水杨酸(分析纯):上海博研生物科技股份公司。
1.2 仪器与设备
高效液相色谱仪(UltiMate 3000):赛默飞世尔科技(中国)有限公司;超纯水系统(Milli-Q):美国密理博公司;超声波清洗器(KQ3200E):昆山市超声仪器有限公司;恒温油浴锅(DF-101):上海秋佐科学仪器有限公司;电热恒温鼓风干燥箱(GZX-GF101-3-BS-Ⅱ):上海跃进医疗器械有限公司;HLB SPE柱(200 mg/6 mL):江苏杰岛高新材料科技有限公司;水热合成反应釜(YZHR-25):上海岩征实验仪器有限公司;真空离心浓缩仪(miVac Quattro):英国GeneVac公司;电子天平(AR224CN):奥豪斯仪器(常州)有限公司;可见分光光度计(V-5600):上海元析仪器有限公司。
1.3 方法
1.3.1 葡萄糖/天冬酰胺模拟体系的建立
配制0.2 mol/L天冬酰胺、0.5 mol/L葡萄糖溶液。提前将水热合成反应釜置于烘箱中预热10 min,分别吸取上述天冬酰胺溶液7.0 mL(1.4 mmol)和葡萄糖溶液2.8 mL(1.4 mmol)于预热好的水热合成反应釜中,置于2 L油浴锅中以160、180、200、220℃分别加热0、5、10、15、20、25、30、35、40 min,反应结束后,冰水浴冷却至室温(18℃~25℃)备用。
1.3.2 模拟体系褐变度的测定
采用消光值法[15]测定。将反应后的产物用超纯水按体积比1∶25稀释,以超纯水为空白对照,于420 nm处测定吸光度A,10为常数,计算褐变度。
褐变度=10×A
1.3.3 葡萄糖含量的测定
1.3.3.1 3,5-二硝基水杨酸溶液配制
称取 6.3 g 3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)溶于2.0 mol/L的262 mL的氢氧化钠溶液中。称取182.0 g酒石酸钾钠于500 mL超纯水中,然后将上述两溶液混合,再加入5.0 g苯酚和5.0 g亚硫酸钠,45℃水浴,搅拌溶解后定容至1 000 mL,充分混匀,存于棕色瓶中备用。
1.3.3.2 标准曲线的制作
准确称取经105℃干燥2 h的葡萄糖0.10 g,溶解定容至100 mL,配制成1.00 mg/mL葡萄糖标准溶液,溶液现用现配。分别移取上述葡萄糖标准液0.25、0.50、0.75、1.00、1.25、1.50、1.75 mL 于试管中,用蒸馏水补至3.50 mL,分别加入2.50 mL DNS试剂,沸水浴加热8 min,取出后流水冷却,加入19.00 mL超纯水,摇匀、静置20 min,以相同条件下的空白溶液为参比溶液,在540nm波长下测定吸光度。以葡萄糖质量浓度为横坐标,吸光度为纵坐标,绘制葡萄糖溶液标准曲线。
1.3.3.3 模拟体系中葡萄糖含量的测定
取0.05 mL模拟体系反应液于试管中,用超纯水补至3.50 mL,加入2.50 mL DNS试剂,沸水浴中加热8 min,取出后用流水冷却,加入超纯水19.00 mL,摇匀、静置20 min,以相同条件下的空白溶液为参比溶液,在540 nm波长下测定吸光度。根据标准曲线计算模拟体系样品的葡萄糖含量[16]。
1.3.4 模拟体系中丙烯酰胺含量的测定
1.3.4.1 色谱条件
色谱柱为Syncronis C18色谱柱(250 mm×4.6 mm×5 μm);流动相为甲醇 ∶水=5 ∶95(体积比);流速为1 mL/min;柱温为25℃;检测波长为210 nm;进样量为10 μL。
1.3.4.2 标准曲线的制作
配制0.1 mg/mL的丙烯酰胺储备液。将储备液稀释为 0.4、1.2、2.0、2.8、3.6 μg/mL 5 个低浓度的标准溶液进样分析;将储备液稀释为 4.0、20.0、36.0、52.0、68.0、84.0 μg/mL 5个高浓度的标准溶液进样分析,以色谱峰的峰面积为纵坐标,以丙烯酰胺浓度为横坐标作标准曲线。
1.3.4.3 样品前处理
准确吸取样品2.0 mL,采用等体积的乙酸乙酯液-液萃取3次,将上层液合并至离心管,用真空离心浓缩仪浓缩至干,加入1.5 mL超纯水重溶,然后选用HLB SPE柱进行纯化,用3.0 mL甲醇活化和3.0 mL超纯水平衡,吸取上述重溶样液通过HLB SPE柱,弃去滤液,然后用3.0 mL超纯水洗脱并收集该洗脱液,过0.22 μm 滤膜,进样分析[17]。
1.3.5 Cys与丙烯酰胺在不同摩尔比下的反应
配制5 mL 0.1 mg/mL(7 nmol)丙烯酰胺溶液加入水热合成反应釜,再分别加入 0、7、42、84、420 nmol Cys,相当于丙烯酰胺摩尔质量的 0、1、6、12、60 倍,用超纯水补足体积至10 mL,分别将水热合成反应釜在180℃下加热25 min,测定丙烯酰胺含量。
1.3.6 丙烯酰胺抑制率计算
丙烯酰胺抑制率按如下公式计算。
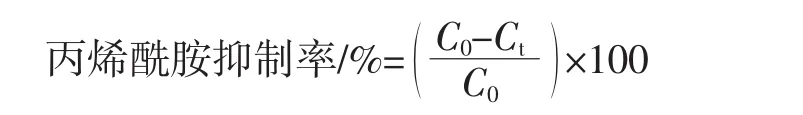
式中:C0为对照组丙烯酰胺含量,μg;Ct为Cys试验组丙烯酰胺含量,μg。
1.4 统计分析
采用Origin 2018软件绘图,应用SPSS Ver.18.0进行显著性分析,P<0.05表示差异显著,结果以平均值±标准差表示。每个样品3个平行。
2 结果与分析
2.1 加热时间和温度对模拟体系的影响
2.1.1 褐变度的变化
试验比较了不同加热温度和不同加热时间下模拟体系褐变度的变化,结果见图1。

图1 不同温度和加热时间模拟体系褐变度的变化Fig.1 The change of browning degree of the model system at different temperature and heating time
由图1可知,在160℃下,模拟体系的褐变度在40 min内随加热时间的延长而升高,未观察到峰值出现,可能需要更长的加热时间才能达到峰值;在180、200、220℃下,体系的褐变度总体上呈现出一个先升高后下降的趋势,峰值出现时间分别为35、20、15 min。说明起始温度越高,模拟体系越易于发生褐变。
美拉德反应从感官上分析首先是一个褐变的过程,引起褐变的主要原因是类黑精的生成,类黑精是美拉德反应后期由二羰基化合物、还原酮类和裂解的醛等物质,经过进一步缩合形成的复杂高分子,虽然其具体结构还不清楚,但有大量的文献表明类黑精是美拉德反应的主要产物,也是主要的呈色产物,其含量可以反映出最终反应程度[18]。本研究对不同温度设定下模拟体系发生褐变反应的研究发现,起始温度较高的条件下更易于在短时间内出现褐变并达到峰值。
2.1.2 丙烯酰胺含量的变化
不同浓度范围的丙烯酰胺标准曲线见图2。
由图2a可知,高浓度范围丙烯酰胺标准曲线方程为 Y=0.9119X+0.5663,R2=0.9996,适用于计算 4μg/mL~84 μg/mL的丙烯酰胺溶液。由图2b可知,低浓度范围丙烯酰胺标准曲线方程为Y=0.966 3X+0.013 7,R2=0.995 2,适用于计算 0.4 μg/mL~3.6 μg/mL 的丙烯酰胺溶液。

图2 丙烯酰胺标准曲线Fig.2 Standard curve for acrylamide
不同加热时间及不同加热温度对模拟体系丙烯酰胺含量影响见图3。

图3 不同温度和加热时间模拟体系丙烯酰胺含量的变化Fig.3 The change of acrylamide content in the model system at different temperature and heating time
由图3可知,加热温度越高,体系产生丙烯酰胺越早,除160℃,丙烯酰胺含量随加热时间延长均呈现出先升高后下降的趋势。在160℃下,丙烯酰胺含量随时间延长而升高,40 min时仍有上升趋势;在220℃下,10 min以内开始生成丙烯酰胺,15 min时达到最大值(720.6±24.1)μg,然后开始下降;在 200℃下,15 min以内生成丙烯酰胺,20 min时达到最大值(675.4±9.7)μg,然后开始下降;在180℃下,15 min以内生成丙烯酰胺,30 min 时达到最大值(711.6±19.5)μg,然后开始下降。温度大于或等于180℃时丙烯酰胺含量随时间延长先升高后下降,这主要是因为温度高于170℃时丙烯酰胺会发生降解[19]。
2.2 Cys对模拟体系的影响
2.2.1 Cys添加量对模拟体系中丙烯酰胺含量的影响
不同Cys添加量对模拟体系中丙烯酰胺含量的影响见图4。

图4 不同Cys添加量对模拟体系中丙烯酰胺含量的影响Fig.4 Effect of different Cys supplemental amount on the content of acrylamide in model system
由图4可知,Cys添加量越高,丙烯酰胺抑制率越高,添加量为5.0 mg时效果开始显著(P<0.05),丙烯酰胺抑制率为(19.9±3.9)%,添加量为50.0 mg时,丙烯酰胺抑制率为(72.2±5.3)%。当Cys添加量为100.0 mg时,丙烯酰胺抑制率达到(93.8±0.2)%。本研究的模拟体系中,Cys添加量越高,对模拟体系的丙烯酰胺抑制效果越好,当添加量达100.0 mg时抑制率在90%以上,Cys的分子结构中含有活泼的巯基,容易与丙烯酰胺中的双键发生加成反应,从而降低丙烯酰胺的含量[20]。
2.2.2 Cys与丙烯酰胺不同摩尔比下对丙烯酰胺抑制率的影响
不同摩尔比下Cys对丙烯酰胺抑制率的影响见图5。
由图5可知,未添加Cys的情况下丙烯酰胺含量降低,这可能是因为高温下丙烯酰胺发生消解,当Cys添加量为42 nmol时,丙烯酰胺抑制率为(89.4±4.4)%;当Cys添加量为84 nmol时,丙烯酰胺抑制率为(92.3±4.3)%;当Cys添加量为420 nmol时,丙烯酰胺抑制率为(99.2±0.5)%。与图4的结果相比,图5中Cys对丙烯酰胺的抑制率升高,这可能是由于在葡萄糖/天冬酰胺模拟体系中,Cys的分子结构中含有活泼的巯基,会与除丙烯酰胺以外的一些美拉德中间产物发生反应,比如和Amadori中间产物反应[21],和醛类等发生反应[22],导致Cys对丙烯酰胺的抑制率降低。

图5 不同摩尔比下Cys对丙烯酰胺的抑制率Fig.5 Inhibition rate of Cys to acrylamide under different molar ratios
2.2.3 Cys对模拟体系加热过程葡萄糖含量变化的影响
图6为葡萄糖含量的标准曲线(Y=0.535 2X-0.010 0,R2=0.996 0),适用于计算含有0.25 mg~1.75 mg葡萄糖的模拟体系样品。

图6 葡萄糖标准曲线Fig.6 Standard curve of glucose
有文献报道,在高温下Cys和葡萄糖会发生美拉德反应,产生吡咯噻唑盐等物质[23],为探究在加热过程中,Cys对模拟体系中葡萄糖含量变化的影响,设立添加50.0 mg Cys组和空白对照组,在180℃下加热0~40 min,测定葡萄糖含量,结果见图7。
由图7可知,在加热初期葡萄糖含量下降缓慢,到15 min时葡萄糖含量开始快速下降。试验组和空白对照组相比,葡萄糖含量下降趋势一致,差异不大,推测在模拟体系中,Cys对葡萄糖含量没有影响。

图7 Cys对模拟体系中葡萄糖含量的影响Fig.7 Effect of Cys on glucose content in model system
2.2.4 Cys对模拟体系加热过程褐变度变化的影响
为探究在加热过程中,Cys对模拟体系褐变度变化的影响,设立添加Cys(50.0 mg)的试验组和空白对照组,在180℃下加热0~40 min,测定褐变度,结果见图8。

图8 Cys对模拟体系褐变度的影响Fig.8 Effect of Cys on browning degree of model system
由图8可知,对照组的褐变度从10 min开始迅速升高,35 min达到峰值后下降,试验组随着时间延长褐变度升高缓慢,在35 min达到峰值,加入50.0 mg Cys后褐变度在峰值处降低了(62.0±1.7)%。说明Cys对模拟体系的褐变度具有显著抑制效果(P<0.05),在反应过程中抑制了类黑素的形成,美拉德反应被一定程度抑制。
2.2.5 Cys对模拟体系加热过程丙烯酰胺含量变化的影响
为探究在加热过程中,Cys对模拟体系丙烯酰胺含量变化的影响,设立添加Cys(50.0 mg)的试验组和空白对照组,在180℃下加热0~40 min,测定丙烯酰胺含量,结果如图9所示。

图9 Cys对模拟体系丙烯酰胺含量的影响Fig.9 Effect of Cys on the content of acrylamide in model system
由图9可知,空白对照组丙烯酰胺含量上升趋势明显,从10 min开始迅速上升,到30 min时达到峰值(711.6±19.5)μg,然后迅速下降;试验组丙烯酰胺含量上升趋势平缓,从15 min开始产生丙烯酰胺,30 min时达到峰值(150.6±4.0)μg,明显小于空白对照组的峰值。Cys在整个反应过程显著降低了丙烯酰胺含量(P<0.05),说明在反应体系中添加Cys,使抑制丙烯酰胺的生成具有可能性。
3 结论
本试验通过建立葡萄糖/天冬酰胺模拟体系,发现加热温度和加热时间对模拟体系的褐变度及丙烯酰胺含量具有重要影响。温度达180℃及以上时,反应在40 min内模拟体系的褐变度和丙烯酰胺含量均能达到峰值,随后降低;反应温度在160℃时,在40 min内模拟体系的褐变度和丙烯酰胺含量随时间延长而升高,推测达到峰值需要更长时间。添加Cys后,Cys含量对模拟体系中丙烯酰胺的形成具有影响,结果显示Cys添加量越高,对丙烯酰胺的抑制效果越强,当Cys添加量为100.0 mg时,丙烯酰胺的抑制率达到(93.8±0.2)%,且Cys对单一丙烯酰胺的抑制效果强于Cys对模拟体系中丙烯酰胺的抑制效果,可能是因为模拟体系中的中间产物影响了Cys的抑制作用,具体原因有待进一步研究。在180℃模拟体系中Cys添加量达50.0 mg时褐变度及丙烯酰胺含量升高趋势与对照组相比较缓慢,且峰值显著降低(P<0.05),对葡萄糖含量的变化趋势无明显影响,推测Cys能在不影响葡萄糖含量的前提下,显著降低反应体系中丙烯酰胺含量及褐变度。本研究可以为后续探究Cys对热加工食品中丙烯酰胺的抑制机理及作用位点提供一定的数据支撑。

