碳酸锂气液固三相反应结晶过程研究
殷海青,马祎明,万旭兴,董伟兵,张玉龙,吴送姑
(1 青海民族大学化学化工学院,青海 西宁 810007; 2 天津大学化工学院,天津 300072)
引 言
溶液结晶提供了一种获得适于处理、存储和销售的纯净固体化学品的实用方法,是应用最为广泛的一种工业结晶技术[1]。常用的溶液结晶方法可分为冷却结晶、蒸发结晶、反应结晶、溶析结晶和盐析结晶等[2]。其中,反应结晶由于具有过饱和度产生速率不均、反应速率与结晶速率相互影响等特点,是最难以实现过程设计与产品质量控制的过程之一[3]。气液固三相反应结晶,作为工业生产中常见的一种反应结晶类型,广泛应用于各个领域,例如CO2捕集、精细化工以及气体净化等[4]。由于其内在复杂性及其与相间传质效应的相互作用,研究者们需要考虑气泡与晶体的传质模型、反应机理、结晶动力学以及粒数衡算方程(population balance equations,PBE)等复杂的热力学和动力学模型,才能实现多产品的质量控制和过程效率优化[5]。Rigopoulos 等[6]利用计算流体力学(CFD)模拟提出了鼓泡塔内颗粒形成的动力学模型,采用欧拉-欧拉法处理气液两相,将气液吸收的渗透理论与PBE 耦合求解,用于模拟预测鼓泡塔内碳酸钙的平均粒径变化,模拟结果与实验结果有合理的一致性,并可用于颗粒产品设计。Tamura 等[7]使用三级柱式结晶器进行碳酸钙的结晶,采用PBE方程求解粒数分布,在实验和理论上研究了多级柱式结晶器的分级效应和操作参数对粒度分布的影响,得到的计算结果与实验结果一致。与标准柱式结晶器相比,多级柱式结晶器可以获得更窄的粒径分布。Lin等[8]探究了在Na5P3O10-Ca(OH)2-CO2-H2O多相体系中,气液反应结晶合成方解石纳米晶体的过程,并根据气液反应结晶的双膜理论以及晶体两步生长模型建立了三聚磷酸钠存在下纳米碳酸钙的生长机理模型。随着反应的进行,反应所处不同步骤的控速步也不同,三聚磷酸钠对于方解石晶体生长有显著影响。尽管目前已有部分研究关注到了气液固三相反应结晶,但仍旧缺乏对包含颗粒溶解-气体吸收反应-溶液结晶等多个过程全面描述与机理探究的研究报道。
碳酸锂是一种高端锂化合物,可以作为原料生产高端锂盐、金属锂等多种含锂工业产品[9]。根据上游资源不同,碳酸锂的生产分为两种:盐湖卤水提锂法与矿石提锂法。相较于矿石提锂,盐湖卤水提锂具有工艺简单、成本低等优点,因此目前世界上主要以盐湖卤水生产碳酸锂。近些年,随着各行业对高纯碳酸锂的需求日益增加,以初级Li2CO3产品为原料制取高纯Li2CO3具有很好的工业应用前景[10-11]。基于此方法制备高纯Li2CO3主要分为沉淀法[12]、电解法[13-14]、Zintl-Harder-Dauth 法[15-16]、碳化分解法[17-18]。其中,由于碳化分解法具有工艺过程简单、生产投资较低、生产不需要引入额外溶剂、产品纯度高、回收率大、钙镁等杂质含量低等显著优势,是应用最广且最具竞争力的高纯碳酸锂生产方法。碳化分解法包含两个连续的步骤,即碳酸锂碳化与碳酸氢锂热析分解,均为典型的气液固三相反应结晶过程。目前,由于碳酸锂三相反应结晶过程涉及多相间的传质过程和多动力学和热力学过程的耦合,没有针对碳酸锂碳化分解法的报道。同时,碳酸锂气液传质机理不明与过程设计和建模研究的缺乏,也导致难以进行工业理想放大应用和流程设计优化。
基于此,本研究首先针对碳酸锂碳化过程,采用缩核模型建立碳酸锂碳化过程的宏观动力学,研究了碳酸锂碳化转化率和反应速率的主要影响因素,确定碳酸锂碳化过程的控速步。利用Matlab pdepe 方法离散求解模型和方程研究了微观的反应机理,并利用Raman 正交实验监测反应过程。随后针对碳酸氢锂分析分解过程,考察反应物浓度等因素对热析过程晶体粒度分布、聚结程度等产品质量的影响。最后,搭建实验室连续结晶装置,模拟工业生产中碳酸锂热析过程严重的结垢问题,探究壁面粗糙度、过饱和度和添加晶种影响结垢现象的机制,并相应提出避免结垢现象发生的策略。通过机理研究与模型构建,以期为碳酸锂生产过程设计与工业放大提供指导。
1 实验材料和方法
1.1 材料
碳酸锂由天齐锂业股份有限公司提供,纯度大于99.5%。高纯二氧化碳购自天津市六方工业气体经销有限公司,纯度大于95%。实验过程中所用水均为实验室自制高纯水,电阻率18.2 MΩ·cm。
1.2 分析测试仪器
分析天平,X620S 型,Mettler Toledo 公司。匀速控温恒温槽,XOYS-2006 型,先欧科技有限公司。机械搅拌器,SL200C 型,优莱博仪器有限公司。鼓风干燥箱,101-2AB 型,天津泰斯特仪器有限公司。夹套式结晶器,100 ml,天津市易普佳科技有限公司。转子流量计,LZB-3WB 型,天津市景泓鑫商贸有限公司。在线拉曼,ReactRaman785 型,Mettler Toledo公司。
1.3 碳酸锂碳化反应实验
碳酸锂碳化反应实验装置见图1。首先在结晶器中加入预设质量的碳酸锂固体与去离子水,开启恒温水浴和预设推进式搅拌,恒温搅拌30 min 以上保证溶液为碳酸锂饱和悬浮液;当溶液状态稳定30 min以上后,称取结晶器质量并开始计时,同时通入二氧化碳气体开始反应。二氧化碳持续在搅拌桨下方通过管路加入。间隔5~10 min 进行结晶器称重并记录相应时间。由于反应过程碳酸锂消耗与二氧化碳等物质的量消耗,因此体系增重就可以代表反应进程及碳酸锂反应消耗速率。由于反应过程伴随着碳酸根减少与碳酸氢根生成,因此可以通过在线拉曼确定反应物与生成物浓度变化,确定反应动力学。每个测量过程重复3次,取平均值。
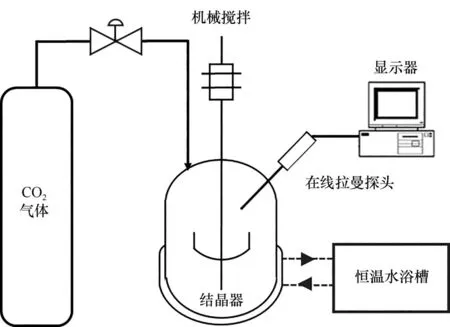
图1 基于在线拉曼的碳酸锂碳化实验装置示意图Fig.1 Schematic diagram of lithium carbonate carbonization experimental device using online Raman
1.4 碳酸锂碳化反应实验


2 实验结果与讨论
2.1 碳化反应过程研究
碳酸锂的碳化过程涉及碳酸锂固体溶解和反应生成碳酸氢锂两个步骤。其中,碳化过程的效率受溶解和反应两个步骤影响。由于碳化过程为非稳态操作,故采用单位时间的转化率和碳化实时效率,即在某一时刻的转化速率(dXs/dt),对碳化过程进行定量描述,以评估不同阶段的碳化效率。碳酸锂的碳化反应过程受到多个操作变量影响,包括初始固体悬浮密度、气速、搅拌和反应体积四个主要因素,这些因素对转化率存在不同程度的影响。为此,研究设计了19 组实验(表1),实验设计与结果详细阐述如下。
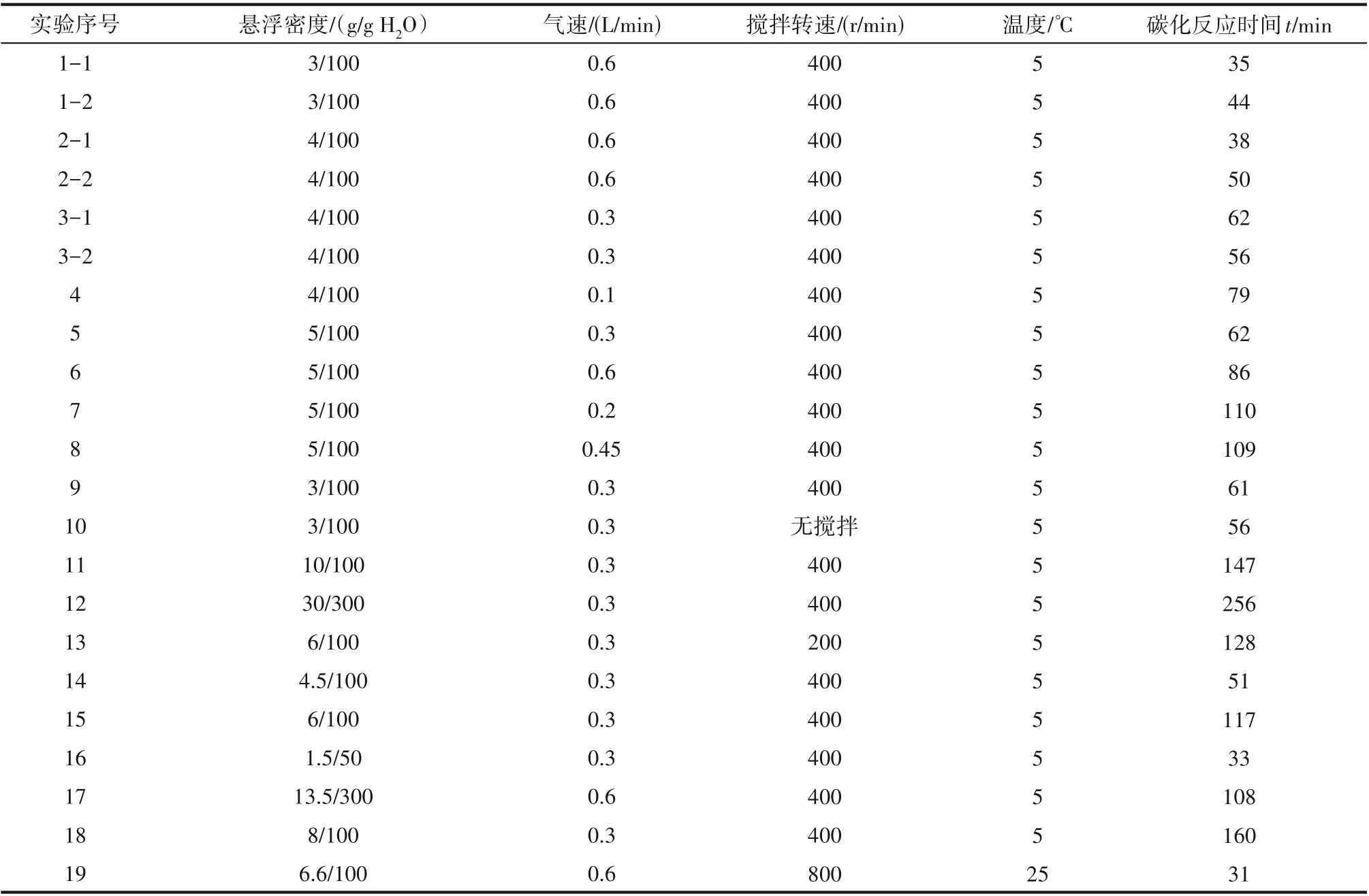
表1 碳化过程研究实验设计Table 1 Experiment design for kinetics of carbonation process
图2给出了典型碳化过程中碳酸锂的转化率随时间的变化关系。由图可知,碳酸锂碳化反应转化率随着时间的增加而增加,这一实验结果与预期相符。此外,尽管增加时间有利于反应转化率和收率,但同时也增加了能耗与操作时间,为了寻找最大转化速率,对转化率进行了再次求微分,得到了图3结果。分析发现,实时转化效率(即转化速率)随着时间增加呈现先增加后减小的趋势,并均在10 min 左右呈现最大转化效率,在10 min 后尽管具有同样的CO2气速,但是反应能力却呈现减弱趋势,表明二氧化碳的利用率降低。
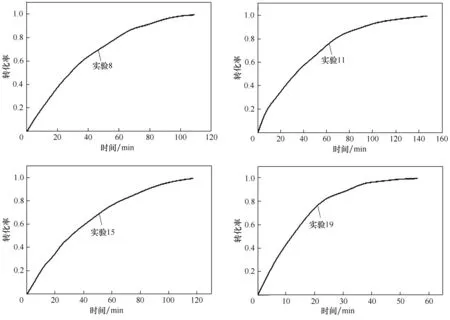
图2 实验8、11、15和19的转化率随时间的变化关系Fig.2 Conversion rate of experiment 8,11,15,and 19 against time
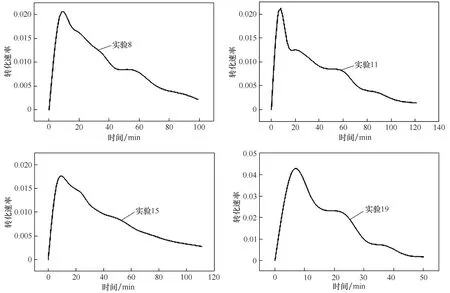
图3 实验8、11、15和19的转化速率随时间的变化关系Fig.3 Conversion rate of experiment 8,11,15,and 19 against time
综合上述分析,碳酸锂转化率随着时间增加而增加,但是转化速率呈现先增加后降低的趋势,说明碳化过程存在最佳操作转化率和时间。实验发现当转化率达到0.8 左右后,收率提高不再明显,因此,从节能降耗的角度考虑,可将碳化反应程度控制在0.8 左右,达此转化率时间占全部碳化时间的60%~70%。
2.1.1 CO2气速对反应过程的影响 以CO2气速作为实验控制变量,并定义转化率达0.8 的时间为有效碳化时间,不同条件下碳化总时间和有效碳化时间如表2 所示。分析可知,实验6 气速最大,总碳化时间最短,但其转化率达到0.8 的有效碳化时间占比最大,说明该碳化过程的CO2的相对利用率最低;相比而言,实验7 和实验8 气速较低,且两者差异不大,有效时间占比都在0.6 左右,表明在低气速下CO2气速对反应平衡影响不显著。值得注意的是,虽然低气速下碳酸锂的相对转化率和CO2利用率更高,这是由于长接触时间促进了碳化溶解,但是,低气速下需要更长的总碳化时间,因此,气速的选择需要综合考虑总碳化时间和有效碳化时间,高气速有利于降低总碳化时间,但单位时间内的碳化效率相对偏低;而低气速有利于提高单位时间的碳化效率,但同时增加了总碳化时间。
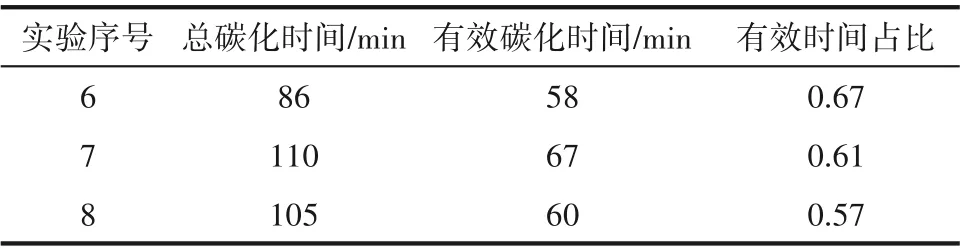
表2 实验6、7和8的总碳化时间、有效碳化时间及其时间占比Table 2 Total carbonization time,effective carbonization time and their proportion in experiment 6,7 and 8
2.1.2 初始固体悬浮密度对反应速率的影响 以0.6 L/min 为反应气速,设计实验1-2、2-2 和6,初始固体悬浮密度(质量分数)选择为3%~5%,考察不同悬浮密度对总碳化时间和有效碳化时间的影响,实验结果如表3 所示。正如预期,初始固体悬浮密度越大,总碳化时间和有效碳化时间均显著增加。此外,有效时间占比也明显增加,表明单位时间内的碳酸锂转化率和CO2气体的相对利用率均降低。这一结论也反映在不同悬浮密度的转化速率与时间演变关系上,如图4所示,高固体悬浮密度导致更低的初始反应转化速率以及更平稳的下降趋势,故而增加了有效碳化时间。
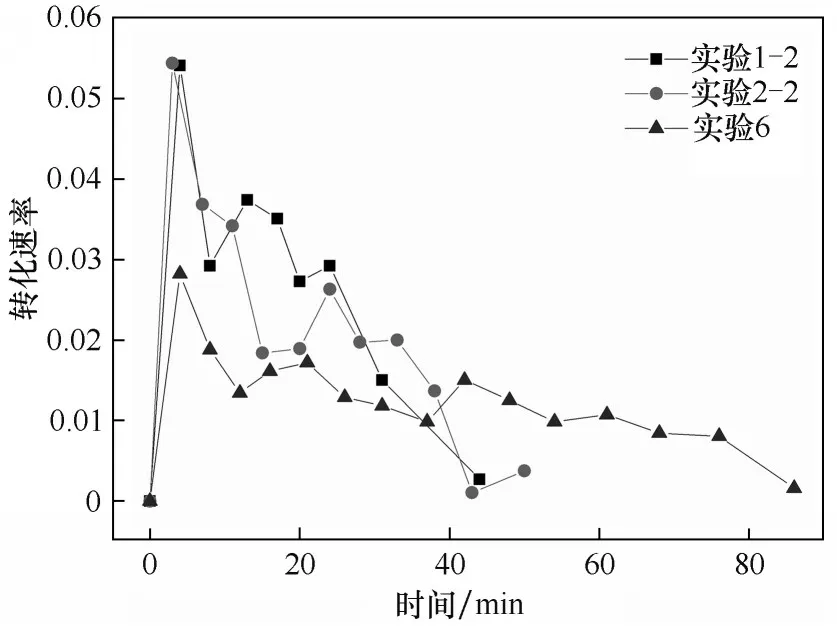
图4 实验1-2、2-2和6反应转化速率与时间的关系Fig.4 Relationship between reaction conversion rate and time in experiments 1-2,2-2 and 6
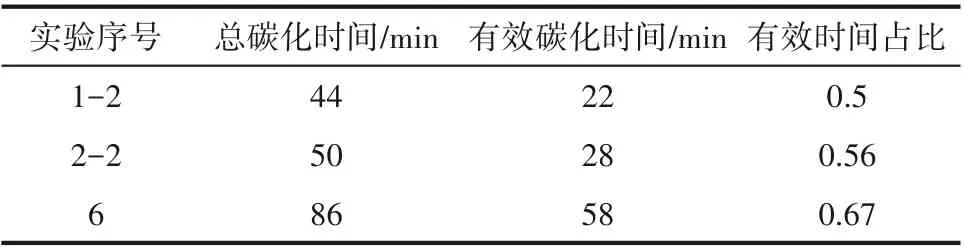
表3 实验1-2、2-2和6的总碳化时间、有效碳化时间及其时间占比Table 3 Total carbonization time,effective carbonization time and their proportion in experiment 1-2,2-2 and 6
2.1.3 反应体积对反应速率的影响 表4列出了不同反应体积下的总碳化时间和有效碳化时间。实验12 选择三倍于实验11 的反应体积,而实验17 的初始体积是实验14 的三倍,但实验14 比实验11 的初始悬浮密度低。对比不同初始反应体积,发现反应体积的增加可显著增加碳化时间,但增加幅度均小于体积增加幅度,表明反应体积对碳化时间的影响是非线性的。如图5 所示,碳化过程的转化速率曲线分析表明,小反应体积单位时间内具有更高的转化速率,而体积越大,其转化速率越低,碳化速率演变得也更加平缓。
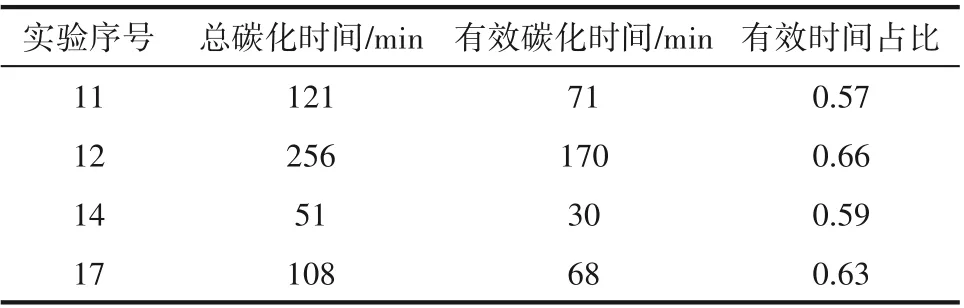
表4 实验11、12、14和17的总碳化时间、有效碳化时间及其时间占比Table 4 Total carbonization time,effective carbonization time and their proportion in experiment 11,12,14 and 17
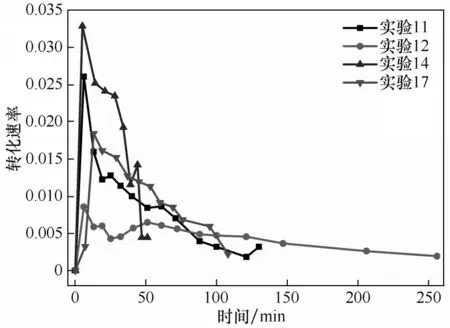
图5 实验11、12、14和17反应转化速率与时间的关系Fig.5 Relationship between reaction conversion rate and time in experiment 11,12,14 and 17
2.1.4 搅拌速率对反应速率的影响 分别考察了无搅拌(实验10)、200 r/min(实验13)和400 r/min(实验9 和15)三种条件下碳酸锂碳化情形,总碳化时间和有效碳化时间如表5所示,结果表明,搅拌不会对有效碳化时间、时间占比以及转化速率产生显著影响(图6),但似乎能够略微缩短总碳化时间。出现这一反常的结果主要是由于搅拌具有双重影响,一方面有利于气液混合,促进碳化反应;另一方面,高搅拌速率下也有利于CO2的逃逸。
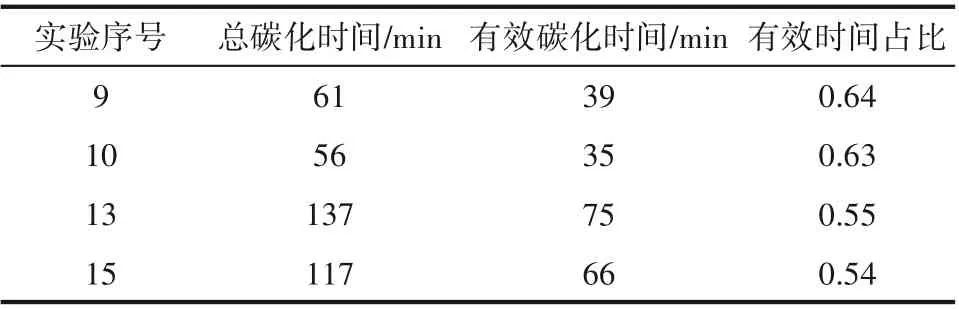
表5 实验9、10、13和15的总碳化时间、有效碳化时间及其时间占比Table 5 Total carbonization time,effective carbonization time and their proportion in experiment 9,10,13 and 15
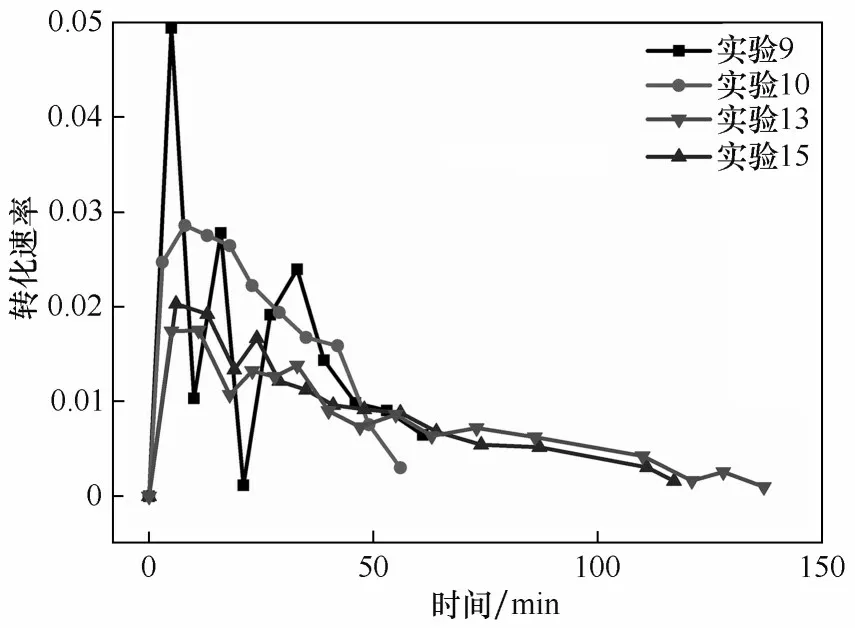
图6 实验9、10、13和15反应转化速率与时间的关系Fig.6 Relationship between reaction conversion rate and time in experiments 9,10,13 and 15
2.2 碳化反应微观机理
为了探究并深入理解碳酸锂碳化过程,基于溶解-反应-传质动力学模型,耦合固体颗粒的粒数衡算模型,建立基于气体传质控制过程的碳酸锂碳化过程模型,可表达为如下形式:
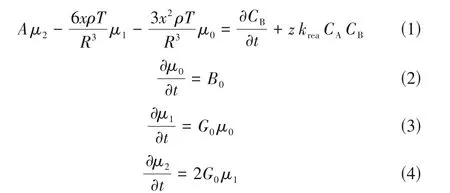
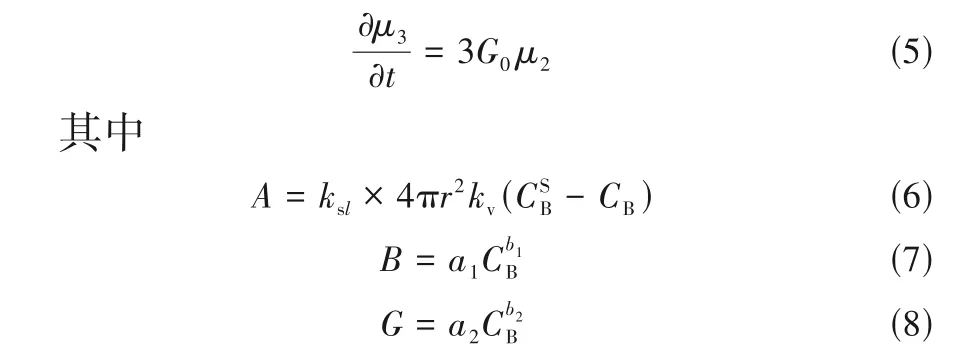
式中,μ0、μ1、μ2、μ3为PBE 离散的四阶矩量;x为边界层恒定厚度;ρ为碳酸锂固体密度;T为溶解常数;R为颗粒平均半径;z为反应计量系数;krea为反应速率常数;CA、CB分别为二氧化碳浓度与碳酸锂浓度;CSB为边界层处碳酸锂的浓度;B0与G0分别表示初始时刻的成核和生长速率;B为成核项;G为生长项;ksl为固液传质系数;kv为体积形状因子;a1、b1、a2、b2均为参数项。在以上参数确定的情况下,原问题就可化简为微分方程组进行求解,利用Matlab pdepe 函数求解,得到了单一颗粒碳酸锂在固-液界面处的浓度分布,如图7所示。
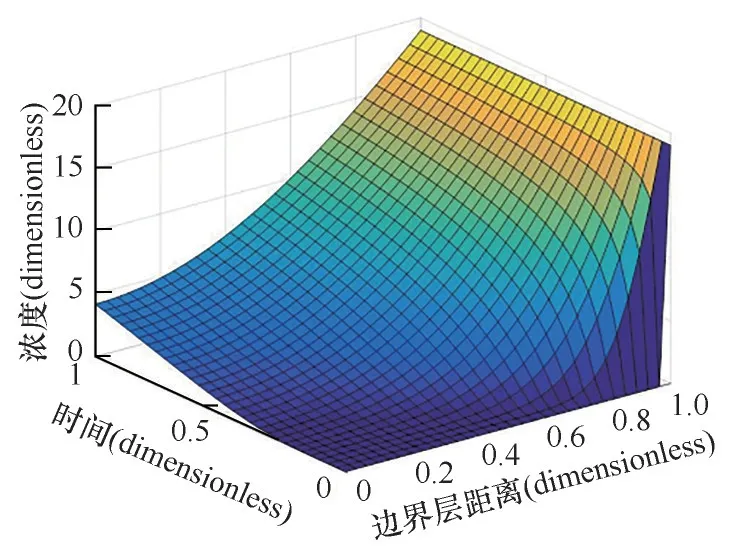
图7 碳酸锂颗粒溶液相浓度随边界层距离和时间的变化情况Fig.7 Concentration during the lithium carbonate carbonization process varied with boundary layer distance and time
基于上述模型和方程,预测了碳酸锂碳化过程中CO2-3浓度随时间的演变变化,预测结果如图8 所示。图中纵坐标表示溶液主体中碳酸锂的浓度,横坐标表示时间。从模拟结果来看,在碳化过程前期,碳酸锂颗粒进入澄清溶液主体中,由于瞬间产生浓度梯度会致使大量碳酸锂颗粒溶解直至溶液饱和,在此过程中是以溶解为主。随着时间的进行,主体浓度在前期均能维持在一个比较理想的高度水平,这是由于碳酸锂颗粒能为溶液提供大量的接触点。当过程进行至中后期时,碳酸锂颗粒并没有足够的能持续为过程提供碳酸锂的能力,此时碳酸锂浓度呈现显著下降趋势,过程下降的程度取决于气液接触情况与混合。
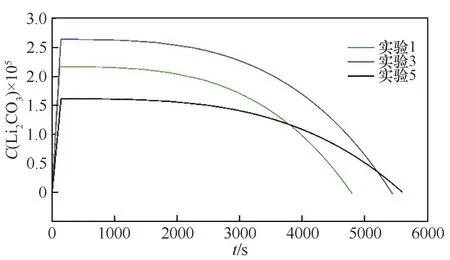
图8 基于碳化微观机理预测的碳化过程CO2-3 浓度演变Fig.8 Evolution of CO2-3 concentration in carbonization process predicted based on carbonization micro-mechanism
为了验证以上预测结果,借助过程在线拉曼分析手段,对碳化反应过程动力学进行了实验监测。据文献[19]报道,碳酸氢根离子在1015 和1365 cm-1处表现较强的—C—O对称振动吸收峰,而碳酸根离子则在1066 cm-1处显示强吸收峰。基于这两个碳酸根不同离子物种的拉曼吸收峰差异,不同实验条件下的在线拉曼实时监测如图9 所示,图中不同实验中的下降曲线代表碳酸根(1066 cm-1峰高)浓度随着碳化过程的变化趋势,而上升曲线则代表碳酸氢根(1365 cm-1峰高)浓度的不断增加。值得注意的是,图中曲线代表拉曼峰强高度的变化与浓度成正比例变化。分析发现,理论预测的模拟值与实验结果完全一致,表明本文提出的理论模型有效。

图9 在线拉曼监测实验3中碳化过程碳酸根与碳酸氢根浓度随时间的演变Fig.9 On-line Raman monitoring of the evolution of carbonate and bicarbonate concentrations over time during carbonization in experiment 3
2.3 热析反应结晶过程优化
2.3.1 热析反应结晶晶体聚结及结垢现象 热析反应结晶作为碳化热析制备高纯碳酸锂(纯度大于99.9%)晶体的最后一步,对于该结晶过程的控制程度直接决定了产品的质量。实验发现碳酸锂极容易聚结(图10),小颗粒会迅速聚结为聚集体,这可能导致溶剂包藏,降低产品纯度,实际生产中需后续工艺将聚结的碳酸锂进行气流粉碎,也会带来能耗增大等问题。Yang 等[20]在原位结晶实验中观察到从前体的聚集体到碳酸锂的伪六边形结构连续转变,量化了团聚程度。Wang 等[21]制备了星形和花朵状的碳酸锂多晶颗粒,并通过添加剂调控得到了球形颗粒。

图10 热析反应结晶过程晶体聚结现象Fig.10 Crystal coalescence in the crystallization process of pyrolysis reaction
实际生产中热析过程结垢严重,而晶垢会引起很多后续问题。表面传热能力和生产率下降,成本和保留时间上升。液体和蒸气界面蒸汽流量下降,液体夹带上升。轴周围功率要求增大,并且通过不平衡的负载导致轴承的损坏。出口大的晶块可能分离并堵塞出口,影响泵叶轮并增加管路堵塞。对输送管线泵功率的需求增大,并且可能导致完全堵塞,从而需要昂贵的清洁操作[22]。
2.3.2 不同初始浓度对产品粒度的影响 设计实验以探究操作条件对热析反应结晶过程的影响。对于LiHCO3热分解过程而言,影响反应速率的主要因素可以概括为操作温度、反应物浓度和搅拌速率。根据Arrhenius 方程,分解温度和LiHCO3浓度是表观反应速率的决定性因素。对于Li2CO3反应结晶而言,操作温度和过饱和度是晶体生长速率最重要的影响因素。
实验发现,在热分解过程中,尤其是80℃以上时,溶液里CO2-3的浓度很低,而变化非常有限,所以Li2CO3的过饱和度基本上可以由Li+单独表征。根据Li2CO3过饱和度的定义式,一个较高的锂离子浓度,必然导致Li2CO3过饱和度更早地达到超溶解度数值。同时为了获得一个较高的反应速率和产品收率,LiHCO3溶液浓度不能太低。考察了三组低中高氧化锂浓度对热析结晶晶体聚结的影响,发现晶体聚结程度和浓度成正比,如图11 所示,低浓度时多为单晶但晶体粒径分布较宽,同时综合考虑过饱和度过小时收率过低,LiHCO3初始浓度以大于18 g/L(以Li2O计)为宜。

图11 热析反应结晶过程初始浓度对晶体形貌及粒度分布影响Fig.11 Effect of initial concentration on crystal morphology and particle size distribution during pyrolysis reaction crystallization
2.3.3 分解温度对产品粒度的影响 LiHCO3溶液分解过程是一个吸热反应,所以提高操作温度,必然促进反应的进行。而且提高操作温度,也促进了溶质传质,促进了晶体的生长。因此,提高操作温度,既有利于LiHCO3的分解,也有利于Li2CO3的结晶过程。实验发现,当加热温度达到90℃时,产品收率得到显著提升,可达80%以上。
但是由于LiHCO3热分解得到的是最终产品,对晶体形貌和粒度分布提出了更高的要求,高温虽然有利于提高反应速率和产品收率,但是在高过饱和度下,晶体爆发成核,同时碳酸锂晶体本身也易于发生聚结现象。团聚的形成,使过滤过程变得十分容易,节省过滤过程的能耗。但是它也会带来不利的影响,使粒度分布变得很宽,产品的体积平均粒度变得很大,不利于产品的实际应用。
如图12所示,低浓度范围内温度对晶体形貌及粒度分布影响较大,晶体聚结程度和温度成反比,反应温度60℃时有大量聚集体产生,而80℃时所得晶体聚结程度下降同时粒度分布变窄。如图13 所示,初始浓度提升至中浓度范围时温度对晶体形貌及粒度分布的影响明显减小,不同温度下所得晶体粒径分布相类似,说明初始浓度对过饱和度进而对结晶过程的影响更大。
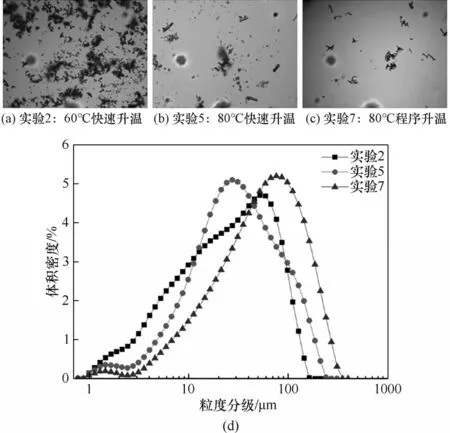
图12 低浓度热析反应结晶过程温度对晶体形貌及粒度分布影响Fig.12 Effect of temperature during crystallization of low concentration pyrolysis reaction on crystal morphology and particle size distribution
对比直接升温到某一温度和以一恒定升温速率升温到某一温度两种操作方式,没有非常明显的改善聚结效果(图13),这是因为在未达到碳酸氢锂表观分解温度前,缓慢升温对体系并不会产生很大的影响。尽管停留时间有明显增加,但无法达到优化过饱和度产生速率的目的。因此需进一步优化变温反应工艺,通过合适的升温速率曲线,调控过饱和度的产生速率,平衡晶体形貌和收率之间的矛盾。
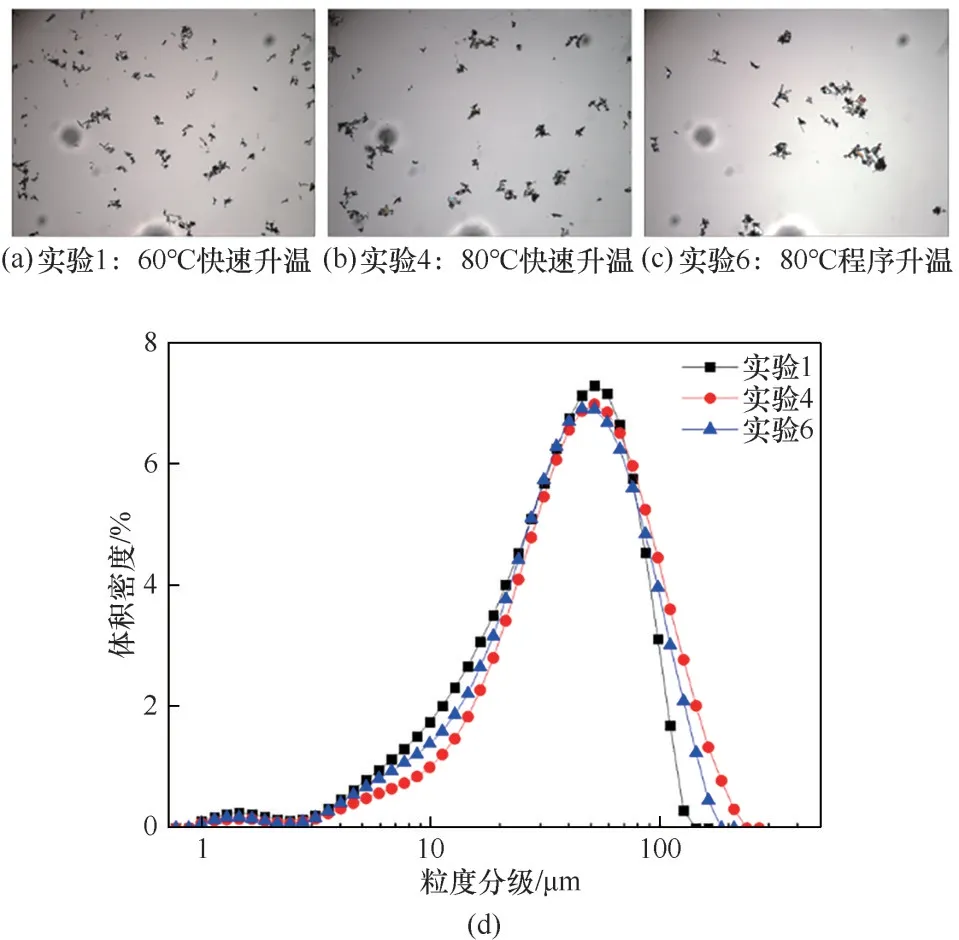
图13 中浓度热析反应结晶过程温度对晶体形貌及粒度分布影响Fig.13 Effect of temperature during crystallization of medium concentration pyrolysis reaction on crystal morphology and particle size distribution
2.3.4 搅拌速率对产品粒度的影响 如图14所示,
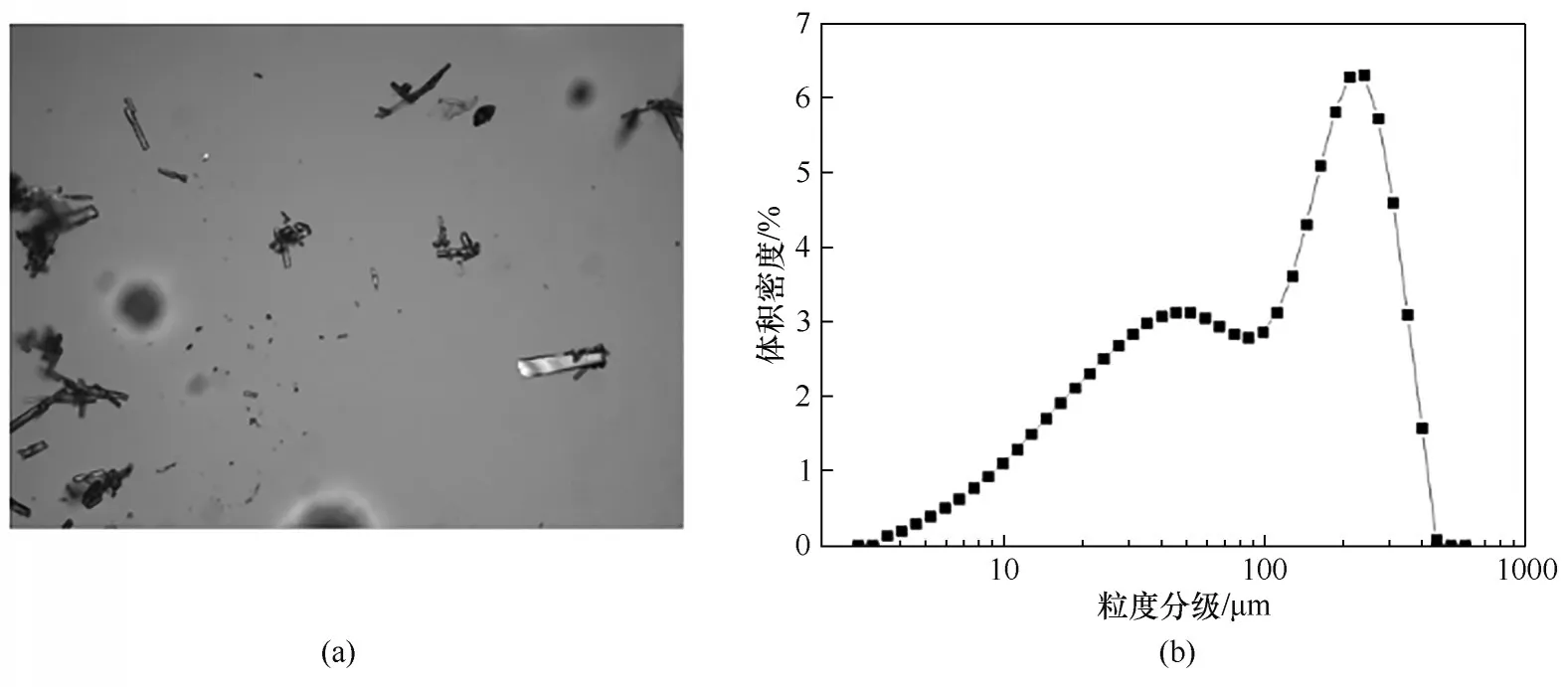
图14 热析反应结晶过程转速对晶体形貌及粒度分布影响Fig.14 Effect of rotating speed of crystallization process on crystal morphology and particle size distribution in pyrolysis reaction
对比实验3和其他组实验可以发现,由于实验3搅拌速率过低,晶体产品粒度呈双峰分布,左峰主要代表了单晶体,而右峰代表了聚结体。偏光显微镜观察结晶产品的形貌,主要由大块的聚结体和散落的棒状单晶体组成,说明了粒度分布呈双峰分布的原因。值得注意的是,在碳酸氢锂溶液热分解结晶过程中,晶体非常容易团聚,使最终结晶产品的粒度很大。碳酸锂晶体的大块聚结体,非常松软,容易压碎,所以可以通过破碎操作,比如超声粉碎、气流粉碎等,减小产品平均粒度,缩小分布范围。因此增加搅拌速率,流场湍动程度的加剧阻止了晶体间的聚结,同时也会加剧晶体间以及它们与搅拌桨和结晶器之间的碰撞,从而促进了磨损成核尤其是表面成核的产生,这在2.3.5 节对反应时间的考察中有所体现。所以搅拌程度应保持在适当的水平,既能够达到良好的混合状态,又能够避免过于激烈的搅拌,产生大量细碎晶体。
在实验室体系下,考察溶液流动状态的影响,包括搅拌形式(锚式、推进式搅拌)和搅拌速率,同时反应产物二氧化碳气泡的扩散也会不可避免地对流场及晶体表面产生一定的影响[23]。通过换用不同形式搅拌桨和增加转速,可以在一定程度上减少大块晶体团聚的产生,但流场剪切无法完全避免聚结的发生,获得单分散的棒状晶体。
2.3.5 反应时间对产品粒度的影响 通过对相同条件不同反应时间晶体产品的分析,可以发现随着反应时间的延长,晶体平均粒径并不是一直增长,如图15所示,低中浓度反应结晶过程都呈先减小后变大的趋势,结合如图16 中对应变异系数CV 值的变化,可以得出结论:结晶过程中由于二次成核出现了大量小颗粒,从而导致晶体平均粒径减小,变异系数增大,晶体粒度分布不均,后基于晶体生长或聚结,小颗粒粒径变大。其中低浓度范围时这一变化趋势更为剧烈,说明不是由于过饱和度大而引起的爆发成核,而是在流场中破碎、磨损、接触碰撞等形成的细小晶体[24]。同时中浓度范围时能提供更大的过饱和度用于生长,可以减轻一部分由二次成核带来的影响。

图15 热析反应结晶时间对晶体平均粒径的影响Fig.15 Effect of crystallization time on crystal average particle size in pyrolysis reaction
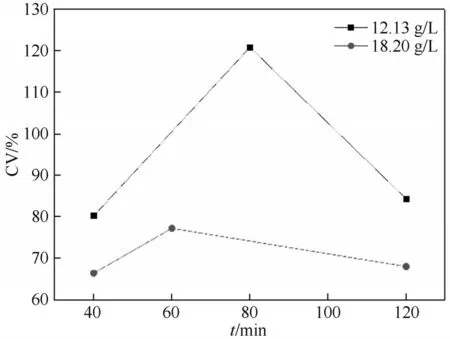
图16 热析反应结晶时间对晶体变异系数的影响Fig.16 Effect of crystallization time on coefficient of variation in pyrolysis reaction
2.3.6 晶种对产品粒度的影响 热析过程出晶时刻取样观察晶体形成的孪晶(图17)。一旦这种聚集体形成,则后续无法通过过程控制使其解除聚结,只会在此基础上进行生长,形貌向球形聚结靠近。当然在过饱和溶液中,粒子碰撞和黏附,若有足够的过饱和度产生接口固化作用力,抵抗流体的剪应力就会产生聚结。但是基于目前的实验结果,碳酸锂晶体的聚结不能简单通过增大流体剪应力解决。

图17 热析反应结晶过程晶种对晶体形貌的影响(加6%晶种)Fig.17 Effect of seed on crystal morphology during pyrolysis reaction crystallization(adding 6%crystal seed)
由热析产品(包括单体和聚集体)筛分得到的晶种,存在粒度和形貌的矛盾,形貌好的晶体粒径较小,碳酸锂颗粒“长不大”,即大颗粒都是聚结形成的。控制过饱和度使得出晶时不聚结,或加入形貌好的晶种分散后不聚结,反应结晶一段时间后发生聚结。说明聚结现象可能是碳酸锂晶体表面二维成核生长,导致交叉生长的发生从而引起的[25],这种聚结可能较难通过加入晶种的方式解决。从图17可以确认,在大晶体表面依附着许多较小晶体,这些小晶体是在大晶体表面发生二次成核而逐渐长大的,并与母体颗粒紧密相连。碳酸锂非常容易发生放射型生长,即以一个晶核为起点,向多个方向进行生长[26]。放射型生长的结果是以一个晶核为起点,晶体生长呈星状,而星状晶体某些位置由于成核等因素会再次成为放射型生长的起点,这样碳酸锂晶体彼此搭接,互相交织,易发生聚结。
2.3.7 超声对产品粒度的影响 超声对于消除碳酸锂晶体的聚结有较好的作用,不仅能通过破碎获得形貌良好的晶种,应用在结晶过程中同样可行。由于空化作用,超声加速了Li2CO3的成核过程并提高了锂的回收率[27]。分别通过快速升温结晶、程序升温结晶以及超声结晶三种方法研究晶体形貌。快速结晶与程序结晶聚结现象明显,并且在结晶器壁与气液相界面均有严重结垢现象产生。而应用超声结晶并在一定程度上控制升温速率后,得到的晶体呈长棒状且分散性良好,粒度均匀,Li2CO3晶体完整且无破碎聚结晶,显微镜照片见图18。

图18 热析反应结晶过程中超声对晶体形态的影响Fig.18 Effect of ultrasound on crystal morphology during thermolysis reaction crystallization
2.4 碳酸锂结垢机理与控制策略
在实验室重复碳酸锂连续反应热析过程并未发现明显的器壁结垢现象,这与实际生产中严重结垢的情况不符,分析差异主要由以下几点导致。
(1)生产中结晶器内各项条件为稳态或小范围周期波动的连续结晶,过饱和度持续恒定,实验室小试过饱和度能达到水平较高,但伴随着成核和生长,过饱和度持续大幅度波动;
(2)生产中的单个结晶器内温度跨度较小,同时生产中升温速度慢,小试升温速度快;
(3)由于实验室小试体系较小,因此传质更均匀;
(4)实验室小试的加热方式为夹套换热,而生产中是以蒸汽加热导致壁面温差大;
(5)实验室小试采用的结晶器壁面与工业生产不同。
因此,通过在实验室条件下模拟生产,确定异相成核是导致工业级碳酸锂连续反应结晶过程结垢的关键因素。一般而言,结晶过程需要在介稳区中操作以避免过量异相成核,这是由于过饱和度高于超溶解度会导致大量成核,产生许多细晶影响后续的过滤操作,过饱和度太低则会使晶体生长速率和生产效率低下。为了获得制备碳酸锂的最佳工艺条件,研究该反应系统的介稳区性质也是非常必要的。
如图19所示,碳酸锂超溶解度随着升温速率的增加而增加。这是因为溶液产生过饱和度后,成核并不马上发生,而是需要经历一个所谓的诱导期,在这段滞后的时间内,较高的升温速率,会使体系上升到更高的温度,这就导致碳酸锂超溶解度的升高。在冷却结晶中,同样有类似的现象,超溶解度随着冷却速率的升高而升高。本质上,无论反应结晶中的升温速率还是冷却结晶中的冷却速率,都决定了过饱和度的增长速率。由于成核的相对滞后,对某一物质而言,其超溶解度随着过饱和度增长速率的升高而升高。碳酸锂的超溶解度与溶解度具有相同的变化趋势,随温度的升高而降低。随着温度升高,碳酸锂的介稳区变窄,因为高温能加速碳酸氢锂分解反应,同时促进离子运动和碰撞,从而促进溶质传递过程,有利于晶核的生成。
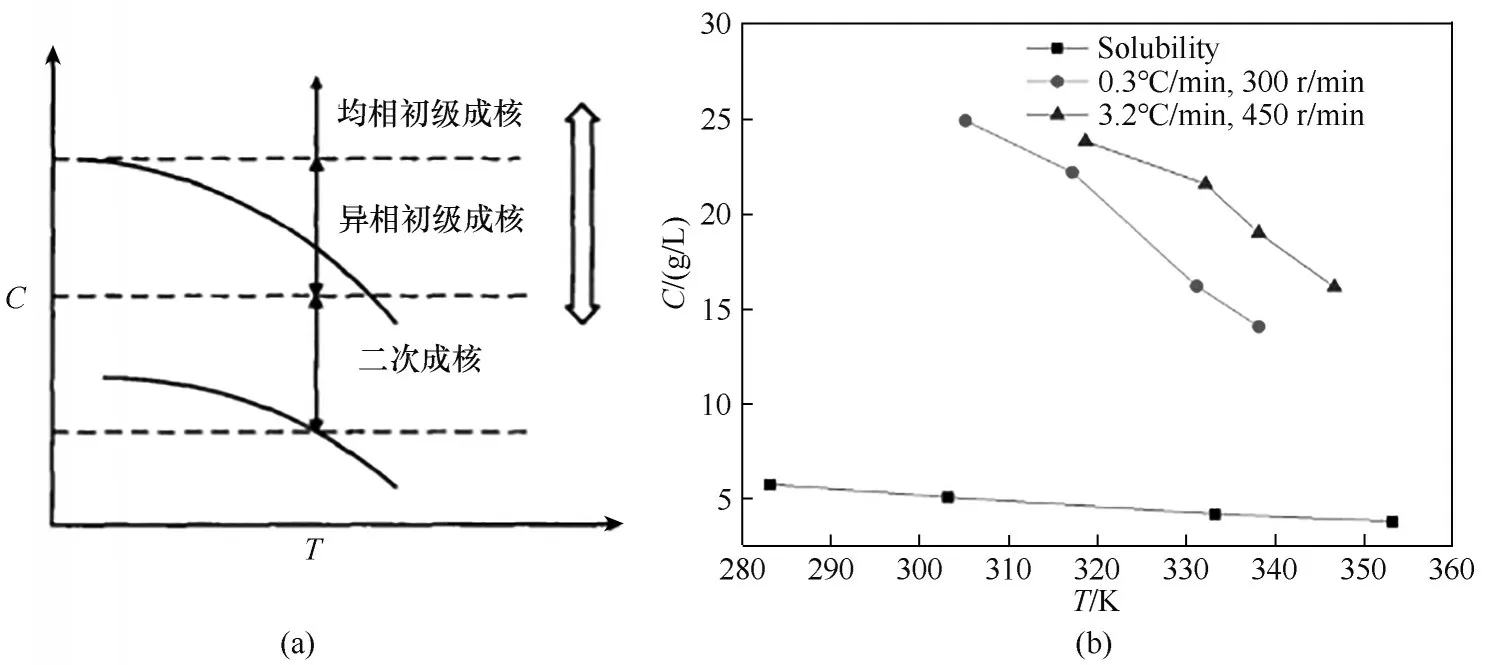
图19 热析反应结晶介稳区内的不同成核方式(a)[28];实测碳酸锂热析结晶的介稳区(b)Fig.19 Different nucleation modes in the metastable zone of the thermolysis reaction crystallization (a);Measured metastable zone of lithium carbonate thermolysis crystallization(b)
综上推测碳酸锂结垢机理为:结晶器器壁异相成核,随后器壁上的晶核交叉生长,不断扩展成片,同时也会产生新的晶核,从而形成紧实的垢。因此相应减少结垢可以从选用表面光滑不相容的材料、介稳区成核控制和添加晶种三个角度出发,设计实验见表6。
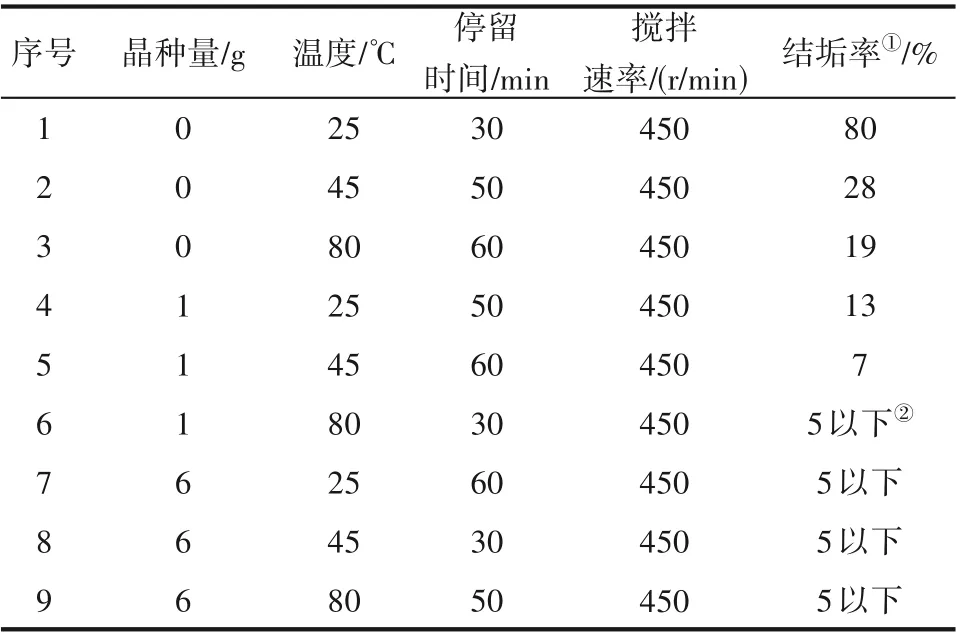
表6 晶种、停留时间和搅拌对结晶器结垢的影响Table 6 Effects of seed,residence time and agitation on fouling in crystallizer
反应温度与停留时间、晶种量综合影响了结晶器内的过饱和度,适宜的停留时间与反应温度组合可以使过饱和度上升到均相成核域,大量的均相成核降低了异相成核的比例,同时成核消耗了过饱和度,减少了器壁上晶核的生长(图20)。对比表6中结垢率发现,温度是导致结垢现象的主要因素,低温时过饱和度小,在不添加晶种的情况下,均相成核动力不足难以突破,易在容器壁面发生异相成核,会发生严重的结垢现象,但在添加少量晶种的情况下粘壁情况的发生大大减少。而添加大量的晶种可以使过饱和度无法过快积累到较高水平,过饱和度控制在二次成核域以下[29-30],保证过饱和度被溶液中悬浮的晶体生长所消耗,从而有效避免结垢现象的发生。
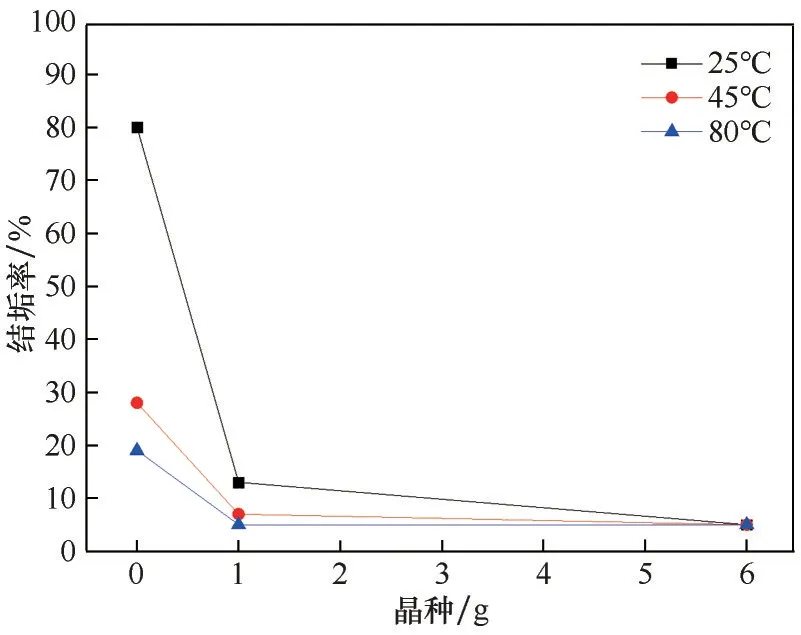
图20 结垢率与晶种量、温度的关系Fig.20 Relationship between scaling rate,seed quantity and temperature
3 结 论
本文以碳酸锂碳化热析反应结晶过程为研究体系,分别从理论和实验层面进行考察并兼顾数值模拟。基于碳化热析的机理研究,运用实验和模拟相结合的方法综合系统地研究了结晶全过程,并对过程优化和产品质量提升提出改进方案,得到结论如下。
(1)通过研究碳酸锂碳化过程并从节能降耗的角度考虑,可将碳化反应程度控制在0.8 左右,达此转化率时间占全部碳化时间的60%~70%。设计实验研究操作变量对碳酸锂碳化反应过程的影响,包括气速、初始固体悬浮密度、反应体积和搅拌四个主要因素。高气速有利于缩短总碳化时间,但单位时间内的碳化效率相对偏低。高固体悬浮密度导致更低的初始反应转化速率及更平稳的下降趋势,故增加有效碳化时间。体积越大转化速率越低,碳化速率演变得更平缓。而搅拌无显著影响。
(2) 确定碳化过程的控速步为气体传质,利用Matlab pdepe 方法进行离散求解,探讨反应微观机理。基于上述模型和方程,预测了三种不同条件碳化过程中C浓度随时间的演变。开展在线拉曼正交实验,借助过程在线分析手段监测反应过程动力学,验证了理论预测结果,表明本文提出的理论模型的有效性。
(3)实验发现碳酸锂聚结现象,从LiHCO3浓度、温度、搅拌以及晶种出发对热析过程进行工艺优化。晶体聚结程度和浓度成正比,综合考虑过饱和度过小时收率低,可确定适宜的LiHCO3初始浓度。低浓度范围晶体聚结程度和温度成反比,而中浓度范围时温度对晶体形貌及粒度分布的影响明显减小。搅拌速率过小则晶体产品粒度分布呈双峰分布,增大搅拌速率无法完全避免聚结的发生,结晶过程发生二次成核,导致晶体平均粒径减小,变异系数增大。引入外场超声结晶可以获得形貌良好的碳酸锂晶体。
(4)工业生产中热析过程结垢严重,设计实验确定结垢现象的产生所需要素包括粗糙的结晶壁面,持续的过饱和度和二次成核。结合碳酸锂的聚结行为,推测结垢机理为结晶器壁面异相成核,晶核放射性交叉生长,扩展成片形成紧实的垢。相应提出策略为选用表面光滑的材料、介稳区成核控制和添加晶种,将过饱和度控制在二次成核域以下,使得过饱和度被溶液中悬浮的晶体生长所消耗,均通过实验验证了可有效避免结垢现象的发生。

