碳基固体酸催化纤维素热解制备左旋葡聚糖和左旋葡萄糖酮
徐飞翔,蒋丽群,郑安庆,赵增立
(1 中国科学院可再生能源重点实验室,广东 省新能源和可再生能源研究开发与应用重点实验室,中国 科学院广州能源研究所,广东 广州 510640; 2 中国科学院大学,北京 100049; 3 广东省科学院生物与医学工程研究所,广东 广州 510316)
引 言
近年来,生物质作为一种可再生新能源备受国内外学者关注,快速热解是一种高效利用生物质的技术,可在无氧的环境下将生物质转化为生物油[1-3]。生物油具有广泛的应用潜力,含有多种化合物(酸、酮、醛、酯、醇、呋喃、脱水糖、酚等),可以用作液体燃料或者作为平台化合物提取有价值的化学品[4-5]。左旋葡聚糖和左旋葡萄糖酮是生物油中的重要化合物。左旋葡聚糖分子结构中C1和C6间含有一个内缩醛环,这使得它成为合成立体化合物的一个重要单体,可以作为手性合成子合成寡糖、高聚物、树脂、药物及相关产品,具有较高的市场价值(约100 美元/克)[6-7]。微生物可以直接或间接地以左旋葡聚糖为底物,生产衣康酸、柠檬酸及乙醇等,其发酵效果可以与葡萄糖媲美[8]。左旋葡萄糖酮是一种具有独特结构(含有两个手性分子以及α,β-不饱和酮的醛官能团)的脱水糖。左旋葡萄糖酮可用于合成治疗癌症、免疫疾病和心脏病的多种药物,具有极高的市场价值(约1000 美元/克)[9-10]。然而,生物油的组分繁杂,各成分的产率及含量低,导致后续分离提纯的成本高,极大地限制了快速热解技术的发展。
催化热解可以通过选择性破坏分子内化学键和定向调控生物质热解产物分布来提高目标产物的产率[11-15]。目前很多研究采用磷酸、硫酸、固体酸、离子液体催化纤维素转化为左旋葡萄糖酮,但对催化热解制取左旋葡聚糖的研究较少[16-20]。相关文献表明在较高的温度下(650℃),添加适量的弱碱(NH4OH),可以促进纤维素热解转化为左旋葡聚糖[21]。稀酸可以在较低温度下(300℃)促进左旋葡聚糖的生成,但强酸会促进左旋葡聚糖脱水,生成左旋葡萄糖酮[22]。此外,液体酸催化前的酸浸渍处理不仅步骤烦琐,处理过程中还会腐蚀设备并产生大量废酸液。此外,由于大部分无机酸具有热不稳定性,在热解过程中容易发生缩合反应生成焦炭。在本研究中,合成固体酸Fe3O4/CT-H3PO4,用于促进纤维素热解生成左旋葡聚糖和左旋葡萄糖酮。
1 实验材料和方法
1.1 固体酸的制备
实验中所需的微晶纤维素、纳米四氧化三铁(≥99.5%,20 nm)和葡萄糖购自上海麦克林生化有限公司。磷酸(≥98%)购自广实代理科技有限公司(广东)。左旋葡聚糖(>96%)和左旋葡萄糖酮(>96%)购自Sigma-Aldrich(上海)。固体酸的制备分为两步:制备碳基载体和负载磷酸。首先,在100 ml 去离子水中加入2 g纳米四氧化三铁和15 g葡萄糖,放置于100°C 油浴锅中,剧烈搅拌以确保颗粒分散均匀。待水分蒸发后,将固体混合物转移到坩埚中,并在管式炉中以6℃/min 加热到500~800℃。煅烧后,取出碳化固体C/Fe3O4,与磷酸按1 g/10 ml 的比例混合。放置于150℃油浴中加热20 h 后,用去离子水洗涤至中性,最后在105℃烘箱中干燥24 h。分别在500、600、700 和800°C 下煅烧制备催化剂,命名为Fe3O4/C500-H3PO4、Fe3O4/C600-H3PO4、Fe3O4/C700-H3PO4和Fe3O4/C800-H3PO4。
1.2 固体酸的表征
催化剂的X 射线衍射分析在X'Pert PRO MPD X 射线衍射仪中进行,使用(Cu Kα)辐射源(λ=0.15418 nm)。扫描电子显微镜(SEM,ZEISS EVO LS10,Cambridge,UK)用于扫描催化剂的表面形貌。采用NH3程序升温脱附法(NH3-TPD,Quantachrome Instruments,Boynton Beach,FL)检测催化剂的酸性。采用热重分析仪(SDT650,TA,USA)对样品进行热重分析。将样品放入氧化铝坩埚中,以10℃/min 的速率从30℃加热至650℃。
1.3 快速热解
在半间歇式热解反应器(CDS 5200,Oxford,PA,USA)中进行快速热解实验,将热解挥发分导入气相色谱-质谱仪(GC-MS)(Agilent 7890A/5975C)分析产物。将纤维素与固体酸混合置于石英管中间,石英管两侧用石英棉堵住。热解温度为300~500℃,热解时间为20 s,进样口温度为280℃,载气为氦气(1 ml/min),分流比设为1∶100,采用毛细管柱(Agilent HP-INNO,30 mm×0.25 mm×0.25 μm)分离样品。柱箱的升温程序为:在40℃下恒温3 min,然后以5℃/min的速度升温至280℃,并在280℃下恒温8 min。每个实验重复3 次,并采用外标法对产物进行定量分析。热解产物的产率计算如下:

2 实验结果与讨论
2.1 固体酸的表征
2.1.1 Fe3O4/CT-H3PO4的SEM 分析 在不同的煅烧温度下,碳基催化剂的SEM 图呈现出不同的表面形态(图1)。Fe3O4/C500-H3PO4呈现片状,表面光滑,Fe3O4/C600-H3PO4同样呈现片状,但有少许絮状固体附着在片状表面。当煅烧温度升高时,催化剂的表面形态发生明显变化,Fe3O4/C700-H3PO4和Fe3O4/C800-H3PO4呈现块状,但是Fe3O4/C700-H3PO4的块状内部充斥了絮状颗粒,而Fe3O4/C800-H3PO4内部只有部分呈现絮状颗粒状。表明700℃的煅烧温度可以增加催化剂的孔隙,从而增加催化剂的表面活性基团。

图1 催化剂的SEM图Fig.1 SEM images of catalysts
2.1.2 Fe3O4/CT-H3PO4的XRD 分析 不同催化剂的XRD 分析表明,Fe3O4/C500-H3PO4和Fe3O4/C600-H3PO4主要含有磁铁矿(Fe3O4)结晶结构,而Fe3O4/C700-H3PO4除了含有Fe3O4结晶结构,还含有磷酸亚铁[Fe3(PO4)2]结晶结构(图2)。由于Fe3O4/C700-H3PO4特殊的表面形态可以负载更多的磷酸,导致在高温下生成少量的磷酸亚铁。而Fe3O4/C800-H3PO4主要是磷酸亚铁结晶结构,还有少量的碳化铁(Fe3C)结晶结构,碳化铁是在高温下形成的间隙化合物。
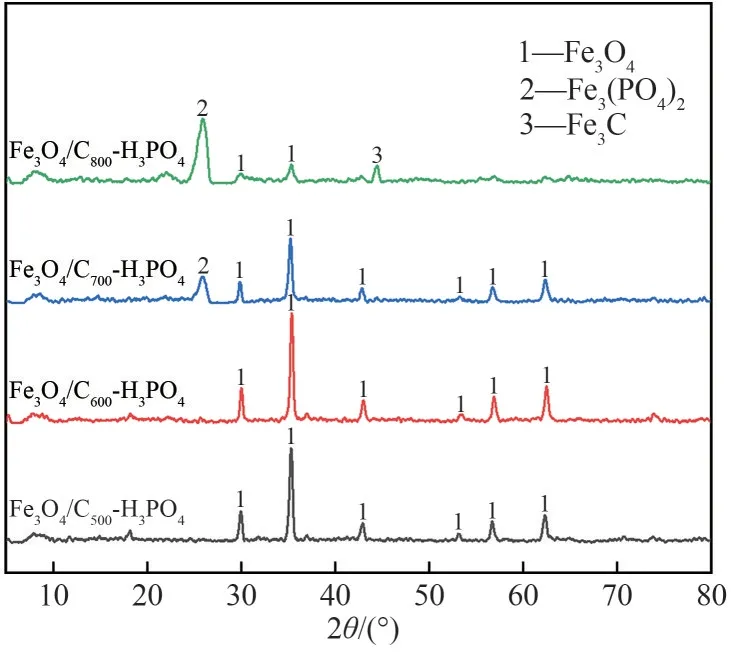
图2 催化剂的XRD分析Fig.2 XRD analysis of catalysts
2.1.3 Fe3O4/CT-H3PO4的NH3-TPD 分析 NH3-TPD 结果(表1)表明,Fe3O4/C700-H3PO4的酸度最高(5.5 mmol/g),其次是Fe3O4/C800-H3PO4(4.5 mmol/g),Fe3O4/C500-H3PO4(3.2 mmol/g)和Fe3O4/C600-H3PO4的酸度较低(2.7 mmol/g)。在700°C 的煅烧温度下,催化剂具有更多的孔隙结构,可以负载更多的磷酸,因此Fe3O4/C700-H3PO4的酸度最高。而在800°C 的煅烧温度下,催化剂形成了具有强结合力的间隙化合物,减少了催化剂的孔隙结构,从而降低负载酸的能力,导致Fe3O4/C800-H3PO4的酸性降低。

表1 不同催化剂的NH3-TPD分析Table 1 NH3-TPD analysis of different catalysts
2.1.4 Fe3O4/CT-H3PO4的TG 分析 不同催化剂与纤维素混合的热重分析如图3 所示,热重特征温度如表2 所示。热重图中仅有一个失重峰,该峰代表了纤维素的热解反应,表明固体酸在热解过程中比较稳定。与纯纤维素相比,固体酸与纤维素混合后,固体酸表面负载的磷酸基团可以降低纤维素的结晶度与聚合度,从而降低纤维素的热稳定性及初始热解温度。350℃之后,纤维素的质量缓慢降低,处于缓慢炭化阶段。纯纤维素热解的最大失重速率(-2.7%/℃)低于与催化剂混合的纤维素(-9.0%/℃~-14.0%/℃)。Fe3O4/C700-H3PO4可以促使纤维素集中且强烈地发生解聚反应,显著缩小了纤维素的主失重区域,提高最大失重速率(-14.0%/℃)。

图3 不同催化剂与纤维素混合的热重分析Fig.3 TG analysis of cellulose mixed with different catalysts
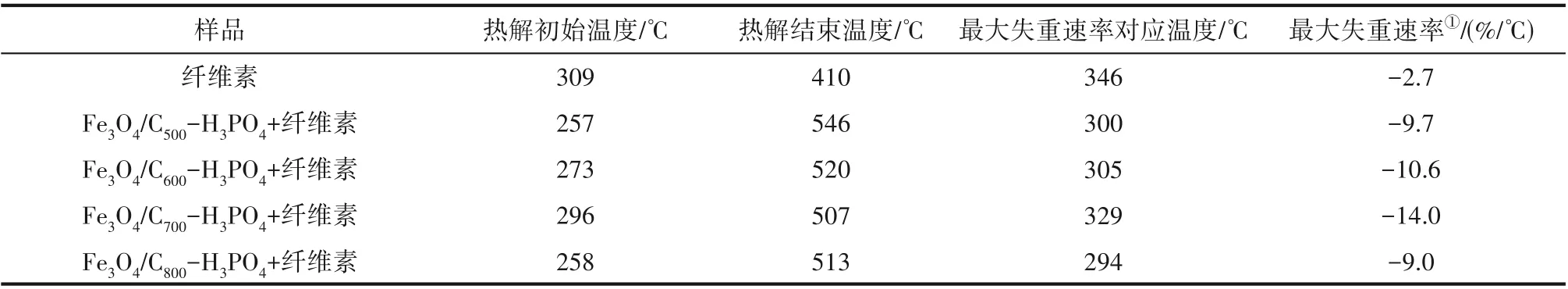
表2 不同催化剂与纤维素混合的热重特征温度Table 2 TG characteristic temperature of cellulose mixed with different catalysts
2.2 纤维素的催化热解
2.2.1 不同固体酸对纤维素催化热解产物的影响将纤维素与固体酸按1∶1的质量比混合,在350℃进行催化热解。纤维素与碳基载体(Fe3O4/C500、Fe3O4/C600、Fe3O4/C700和Fe3O4/C800)混合后,左旋葡聚糖以及左旋葡萄糖酮的产率[0.7%~0.8%(质量)]与纤维素热解[0.6%(质量)]相比并没有明显变化(图4)。碳基载体负载磷酸后可以促进纤维素热解生成左旋葡萄糖酮。四种催化剂中,Fe3O4/C700-H3PO4催化纤维素快速热解获得最高的左旋葡萄糖酮产率[8.8%(质量)]。催化剂的酸性位点对催化剂的性能有重要影响,Fe3O4/C700-H3PO4的酸度最高(5.5 mmol/g),所以表现出较强的催化性能。Fe3O4/C600-H3PO4的酸度仅为2.7 mmol/g,酸度最低,导致其催化性能较弱。虽然Fe3O4/C800-H3PO4的酸度高于Fe3O4/C500-H3PO4,但在煅烧过程中形成过多磷酸亚铁以及碳化铁,降低其催化性能。此外,当左旋葡萄糖酮的产率达到最高时,左旋葡聚糖的产率最低[6.3%(质量)],可能是因为Fe3O4/C700-H3PO4的酸性增强了脱水反应,促使左旋葡聚糖脱水生成左旋葡萄糖酮[23]。由于Fe3O4/C700-H3PO4的催化效果最强,因此进一步优化其催化热解条件。

图4 不同催化剂对纤维素热解产物的影响Fig.4 Effects of different catalysts on cellulose pyrolysis products
2.2.2 不同热解温度对纤维素催化热解产物的影响 Fe3O4/C700-H3PO4与纤维素按1∶1 的质量比混合,在不同热解温度下快速热解产生左旋葡聚糖和左旋葡萄糖酮。当热解温度从300°C升至500°C,左旋葡萄糖酮的产率先上升后下降,在350°C 时达到了最高值[8.8%(质量)],然后逐渐降低至2.8%(质量),然而随着温度的变化,左旋葡聚糖的产率变化不明显(图5)。在快速热解过程中,纤维素首先受热导致糖苷键断裂,解聚生成左旋葡聚糖,然后脱水生成左旋葡萄糖酮,当热解温度太低时,纤维素无法完全分解,抑制了热解产物的生成;随着热解温度的升高,左旋葡萄糖酮的产率也随之降低,有如下几个原因:一是因为纤维素解聚生成左旋葡聚糖的速率加快,抑制了左旋葡聚糖脱水生成左旋葡萄糖酮的反应;二是因为在高温区域,纤维素热解反应途径变多,从而抑制了左旋葡萄糖酮的形成[24-25]。酸性催化剂促进纤维素在较低温度下完成解聚反应,随着温度升高,左旋葡聚糖的产率保持相对稳定。
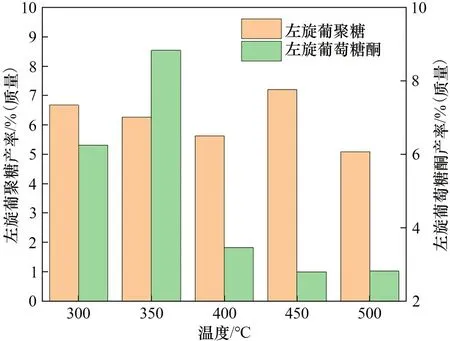
图5 不同热解温度对纤维素热解产物的影响Fig.5 Effects of different pyrolysis temperatures on cellulose pyrolysis products
2.2.3 固体酸与纤维素的不同比例对热解产物的影响 在350℃下,Fe3O4/C700-H3PO4与纤维素以不同质量比例(3∶1,2∶1,1∶1,1∶2,1∶3,1∶4)混合进行催化热解。当催化剂与纤维素的比例从1∶4逐渐上升至3∶1,左旋葡聚糖与左旋葡萄糖酮的产率都呈现先增加后降低的趋势(图6)。当催化剂与纤维素的比例为1∶3时,催化热解的效果最佳,左旋葡聚糖的产率增加至40.7%(质量),同时左旋葡萄糖酮的产率[13.5%(质量)]也达到最高。在快速热解过程中,Fe3O4/C700-H3PO4降低了纤维素的热解温度,促进左旋葡聚糖和左旋葡萄糖酮的生成。但是过多的催化剂会增大快速热解过程中的传热阻力,导致受热分解不能吸收到足够的热量,限制左旋葡聚糖和左旋葡萄糖酮的生成;此外,过多的催化剂也会导致酸性过强,促进左旋葡萄糖酮进一步脱水生成其他小分子产物[26]。
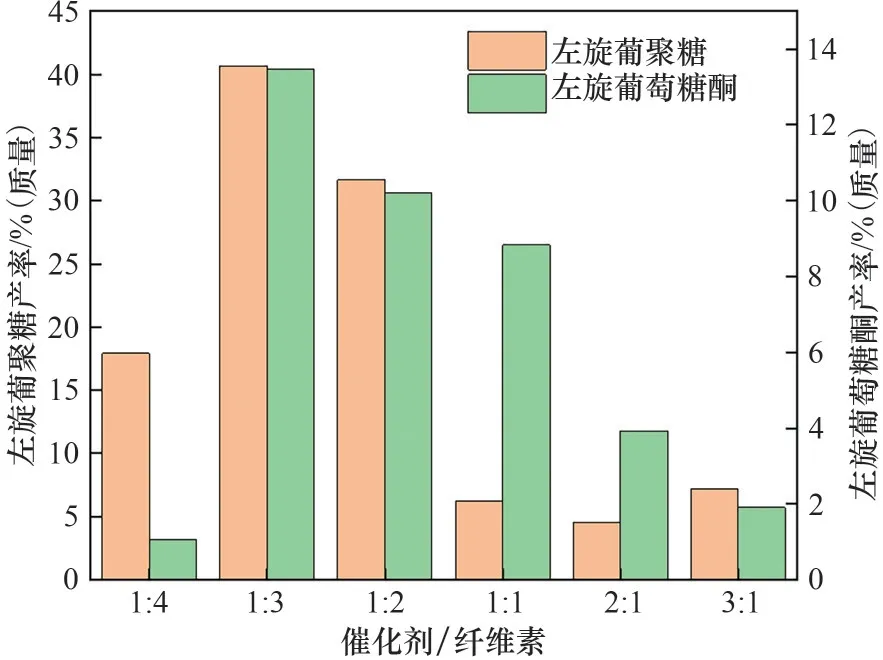
图6 不同催化剂/纤维素比例对热解产物的影响Fig.6 Effects of different catalyst/cellulose ratio on pyrolysis products
2.3 纤维素催化热解产物分布
纤维素快速热解反应可以分为解聚反应和开裂反应。纤维素热解解聚可以生成脱水糖和呋喃类物质,而热解产物中的小分子化合物主要由开裂反应获得[27-29]。纯纤维素以及Fe3O4/C700-H3PO4与纤维素以1∶3 比例混合在350°C 下热解的总离子流图如图7 所示。纤维素在350°C 时热解产物较少,且产物峰面积相对较低,表明在该热解温度下,纤维素未能完全热解。在Fe3O4/C700-H3PO4的催化下,纤维素快速热解产物分布较广,且峰面积较大,可见固体酸可以实现纤维素在较低温度下的完全热解。纤维素在350°C 时的热解产物主要是脱水糖类(左旋葡聚糖和1,6-脱水-β-D-呋喃葡萄糖)以及少量的小分子化合物。在该温度下,纤维素的反应以解聚反应为主。在Fe3O4/C700-H3PO4的催化作用下,左旋葡聚糖和1,6-脱水-β-D-呋喃葡萄糖仍然为主要产物,同时生成了左旋葡萄糖酮、糠醛、5-羟甲基糠醛、1,4∶3,6-二脱水-α-D-吡喃葡萄糖以及其他小分子化合物。左旋葡萄糖酮是由左旋葡聚糖脱水生成,吡喃糖环内发生脱水反应生成3,6-酐键,从而形成1,6-脱水-β-D-呋喃葡萄糖[30]。糠醛和5-羟甲基糠醛是呋喃类物质,主要来源于左旋葡聚糖的进一步分解。吡喃糖环发生断键反应后形成葡萄糖链,随后碳键上的羟基发生脱水反应生成5-羟甲基糠醛,5-羟甲基糠醛进一步分解生成糠醛[31]。Fe3O4/C700-H3PO4可以降低纤维素的热解温度,促进纤维素生成更多的左旋葡聚糖,由于催化剂自带酸性,增强了脱水反应,促进左旋葡萄糖酮、1,6-脱水-β-D-呋喃葡萄糖、5-羟甲基糠醛和糠醛的形成,其中左旋葡萄糖酮产率增加最明显。
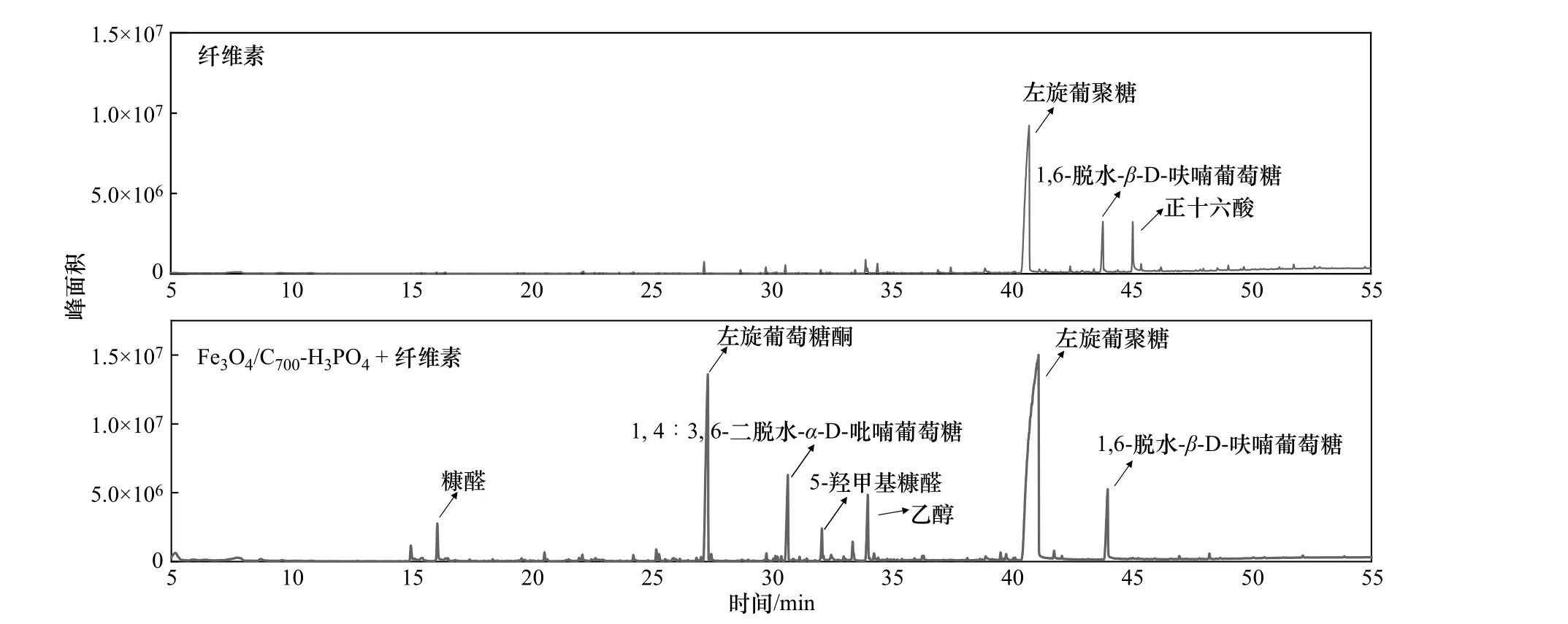
图7 纤维素催化热解产物分布Fig.7 Cellulose catalytic pyrolysis products distribution
3 结 论
本文制备了固体酸催化剂,用于促进纤维素快速热解生成左旋葡萄糖酮和左旋葡聚糖。在700°C的煅烧温度下,碳基载体可负载更多的磷酸并保持稳定的物性,使其拥有较强的催化效果。在350°C,Fe3O4/C700-H3PO4与纤维素以1∶3 的比例混合,可以降低纤维素的热解温度,强化纤维素在低温时的解聚反应,从而将左旋葡聚糖的产率从12.6%(质量)增加到40.7%(质量)。同时也明显提高了左旋葡萄糖酮的产率,从0.6%(质量)提升至13.5%(质量)。该研究为纤维素定向热解的生物质精炼工艺提供了前瞻性指导。

