口服β-内酰胺酶保护SD 大鼠肠道双歧杆菌/乳酸杆菌免受β-内酰胺抗生素所致损伤研究
罗启剑
摘要抗生素经注射给药后排泄进入肠道并非治疗所需,并且会破坏肠道菌群并导致一些不利临床后果。为了减轻这种不利影响,我们开发了一种重组β-内酰胺酶--BL,并制备成肠溶包衣微丸,用于降解排泄进入肠道的 β-内酰胺抗生素。在此,我们报告了其在大鼠中进行的临床前药效评估,使用氨苄西林和头孢替安作为模型抗生素。在其中一项研究中,动物经尾静脉注射1剂抗生素,经过口给予3剂赋形剂或不同剂量的 BL(24~144μg/剂量),收集血液和肠道样本,并测定抗生素浓度。在另一项研究中,动物每天腹腔注射1剂抗生素,连续3天,并每天经口给予3剂赋形剂或不同剂量的 BL(72~216μg/剂),另有一组不进行任何给药处理;在抗生素治疗前后收集粪便样本,培养用于双歧杆菌、乳酸杆菌计数。结果显示,经口给予 BL 显著降低了抗生素肠道浓度,而对血清抗生素浓度没有明显影响;抗生素治疗导致双歧杆菌、乳酸杆菌数量降低 5-6 个数量级,而 BL 干预可以防止肠道双歧杆菌、乳酸杆菌受到这种损害,并保持其水平与未治疗组相近。这些临床前研究表明,BL 可以降解排泄进入肠道的 β-内酰胺抗生素,并防止其对肠道益生菌造成的损害。
关键词:重组β-内酰胺酶,β-内酰胺类抗生素,肠道菌群,双歧杆菌,乳酸杆菌
1.简介
肠道内存有数以万亿计的微生物,分属于多个细菌种类,共同构成了肠道菌群。 数百万年的共同进化,导致宿主和肠道菌群在代谢和其他一些方面(例如促进形成肠上皮屏障)建立起互利共生关系。
肠道本土菌群可以通过刺激宿主黏膜免疫防御间接调节定植抗性,防止潜在致病性非本土微生物的生长和后续感染。越来越多的证据表明,肠道菌群在宿主先天性和获得性免疫系统的主要成分的训练和发育中发挥着关键作用,涉及针对炎症性疾病、自身免疫性疾病和其他一些疾病(如阿尔茨海默病)的免疫调节机制。
虽然抗生素治疗可以降低某些微生物感染的发生率,但这些抗生素会被排泄进入肠道中,显著降低肠道本土菌群的防御能力 。 抗生素,尤其是一些广谱抗生素,给药后可通过胆汁排泄,并以高浓度在粪便中蓄积,对肠道菌群组成造成长期影响,即使在停药后也是如此。抗生素排泄进入肠道,造成耐药性病原体进入肠道、过度生长以及某些疾病发展的发生率增加。
β-内酰胺类抗生素是目前使用最广泛的抗菌药物之一,其中许多以高浓度排泄入肠道中。然而,据我们所知,迄今为止,还没有任何产品上市并临床用于降解肠道中的抗生素,减轻其对宿主和社区的潜在不良后果。
受某些细菌产生的β-内酰胺酶可以打开β-内酰胺环并使β-内酰胺抗生素失活这一事实的启发,我们开发了BL,一种重组β-内酰胺酶,通过降解排泄的β-内酰胺抗生素来保护肠道菌群免受β-内酰胺抗生素的损害,同时不影响注射抗生素治疗的全身性药效。
在对BL产品的初步药效评价中,我们分步设计了两项研究。第一项研究旨在考察口服BL对排泄入肠道抗生素浓度的变化,第二项旨在观察BL对排泄进入肠道抗生素对肠道主要益生菌菌群破坏的保护作用。
氨苄西林和头孢替安分别被选为青霉素和头孢菌素类抗生素的模型抗生素,这两类抗生素是使用最广泛的两类β-内酰胺类抗生素。模型抗生素的选择是根据这些抗生素的临床使用率以及抗生素胆汁排泄率水平做出的。
2.材料与方法
2.1试验样品
BL是一种重组β-内酰胺酶,通过大肠杆菌表达、收获以及色谱柱纯化得到原液,然后将原液通过流化床喷雾干燥方法制备成肠溶包衣微丸,微丸制备时以蔗糖丸芯,逐层包衣。 每个微丸含有约 12μg 的 BL,包衣在 pH ≥5.5 时溶解。赋形剂微丸采用和BL肠溶包衣微丸类似的方法制备,但不含活性药物成分。
2.2动物和试剂
使用健康SPF级SD大鼠,6-8周龄,一半雄性一半雌性。 第一项研究中的动物由昭衍(苏州)新药研究中心有限公司提供,第二项研究中的动物购自上海斯莱克实验动物有限公司。氨苄西林钠(华北制药集团)和头孢替安(大熊制药)购自于商业供应商。
2.3动物试验流程及样品采集
我们设计了两项大鼠研究,以逐步递进方式对 BL 产品进行初步动物药效评估。
为了考察口服BL对肠道抗生素浓度的影响,在第一项研究中,使用96只SD大鼠,将动物随机分为四组,包括赋形剂组、BL 24μg/剂量组、BL 60μg/剂量组和BL 144μg/剂量组。每组中一半的动物通过尾静脉注射接受1剂氨苄西林钠 (150mg/大鼠),其他动物接受1剂头孢替安 (40mg/大鼠)。在抗生素给药前 60、10 分钟和 给药后60 分钟,通过口腔导管向动物给予赋形剂或 BL 微丸。在抗生素注射给药后 15 和 45 分钟,通过下颌下静脉或眼眶收集血液样本。所有动物在抗生素给药后 120 分钟使用二氧化碳过量吸入处死,将十二指肠到盲肠前段的肠道部分切成两个相等长度的部分(即肠段1和肠段2)。将血样置于含有pH7.4 PBS缓冲液和200 mmol/L EDTA的离心管中,1000g离心10分钟,收集血浆并在-20℃以下保存至分析。将肠段样品用剪刀剪碎,转移至50 mL离心管中,立即加入2 mL含20 mmol/L EDTA的pH7.4 PBS缓冲液,涡旋2 min,10000 g、4℃离心10 分钟,收集上清液并储存在-20°C 以下用于分析。
为了考察BL对排泄至肠道抗生素所致双歧杆菌和乳酸杆菌损伤的保护作用,第二项研究采用 144 只 SD 大鼠,其中一半用于氨苄西林钠队列,另一半用于头孢替安队列。对于每个抗生素队列,将SD大鼠随机分为六组,包括未治疗组、仅抗生素组、赋形剂组、BL 72μg/剂量组、BL 144μg/剂量组和BL 216μg/剂量组。除未治疗组外,所有组动物每天腹腔注射抗生素(氨苄西林钠150mg/剂或头孢替安160mg/剂),连续3天。在与第一项研究中抗生素施用前后相同的预定时间点,分别向赋形剂组和三个 BL 组的动物每天三次给予赋形剂和 BL 微丸。在治疗前(第 0 天)和治疗开始后 1、3 天(第 1、3 天)从每只动物中采集粪便样品。未治疗组动物仅采集粪便样品,不给予抗生素、赋形剂或BL处理。对粪便樣品称重,用PBS缓冲液对粪便样品进行10至10的系列稀释,用于双歧杆菌和乳酸菌培养。
2.4抗生素浓度检测
使用液相色谱涡轮离子喷雾串联质谱法(LC/MS/MS)分析血浆和肠段上清液样品的抗生素浓度。采用Ultimate XB-C18 分析柱,以 5 mM 甲酸铵(0.1% 甲酸)-乙腈为流动相进行梯度洗脱,用于氨苄青霉素浓度测定。 对于头孢替安,选择 Waters AltlantisT3柱,使用 5 mM 甲酸铵(0.1% 甲酸)-甲醇作为流动相进行梯度洗脱。 检测词用多反应监测 (MRM) 模式在正离子模式下使用电喷雾电离进行的。
2.5双歧杆菌和乳酸杆菌粪便样品培养和计数
涡旋后,将 5 个稀释度的液体(10、10~10)各取 50 μl 涂在新鲜制备的 TPY 和 MRS 琼脂平板上(培养基购于青岛海博生物),然后在厌氧罐中用三元混合气体(氧气:氮气:二氧化碳=5%:80-85%:10-15%)37°C 孵育过夜。
培养的双歧杆菌和乳酸菌的计数方法采用之前报道并收载于FDA Bacteriological Analytical Manual中的常规平板计数法,稍作修改,包括将30~300设为正常平板的优选范围。
2.6数据及统计分析
所有统计分析采用双侧检验,设置显著性水平为0.05。
首先采用Levene 检验检测方差齐性。如果结果不显著,则进行单因素方差分析 (ANOVA),否则进行 Kruskal-Wallis 检验。 如果ANOVA检测出显著性,进一步采用Dennett 检验进行多重比较;如果在 Kruskal-Wallis 检验中发现差异,多重比较采用 Mann-Whitney U 检验。
3结果
3.1 BL对血清β-内酰胺抗生素水平无治疗相关影响
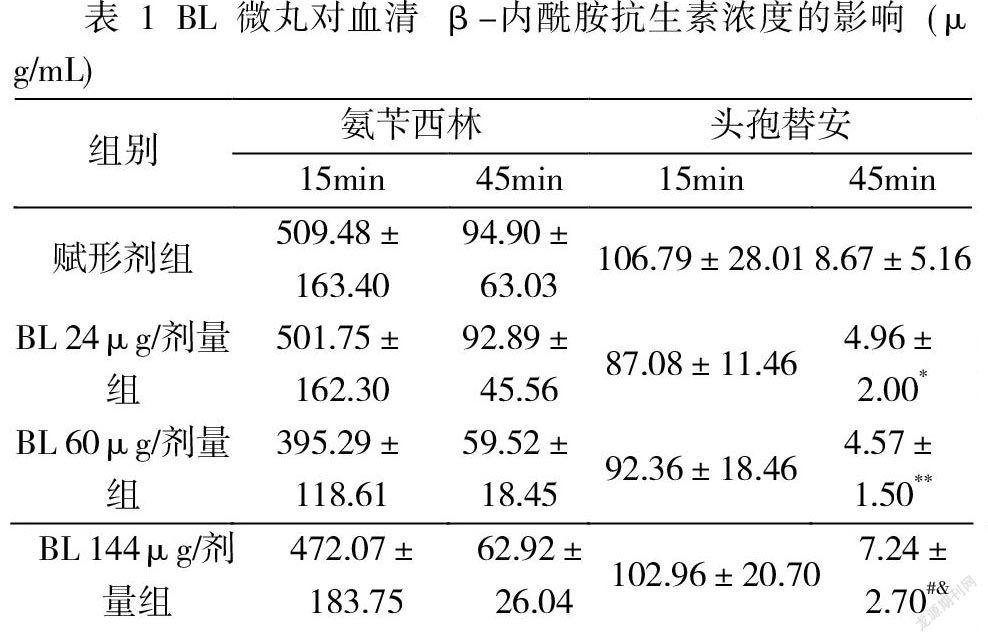
在静脉注射两种抗生素后,在两个给药后时间点,所有动物的血浆中均可检出抗生素。在两个时间点的血清氨苄西林浓度和15min时间点血清头孢替安浓度,所有四组之间均无显著差异(表 1)。
对于45 min时的血清头孢替安浓度,BL 60μg/剂量组、BL 144μg/剂量组与其他两组差异有统计学意义。 然而,由于在考察剂量范围内没有发现这种浓度降低具有剂量-反应效应,并且变化幅度较小,因此推测这种变化与 BL 无关。
3.2 BL降低排泄入肠道的β-内酰胺抗生素浓度
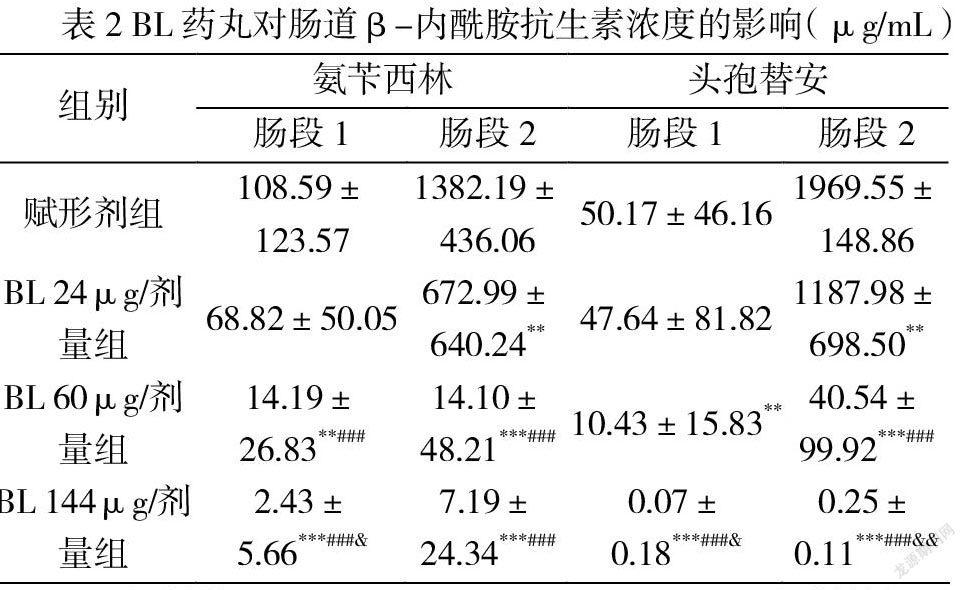
静脉给药后 120 分钟,赋形剂组动物肠段两种β-内酰胺类抗生素均处于高浓度水平,氨苄青霉素最高至1881μg/mL,头孢替安最高至 2274μg/mL。 肠段2氨苄西林和头孢替安浓度分别比肠段1高3~65倍和13~237倍,表明静脉注射2小时后排泄的抗生素大部分已进入肠道后半段(表2) 。
对于两种抗生素及相应两个肠段,三个 BL 治疗组均呈剂量依赖性降低抗生素浓度,并且在 BL 144μg/剂量组中只有很少肠段样品可检出抗生素。 BL三个剂量均显著降低了肠段2抗生素浓度,中高剂量BL(60~144μg)显著降低了肠段1抗生素浓度。60μg/剂量被认为当前试验条件下BL降解排泄入肠道氨苄青霉素和头孢替安的有效剂量。
3.3 BL保护肠道益生菌免受β-内酰胺类抗生素损伤
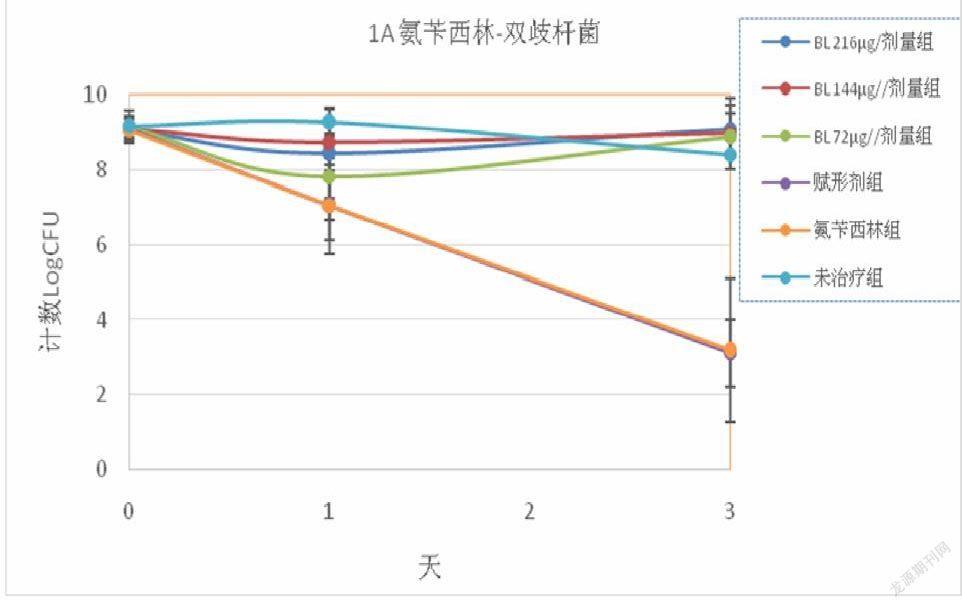
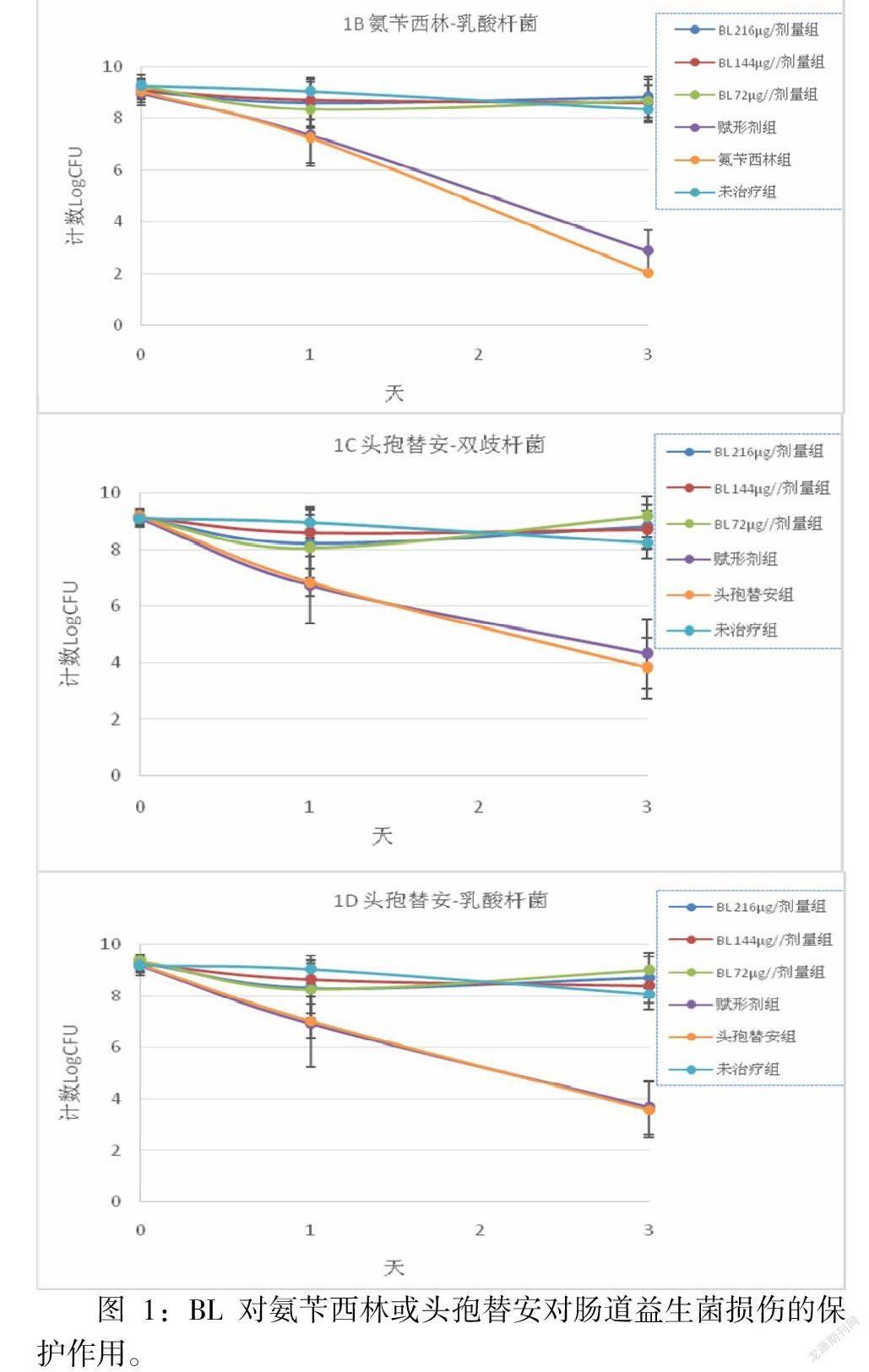
两种β-内酰胺抗生素均导致双歧杆菌和乳酸杆菌水平随时间显著下降。 与未治疗组相比,氨苄西林导致第 1 天双歧杆菌和乳酸杆菌水平分别下降 1.79 和 2.22 logCFU,第 3 天下降 5.23 和 6.33 logCFU。头孢替安表现出类似的变化趋势,第 1 天下降 2.12 和 1.99 logCFU,第 3天下降 4.44 和 4.48 logCFU(图 1),赋形剂处理与仅抗生素组相比没有任何显著差异。 然而,即使在最低剂量(72μg/剂量)下,BL干预也可以减轻这些抗生素对肠道益生菌的负面影响。对于两种抗生素,BL组和未治疗组之间以及三种BL治疗之间的双歧杆菌和乳酸菌计数均未观察到统计学差异。
A和B:用氨苄青霉素处理动物和未治疗组动物的双歧杆菌和乳酸杆菌菌落计数(LogCFU)。 C和D:用头孢替安处理动物和未治疗组动物的双歧杆菌和乳酸杆菌菌落计数(LogCFU)
4讨论
我们在这些大鼠模型中表明,口服给予我们的重组β-内酰胺酶--BL可以降解注射后排泄进入大鼠肠道中β-内酰胺抗生素,同时维持抗生素高血清浓度和系统暴露水平,因此推测不会这些抗生素注射后的药效作用产生不利影响。该发现与之前另一种重组 β-内酰胺酶产品 P1A 的报告一致,后者在狗空肠瘘手术模型中证明口服 β-内酰胺酶对血清抗生素浓度无不利影响,这可能是因为, 25kD 大分子量的蛋白质在保持其功能构象的同时被吸收到血液循环中理论上是难以实现的。
保护肠道菌群免受抗生素引起的损害对于维持人类健康至关重要。 数千年来,肠道菌群与其哺乳动物宿主共同进化,并在消化、大量营养素代谢、解毒、抵御病原体和许多其他方面使宿主受益。 据报道,菌群在宿主免疫系统的诱导、教育和功能中也具有重要作用。 在庞大的肠道细菌群落中,双歧杆菌是婴儿肠道中占主导地位的一个属,而在成年后水平降低但保持稳定。
值得注意的是,如我们的研究所示,β-内酰胺类抗生素会以时间依赖性方式显著破坏肠道菌群落,如双歧杆菌数量降低最大约 10 倍,乳酸杆菌最大约 10 倍。 肠道菌群紊亂可能促进传染病的发展,病原体经常利用来自宿主肠道菌群的信号来传播和加速感染进程。
BL干预可以保护肠道菌群双歧杆菌和乳酸杆菌免受排泄入肠道β-内酰胺抗生素造成的损害。 这种对肠道菌群的保护作用对于预防 β-内酰胺抗生素导致的潜在不利后果,例如腹泻、艰难梭菌感染假膜性肠炎等,具有重要临床意义。
5结论
总之,我们在大鼠模型中证明,口服给予BL可以降解注射给药后排泄入肠道中的青霉素和头孢菌素类抗生素,并可以保护肠道益生菌免受β-内酰胺类抗生素引起的破坏。
BL 在人类中的有效性需要进一步的研究来证明。
参考文献
[1]Ubeda C, Djukovic A, Isaac S. 2017. Roles of the intestinal microbiota in pathogen protection. Clin Transl Immunology. 6, 2(Feb, 2017), e128.
[2]Libertucci J, Young VB. 2019. The role of the microbiota in infectious diseases. Nat Microbiol. 4, 1(Jan, 2019), 35-45.
[3]Zheng D, Liwinski T, Elinav E. 2020. Interaction between microbiota and immunity in health and disease. Cell Res. 30, 6(Jan, 2020), 492-506.
[4]Sochocka M, Donskow-Łysoniewska K, Diniz BS, Kurpas D, Brzozowska E, Leszek J. 2019. The Gut Microbiome Alterations and Inflammation-Driven Pathogenesis of Alzheimer's Disease-a Critical Review. Mol Neurobiol. 56, 3(Mar, 2019), 1841-1851.
[5]Newton DF, Macfarlane S, Macfarlane GT. 2013. Effects of antibiotics on bacterial species composition and metabolic activities in chemostats containing defined populations of human gut microorganisms. Antimicrob Agents Chemother. 57, 5(May, 2013), 2016-2025.
[6]Yoon MY, Yoon SS. 2018. Disruption of the Gut Ecosystem by Antibiotics. Yonsei Med J. 59, 1(Jan, 2018), 4-12.
[7]Becattini S, Taur Y, Pamer EG. 2016. Antibiotic-Induced Changes in the Intestinal Microbiota and Disease. Trends Mol Med. 22, 6(Jun, 2016), 458-478.
[8]Brogard JM, Arnaud JP, Blickle JF, Levy P, Dorner M, Lautier F. 1986. Biliary elimination of cefotiam, an experimental and clinical study. Chemotherapy. 32, 3, 222-235.
[9]Larry M,James T. P. 2001. Bacteriological Analytical Manual, Chapter 3: Aerobic Plate Count. FDA, 2001.
[10]Harmoinen J, Vaali K, Koski P, et al.2003. Enzymic degradation of a beta-lactam antibiotic, ampicillin, in the gut: a novel treatment modality. J Antimicrob Chemother. 51, 2(Feb 2003), 361-365.
[11]Wu HJ, Wu E. 2012. The role of gut microbiota in immune homeostasis and autoimmunity. Gut Microbes. 3, 1(Jan-Feb, 2012), 4-14.
[12]Belkaid Y, Harrison OJ. 2017. Homeostatic Immunity and the Microbiota. Immunity. 46, 4(Apr, 2017), 562-576.
[13]Arboleya S, Watkins C, Stanton C, Ross RP.2016. Gut Bifidobacteria Populations in Human Health and Aging. Front Microbiol. 7(Aug, 2016), 1204.
[14]Lv L X, Jiang H Y, Yan R, et al. 2019. Interactions Between Gut Microbiota and Hosts and Their Role in Infectious Diseases. Infectious Microbes & Diseases. 1, 1(Sep, 2019), 3-9.
姓名 :羅启剑、性别 :男、出生年月:1978.12、籍贯(精确到市):安徽省庐江县(现属合肥市)、学历:研究生、职称:中级工程师、研究方向:生物医药
单位:上海联合赛尔生物工程有限公司、单位邮编 :201206
2321500783254

