依托泊苷脂质微球注射液热原及细菌内毒素检查方法
孙 丹
辽宁省检验检测认证中心辽宁省药品检验检测院药理室,辽宁沈阳 110036
依托泊苷是肺癌患者临床化学治疗的重要一线药物,尤其针对广泛期、预后较差的小细胞肺癌,其联合顺铂方案的治疗有效率高,已沿用数十年。市售依托泊苷一般会具有骨髓抑制等明显不良反应,并且水中的溶解度差(溶解度为58.7 mg/L)[1-2],常会诱发刺激等不良反应[3]。最近几年来逐步开展的有关依托泊苷脂质体类药物新剂型研究,都在力求降低该品种的毒副作用,同时最大限度保留其抗癌细胞增殖生长的相关药效[2]。
依托泊苷脂质微球注射液包含依托泊苷、脂溶性介质、水和表面活性剂,这些成分使依托泊苷在油水两相的界面膜中都会有一定比例的分布,从而可提高在油水均难溶的依托泊苷在乳剂介质中的稳定性和载药量,并可降低其毒性及血管刺激性,同时可提高药物的化学稳定性及疗效,使得该制剂在临床应用中具有高效性、低毒性和低刺激性的优势。目前来看,国内已批准上市的脂质体注射剂类型还比较少,其产业化规模、生产工艺水平同国外相关制剂相比还有一定差距,质量控制中的热原检查项也未有文献报道[4-5]。本研究通过按照《中华人民共和国药典》2015年版四部通则[6-7]中收载的“热原检查和细菌内毒素检查法”,旨在探讨依托泊苷脂质微球注射液2种药典方法的可操作性与可行性,从而找出适用于该品种的相关检查方法,以控制药品质量。
1 仪器与材料
ZRY-2D智能热原仪(天津天大天发科技公司),ET-96内毒素凝胶法测定仪(天津天大天发科技公司),vortex-5涡旋混合器(海门市其林贝尔仪器制造公司),omh180烘箱(赛默飞世尔科技公司)。
细菌内毒素工作标准品(中国食品药品检定研究院,批号:150601-201885,规格:80 EU/支);细菌内毒素检查用水(BET水,湛江博康海洋生物有限公司,批号:151210,2 ml/支);鲎试剂(湛江安度斯生物有限公司,批号: 1307031,规格:0.1 ml/支,灵敏度:0.06 EU/ml;福州市新北生化工业有限公司,规格:0.1 ml/支,批号:14111112,灵敏度:0.06 EU/ml)。依托泊苷脂质微球注射液(沈阳药科大学,批号:20131101、20131102、20131103,规格:50 ml∶50 mg)。
日本大耳白兔,体重2.6~3.0 kg,雄雌不限,雌兔无孕,由沈阳药科大学实验动物中心供应,实验动物生产许可证号:SCXK(辽)2014-0002。
2 方法与结果
2.1 热原检查
本品临床最大给药量为静脉滴注,一日按体表面积100~150 mg/m2。参照《中华人民共和国药典》2015年版四部通则中“9301注射剂安全性检查法应用指导原则”[8],热原检查设定限值可参照临床剂量计算,样品的注射体积每千克体重一般不少于0.5 ml,不超过10 ml。另样品每平方米体表面积的剂量乘以0.027即可换算为每千克的体重剂量(M),故样品临床用量为4.05 mg/kg,热原检查实验给药体积设定为最大给药剂量的2倍,即8 ml/kg·BW。
按《中华人民共和国药典》2015版四部通则中“1142热原检查法”[6]进行实验。取检体温合格的家兔,每批3只,耳静脉注射本品,8 ml/kg·BW,给药后测定体温,共测定6次,每次间隔30 min,以6次测量体温中最高温度值减去基础测量体温值,即为该只家兔体温升高温度。结果表明,三批样品中每只家兔体温升高值均低于0.6 ℃,3只家兔的体温升高数值总和均低于1.3℃。热原检查实验结果均符合规定。见表1。
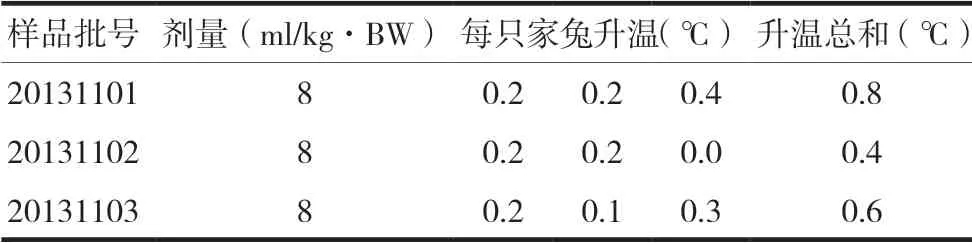
表1 依托泊苷脂质微球注射液热原实验结果
2.2 细菌内毒素
2.2.1 鲎试剂灵敏度复核标定根据《中华人民共和国药典》2015年版四部通则中“1143细菌内毒素检查法”[7],进行鲎试剂的灵敏度复核。结果显示,2个批次的鲎试剂标定结果均在0.5~2λ之间。见表2。2个批次鲎试剂的灵敏度均符合规定。

表2 鲎试剂灵敏度复核标定(EU/ml)
2.2.2 细菌内毒素限值的确定参照《中华人民共和国药典》2015年版四部通则中“9301注射剂安全性检查法应用指导原则”[8]进行样品细菌内毒素限值的确定。计算公式:L=K/M,其中M为人使用该制剂每千克体重每小时的最大给予剂量,本品为100 mg/m2×0.027=2.7 mg/kg,K为静脉给药途径,人使用该制剂每千克体重每小时最大可接受的内毒素剂量,注射剂品种K值为5 EU/(kg·h),L=K/M=5 EU/(kg·h)/2.7 mg/(kg·h)=2 EU/mg。
2.2.3 干扰实验预实验经过对体积分数为1.25%、2.5%、5%乙醇溶液的考察,结果显示,体积分数为1.25%的乙醇对内毒素检查方法无影响,说明在实验过程中,要保证乙醇最后稀释成终浓度为1.25%的乙醇溶液,才不会干扰内毒素与鲎试剂的反应。见表3。
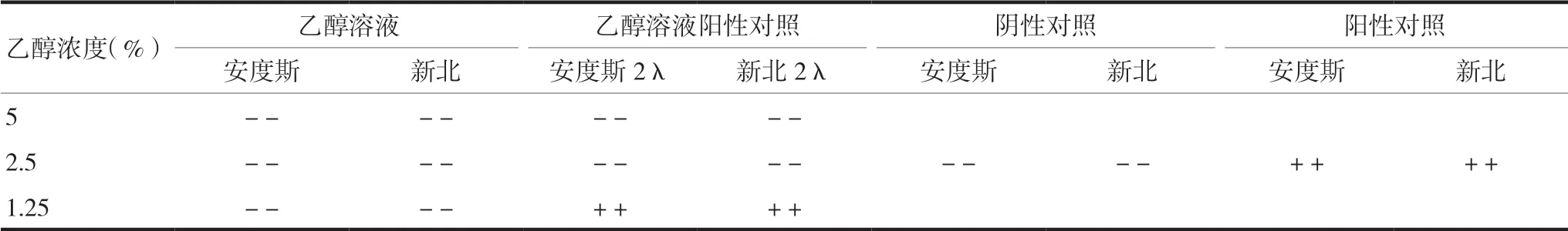
表3 乙醇内毒素检查法考察结果
按《中华人民共和国药典》2015年版四部通则中“1143细菌内毒素检查法”[7]检查。取3批样品,使用灵敏度为0.06 EU/ml的鲎试剂。先使用60%乙醇代替内毒素检查用水稀释样品原液,并在涡旋混合器上振荡5 min,经过步骤稀释后样品终浓度为0.03 mg/ml(与λ=0.06 EU/ml鲎试剂相对应的稀释液浓度)及0.06 mg/ml(用于考察)。阴性对照(NC)为细菌内毒素检查用水,阳性对照(PC)为0.125 EU/ml内毒素溶液,样品阳性对照(PPC)为含0.125 EU/ml内毒素的相应浓度的样品溶液。加完样品后,轻轻混匀,37℃±1℃保温1 h后记录试验结果。见表4。结果表明,依托泊苷脂质微球0.03 mg/ml稀释液(NPC)细菌内毒素检查符合规定,初步确定该样品0.03 mg/ml浓度为最大无干扰浓度。
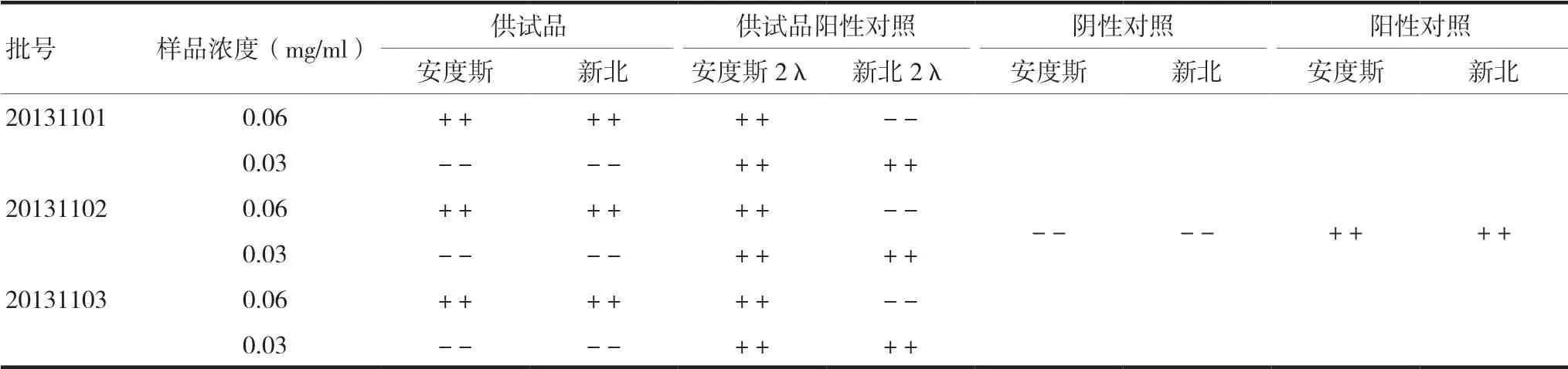
表4 依托泊苷脂质微球注射液细菌内毒素干扰实验预实验结果
2.2.4 干扰试验按《中华人民共和国药典》2015年版四部通则中“1143细菌内毒素检查法”[7]进行干扰实验,依托泊苷脂质微球稀释液浓度为0.03 mg/ml。将细菌内毒素工作标准品分别用BET水和样品稀释液稀释至0.125、0.06、0.03、0.015 mg/ml浓度,平行4管,同时用上述样品稀释液及BET水分别做平行2管阴性对照,轻轻混匀,37℃±1℃测定仪保温1 h后,记录实验结果。见表5。结果表明,用上述两个厂家鲎试剂分别进行干扰试验,Es均在0.5~2.0λ,Et均在0.5~2.0 Es,依托泊苷脂质微球注射液0.03 mg/ml浓度稀释液无干扰。
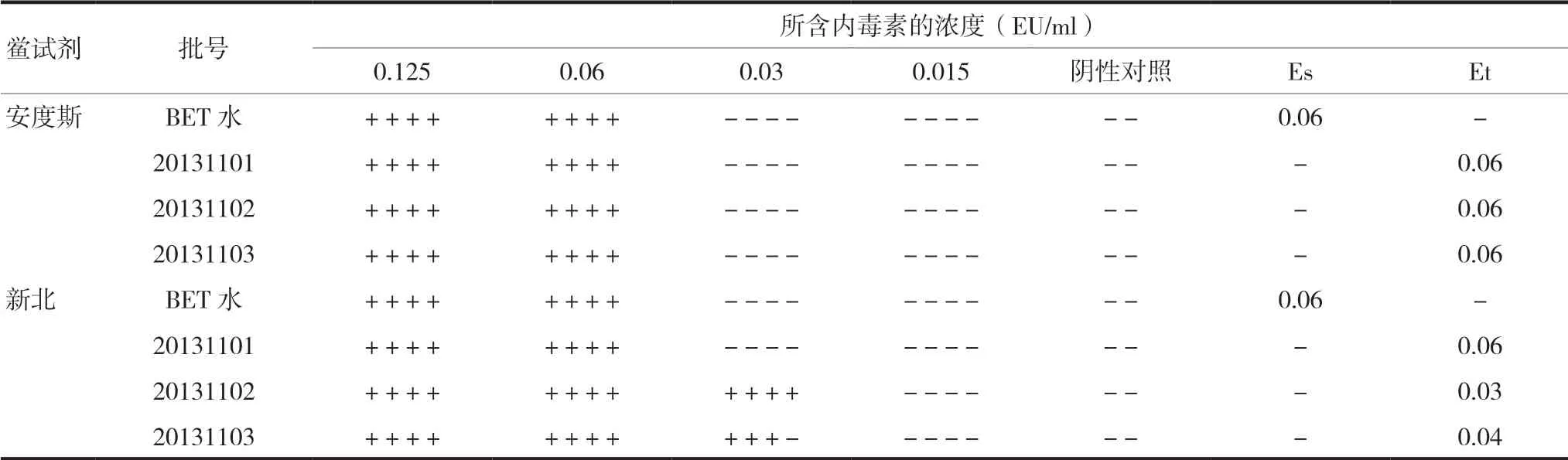
表5 依托泊苷脂质微球注射液的干扰实验结果(λ=0.06 EU/ml)
2.2.5 细菌内毒素检查样品细菌内毒素限值拟定为:每1 mg依托泊苷脂质微球注射液中含内毒素的量应小于2 EU。按《中华人民共和国药典》2015年版四部通则中“1143细菌内毒素检查法”[7]进行检查。使用鲎试剂的灵敏度为0.06 EU/ml,样品浓度为0.03 mg/ml稀释液,阴性对照为BET水,阳性对照为0.125 EU/ml内毒素溶液,样品阳性对照是以样品0.03 mg/ml浓度稀释液来稀释0.125 EU/ml的内毒素溶液,样品加完后,注意轻轻混匀,37℃±1℃保温1 h并记录实验结果。见表6。结果表明,按照拟定标准检验,三批依托泊苷脂质微球注射液细菌内毒素检查均符合设定限值规定。

表6 依托泊苷脂质微球注射液细菌内毒素检查结果(安度斯λ=0.06 EU/ml)
3 讨论
参照《中华人民共和国药典》2015年版四部通则中“9301注射剂安全性检查法应用指导原则”[8],热原检查限值参照临床使用剂量计算,对于重症用药、需联合用药的药品,一般为人用每千克体重每小时最大给予供试品剂量的2~5倍。依托泊苷脂质微球注射液适用于与其他抗肿瘤药物如顺铂等合用,治疗支气管肺癌及睾丸癌。也可用于恶性淋巴瘤、急性非淋巴细胞性白血病、尤文氏癌和消化道恶性肿瘤的联合化疗。故热原检查试验剂量设定为8 ml/kg,相当于临床人用剂量的2倍,从严保障临床用药安全性。
预实验时直接使用BET水稀释依托泊苷脂质微球注射液进行干扰预实验,但从结果来看样品稀释液对鲎试剂有增强型的干扰作用。故参照文献[9]实验方法,以60%乙醇溶液溶解本品,再进行细菌内毒素检查。具体操作使用0.67 ml 60%乙醇溶液加入1 ml样品原液,振荡5 min。接下来按照一般样品稀释步骤进行,即保证乙醇溶液终体积分数为1.25%。本品内毒素限值拟定为计算限值,即2 EU/mg,三批样品的内毒素检查结果均符合制定限值规定。但本品有干扰作用,需用60%乙醇溶解本品,同时鲎试剂中含有多种蛋白质,而乙醇则使蛋白质变性,从而干扰鲎试剂与内毒素产生凝胶反应[10],这就决定了供试品中乙醇含量不能过高,且还需选用高灵敏度的鲎试剂才能排除干扰。
因各生产企业在鲎试剂生产过程中原料、工艺、批次、质量控制等方面的不同,本实验前期选用不同品牌鲎试剂进行了预实验,结果发现本研究使用的两家鲎试剂干扰较小,适用于该品种的检查。
和传统热原检查法相比较[11-14],细菌内毒素检查法因其具有多种优点而被各国药典采用,并逐步替代家兔热原检查法控制注射剂内毒素的相关安全性。现在已经有越来越多的药品施行细菌内毒素检查。但与此同时,某些中药、抗生素、生物制品、氨基酸相关注射剂、医疗器械等品种,因其与内毒素产生的致热协同反应或干扰作用或因样品材料的特殊、复杂性,仍需使用家兔法对特殊样品进行热原控制[15]。
依托泊苷为植物成分鬼臼毒素的衍生物,临床上主要用于小细胞肺癌、恶性生殖细胞瘤、恶性淋巴瘤、白血病等癌症的治疗。其具有广谱抗癌症活性及较高的治疗指数,尤其对小细胞肺癌的治疗效果非常好,能提高2年生存率并改善患者生存质量。但依托泊苷在临床使用过程中最常见不良反应为Ⅲ~Ⅳ度血液学不良反应、发热及感染,成因主要是药理作用通过抑制拓扑异构酶Ⅱ,导致DNA结构被破坏造成永久损伤,引发肿瘤细胞凋亡而起到治疗作用。故骨髓抑制为药物的主要毒性,其中嗜中性白细胞会显著减少。而肝脏、肾脏、心脏及神经系统的不良反应比较少[16]。需要严格控制药品质量,以排除因药品质量问题引起的发热反应,保证临床用药安全。以目前对依托泊苷脂质微球的研究发展程度来看,以后必然会出现越来越多相关制剂,本研究尽早制订其热原、内毒素标准,为以后该品种的发展尽一份绵薄之力。

