化学模式识别结合HPLC指纹图谱的僵蚕质量评价研究
王 梅,万子玉,陈 辉,张德林,喻 文,李 敏*,肖 禾
1成都中医药大学 中药材标准化教育部重点实验室,成都 611137;2四川广元岷江中药材种植有限责任公司,广元 628000
僵蚕为临床常用大宗动物药之一,主要用于治疗肝风夹痰,惊痫抽搐,小儿急惊,破伤风等疾病[1],其来源为蚕蛾科昆虫家蚕BombyxmoriLinnaeus 4~5龄的幼虫感染白僵菌Beauveriabassiana(Bals.)Vuillant 而致死的干燥体。化学研究表明其主要活性成分为蛋白质、氨基酸类、黄酮类等成分[2]。现代药理研究表明僵蚕富蛋白提取物具有抗癫痫[3]、免疫调节及抑制E.G7荷瘤小鼠的肿瘤生长有增强的保护作用[4]、促进MPTP诱导的帕金森病小鼠的运动受损的恢复,防止多巴胺的耗竭等等。
作为食性单一的家蚕,其仅以桑为食的特点决定了家蚕体内对桑叶主要的黄酮类成分的吸收、转化和代谢的丰富多样。研究表明白僵菌感染家蚕后,在其体内对黄酮类成分进行了生物转化,例如将槲皮素和山奈酚等黄酮类物质进行4-O-甲基葡萄糖苷化反应转化成槲皮素-7-O-β-D-4-O-甲基葡萄糖苷和山奈酚-7-O-β-D-4-O-甲基葡萄糖苷等[4]。Xing等[5]研究发现,随着僵死时间的延长,其体内黄酮化合物的含量和转化也不同,并推测出槲皮素-7-O-β-D-4-O-甲基葡萄糖苷和山奈酚-7-O-β-D-4-O-甲基葡萄糖苷可作为其质量控制指标之一。由此,黄酮类化合物可作为僵蚕质量评价的重要指标。
指纹图谱结合化学模式识别是评价中药材质量的有效手段,已广泛应用于中药材、中药饮片、配方颗粒等的质量评价[6-8]。目前针对僵蚕开展的相关指纹图谱研究多样,包括紫外指纹、红外指纹[9]、HPLC[10,11]、HPCE[12]以及蛋白指纹图谱[13,14]等,其成分类别涵盖了水溶性成分、脂溶性成分、醇溶性成分等。但均存在分离效果不佳,指认峰较少的问题,难以表征其质量特征。有研究者表明川产僵蚕质较优[15],白僵菌素含量较于广西、云南、浙江等产地高[16,17]。虽然目前针对僵蚕化学成分和质量控制已有部分研究报道,但因其成分复杂、含量较低,尚无较好的质量控制手段。因此,本研究采用高效液相色谱法建立20批次不同产地的僵蚕药材指纹图谱,并结合相似度分析、聚类分析、主成分分析等化学识别模式展开区分研究,并参照《中国药典》2020年版一部僵蚕项下要求测定其水分、总灰分、酸不溶性灰分、浸出物,采用课题组前期方法测定有效成分白僵菌素含量,旨在综合评价不同产地药材质量,为僵蚕药材质量控制和标准完善提供科学依据,同时为其他药材的研究提供借鉴。
1 实验仪器与材料
1.1 仪器
Agilent 1200 HPLC高效液相色谱仪;BP-121s精密电子天平(十万分之一,浙江精密仪器有限公司);BS-200S-WEI精密电子天平(千分之一,北京赛多利斯仪器系统有限公司);KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2 试剂与材料
对照品:芦丁(批号:100080-20070,中国食品药品检定研究院);金丝桃苷(批号:111521-200303,中国食品药品检定研究院);槲皮素(批号:100081-200907,中国食品药品检定研究院);山奈酚(批号:MUST-16102605,成都曼思特生物科技有限公司);紫云英苷(PS1099-0010MG,成都普斯生物科技有限公司);白僵菌素(批号:L280Q50,北京百灵威科技有限公司)纯度均大于98%。
乙腈、磷酸均为色谱纯;甲醇为分析纯;水为超纯水。
20批僵蚕药材信息见表1。经成都中医药大学中药鉴定教研室李敏教授鉴定为蚕蛾科昆虫家蚕BombyxmoriLinnaeus 4~5龄的幼虫感染(或人工接种)白僵菌Beauveriabassiana(Bals.)Vuillant而致死的干燥体。

表1 样品信息Table 1 Sample information

续表1(Continued Tab.1)
2 方法与结果
2.1 HPLC指纹图谱建立
2.1.1 样品制备
取僵蚕粉末(过四号筛)约2 g,精密称定,置具塞锥形瓶中,精密加入80%甲醇20 mL,称定质量,超声提取(功率250 W,频率100 kHz)30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,用0.45 μm微孔滤膜过滤即得。
2.1.2 对照品溶液制备
取芦丁、金丝桃苷、槲皮素、山奈酚对照品适量,精密称定,加甲醇制成混合对照品溶液,即得。
2.1.3 色谱条件
色谱柱为 Insertsil ODS-3(4.6 mm×250 mm,5 μm);流动相为乙腈(A)-0.1%磷酸溶液(B);柱温30 ℃;检测波长为365 nm;进样量10 μL;流速为0.8 mL/min;梯度洗脱程序:0~10 min(10%→20%A);10~30 min(20%→35%A);30~35 min(35%→95% A);35~55 min(95%A);55~60 min(95%→10%A)。
2.2 指纹图谱的方法学考察
2.2.1 精密度考察
取同一份僵蚕粉末,按照“2.1.1”项下方法制备供试品溶液,连续进样5次,记录液相色谱图。以芦丁为参照峰,计算主要共有色谱峰的相对保留时间的RSD的范围为0.12%~1.56%,相对峰面积RSD范围为0.36%~1.12%,表明仪器精密度良好。
2.2.2 稳定性
取同一份僵蚕样品,按照“2.1.1”项下方法制备供试品溶液,在室温下放置,分别于0、2、4、8、12、24 h进行检测,记录液相色谱图。结果表明,僵蚕主要色谱峰的相对保留时间的RSD的范围为0.23%~1.35%,共有峰的峰面积RSD范围为0.61%~1.27%,表明供试品溶液在24 h内稳定。
2.2.3 重复性考察
取同一份僵蚕样品,按照“2.1.1”项下方法制备6份供试品溶液进行检测。结果表明,僵蚕主要色谱峰的相对保留时间的RSD的范围为0.05%~1.12%,共有峰的峰面积RSD范围为0.08%~1.45%,说明该方法重现性好。
2.3 指纹图谱的生成
20批僵蚕药材按照样品制备方法制备,再按“2.1.3”项下色谱条件进样测定,记录液相色谱图。采用中药色谱指纹图谱相似度评价软件(2012版),以S1为参照图谱,采用中位数法,时间窗宽度为0.1 min,建立对照图谱,运用多点校正Mark峰匹配,建立20批僵蚕药材的指纹图谱,结果见图1。

图1 20批僵蚕药材指纹图谱Fig.1 Fingerprint of 20 batches Bombyx Batryticatus
2.3.1 共有峰的指认
从20批僵蚕药材中标定了9个共有峰,通过与对照品比对,指认出5个成分,分别是1号峰为芦丁,2号峰为金丝桃苷,4号峰为紫云英苷,6号峰为槲皮素,7号峰为山奈酚。混合对照品溶液的HPLC图谱见图2。

图2 对照品指认图Fig.2 Reference standards identification of fingerprint
2.3.2 相似度分析
采用中药色谱指纹图谱相似度评价软件(2012版)软件建立20批僵蚕药材的指纹图谱,其相似度评价结果见表2。结果显示相较于对照指纹图谱,所有样品相似度在0.92~0.99之间,均大于0.90,不同产区药材相似度均较好。

表2 20批僵蚕药材相似度结果Table 2 Similarity evaluation results of 20 batches of samples
2.3.3 聚类分析
以5个指认共有峰峰面积为变量,导入SPSS 22.0软件,采用平均联接法,选择平方欧氏距离为测度对其进行系统聚类分析。聚类分析结果见图3,当判别距离为7.5时,可将其分为3类。其中,来自四川广元产区的样品S1~S4可聚为一类,来自四川省中药饮片有限责任公司的样品S5~S11可聚为一类,来自不同药材市场的可聚为一类。说明不同厂家生产的药材质量有差异,且同一产区质量相对稳定,而市场流通的僵蚕药材来源相似,可能主要为自然染病僵蚕或质量差异较大。
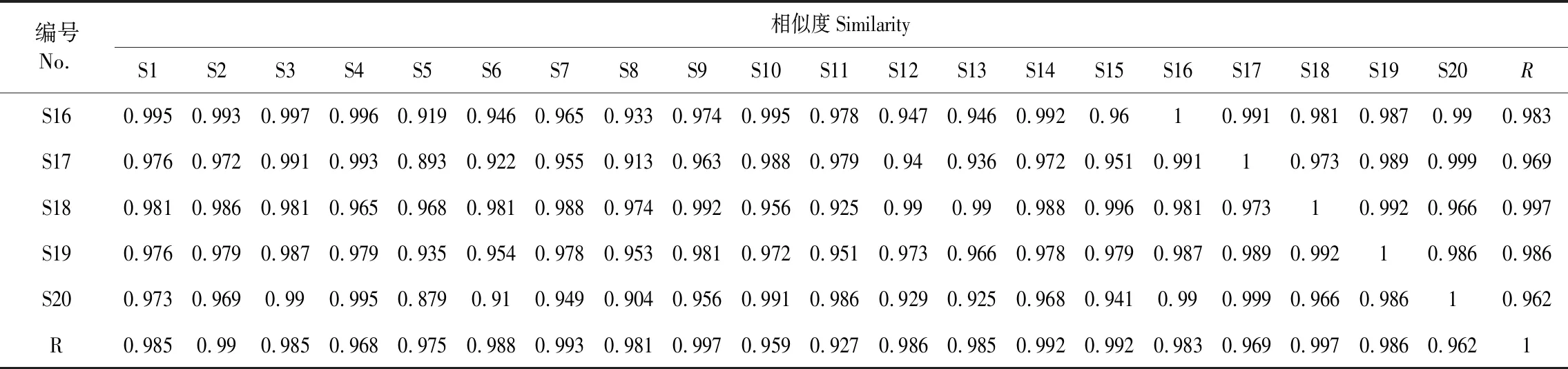
续表2(Continued Tab.2)

图3 20批僵蚕药材的聚类分析谱系图Fig.3 Cluster family correlationgship of 20 batches of samples
2.3.4 主成分分析(PCA)
利用SPSS 22.0软件对数据进行主成分分析,由特征值大于1且贡献率大于70%的标准来看,前2个特征值均大于1(见图4),累计贡献率大于85%,即提取的2个主成分包含了9个共有成分的89.221%的信息,符合主成分分析条件,结果见表3。采用SIMCA 14.1软件,以20批次僵蚕样品的共有峰峰面积为数据阵,对不同产区的药材进行主成分分析,得分图如图5所示,与聚类分析结果一致。因此,在指纹图谱的基础上,利用聚类分析和主成分分析可以进一步对不同产区药材进行区分。
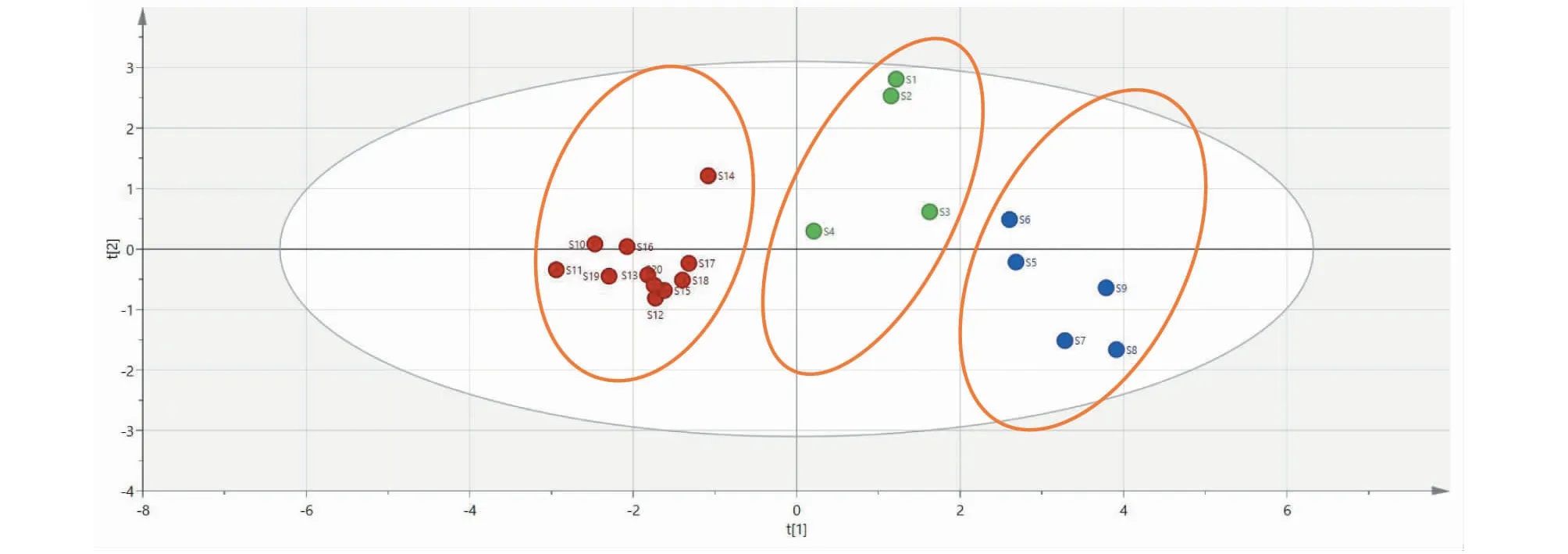
图5 20批僵蚕药材的PCA得分图Fig.5 PCA scores of 20 batches of samples

图4 20批僵蚕药材的主成分分析碎石图Fig.4 Principal component analysis of 20 batches of samples
2.4 质量评价
僵蚕药材水分、浸出物、总灰分、酸不溶性灰分参照《中国药典》2020年版[1]一部僵蚕项下进行测定,白僵菌素含量参照课题组前期方法[18]进行。
2.4.1 性状测定
参照《中国药典》2020年一部僵蚕项下性状描述对僵蚕药材的形状、表面、断面进行评分量化。评分细则如下,形状:条顺直或略弯曲、形体饱满:9~10分;条弯曲、形体饱满:7~8分;条弯曲、形体皱缩:5~6分;条弯曲皱缩、形体干瘪0~4分。断面:亮棕色或亮黑色的丝腺环多4个:10分;亮棕色或亮黑色的丝腺环2~4个:8~9分;亮棕色或亮黑色的丝腺环2~3个:6~7分;亮棕色或亮黑色的丝腺环多2个:6分;无亮棕色或亮黑色的丝腺环:5分。20批僵蚕药材性状测定及评分结果见表4。

表4 20批僵蚕药材外观性状观测结果Table 4 Observation results of appearance characters of 20 batches of s,n =50)

续表4(Continued Tab.4)
2.4.2 水分、总灰分、酸不溶性灰分、浸出物、白僵菌素含量的测定
由表5可知,20批药材的水分、酸不溶性灰分、浸出物均符合药典要求。S11、S12、S13、S16、S18总灰分不合格,超过药典标准,说明市场药材质量参差不齐,尤以石灰包裹家蚕、死蚕等伪劣品较多,总灰分超标严重。此外,白僵菌素作为僵蚕抗惊厥的有效成分之一,规范化生产所得药材(S1~S9)白僵菌素平均含量(0.026 7%)大于市场药材(S10~S20)白僵菌素平均含量(0.025%),不同市场的白僵菌素含量以荷花池药材市场药材大于其他药材市场,荷花池药材市场药材主要产地为四川,这与Shi等[15]的研究结果“四川产者较优”一致。

表5 20批僵蚕药材水分、总灰分、酸不溶性灰分、浸出物、白僵菌素含量的测定结果Table 5 Determination results of moisture,total ash,acid-insoluble ash,extract and beauvericin of 20 batches of =3)
2.5 相关性分析
将20批药材性状(形状、长度、直径、重量、断面特征)、总灰分、酸不溶性灰分、浸出物、白僵菌素含量、9个共有峰峰面积进行相关性分析,结果如图6所示。所有共有峰与药材长度、表面性状、重量呈正相关,1号峰~7号峰均与药材断面性状正相关,说明该指纹图谱能有效反映出药材的性状特征;3号峰、5号峰、6号峰、7号峰、8号峰、9号峰与药材总灰分、浸出物呈负相关,总灰分与浸出物呈正相关,且药材总灰分越高,劣质品和掺伪品比例越大,不符合药典要求。综上,本文所建立的指纹图谱能一定程度反映出药材的性状特征、质量优劣。

图6 相关性分析图Fig.6 Correlation analysis diagram注:1~9为1~9号峰峰面积;10-水分;11-总灰分;12-酸不溶性灰分;13-浸出物;14-白僵菌素含量;15-形状评分;16-长度;17-直径;18-断面评分;19-重量。Note:1~9:No.1~No.9 peak area;10-Moisture;11-Total ash;12-Acid-insoluble ash;13-Extract;14-Beauvericin content;15-Shape score;16-Length;17-Diameter;18-Section score;19-Weight.
3 讨论与结论
本实验分别考察了提取方法、提取溶剂、提取时间等前处理条件,确定了提取方法(回流提取、超声提取)以超声提取最佳,提取溶剂(甲醇、80%甲醇、乙腈和水)以80%甲醇最佳,提取时间(15、30、45 min)以30 min最优。所建立的僵蚕指纹图谱,其相似度在0.92~0.99之间,相似度较高,为僵蚕的质量评价提供依据。
本研究所建立的指纹图谱主要针对于僵蚕药材的黄酮类成分,Wang等[19]采用网络药理学和分子对接技术研究结果表明槲皮素、山奈酚等成分可能为僵蚕息风止痉的主要物质基础成分。多项研究[20,21]也表明槲皮素、山奈酚为治疗癫痫的主要药效成分之一,僵蚕作为息风止痉要药,其作用物质基础之一可能为黄酮类成分。此外,本研究还将各共有峰峰面积与药材的性状、浸出物、总灰分、白僵菌素含量进行了相关性分析,结果表明断面性状与表面性状、药材长度、白僵菌素含量正相关,与峰1号峰、2号峰、3号峰、4号峰、6号峰、7号峰峰面积正相关,1号峰、2号峰、4号峰、6号峰、7号峰经比对指认分别为芦丁、金丝桃苷、紫云英苷、槲皮素、山奈酚,均为桑叶中主要的黄酮类成分,说明僵蚕形成过程中黄酮类成分的转化与断面“玻璃体”等药材品质形成具有较强的相关性,也印证了自古以来“僵蚕以色白、条直、断面黑亮者为佳”的品质特征点。
综上,本文所建立的指纹图谱不仅包含了僵蚕“息风止痉”药效可能的物质基础成分,还与僵蚕药材本身质量品质指标具有一定的相关性,能综合体现僵蚕药材的质量,为僵蚕药材的质量控制提供科学依据。在对僵蚕药材的质量控制标准中,应充分考虑到其本身为“菌-虫-叶”的复合体,采用多指标综合评价其质量,建立更为科学合理的药材质量标准。

