蓍草化学成分研究
赵晨光,薛金凤,马睿骁,梁旭博,杜 锟,司盈盈,冯卫生*,薛贵民*
1河南中医药大学药学院;2河南省中药开发工程技术研究中心,郑州450046
蓍属(Achillea)(菊科)约有200种,广泛分布于北温带,我国产有10种,如今从中分离得到的化合物主要有倍半萜、黄酮、木脂素等[1,2]。现代药理学研究表明该属植物具有显著的抗炎[1]、降糖活性[3,4]。蓍草为菊科植物蓍AchilleaalpineL的地上干燥部位,又名一支蒿、高山蓍、千条蜈蚣等。蓍草味苦、酸、性平,归肺、脾、膀胱经。具有解毒利湿、活血化瘀的功能[5]。复方“蓍草散”能有效的改善溃疡病的胃酸[6]。在民间蓍草也常用来清热解毒[7]。《中华本草》中描述蓍草具有不错的抗炎、解热镇痛等活性。主要分布于我国西南的云南,西北的甘肃,华北的河南,山西等地,夏、秋两季开花时采割[8]。现代药理学研究表明蓍草中化学成分具有显著的抗炎活性,还有抗氧化、抗病毒、解痉挛及治疗胃溃疡等作用[9-12],但是如今缺少对该植物系统的化学成分及相关药理学研究。现仅报道了少量的倍半萜、生物碱以及挥发油等[13,14]。因此,为了进一步了解蓍草的物质基础,提高其资源综合利用效率,本文对蓍草95%乙醇部位的化学成分进行了分离纯化和结构鉴定,并测试了分离化合物的活性,以期发现具有抗胃癌作用的先导化合物。
1 材料与方法
1.1 仪器与材料
预制硅胶薄层G板(10~40 μm青岛海洋化工厂);大孔树脂Diaion HP-20(日本三菱化学);ODS(40~60 μm,YMC);Sephadex LH-20(40~70 μm,Amersham Pharmacia Biotech AB,Uppsala,瑞士);LC-52型高压制备液相色谱仪(赛谱锐思(北京)科技有限公司);Bruker AVANCE 500核磁共振仪(TMS为内标)Bruker maxis HD型飞行时间质谱仪(德国Bruker公司);SCIEX Qtrap 5500质谱仪(美国应用生物系统公司),所用分析纯和色谱纯试剂为天津恒兴和天津四友精细化学有限公司生产。显色剂:10%浓硫酸乙醇,同时结合紫外灯(254 nm)观察。
2020年5月15日购买自于云南省昆明市,经河南中医药大学董诚明教授鉴定为AchilleaalpineL的地上干燥部位,标本(20200515)收藏于河南中医药大学天然产物研究室。
1.2 实验方法
1.2.1 提取分离
蓍草(800 g)用95%乙醇超声提取,滤过,将提取液减压浓缩得浸膏50 g。将所得浸膏用甲醇溶解,与大孔树脂材料(Diaion HP-20)进行拌样(1∶1),然后装载于大孔树脂填料上方,依次用10%、30%、60%、75%、95%的乙醇/水梯度洗脱,一共得到5个馏分,分别为Fr.1~Fr.5。对这五个馏分进行分析液相分析,根据液相结果,将Fr.3与Fr.4合并,并命名为A1组分。将A1组分过Sephadex LH-20处理,以甲醇为流动相得3个组分(A1-1、A1-2、A1-3)。将组分A1-2进行ODS色谱柱处理,用甲醇/水梯度洗脱得到15个馏分(A1-2-1~A1-2-15)。组分A1-2-7经半制备液相(54%乙腈/水)得到化合物2(tR=24.1 min,4.8 mg)。组分A1-2-9经半制备液相(56%乙腈/水)得到化合物3(tR=32.5 min,5.7 mg)。组分A1-2-7以40%→90%乙腈梯度洗脱经半制备液相制备得到化合物1(tR=41.2 min,2.4 mg)和4(tR=48.6 min,3.7 mg)。组分A1-2-11经半制备液相70%乙腈/水等度洗脱制备得化合物5(tR=35.0 min,5.7 mg)和6(tR=40.2 min,1.8 mg)。将A1-3组分进行ODS色谱柱处理,用10%→100%甲醇/水梯度洗脱得到20个馏分依次为A1-3-1至A1-3-20。组分A1-3-11经半制备液相(10%→80%乙腈/水)得到化合物7(tR=43.2 min,2.6 mg)。组分A1-3-13经半制备液相(20%→80%乙腈/水)得到化合物8(tR=45.2 min,1.8 mg)。组分A1-3-16以60%→100%乙腈/水为流动相经半制备液相制备得到化合物9(tR=29.1 min,5.4 mg)和10(tR=35.2 min,4.7 mg)。组分A1-3-17经半制备液相(65%→100%乙腈/水)制备得到化合物11(tR=35.6 min,4.2 mg)。组分A1-3-14经半制备液相采用70%甲醇等度洗脱制备得化合物12(tR=30.5 min,2.4 mg)。
将Fr.2命名为A2组分,将A2组分进行Sephadex LH-20处理,经合并共得到5个组分(A2-1~A2-5)。其中组分A2-3进行ODS色谱柱处理,用10%→100%甲醇/水梯度洗脱,共得到17个组分(A2-3-1~A2-3-17)。组分A2-3-7经半制备液相制备(35%甲醇/水)得到化合物13(tR=20.2 min,8.2 mg)。组分A2-3-8经半制备液相以20%→85%甲醇/水梯度洗脱得到化合物14(tR=30.0 min,12.7 mg)。组分A2-3-3经半制备液相制备(10%→70%甲醇/水)得到化合物15(tR=29.2 min,7.9 mg)。组分A2-3-12经半制备液相以35%乙腈/水等度洗脱得到化合物16(tR=35.3 min,9.0 mg)。
1.2.2 细胞毒活性筛选
分别取对数生长期的四种不同的人胃癌细胞MGC-803、MKN-45、HGC-27和AGS细胞,用0.25%胰酶消化离心后用完全培养基稀释,用细胞计数仪计数后,调整细胞密度为5.0×103个/孔,然后每孔190 μL接种于96孔培养板中,在培养箱中培养过夜,加入配置好的化合物1~11和阳性药5-氟尿嘧啶溶液继续培养48 h。然后每孔再加入配置好的MTT溶液(浓度为5 mg/mL),置于CO2培养箱37 ℃孵育,孵育4 h后弃去培养液。最后每孔加入150 μL DMSO,振荡10 min,用酶标仪检测。在570 nm检测波长(参比波长:630 nm)下测定每个孔的OD值,计算不同浓度的药物对细胞的抑制率,实验重复3次。抑制率的计算公式为:抑制率=(1-OD加药组/OD空白组)× l00%。
2 结果
2.1 结构鉴定
化合物1~16的化学结构见图1。

图1 化合物1~16的化学结构Fig.1 The chemical structures of compounds 1-16
化合物1黄色油状(甲醇),易溶于甲醇、氯仿。HR-ESI-MS测定其准分子离子峰为m/z182.154 1 [M+H]+(Calcd for C11H20NO,182.154 5),结合13C NMR谱图分析,确定其分子式为C11H19NO,不饱和度为3。其紫外吸收为UV(MeOH)λmax262 nm(3.49)。IR光谱显示该化合物含有-NH2吸收峰(3 397 cm-1)以及酰胺羰基(1 634 cm-1)的伸缩振动吸收峰。根据蓍草中已报道化学成分,其结构中含有氮原子,推测其应为酰胺类结构[15]。1H NMR图谱可以明显看出1个甲基氢信号δH0.89(3H,t);2组烯氢信号δH:6.25(1H,d,J=15.0 Hz),7.22(1H,dd,J=15.0,10.5 Hz,H-3)和δH6.17(1H,dd,J=15.0,10.5 Hz),6.06(1H,m)(表1),根据其偶合常数以及查阅相关文献[15]可以判断出有两个共轭的反式双键。13C NMR图谱显示其含有11个碳信号,结合HSQC谱图其分别归属为4个次甲基(皆为烯碳δC118.7、143.0、129.0、142.7),5个亚甲基(δC22.6、31.5、24.8、28.7、33.1),1个甲基(δC14.2),1个酰胺羰基(δC165.9)信号(表1)。该化合物结构可进一步由HMBC谱图确定。在HMBC谱(图2)中,显示H-2(δH6.25,1H,d,J=15.0 Hz)与C-1(δC165.9),C-3(δC143.0),C-4(δC129.0)相关,H-3(δH7.22)和C-5(δC142.7)、C-4(δC129.0)、C-2(δC118.7)、C-1(δC165.9),H-4(δH6.17)和C-3、C-2相关,H-5(δH6.06)和C-4,C-3相关说明两个双键相连且与羰基共轭。H-6(δH2.14)与C-5,C-6(δC33.1),H-7(δH1.44)与C-5,以及H-5(δH6.06)与C-6,C-7(δC28.7)存在HMBC相关,说明6与7位是5位相连的亚甲基信号。H-11(δH0.89)位甲基信号与亚甲基碳C-10(δC22.6)和C-9(δC31.5)相关,H-9(δH1.31)与亚甲基碳C-8(δC24.8)和C-10,H-8(δH1.67)与C-7和C-8存在HMBC相关信号,确定C-6至C-11位为6个碳连接形成的饱和碳链。根据以上结果,最终确定新化合物1为一个6个饱和碳链与两个共轭双键相连形成酰胺类化学成分,结构如图2所示。该化合物命名为(2E,4E)-N-(2-methylbutyl)deca-2,4-dienamide。化合物1的详细结构鉴定数据原始图谱可从本刊官网免费下载(www.trcw.ac.cn)。

表1 化合物1的1H NMR和13C NMR数据(500和125 MHz,CDCl3)Table 1 1H NMR and 13C NMR spectroscopic data for compound 1 (500 and 125 MHz,CDCl3)
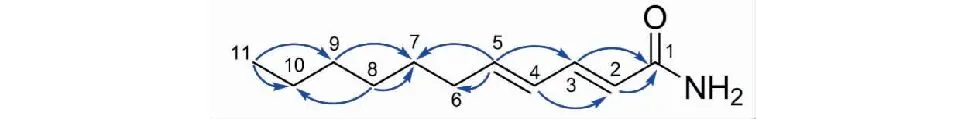
图2 化合物1的结构及关键HMBC相关信号Fig.2 The structure and key HMBC correlations of compound 1
化合物2白色晶体(甲醇);ESI-MS:m/z224.20[M+H]+;1H NMR(500 MHz,CDCl3)δ:5.75(1H,J=15.0 Hz,H-2),7.18(1H,dd,J=15.0,10.0 Hz,H-3),6.12(1H,dd,J=15.0,10.0 Hz,H-4),6.07(1H,dt,J=14.0,7.5 Hz,H-5),2.14(2H,dd,J=14.0,7.0 Hz,H-6),1.41(2H,dd,J=14.0,7.0 Hz,H-7),1.30(4H,m,H-8,H-9),0.86(3H,t,J=6.5 Hz,H-10),3.16(2H,t,J=6.5 Hz,H-1′),1.79(1H,tt,J=13.5,6.5 Hz,H-2′),0.92(6H,t,J=6.5 Hz,H-3′,H-4′),5.52(1H,br s,-NH);13C NMR(125 MHz,CDCl3)δ:166.4(C-1),121.6(C-2),143.5(C-3),128.6(C-4),141.7(C-5),32.8(C-6),31.5(C-7),28.3(C-8),22.2(C-9),14.0(C-10),47.0(C-1′),28.7(C-2′),20.1(C-3′),20.1(C-4′)。以上数据与文献[15]报道一致,故鉴定化合物2为墙草碱。
化合物3白色晶体(甲醇);EI-MS:m/z221.18[M]+;1H NMR(500 MHz,CDCl3)δ:5.75(1H,d,J=15.0 Hz,H-2),7.19(1H,dd,J=15.0,10.5 Hz,H-3),6.15(1H,dd,J=15.0,10.5 Hz,H-4),6.08(1H,m,H-5),2.28~2.10(4H,m,H-6,H-7),5.36(1H,dd,J=16.0,7.0 Hz,H-8),5.50(1H,m,H-9),1.60(3H,d,J=6.0 Hz,H-10),3.17(2H,t,J=6.5 Hz,H-1′),1.79(1H,tt,J=13.5,6.5 Hz,H-2′),0.92(6H,t,J=6.5 Hz,H-3′,H-4′),5.52(1H,brs,-NH);13C NMR(125 MHz,CDCl3)δ:166.4(C-1),122.1(C-2),141.3(C-3),128.6(C-4),142.4(C-5),32.9(C-6),26.3(C-7),129.3(C-8),124.8(C-9),12.9(C-10),47.0(C-1′),28.37(C-2′),20.2(C-3′),20.2(C-4′)。以上数据与文献[15]报道一致,故鉴定化合物3为(E,E,Z)-2,4,8-decatrienoicacid isobutylamide-8,9-dehydropellitorine。
化合物4无色油状(甲醇);EI-MS:m/z237.20[M]+;1H NMR(500 MHz,CDCl3)δ:5.74(1H,d,J=15.0 Hz,H-2),7.19(1H,dd,J=14.5,10.0 Hz,H-3),6.10(1H,dd,J=15.5,10.0 Hz,H-4),6.06(1H,dd,J=15.0,7.5 Hz,H-5),2.29(2H,m,H-6),1.40(2H,m,H-7),1.29(4H,m,H-8,H-9),0.89(3H,t,J=10.0 Hz,H-10),3.15(1H,m,H-1′),3.26(1H,m,H-1′),1.59(1H,m,H-2′),0.92(3H,d,J=6.5 Hz,H-3′),1.15(2H,m,H-4′),0.91(3H,dd,J=7.5,6.5 Hz,H-5′),5.43(1H,br s,-NH);13C NMR(125 MHz,CDCl3)δ:166.6(C-1),121.8(C-2),141.5(C-3),128.3(C-4),143.4(C-5),33.1(C-6),28.6(C-7),31.5(C-8),22.6(C-9),14.2(C-10),45.3(C-1′),35.2(C-2′),27.1(C-3′),11.4(C-4′),17.3(C-5′)。以上数据与文献[16]报道一致,故鉴定化合物4为N-2′-methylbutyl-(E,E)2,4-decadienam。
化合物5黄色油状(甲醇);EI-MS:m/z308.23[M]+;1H NMR(500 MHz,CDCl3)δ:2.28(2H,t,J=7.5 Hz,H-2),1.59(2H,m,H-3),1.28(6H,m,H-4,H-5,H-6),1.59(2H,m,H-7),2.50(2H,t,J=7.5 Hz,H-8),6.05(1H,d,J=15.5 Hz,H-10),7.10(1H,m,H-11),6.17(1H,m,H-12),6.14(1H,m,H-13),2.14(2H,dd,J=12.5,7.5 Hz,H-14),1.34(2H,m,H-15),1.28(4H,m,H-16,H-17),0.87(3H,t,J=7.0 Hz,H-18),3.64(3H,s,-OCH3);13C NMR(125 MHz,CD3OD)δ:174.4(C-1),34.2(C-2),25.0(C-3),29.1(C-4),29.2(C-5),29.2(C-6),24.3(C-7),40.7(C-8),201.3(C-9),128.1(C-10),143.0(C-11),129.1(C-12),145.6(C-13),33.2(C-14),28.7(C-15),31.6(C-16),22.6(C-17),14.1(C-18),51.6(-OCH3)。以上数据与文献[17]报道一致,故鉴定化合物5为methyl(E,E)10,12-9-oxooctadeca-10,12-dienoate。
化合物6黄色油状(甲醇);EI-MS:m/z308.23[M]+;1H NMR(500 MHz,CDCl3)δ:2.29(2H,t,J=7.5 Hz,H-2),1.61(2H,m,H-3),1.31(6H,m,H-4,H-5,H-6),1.61(2H,m,H-7),2.52(2H,t,J=7.5 Hz,H-8),6.07(1H,d,J=15.5 Hz,H-10),7.13(1H,dd,J=15.5,6.5 Hz,H-11),6.17(4H,m,H-12,H-13),2.17(2H,dd,J=12.5,7.0 Hz,H-14),1.46(2H,m,H-15),1.31(4H,m,H-16,H-17),0.89(3H,t,J=7.0 Hz,H-18),3.66(3H,s,-OCH3);13C NMR(125 MHz,CD3OD)δ:174.4(C-1),34.2(C-2),25.0(C-3),29.1(C-4),29.2(C-5),29.3(C-6),24.5(C-7),40.6(C-8),201.2(C-9),128.0(C-10),143.1(C-11),129.0(C-12),145.8(C-13),33.2(C-14),28.5(C-15),31.5(C-16),22.6(C-17),14.1(C-18),51.6(-OCH3)。以上数据与文献[18]报道一致,故鉴定化合物6为(S)-14-(E,E)-10,12-methyl-14-hydroxy-9-oxo-octadeca-10,12-dienoate。
化合物7淡黄色油状物(甲醇);EI-MS:m/z229.15[M]+;1H NMR(500 MHz,CDCl3)δ:5.80(1H,d,J=15.0 Hz,H-2),7.18(1H,dd,J=15.0,11.0 Hz,H-3),6.20(1H,dd,J=15.0,11.0 Hz,H-4),6.07(1H,dt,J=15.0,7.0 Hz,H-5),2.39(4H,m,H-6,H-7),1.98(3H,s,H-11),3.15(2H,m,H-1′),1.80(1H,m,H-2′),0.93(6H,d,J=7.0 Hz,H-3′,H-4′),5.49(1H,br s,-NH);13C NMR(125 MHz,CDCl3)δ:166.2(C-1),123.3(C-2),140.6(C-3),129.9(C-4),139.2(C-5),31.4(C-6),19.0(C-7),77.0(C-8),65.6(C-9),65.2(C-10),68.4(C-11),47.1(C-1′),28.8(C-2′),20.3(C-3′),20.3(C-4′)。以上数据与文献[15]报道一致,故鉴定化合物7为(E,E)-2,4-undecadiene-8,10-diynnoic acid isobutylamide。
化合物8粉色羽状(甲醇);EI-MS:m/z287.19[M]+;1H NMR(500 MHz,CDCl3)δ:5.69(1H,d,J=15.0 Hz,H-2),7.19(1H,dd,J=15.0,9.5 Hz,H-3),6.10(1H,dd,J=15.0,9.5 Hz,H-4),6.06(1H,dt,J=15.0,7.0 Hz,H-5),2.13(2H,m,H-6),1.39(2H,m,H-7),1.28(4H,m,H-8,H-9),0.88(3H,t,J=7.0 Hz,H-10),3.56(2H,q,J=7.0 Hz,H-1′),2.76(2H,t,J=7.0 Hz,H-2′),7.02(2H,d,J=8.0 Hz,H-4′,H-8′),6.80(2H,d,J=8.0 Hz,H-5′,H-7′),5.54(1H,brs,-NH);13C NMR(125 MHz,CDCl3)δ:166.6(C-1),121.9(C-2),143.7(C-3),128.1(C-4),143.7(C-5),32.9(C-6),28.5(C-7),31.4(C-8),22.5(C-9),14.0(C-10),41.0(C-1′),34.8(C-2′),130.4(C-3′),129.8(C-4′),115.6(C-5′),154.8(C-6′),115.6(C-7′),129.8(C-8′)。以上数据与文献[19]报道一致,故鉴定化合物8为(E,E)-2,4-decadienoic acid p-hydroxyphenethylamide。
化合物9黄色油状(甲醇);EI-MS:m/z378.20[M]+;1H NMR(500 MHz,CDCl3)δ:6.63(2H,s,H-3,H-5),6.59(1H,d,J=15.0 Hz,H-7),6.23(1H,d,J=15.0 Hz,H-8),4.75(2H,m,H-9),2.48(2H,d,J=7.0 Hz,H-2′),2.30(1H,m,H-3′),0.98(6H,d,J=7.0 Hz,H-4′,H-5′),2.24(2H,d,J=7.0 Hz,H-2′′),2.27(1H,m,H-3′′),1.07(6H,d,J=6.5 Hz,H-4′′,H-5′′),3.82(s,6H,-OCH3);13C NMR(125 MHz,CDCl3)δ:134.7(C-1),152.4(C-2),103.5(C-3),128.9(C-4),103.4(C-5),152.4(C-6),134.1(C-7),123.8(C-8),64.8(C-9),170.9(C-1′),43.2(C-2′),25.9(C-3′),22.5(C-4′),22.5(C-5′),173.1(C-1′′),43.6(C-2′′),26.2(C-3′′),22.6(C-4′′),22.6(C-5′′)。数据与文献[20]报道基本一致,故鉴定化合物9为sinapyl alcohol diisovalerate。
化合物10黄色油状(甲醇);EI-MS:m/z310.25[M]+;1H NMR(500 MHz,CDCl3)δ:2.30(2H,t,J=7.5 Hz,H-2),1.17~1.12(10H,m,H-3,H-4,H-5,H-6,H-7),2.18(2H,m,H-8),5.45(1H,dt,J=11.0,7.5 Hz,H-9),5.97(1H,t,J=11.0 Hz,H-10),6.48(1H,dd,J=15.0,11.0 Hz,H-11),5.66(1H,dd,J=15.0,7.0 Hz,H-12),4.16(1H,q,J=7.0 Hz,H-13),1.17~1.12(8H,m,H-14,H-15,H-16,H-17),0.89(3H,t,J=7.0 Hz,H-18),3.66(3H,s,-OCH3);13C NMR(125 MHz,CDCl3)δ:174.3(C-1),37.3(C-2),25.3(C-3),29.0(C-4),29.1(C-5),29.3(C-6),24.9(C-7),34.1(C-8),125.9(C-9),133.1(C-10),135.1(C-11),127.7(C-12),72.9(C-13),27.8(C-14),29.3(C-15),31.5(C-16),22.5(C-17),14.0(C-18),51.44(-OCH3)。以上数据与文献报道一致[21],故鉴定化合物10为(S)-13-hydroxyoctadeca-(Z,E)-9,11-dienoic acid。
化合物11无色油状(甲醇);EI-MS:m/z301.20[M]+;1H NMR(500 MHz,CDCl3)δ:5.67(1H,d,J=15.0 Hz,H-2),7.18(1H,dd,J=15.0,9.5 Hz,H-3),6.11(1H,dd,J=15.0,9.5 Hz,H-4),6.06(1H,dd,J=15.0,6.0 Hz,H-5),2.14(2H,dd,J=13.5,7.0 Hz,H-6),1.41(2H,dd,J=14.0,7.0 Hz,H-7),1.28(4H,m,H-8,H-9),0.88(3H,t,J=7.0 Hz,H-10),5.40(1H,br s,-NH),3.56(2H,dd,J=13.0,7.0 Hz,H-1′),2.79(2H,t,J=7.0 Hz,H-2′),7.11(2H,d,J=8.5 Hz,H-4′,H-8′),6.85(2H,d,J=8.5 Hz,H-5′,H-7′);13C NMR(125 MHz,CDCl3)δ:166.9(C-1),121.4(C-2),143.0(C-3),128.2(C-4),144.7(C-5),34.1(C-6),28.6(C-7),31.5(C-8),22.6(C-9),14.2(C-10),41.2(C-1′),33.8(C-2′),130.2(C-3′),130.8(C-4′),114.2(C-5′),151.2(C-6′),114.2(C-7′),130.8(C-8′)。以上数据与文献[22]报道一致,故鉴定化合物11为(E,E)-2,4-decadienamide acid p-methoxyphenethylamide。
化合物12黄色油状(甲醇);EI-MS:m/z257.20[M]+;1H NMR(500 MHz,CDCl3)δ:6.13(1H,d,J=15.0 Hz,H-2),6.88(1H,dd,J=15.0,4.5 Hz,H-3),4.36(1H,m,H-4),3.78(1H,m,H-5),1.49(1H,m,H-6),1.50(1H,m,H-7),1.33(1H,m,H-7),1.32(2H,m,H-8),1.33(2H,m,H-9),0.91(3H,m,H-10),3.19(2H,t,J=6.5 Hz,H-1′),1.83(1H,m,H-2′),0.96(6H,t,J=6.5 Hz,H-3′,H-4′),5.50(1H,br s,NH);13C NMR(125 MHz,CDCl3)δ:165.4(C-1),125.2(C-2),141.1(C-3),74.2(C-4),74.5(C-5),32.1(C-6),25.7(C-7),31.9(C-8),22.7(C-9),14.1(C-10),47.1(C-1′),28.3(C-2′),20.3(C-3′),20.3(C-4′)。以上数据与文献[23]报道一致,故鉴定化合物12为erythro-N-isobutyl-4,5-dihydroxy-2-(E)-decenamide。
化合物13淡黄色粉末(甲醇);EI-MS:m/z368.11[M]+;1H NMR(500 MHz,CDCl3)δ:2.15(2H,m,H-2),5.07(1H,dd,J=9.0,5.5 Hz,H-3),3.65(1H,m,H-4),3.94(1H,dd,J=5.5,3.0 Hz,H-5),1.82(1H,dd,J=12.5,9.5 Hz,H-6),1.99(1H,dd,J=13.5,3.0 Hz,H-6),7.09(1H,d,J=2.0 Hz,H-2′),7.03(1H,dd,J=8.0,2.0 Hz,H-6′),6.83(1H,d,J=8.0 Hz,H-5′),7.44(1H,d,J=16.0 Hz,H-7′),6.16(1H,d,J=16.0 Hz,H-8′),3.62(s,3H,-OCH3);13C NMR(125 MHz,CDCl3)δ:75.7(C-1),37.6(C-2),72.4(C-3),72.0(C-4),69.9(C-5),38.4(C-6),175.7(C-7),127.5(C-1′),116.8(C-2′),146.8(C-3′),149.5(C-4′),115.2(C-5′),124.1(C-6′),145.4(C-7′),115.2(C-8′),169.0(C-9′),56.5(-OCH3)。以上数据与文献[24]报道一致,故鉴定化合物13为3-O-阿魏酰-奎宁酸。
化合物14白色针晶(甲醇);EI-MS:m/z180.04[M]+;1H NMR(500 MHz,CDCl3)δ:7.06(1H,d,J=2.0 Hz,H-2),7.00(1H,dd,J=8.0,2.0 Hz,H-6),6.77(1H,d,J=8.0 Hz,H-5),7.49(1H,d,J=16.0 Hz,H-7),6.27(1H,d,J=16.0 Hz,H-8);13C NMR(125 MHz,CDCl3)δ:129.3(C-1),116.4(C-2),146.5(C-3),147.9(C-4),121.7(C-5),123.1(C-6),141.5(C-7),114.6(C-8),176.2(C-9)。以上数据与文献[25]报道一致,故鉴定化合物14为肉桂酸。
化合物15淡黄色粉末(甲醇);EI-MS:m/z354.09[M]+;1H NMR(500 MHz,CDCl3)δ:2.00(2H,m,H-2),5.08(1H,dd,J=9.0,5.5 Hz,H-3),3.57(1H,m,H-4),3.93(1H,m,H-5),1.98(1H,m,H-6),1.79(1H,m,H-6),7.04(1H,d,J=1.5 Hz,H-2′),6.98(1H,dd,J=8.0,1.5 Hz,H-6′),6.77(1H,d,J=8.0 Hz,H-5′),7.43(1H,d,J=16.0 Hz,H-7′),6.16(1H,d,J=16.0 Hz,H-8′);13C NMR(125 MHz,CDCl3)δ:72.3(C-1),37.7(C-2),71.3(C-3),71.1(C-4),68.9(C-5),38.7(C-6),175.6(C-7),121.8(C-1′),114.8(C-2′),148.8(C-3′),146.0(C-4′),116.2(C-5′),126.1(C-6′),145.4(C-7′),115.2(C-8′),166.3(C-9′)。以上数据与文献[26]报道一致,故鉴定化合物15为绿原酸。
化合物16淡黄色粉末(甲醇);EI-MS:m/z530.14[M]+;1H NMR(500 MHz,CDCl3)δ:2.24(2H,m,H-2),4.97(1H,dd,J=6.5,3.0 Hz,H-3),4.14(1H,m,H-4),5.27(1H,m,H-5),2.00(1H,m,H-6),1.89(1H,m,H-6),7.04(2H,d,J=1.5 Hz,H-2′,H-2′′),6.99(2H,dd,J=8.0,1.5 Hz,H-6′,H-6′′),6.76(1H,d,J=8.0 Hz,H-5′,H-5′′),7.51(1H,d,J=16.0 Hz,H-7′),6.26(1H,d,J=16.0 Hz,H-8′),7.42(1H,d,J=16.0 Hz,H-7′′),6.13(1H,d,J=16.0 Hz,H-8′′),3.66(3H,s,-OCH3);13C NMR(125 MHz,CDCl3)δ:74.5(C-1),37.9(C-2),72.3(C-3),71.0(C-4),72.0(C-5),36.5(C-6),177.6(C-7),127.8(C-1′),115.8(C-2′),146.7(C-3′),149.0(C-4′),116.4(C-5′),123.1(C-6′),147.4(C-7′),115.5(C-8′),168.3(C-9′),127.6(C-1′′),115.8(C-2′′),146.8(C-3′′),149.3(C-4′′),116.2(C-5′′),123.1(C-6′′),145.8(C-7′′),115.6(C-8′′),169.2(C-9′′),56.1(-OCH3)。以上数据与文献报道一致[27],故鉴定化合物16为3-O-咖啡酰-5-O-阿魏酰奎宁酸。
2.2 体外细胞毒活性筛选
对蓍草95%乙醇提取物分离得到化合物1~11在不同人胃癌细胞株MGC-803、MKN-45、HGC-27和AGS进行活性筛选。结果显示在50 μM时,化合物2、5与9对MGC-803抑制率依次为38.7%、34.7%、31.5%(阳性药5-氟尿嘧啶10 μM:抑制率为43.72%),统计学分析显示P<0.05,与空白组对比具有显著差异,表明化合物2、5与9对MGC-803细胞株具有一定的抑制活性。化合物1~11在50 μM时对MKN-45、HGC-27和AGS胃癌细胞未显示出明显的抑制活性(见表2)。
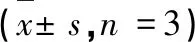
表2 化合物1~11对HGC-27、MGC-803、AGS及MKN-45的细胞毒活性Table 2 Cytotoxicity of compounds 1-11 on HGC-27,MGC-803,AGS and MKN-45 cell lines s,n =3)
3 结论
通过对蓍草进行提取分离,共得到16个单体化合物,其中化合物1是一个新的酰胺类化合物,化合物4~6、9、10、12、13、16均为首次从蓍属植物中分离得到,化合物8、11为首次从蓍草中分离得到。对这些化合物进行抗肿瘤活性筛选(胃癌细胞株MGC-803、MKN-45、HGC-27和AGS)发现不同结构类型的化合物2、5与9对MGC-803胃癌细胞株有选择抑制活性,这为发现具有选择性抗胃癌作用的先导化合物提供了思路。在蓍草的文献报道中,对其化学成分的报道较少,药理研究主要为抗炎活性,但对细胞毒活性鲜有报道[1,14]。我们首次对其含有的主要化学成分进行系统分离及抗肿瘤活性的筛选,部分化合物显示出一定的胃癌细胞抑制活性,为更好地开发利用该植物,丰富该植物化学成分的种类以及探究其有效活性成分奠定了一定的理论基础。

