临床诊断的类风湿性脑血管炎1例报告
陈 怡, 雷晓阳, 蒲 胤, 贺 电
类风湿关节炎(rheumatoid arthritis,RA)患者的中枢神经系统受累主要包括脑膜炎、类风湿结节和类风湿性脑血管炎(rheumatoid cerebral vasculitis,RCV)[1],以上关节外并发症的确诊依赖于组织病理学。然而,在临床工作中病理活检的开展并不是总能进行,临床诊断作为最高诊断更为普遍。本文报道1例临床诊断的类风湿性脑血管炎。
1 临床资料
男性患者,54岁,因“精神行为异常1 y余伴四肢抽动4 d”于2020年1月首次入院。患者1 y余前突发胡言乱语、双手挥舞,持续十余分钟后逐渐好转,伴头痛、反应迟钝,反复发作,未诊治;4 d前出现四肢抽动,期间发生一次痫样发作,表现为四肢抽搐,双眼向右凝视、呼之不应,伴双手麻木、无大小便失禁等。既往双手近端指间关节麻木、僵硬、疼痛病史,以晨起为重,活动后好转。查体:双手近端指间关节略成梭形肿胀。反应迟钝,言语欠流利,对答不切题。颅神经(-)。双上肢肌力4级,双下肢肌力5级,四肢肌张力稍高。病理征及脑膜刺激征阴性。查血常规、肝肾功能、血糖水平、类风湿因子(RF)水平正常,HIV抗体、TP抗体、甲状腺抗体、抗核抗体谱均阴性。血沉(ESR)、C反应蛋白(CRP)、抗环瓜氨酸肽抗体(CCP)存在异常(见表1)。行腰椎穿刺术:颅内压130 mmH2O,脑脊液常规、生化指标、白介素6水平均正常,脑脊液革兰染色、墨汁染色、抗酸染色、脑脊液病毒抗体全套(TORCH)、细菌培养、结核分枝杆菌核酸检测均无异常。颈部血管超声、胸部CT均未见异常。患者拒做双手MR平扫。头部MR平扫示左侧顶枕叶交界区异常信号(见图1A),增强示同部位异常强化结节(见图1B)。头部SWI、DWI、MRA均无异常。临床诊断为左侧顶枕叶炎性肉芽肿 继发性癫痫,予丙戊酸钠缓释片(500 mg Bid)控制癫痫,甲泼尼龙(250 mg,阶梯式减量)抗炎后,未再出现癫痫发作。出院后继续口服丙戊酸钠缓释片、甲泼尼龙片(40 mg,1 w减4 mg),减至8 mg时,患者自行停服丙戊酸钠和甲泼尼龙。
2020年3月患者再因四肢抽搐入院,主要症状与上一次发病类似,但出现右侧肢体无力(肌力3+级)。入院查ESR、CRP、CCP仍存在异常(见表1),余血液生化指标正常。脑脊液常规、生化指标无异常。头部MR平扫示左侧顶枕叶皮质区异常信号影(见图1C、D),增强未见强化结节,新增双侧枕部脑膜强化(见图1E)。临床诊断考虑RCV,建议患者行脑组织活检以明确,但患者拒绝,予甲泼尼龙抗炎、丙戊酸钠控制癫痫(同首次入院),患者未再出现肢体抽搐,但右侧肢体无力无改善。查PET-CT示左侧枕叶片状密度减低影(见图2A~C);左侧顶枕叶皮质区葡萄糖代谢减低,而邻近皮质区深部葡萄糖代谢增高(见图2D~F)。头部MR平扫示左侧顶枕叶皮质区病灶范围较前扩大且出现脑白质深部高信号(见图1F、G),与PET-CT葡萄糖代谢分布一致。患者自行停药后对激素不敏感,立予甲泼尼龙(1 g静滴,阶梯式减量)冲击联合环磷酰胺(前两日各400 mg,第三、四日各600 mg)治疗,右侧肢体无力症状改善(肌力4+级)。出院后于当地医院输过一次环磷酰胺(800 mg)。
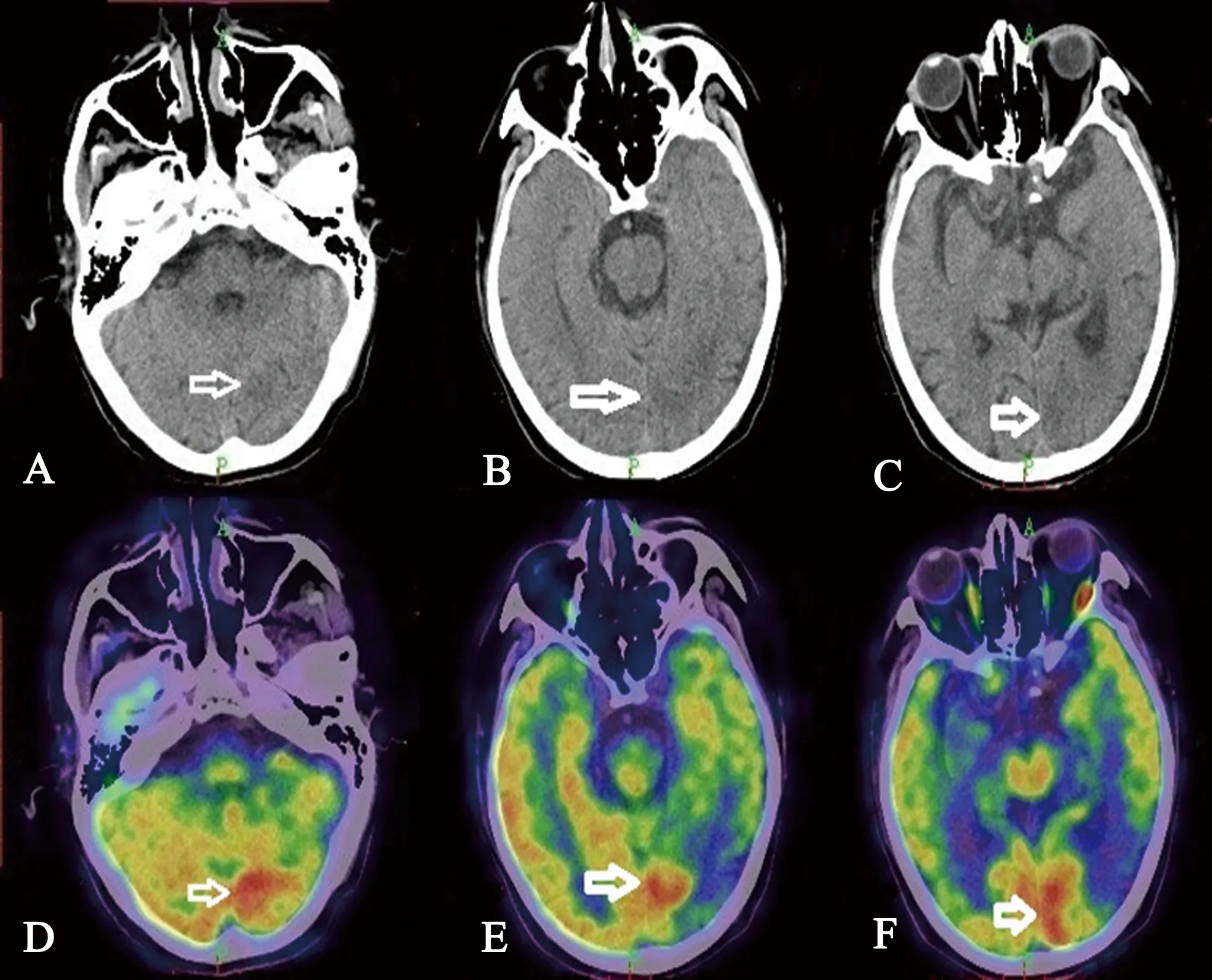
图2 A~C:患者第二次入院头部PET-CT表现:左侧枕叶片状密度减低影;D~F:左侧顶枕叶皮质区葡萄糖代谢减低,而邻近皮质区深部葡萄糖代谢增高
2020年5月患者返院输环磷酰胺(800 mg),查血仅CCP存在异常(见表1)。头部MR T2WI/FLAIR像左侧顶枕叶皮质区病灶改善,但脑白质深部高信号仍存在(见图1H、I),增强扫描未见脑膜强化。出院后患者未继续输环磷酰胺,继续口服丙戊酸钠控制癫痫。目前已随访患者1 y,癫痫未再发作,右侧肢体肌力4+级。
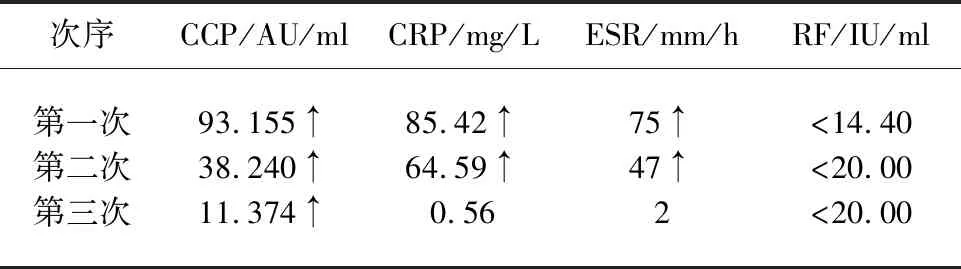
表1 患者3次入院血清学指标变化水平
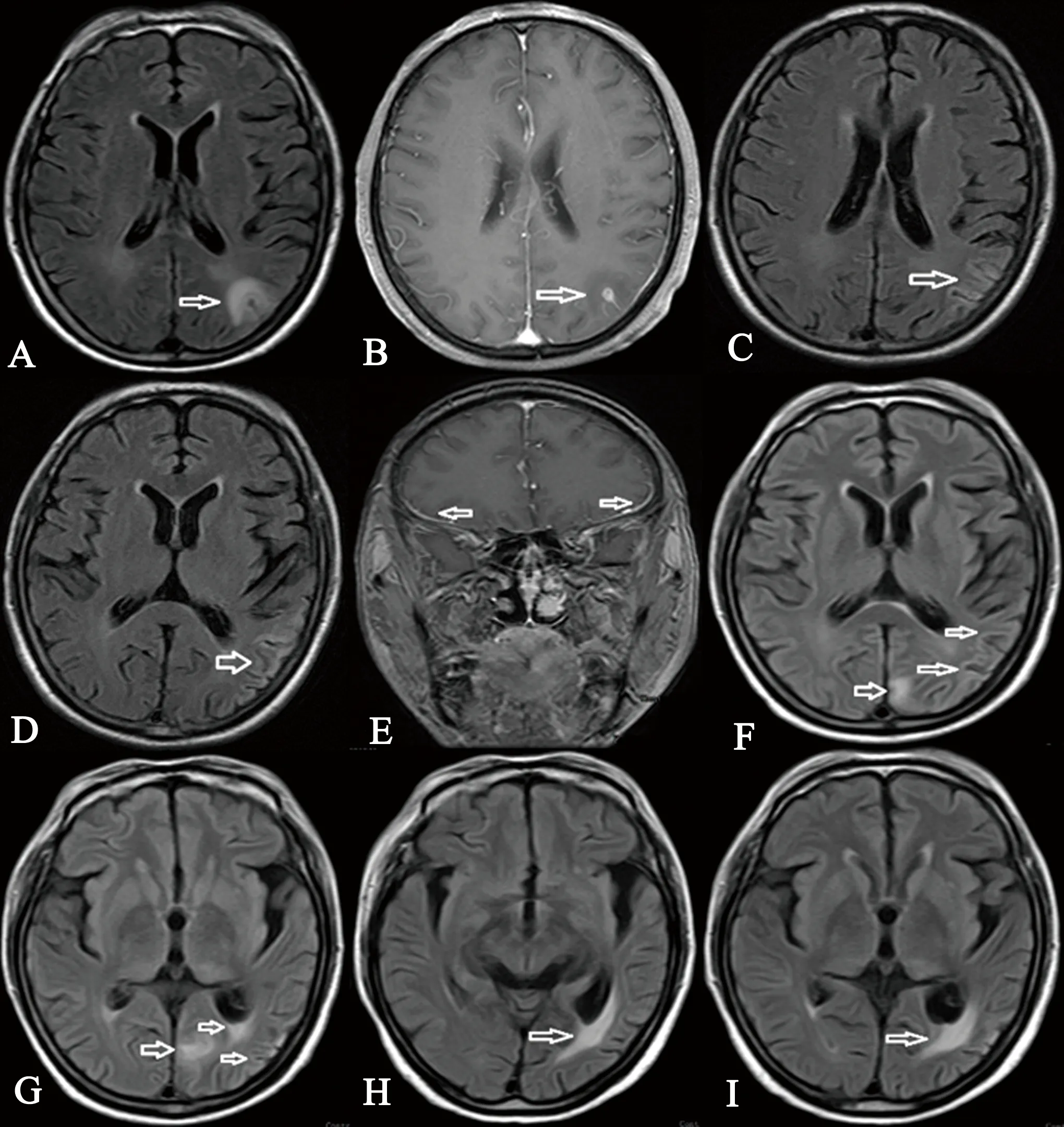
图1 A:患者首次入院头部MR平扫示左侧顶枕叶交界区异常信号;B:增强示左侧顶枕叶交界区异常强化结节;C、D:第二次入院头部MR平扫示左侧顶枕叶皮质区异常信号影;E:增强示双侧枕部脑膜异常强化;F、G:复查头部MR平扫示左侧顶枕叶皮质区病灶范围较前扩大,新增脑白质深部高信号;H、I:第三次入院头部MR T2WI/FLAIR像左侧顶枕叶脑白质深部高信号,皮质区病灶范围缩小
2 讨 论
RCV是RA罕见但严重的关节外表现,是一种中小型血管坏死性血管炎,确诊常需有创的脑组织活检,纤维蛋白样坏死和内膜增生是其常见的组织病理学表现,卒中、癫痫、痴呆及神经精神障碍是常见的临床表现[1]。RCV尚无明确的临床诊断标准。在本案例中,高水平的ESR、CRP,头部MR平扫皮质区病灶范围扩大的部分在PET-CT上表现为葡萄糖代谢增高,结合头部CT未见占位病变,故考虑左侧顶枕叶皮质区病灶为炎性病灶。另外,脑脊液相关检查无异常可排除感染性脑病。抗核抗体谱、心磷脂抗体、抗中性粒细胞胞浆抗体均无异常,不优先考虑其他结缔组织病所致炎性脑病。
值得注意的是3次入院始终高水平的CCP,虽然RF阴性,但CCP对诊断RA高度特异且疾病发作时CCP阳性是进展为RA的良好预测因子[2],结合患者早期手关节受累的典型症状与体征,临床诊断RA。Turesson C发现CCP与RA严重的关节外表现密切相关,而RCV作为RA严重的关节外表现,有研究指出内皮细胞功能障碍是类风湿性血管炎发生的潜在机制[3,4]。Hjeltnes G等人发现CCP与RA患者的内皮功能受损相关[5],可能是反应内皮功能障碍的一项早期指标。
另有文献指出,肿瘤坏死因子(TNF)参与内皮细胞活化[6],后者是内皮功能障碍的先兆[7],而CCP本身或含有CCP的免疫复合物可促进TNF的产生[8],TNF抑制剂治疗RCV有效能够证明这一点。至此,认为CCP与RCV存在密切关系,而内皮细胞功能障碍是否作为中间的直接或间接的联系桥梁值得进一步研究。提示临床医生在评估病因不明的脑部疾患时,若持续出现高水平的CCP,能够相应地考虑到RCV的可能。
就既往报道的RCV影像学表现而言,双侧病变与单侧病变的发病率几乎相同,且大部分病变位于皮质下或白质[9],结合本报告影像学表现与文献报道相符,支持RCV的临床诊断。
患者停服激素1 w后症状复发并出现右侧肢体无力,头部MR增强示双侧枕部脑膜强化,继续单用激素治疗无效且复查的头部MR平扫提示病灶范围扩大,故联合环磷酰胺治疗,患者症状、血清学指标明显改善,影像学显示病灶范围缩小,未见脑膜强化,对治疗的反应性也支持RCV的临床诊断。另外,联合治疗后脑白质深部病变无缩小趋势,解释可能为在整个诊疗过程中晚期才联合环磷酰胺治疗且累计剂量(3.6 g)似乎才刚刚起效,患者便停止继续使用环磷酰胺,提示更早期、长疗程、足剂量的包括环磷酰胺在内的联合免疫抑制治疗可能会更有效。

