系统性硬皮病合并肝损伤1 例并文献复习
于研,李梦琳,郭涛,王磊,马秀亮,张峻岭
(天津市中医药研究院附属医院,天津 300120)
1 临床资料
患者女,72 岁,主因“面部、双手硬化性斑块10余年,加重1 个月余”,于2020 年10 月入院。患者10 余年前自面部及双手出现硬化性斑块,就诊于外院,考虑“硬皮病”,予中药汤剂口服,期间病情反复,遇冷时加重,双手可出现白-紫-红的变化。1 个月前双手症状较前加重,双上肢疼痛明显,随就诊于我院,以“系统性硬皮病(SSc)”收入院治疗。患者自发病以来,无畏寒发热、咳嗽咳痰、吞咽困难、胸闷憋气、腹痛腹泻等不适。患者既往高血压病史2 年,否认呼吸系统疾病、肝肾疾病、慢性胃炎等慢性病史,否认传染病史,否认食物药物过敏史及家族史。
体格检查:神清,精神可,发育正常,营养中等,浅表淋巴结未触及肿大,心肺腹查体未见明显异常。皮肤科查体:面部、双手肿胀性斑块,颜色暗红,可见蜡样光泽,触之质韧,双手握拳困难、皮温偏低,雷诺现象(+),口周放射性条纹,鼻端稍尖,张口受限,双下肢未见明显肿胀,见图1。

图1 患者临床照片
实验室检查:血、自身免疫性肝病抗体、乙肝两对半、丙肝、尿、便常规、心电图未见明显异常。生化全项:γ-谷氨酰转肽酶62.1 U/L(正常值7~45)。肿瘤标志物:CA19~9 60.04 IU/mL(正常值<28)。免疫全项:抗核抗体1∶320(+),抗可溶性核抗原抗体(+),抗U1-snRNP 抗体(+),抗Sm 抗体(+),抗Scl-70 抗体(+),IgG 26.5 g/L(正常值8.6~17.4)。IgG4 580.7 mg/L(正常值39.2~864)。风湿两项:类风湿因子33.4 IU/mL(正常值0~30)。出院前复查肝功能:丙氨酸转氨酶47.2 U/L(正常值7~40),γ-谷氨酰转肽酶140.8 U/L(正常值7~45)。胸部计算机断层扫描(CT):考虑双肺间质病变,间质性炎炎性反应及间质纤维化不除外;双侧胸膜增厚,钙化;考虑气管憩室;动脉硬化;心影增大,主肺动脉增宽。腹部超声:肝损害;肝多发囊肿;胆总管上段扩张。双肾彩超未见明显异常。心脏彩超:左室舒张功能减低;二尖瓣、肺动脉瓣反流(轻度)。上腹部CT:考虑多囊肝并硬化;肝右叶疑似片状低密度影;脾边缘钙化灶;考虑右肾错构瘤;左肾边缘点片状高密度影;动脉硬化。电子胃镜:食管炎,食管白斑,Barrett 食管,慢性胃炎伴糜烂,十二指肠球炎。
病理检查示:表皮变化不明显,真皮内胶原纤维增生、硬化,透明变性,血管周围少数淋巴细胞浸润。直接免疫荧光:基底膜IgG(-),IgM(±),IgA(-),C3(±)。结合临床符合硬皮病变化,见图2。
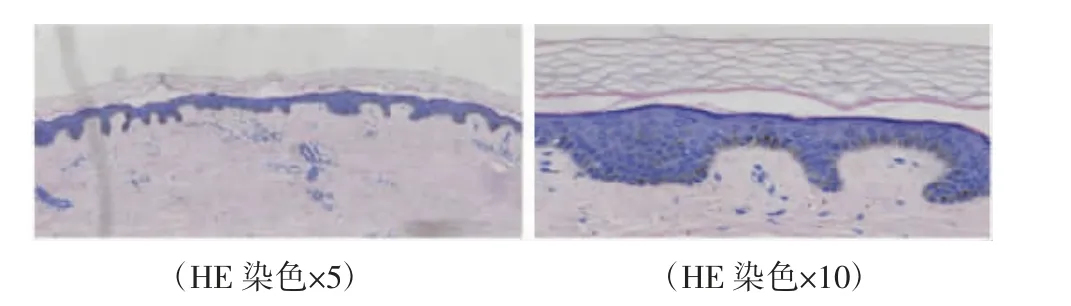
图2 患者皮损病理组织图
诊断:①SSc;②高血压病;③慢性胃炎;④肺间质纤维化?
治疗:入院后予甲强龙60 mg/d(合泼尼松75mg/d)静脉滴注抗炎,谷胱甘肽、双环醇片保肝护肝治疗,予桂枝红花汤煎服,出院时双手斑块颜色较前变淡,肿胀明显消退,面部及双手皮疹较前变软,皮温较前稍增高,复查肝功能仍有异常,肝酶升高:丙氨酸转氨酶47.2 U/L(正常值7~40),γ-谷氨酰转肽酶140.8 U/L(正常值7~45)。出院后激素逐渐减量,目前门诊继续治疗中。
2 讨论
硬皮病是皮肤局部或广泛硬化以及全身各器官受累的结缔组织病,按照累及范围可分为局限性硬皮病和SSc。SSc 是一种少见的自身免疫性结缔组织疾病,其特征是慢性、进行性的组织和器官纤维化及血管改变。
SSc 病因尚不明确,感染、寒冷、化学物质等外界因素均可诱导疾病发生,也有观点认为,SSc 与恶性肿瘤存在一定相关性,本病例中肿瘤标志物CA19-9 偏高,结合影像学检查未观察到肿瘤,但考虑SSc 与恶性肿瘤的相关性,仍需定期复查。SSc 是一种复杂的自身免疫反应,包括先天免疫和适应性免疫。SSc 患者可观察到特异性自身抗体,如拓扑异构酶Ⅰ(抗TOPO/抗Scl-70)、抗着丝点抗体、核糖核蛋白、抗RNA 聚合酶Ⅲ(RNApol3)。本病例中患者入院时即表现出硬化性斑块和雷诺现象,并伴有抗核抗体1∶320(+),抗Scl-70 抗体(+),结合患者病理学表现,根据2013 年美国风湿病学会(ACR)/欧洲抗风湿病联盟(EULAR)SSc 分类标准,患者总分12 分,可诊断为SSc。
SSc 发病早期表现为微血管改变和内皮细胞功能障碍,随后是自身免疫反应和炎性反应,许多细胞因子和趋化因子都参与了SSc 的发病过程,如转化生长因子-β(TGF-β)、白细胞介素-18(IL-18)、IL-23、IL-17、IL-6、趋化因子4(CXCL4)[1]。针对IL-23 和IL-17 的生物制剂目前以被批准用于治疗斑块型银屑病,因此也可能在SSc 治疗上有一定疗效。细胞外基质蛋白在皮肤和多个器官中进行性积累,胶原纤维增加增粗,最后表现为弥漫性纤维化[2]。
SSc 累及多个器官,可表现为肺纤维化、肺动脉高压、肾脏受累和胃肠道受累等,是目前该病患者重点关注的问题。
肺纤维化和肺动脉高压是SSc 显著的肺部并发症。间质性肺病是SSc 患者最常见的死亡原因,其患病率高达30%,10 年死亡率高达40%[3]。与硬皮病相关的间质性肺病胸部CT 的表现为呼吸困难、咳嗽和非特异性间质性肺炎。肺动脉高压则可通过超声心动图检测。与系统性硬化症相关的最特殊的肾脏疾病是硬皮病肾危象,其特征是急性肾功能衰竭和严重的高血压,可能出现头痛、高血压性视网膜病变、脑病、癫痫发作、发热、肺水肿和全身不适[4]。心脏受累可表现为心包/心肌纤维化和心包积液,表现主要包括心脏瓣膜和传导系统的硬化以及心律失常。SSc 最常见的内脏并发症是胃肠道受累,临床表现为食管动力受损、胃食管反流和Barrett 食管。本病例中患者胸部CT 显示间质性纤维化,电子胃镜下显示食管病变,可见多系统受累。患者高血压病史2 年,肾功能、尿常规及肾脏超声未见明显异常,但考虑SSc 相关的肾脏受累临床检查阳性率偏低,不排除其高血压与肾脏受累相关。此外,在本病例还观察到患者肝损害、肝功能异常,结合患者腹部超声及上腹部CT 排除肝脏肿瘤,予常规保肝护肝治疗后未见明显好转,肝酶持续性增高,考虑其不除外自身免疫性肝病。目前,关于SSc与自身免疫性肝病的报道较少,其中最常见的是原发性胆汁性肝硬化。1970 年Murray-Lyon[5]等首次报道了SSc 与原发性胆汁应肝硬化相关的案例。Coelho 等[6]报道1 例考虑自身免疫性肝炎和SSc 可能相关的案例。Assandri 等[7]报道了2 例自身免疫性肝炎患者合并SSc。国内高卉等[8]、卞璐等[9]也分别报道了原发性胆汁性胆管炎合并SSc 的病例。SSc 与自身免疫性肝病二者的相关性尚不明确,关于二者之间是因果关系或是偶然发生的关系未得到解决。自身免疫性肝病被认为可能是与SSc 相关的肝脏表现之一。尽管此次未能明确患者肝损伤的原发疾病,针对患者肝脏仍需定期检查。
SSc 临床上可累及多个器官,个体器官受累的严重程度,对患者的生活质量和生存预后有显著影响。因此,应密切监测患者的病情变化,希望在疾病的评估和治疗继续取得新的进展。

