贝伐单抗靶向联合FOLFOX化疗方案对结肠癌患者免疫功能及毒副反应的影响
赵伶伶
(铁岭市中心医院肿瘤内科,辽宁 铁岭 112000)
结肠癌是一种常见的发于结肠黏膜上皮部位的恶性肿瘤,内镜微创手术以及术后化疗是临床治疗的主要方法,但化疗药物在杀灭癌细胞的同时也会破坏机体免疫功能,损害患者身心健康并影响预后[1]。FOLFOX 化疗为临床常见的结肠癌化疗方案,可使癌细胞DNA损伤,破坏其转录及复制过程,产生细胞毒性,促使癌细胞死亡[2]。贝伐单抗为抗肿瘤血管生成药,对血管内皮生长因子(VEGF)有抑制作用,能阻止其与内皮细胞表面受体结合,抑制血管生成。但目前关于二者联合治疗结肠癌的报道较少。基于此,本研究采用贝伐单抗靶向联合FOLFOX化疗方案治疗结肠癌患者,旨在探究其疗效,为结肠癌的治疗提供指导,现报道如下。
1 资料与方法
1.1 临床资料 选取2018年6月至2019年11月本院收治的71例结肠癌患者作为研究对象,根据治疗方法的不同分为对照组(n=35)与观察组(n=36)。对照组男 19 例 ,女 16 例 ;年龄 32~71 岁 ,平均(47.52±8.25)岁;肿瘤分化程度:低8例,中19例,高8例。观察组男18例,女18例;年龄32~70岁,平均(48.39±8.45)岁;肿瘤分化程度:低9例,中20例,高7 例。两组临床资料比较差异无统计学意义,具有可比性。本研究获得医院伦理委员会审核批准。
1.2 纳入及排除标准 纳入标准:符合《中国结直肠癌诊疗规范(2017年版)》[3]诊断标准;患者自愿签署知情同意书;无既往免疫治疗或放化疗史;预计生存期>6个月。排除标准:直肠癌、胃癌等其他恶性肿瘤;有交流障碍不能配合者;腹内疝、骶前出血等术后严重并发症;对本研究药物不耐受者。
1.3 方法
1.3.1 对照组 对照组采用FOLFOX 化疗方案。奥沙利铂(江苏奥赛康药业股份有限公司,生产批号20180503,规格:50 mg),静脉滴注注射135 mg/m2,每天1次,每次2 h;亚叶酸钙(福建省闽东力捷迅药业有限公司,生产批号20180104,规格:100 mg),静脉注射,每次200 mg,每天1次,每次2 h;氟尿嘧啶注射液(海尔滨三联药业有限公司,生产批号20171205,规格:10 m∶l0.25 g),静脉滴注400 mg/m2,每天1 次,每次2 h。每2周重复用药1次,治疗24周。
1.3.2 观察组 观察组在对照组基础上联合贝伐珠单抗注射液[Roche Pharma(Switzerland)Ltd,生产批号20180402,规格:100 mg∶4 ml]治疗,静脉滴注5 mg/kg,每2周1次,患者首次用药滴注时间需持续1.5 h,患者适应后滴注时间缩短为1 h,治疗24周。
1.4 观察指标 ①免疫功能和血管内皮生长因子(VEGF):于治疗前、治疗24周后,清晨空腹时取患者静脉血5 ml,采用酶联免疫吸附法检测成熟T 细胞(CD3+)、辅助性T细胞(CD4+)、抑制性T细胞(CD8+)及VEGF水平;②毒副反应:参照WHO制定的抗癌药物急性与亚急性反应分度标准[4]评价两组治疗期间的腹泻、白细胞减少、骨髓抑制、神经病变等发生情况。
1.5 统计学方法 采用SPSS 25.0统计学软件进行数据处理,计量资料以“”表示,组间比较用独立样本t检验,组内比较用配对样本t检验,计数资料用百分比(%)表示,采用χ2检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组治疗前后免疫功能比较 治疗前,两组CD3+、CD4+、CD8+水平比较差异无统计学意义;治疗 24 周后,两组 CD3+、CD4+、CD8+水平均高于治疗前,且观察组高于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组治疗前后免疫功能比较(,%)
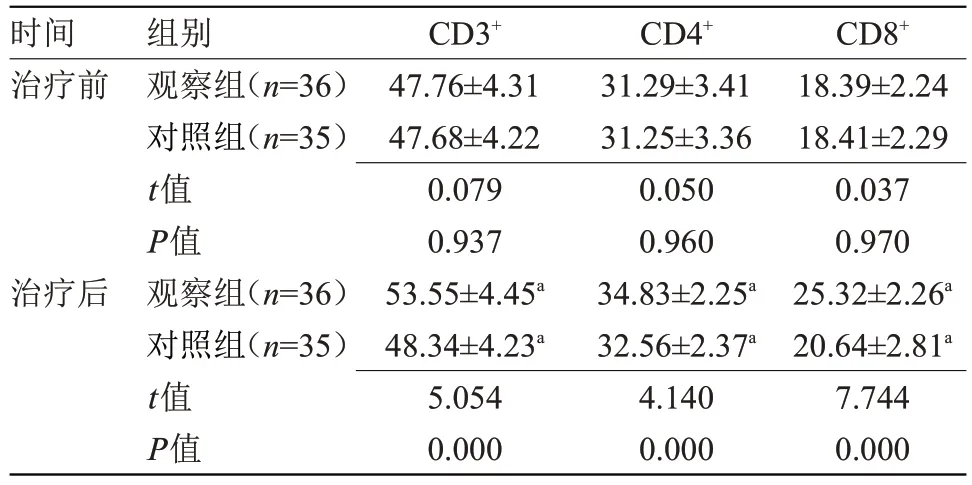
表1 两组治疗前后免疫功能比较(,%)
注:CD3+,成熟T淋巴细胞;CD4+,诱导性T细胞/辅助性T细胞;CD8+,抑制性T细胞/细胞毒性T细胞。与本组治疗前比较,aP<0.05
CD8+18.39±2.24 18.41±2.29 0.037 0.970 25.32±2.26a 20.64±2.81a 7.744 0.000时间治疗前治疗后组别观察组(n=36)对照组(n=35)t值P值观察组(n=36)对照组(n=35)t值P值CD3+47.76±4.31 47.68±4.22 0.079 0.937 53.55±4.45a 48.34±4.23a 5.054 0.000 CD4+31.29±3.41 31.25±3.36 0.050 0.960 34.83±2.25a 32.56±2.37a 4.140 0.000
2.2 两组治疗前后VEGF水平比较 治疗前,两组VEGF 水平比较差异无统计学意义;治疗24 周后,两组VEGF 水平均低于治疗前,且观察组低于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组治疗前后VEGF水平比较(,pg/ml)
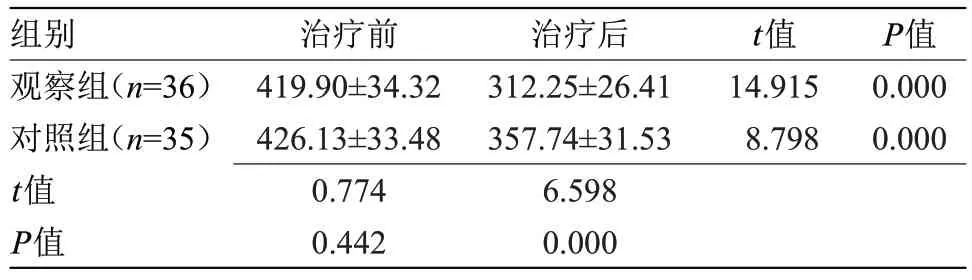
表2 两组治疗前后VEGF水平比较(,pg/ml)
组别观察组(n=36)对照组(n=35)t值P值治疗前419.90±34.32 426.13±33.48 0.774 0.442治疗后312.25±26.41 357.74±31.53 6.598 0.000 t值14.915 8.798 P值0.000 0.000
2.3 两组毒副反应发生率比较 两组腹泻、白细胞减少、骨髓抑制、神经病变发生率比较差异无统计学意义,见表3。
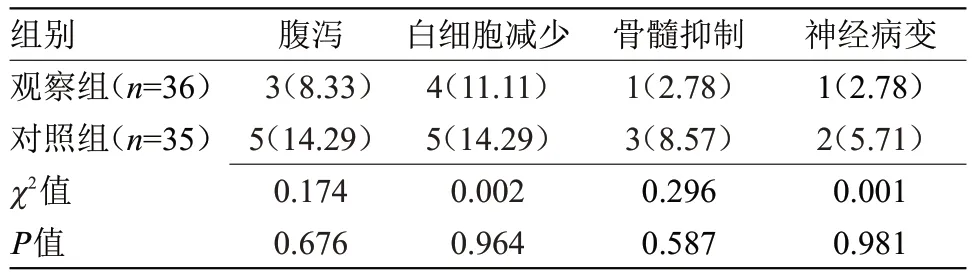
表3 两组毒副反应发生率比较[n(%)]
3 讨论
结肠癌多发于中老年人群,发病较为隐匿,早期症状无特异性,因此,通常出现漏诊、误诊,患者确诊时,多已处于中晚期,单纯的手术已无法根治结肠癌,预后较差[5]。FOLFOX 化疗方案是使用氟尿嘧啶、奥沙利铂、亚叶酸钙3 种药物联合治疗,其中奥沙利铂可产生烷化物,与DNA 链发生共价结合,从而影响癌细胞的DNA 合成复制,促使细胞死亡[6]。氟尿嘧啶对胸腺嘧啶核苷酸合成酶(TS酶)有较强的抑制作用,能抑制癌细胞DNA 的复制,进而阻止肿瘤细胞增殖[7]。亚叶酸钙对TS 酶有较强的抑制作用,可抑制DNA合成,对治疗结肠癌、直肠癌有很好的效果[8]。但FOLFOX化疗方案在临床治疗中会发生呕吐、恶心等胃肠道不良反应,剂量加大时还会出现神经毒素反应,不利于患者预后。
本研究结果显示,治疗后,两组CD3+、CD4+、CD8+水平均高于治疗前,且观察组高于对照组;两组患者VEGF 水平均低于治疗前,且观察组低于对照组;两组毒副反应发生率均较低,表明贝伐单抗靶向联合FOLFOX化疗方案可有效提升治疗效果,并提升患者免疫能力。分析其原因为,VEGF具有高度特异性,能与肿瘤血管内皮表面受体特异性结合,改变细胞外基质,调节肿瘤血管的形成,为肿瘤组织扩散提供必要的营养物质。而贝伐单抗可与VEGF结合,阻止其与内皮细胞表面受体结合,从而抑制肿瘤新生血管的形成并导致肿瘤组织供血不足,使其因缺血、缺氧而坏死,由此阻止肿瘤生长[9]。贝伐单抗的主要不良反应,如心力衰竭、贫血等,可得到有效控制,与FOLFOX化疗方案联合时不会增加患者毒副作用,且该药物能使化疗药物对肿瘤组织的持续作用加强,减轻肿瘤对患者免疫细胞的损害,继而提升机体抗肿瘤能力。
综上所述,贝伐单抗靶向联合FOLFOX化疗方案可提高结肠癌患者免疫功能,改善VEGF水平,促进疾病转归,且安全性较高,值得临床推广。

