变色泡桐木材脱色后组分及热稳定性
许雅雅,常德龙,楚 杰,胡伟华,黄文豪,张云岭,陈 妮,谢非凡
(1.国家林业和草原局泡桐研究开发中心 经济林种质创新与利用国家林业和草原局重点实验室,河南 郑州 450003;2.南京林业大学,江苏 南京 210037;3.西北农林科技大学,陕西 杨凌 712100)
我国是世界第一泡桐大国,每年泡桐木材产量超过1 000 万m3[1]。泡桐作为重要的工业用材,广泛用于室内建筑装修及家具和工业建筑等行业,我国每年有200 万m3左右的桐木制品出口日本、韩国等国家[2]。泡桐的生产利用已经得到越来越多专家的青睐。但是实际生产中,因泡桐易变色使得其材色品质降低,造成板材综合利用率不足40%,大大限制了桐木产业的发展[1,3]。
关于泡桐木材的变色成分,文献报告中有糖类、多酚类[4]、水溶性的无色花色苷和原花色苷[5]、梓醇、芝麻素和泡桐素以及类似木素模型化合物的酚类物质等多种说法,同时发现pH 值、光照和氧气都是造成桐木变色的环境因素[6]。长期以来,通常认为泡桐木材变色由化学因素引起,常德龙等[7]从新伐泡桐材和变色泡桐板材中分离出两种变色真菌,说明微生物也是引起泡桐材变色的原因之一。高温高湿的条件容易使木材发生变色,高温干燥对木材颜色变化具有显著影响[8]。泡桐木材变色成分说法不一,成因及变色机理复杂,使得脱色研究进展缓慢。科研人员始终致力于更高效环保的脱色配方与工艺的研究。陈玉和等[9]指出NaOH 稀溶液对泡桐木材颜色没有明显损害作用,能显著提高泡桐的渗透性,促进木材漂白效果;常德龙等[3]研究出了TSBL 脱色剂,成功脱除了蓝变泡桐材的色斑。但对脱色后泡桐木材的特性,如组分变化和热解特性等的研究还未见报道。
木材主要是由纤维素、半纤维素和木质素以及少量抽提物组成的复杂天然高分子化合物。脱色会造成木材组分结构中羰基、羧基、不饱和双键、共轭体发色基团和羟基等助色基团的结构改变。色度指标ΔL*(亮度的变化量)、Δb*(黄蓝色品指数的变化量)和ΔE*(色差)与木材化学组分有很强的相关性,而Δa*(红绿色品指数的变化量)与任何化学组分的相关性都最弱[10]。石江涛等[11]采用酸和碱的水溶液对杨木进行热处理,结果表明亮度值随温度降低,化学结构发生变化,半纤维素和木质素有所降解。木质素中的羰基结构有助于a*(红绿色品指数)的色度值在热处理过程中增加,b*(黄蓝色品指数)的色度值受C-O基团的影响,并且显示出与木质素的O/C 比相反的趋势[12]。关于木材组分及光谱特性的研究多集中于高温热处理材和酸碱处理材,对于常温脱色材的相关报道很少。因此,本研究从低成本、温和温度作用机制脱色泡桐基材入手,采用不同的溶剂和调控温度,探讨不同处理条件下泡桐材色变化规律,采用傅里叶红外光谱,分析桐木组分结构官能团变化机理,采用热重曲线来分析脱色材的热稳定性,为揭示脱色色度参数与组分结构之间的关系提供科学数据与理论支撑,同时探索低成本、高效率、易操作的泡桐木材脱色工艺,为泡桐木材脱色提供理论参考依据。
1 材料与方法
1.1 材料与仪器
试验材料为老化变色的兰考泡桐Paulownia elongata,采自河南省兰考县,制成尺寸为50 mm(L)×50 mm(T)×5 mm(R)的木块,晾干装袋备用,含水率保持在10%左右。
试验中使用的过氧化氢、次氯酸钠、亚氯酸钠、浓硫酸、甲苯、无水乙醇、甲醇、溴化钾等均为市售分析纯试剂。脱色处理及化学组分测定所用仪器均为实验室常用仪器,包括水浴锅、电子天平、真空泵、干燥箱、高速离心机、振荡器、高压灭菌锅、粉碎机等。
1.2 脱色处理
将泡桐试件分别在不同的脱色试剂和不同温度条件下进行脱色处理,采用对温度响应较明显的NaClO2测定不同温度条件下的脱色效果,处理时间为24 h(表1)。
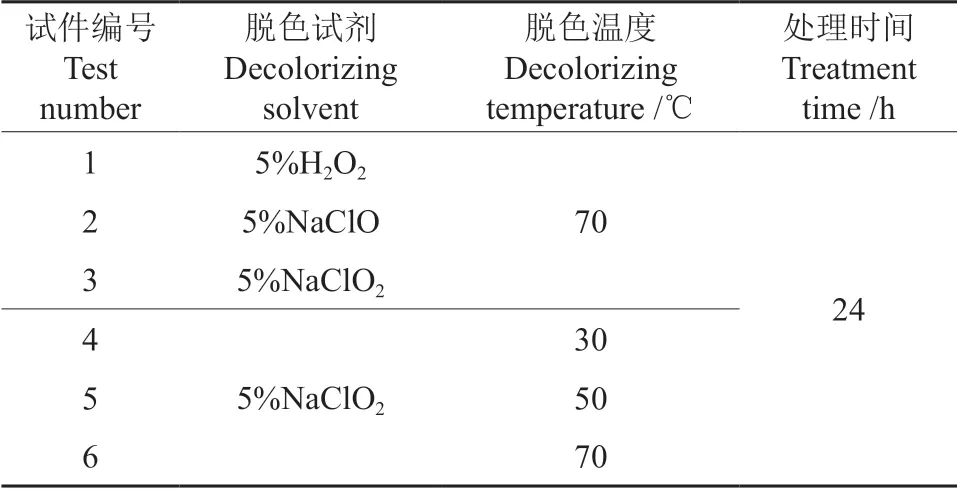
表1 脱色处理试验方案Table 1 Decolorization test programs
将冲洗干净的木块置于1%的NaOH 溶液中,抽真空5 min,根据试验方案配制脱色试剂并设置温度,24 h 后将木块取出,冲洗干净,自然晾干。
1.3 色度指标的测定
使用色差计测量脱色处理前后泡桐木材试样表面的明度值L*、红绿轴色品指数a*、黄蓝轴色品指数b*,每个处理设置3 块重复试样,在每块试样的脱色面上平均取上下左右4 个点,共12 个测色点,取12 个测色点的平均值作为相应处理条件下的颜色指数。各参数的变化用脱色处理前后参数的差值表示,得到ΔL*、Δa*、Δb*、色差ΔE和亨特白度WH,计算方法如公式(1)~(4)所示:
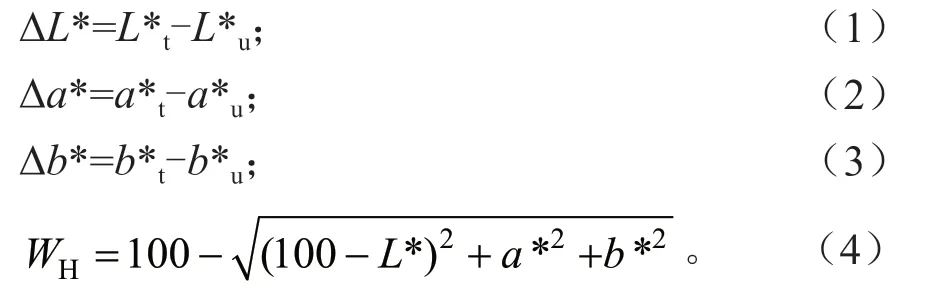
式中:t 表示脱色处理后的试样;u 表示未处理的试样。
1.4 化学组分的测定
纤维素、半纤维素、酸溶木质素的含量参照实验室分析处理程序NREL/TP-510-42618、抽提物参照GB/T35816—2018、酸不溶木质素参照GB/T35818—2018 的方法进行测量。
1.5 FTIR 数据的采集
试验所用红外光谱仪为美国ThermoNicolet公司生产的NicoletiS50 型傅里叶变换红外光谱仪,测试光谱范围4 000~400 cm-1,分辨率为4 cm-1,扫描次数为64 次。
1.6 热重分析
热重分析(TGA)采用TGA(Q50)热重分析仪。称取2 mg 热分析样品进行分析,升温速率为20 ℃/min,同时加入氮气(60 m L/min)作为惰性载体,温度范围在30~800℃之间。
2 结果与分析
2.1 脱色前后泡桐木材的材色分析
泡桐木材采用不同脱色剂进行脱色后,其亮度L*、红绿色品指数a*、黄蓝色品指数b*以及亨特白度WH和色差ΔE如图1所示。经H2O2、NaClO、NaClO2处理后桐材的L*、b*、WH值均有明显提高,说明3 种试剂的脱色效果明显。其中脱色效果最好的是H2O2,色差值达到了23.84,NaClO2次之,色差值为15.08,NaClO 是11.68。经H2O2脱色的桐木的L*值由未处理的63.47 提高到85.67,提高了22.32,WH值由60.29 提高到72.57,提高了12.28,b*值由未处理的15.05 提高到了23.32,经脱色后的桐木黄度增大。从图1可以看出,经H2O2脱色后木材的L*、b*、WH提高最大,a*减小最少,色差达到最大。根据色度参数的变化,H2O2脱色效果最好,NaClO2次之,NaClO 不明显,脱色后色差、白度和亮度值分别为11.68、64.12 和72.27,均为3 种脱色剂中最小。

图1 不同脱色剂脱色条件下木材的色度学参数Fig.1 Color parameters of wood under different solvent decolorizing conditions
泡桐木材在不同温度条件下,以NaClO2溶液作为脱色剂进行脱色后,其亮度L*、红绿色品指数a*、黄蓝色品指数b*以及亨特白度WH和色差ΔE如图2所示。L*和WH均随着温度的升高而增大,其中L*在70℃时的最大值为76.82,在30℃时的最小值为74.08,WH的最大值为67.96,最小值为63.45;a*和b*均随着温度的升高而减小。70℃时色差达到最大,为15.08,50℃时色差略低于30℃和70℃。综合各色度参数分析,在温和温度条件下,温度越高,NaClO2溶液脱色效果越好。此外,通过对比图1和图2中试件色差以及白度曲线发现,试剂、温度因素对比条件下,不同试剂的脱色效果差异要比不同温度效果差异更明显。

图2 不同温度脱色条件下木材的色度学参数Fig.2 Color parameters of the wood decolorized under different temperature conditions
图3为不同条件脱色后部分试样的脱色效果对比图。如3 图所示,左边为未脱色木材试样,木材老化变色严重,表面产生很多宽窄不一的深褐色和浅褐色条纹;中间为采用H2O2做脱色剂,在70℃条件下脱色后的试样,脱色后材色品质得到大幅提升,材面变得均匀白净;右边为采用NaCLO2做脱色剂,在70℃条件下脱色后的试样,脱色后材色品质也得到较大幅度提升,但效果略低于中间试样。

图3 不同条件(左:未脱色;中:H2O2,70℃;右:NaCLO2,70℃)的脱色效果Fig.3 Decolorization effect after different decolorizing conditions (From left to right:untreated;H2O2,70℃,NaCLO2,70℃)
2.2 脱色前后泡桐木材的化学组分分析
经过不同脱色剂脱色处理后,泡桐木材样品的化学组分变化如图4所示。从图4中可以看出,经3 种脱色剂分别脱色后,桐木样品的主要组分相对含量发生了明显变化,且不同试剂处理后变化不同,但相同的是,经过脱色后,纤维素相对含量均有所增加,半纤维素、木质素、抽提物相对含量均减少。其中经H2O2溶液脱色后组分相对含量变化最大,纤维素由47.9%增大到63.62%,半纤维素由19.39%降低到8.21%,酸不溶木质素由27.02%降低到26.32%,酸溶木质素由6.84%降低到5.65%,抽提物相对含量由3.18%降低到0.12%,结合色度参数分析,抽提物含量大幅降低,也是H2O2对桐材的脱色效果好的重要原因之一。经NaClO2脱色后泡桐样品的主要组分相对含量变化居中。NaClO溶液脱色后组分相对含量变化最小,纤维素含量为51.02%,仅增加了4.02%;酸不溶木质素减少了0.54%,酸溶木质素仅减少了1.61%,木质素共减少了2.15%,抽提物含量为2.75%,仅减少了0.43%。此结果与色度参数变化相吻合。

图4 不同脱色剂脱色条件下泡桐的化学组分变化Fig.4 Chemical composition changes of Paulownia treated with different decolorizers
在不同温度条件下脱色后,泡桐木材样品的化学组分变化如图5所示。从图5中可以看出,脱色后,各组分相对含量均产生了明显变化,其中纤维素相对含量增加,半纤维素、木质素、抽提物相对含量降低。不同温度下各组分变化不同,其中纤维素相对含量随温度增大而增加,在30、50、70℃条件下,其相对含量分别为54.45%、56.16%、58.38%。随着温度的升高,NaClO2分解率提高,ClO2浓度增大,使脱色效果更好。酸不溶木质素相对含量随温度升高而降低,在30、50、70 ℃条件下分别下降为26.44%、25.06%、24.44%。半纤维素、酸溶木质素和抽提物的相对含量不随温度的升高而呈现规律性变化,此时可能不止ClO2在起作用,可能是新生态氧[O]在起作用。半纤维素和酸溶木质素的相对含量在70℃时达到最低值,分别为12.54%、4.64%。抽提物在50℃时达到最低值(0.32%)。综合来看,70℃条件下NaClO2的脱色效果最为明显,结果与色度参数变化吻合。

图5 不同温度脱色条件下泡桐的化学组分变化Fig.5 Chemical composition changes of Paulownia decolorized under different temperature conditions
2.3 脱色前后泡桐木材的红外光谱特征及分析
木材组分结构中发色基团C=C、C=O、苯环等多存在于木质素,半纤维素和纤维素中也存在—OH、—COOH 等助色基团。脱色的目的是通过不同的试剂和工艺条件处理,尽可能脱除木材细胞内含有较多发色基团的木质素[13-14]和含有易变色物质的抽提物,同时使助色基团转变为更稳定的结构。这里以FTIR 分析为手段,以未处理泡桐材为参照,分析纤维素、半纤维素、木质素的基团在不同脱色工艺条件下特征吸收峰的细微变化,与未处理材的红外光谱图进行对比,进而分析其官能团和化学组分的变化。
泡桐木材经不同脱色剂脱色处理前后红外光谱如图6所示。在3 390 cm-1处出现了羟基中的O—H伸缩振动[15-16],2 910 cm-1为甲基、亚甲基中的C—H 伸缩振动[16],1 740 cm-1是表征木聚糖中酮、羰基的C=O 伸缩振动[11,15-17],1 430 cm-1是表征苯环骨架结合C—H 的平面变形伸缩振动[15,17],1 325 cm-1是紫丁香核的特征振动峰[15,17],1 253 cm-1是木质素酚醚键的伸缩振动[11,16],1 161 cm-1是吡喃糖环上的C—O—C 伸缩振动[15,17]。脱色后表征木聚糖的特征峰1 740 cm-1和表征木质素的1 325 cm-1和1 253 cm-1强度均有所降低,说明半纤维素有所降解,木质素被有效脱除。羟基和亚甲基的吸收峰强度为未脱色材<NaClO<NaClO2<H2O2,与化学组分变化规律相符。

图6 不同脱色剂脱色条件下泡桐的傅里叶红外光谱Fig.6 Infrared spectra of Paulownia wood treated with different decolorizers
泡桐木材在不同温度条件下脱色后红外光谱如图7所示。3 363 cm-1是羟基中的O—H 伸缩振动[15-16],2 887 cm-1为甲基、亚甲基中的C—H 伸缩振动[16],羟基、甲基和亚甲基的吸收峰发生了红移,1 738 cm-1是表征木聚糖中酮、羰基的C=O伸缩振动[11,15-17],1 430 cm-1是表征苯环骨架结合C—H 的平面变形伸缩振动[15,17],1 333 cm-1是紫丁香核的特征振动峰[15,17],1 242 cm-1是木质素酚醚键的伸缩振动[11,16],1 161 cm-1是吡喃糖环上的C—O—C伸缩振动[15,17],893 cm-1是β-葡萄糖苷键、纤维素C-H 弯曲振动[16]。纤维素的特征吸收峰是3 363 cm-1和2 887 cm-11,不同温度条件下这两个峰的强度变化明显,表明不同温度条件下纤维素含量变化有差异。半纤维素的特征吸收峰为1 738 cm-1和1 242 cm-1,这两个峰表现出相似的变化规律,随着温度的升高,峰强变弱,表明半纤维素随着温度的升高降解的程度越来越大。木质素的特征振动峰1 333 cm-1随着温度的升高,也有逐渐减弱的趋势,说明木质素的脱除效果也随着温度的升高越来越好。红外光谱分析所得结论进一步验证了化学组分的变化规律。

图7 不同温度脱色条件下泡桐的傅里叶红外光谱Fig.7 Infrared spectra of Paulownia wood decolorized under different temperature conditions
2.4 热重分析
热重分析是用来检测物质物理化学性能的重要手段之一,能够反映物质的热稳定性以及热分解机理。通过热重分析,可获得木材样品热解过程的失重率以及热解速率等关键参数,进而确定其热解特征指标。使用不同脱色剂脱色处理后样品的热分解变化情况如图8所示。图8a 表示样品的热分解过程可分为三个阶段:平稳热解阶段(热分解起始阶段),第一阶段发生在室温200℃左右,此时样品的内部分子结构重新发生排列,水分出现大量的流失[18];主要热解阶段,基本发生在200~400℃之间,纤维素、半纤维素、木质素等固体组分吸收了大量的热量而进行分解,大量挥发份析出,生物质质量大幅度地下降;炭化阶段,一般发生在450℃之后,生物质发生炭化,生物炭逐渐形成,产生富含炭的残留物[19]。未处理样品在室温至65℃之间有轻微的质量损失,主要是水分的释放阶段。经H2O2脱色的样品DTG 曲线在353℃达到峰值,此时是该样品的最大热降解速率,样品的热重损失为47%。经NaClO 和NaClO2处理后DTG 曲线分别在328℃和330℃达到峰值,相应温度下样品的热重损失分别为55%和54%,略高于未处理材。根据图8b 可知,H2O2和NaClO脱色后热解起始温度高于未处理材,经H2O2脱色样品的热解起始温度更高,NaClO2脱色后热解起始温度低于未处理材。综上,H2O2和NaClO 脱色的样品热稳定性有所提升,NaClO2脱色使得热稳定性略有下降。不同溶剂处理的泡桐材热解温度和质量损失速率不同,这是由于不同的试剂处理导致化学成分的热解过程和成分转化存在差异[20]。

图8 不同脱色剂脱色条件下泡桐的热重分析曲线Fig.8 TG and DTG of Paulownia treated with different decolorizers
在不同温度条件下脱色处理后样品的热分解变化情况如图9所示。从图9a 中可以看出,不同的温度处理导致化学成分的热解过程和成分转化的差异很小。在平稳热解阶段,热重损失量为70℃>30℃>50℃,但是差异幅度不超过10%。30、50、70℃条件脱色样品的DGT 曲线在335、330、333℃温度下的热重损失分别为44%、56%、46%,从图9b 可以看出30℃和70℃热解起始温度几乎相同,50℃条件下略高30℃和70℃。综合分析认为NaClO2在50℃条件下脱色后热稳定性略低于30℃和70℃,这可能与该条件下抽提物含量大量降低有关。

图9 不同温度脱色工艺条件下泡桐的热重分析曲线Fig.9 TG and DTG of Paulownia wood decolorized under different temperature conditions
3 结论与讨论
3.1 结 论
1)兰考泡桐经H2O2脱色后,与未脱色材色差达到23.84,亮度L*和白度WH有较大幅度的提高,显示出最佳的脱色效果;30~70℃温度变化条件下,NaClO2的脱色效果在70℃时达到最佳。
2)脱色后纤维素相对含量大幅增加,半纤维素、木质素和抽提物相对含量均减少,经H2O2溶液脱色后组分相对含量变化最大。化学组分的变化一定程度上揭示了表观色度参数变化的原因和机理。
3)FT-IR 分析结果表明,脱色后,表征木质素和半纤维素的特征基团的吸收峰明显减弱,进一步验证了脱色后木质素、半纤维素含量降低的结果,同时发现C=O 等发色基团的吸收强度减弱,从基团变化的角度揭示材色变化的机理。
4)TG 和DTG 曲线表明脱色前后以及不同脱色工艺获得的样品热解特性有差异,H2O2和NaClO 脱色的样品热稳定性有所提升,NaClO2脱色使得热稳定性略有下降。
3.2 讨 论
泡桐木材的脱色涉及到复杂物理化学变化过程,本研究通过对脱色后的色度、成分、官能团的变化以及热稳定性进行分析,对泡桐木材的脱色机理进行了初步探索,更具体的分子和颜色调控机制还需要在今后进一步开展研究。同时,桐木产业生产实践中,迫切需要高效环保的脱色技术,以提高桐木产品的品质,因此,在进行机理研究的同时,也要结合生产实践,研究高效脱色方法,促进桐木产业提质升级。

