纳米人工骨治疗胸腰椎骨折复位后骨缺损的临床疗效
周 波,王 强,蒋俊锋,钱玉强,陈 亮,杨 斐,张 行,江 龙
宜兴市人民医院骨科,宜兴 214200
胸腰椎骨折常合并疼痛及后凸畸形,严重者可伴神经功能损伤。单纯后路椎弓根钉棒系统复位骨折椎体是目前常用的手术方式,术中采用撑开复位技术可显著改善骨折椎体的高度、椎管占位程度及矢状面形态,然而,术后椎体内常发生骨缺损[1-2]。后路椎弓根钉棒系统虽可复位椎体外形,但无法修复椎体内部支架结构,远期骨折不愈合及内固定失败的风险亦随之增加[3-4]。本研究应用术中三维CT评估胸腰椎骨折复位后骨缺损情况并使用纳米人工骨填充,取得了满意效果,现报告如下。
1 资料与方法
1.1 一般资料
2017年2月—2019年3月,收治单节段胸腰椎骨折患者64例(排除骨质疏松、陈旧性骨折、感染、结核或病理性骨折),术前X线片示骨折椎体压缩程度> 50%,采用后路椎弓根钉棒系统固定复位,其中32例术中采用纳米人工骨修复骨缺损(观察组),另32例未行纳米人工骨填充(对照组)。
观察组男23例,女9例 ;年龄为21 ~ 56岁,中位年龄41岁;骨折椎体:T102 例,T115 例,T1212例,L17例,L24例,L32 例 ;AO分型[5]:A3型5例,A4型11例,B2型16例;胸腰椎损伤分型及评分系统(TLICS)评分[6]:4分9例,5分18例,6分5例;就诊时3例存在双侧或单侧下肢感觉和肌力减退。对照组男24例,女8例;年龄为24 ~ 61岁,中位年龄42岁;骨折椎体:T101例,T117例,T1214例,L17例,L23例;AO分型:A3型5例,A4型9例,B2型18例;TLICS评分:4分8例,5分17例,6分7例;就诊时4例存在双侧或单侧下肢感觉和肌力减退。2组患者一般资料差异无统计学意义(P> 0.05),具有可比性。
1.2 手术方法
患者全身麻醉后俯卧于拱形垫,通过C形臂X线机透视定位骨折椎体及预固定节段,做后正中纵向切口并沿椎旁肌行骨膜下剥离,在骨折椎体的上、下椎体双侧置入椎弓根螺钉。安装连接棒后撑开复位骨折椎体。观察组术中即刻行三维CT(西门子公司,德国)检查椎体复位程度及前方骨缺损情况,拆除一侧连接棒后沿骨折椎体单侧椎弓根开孔并制备骨性通道直至椎体前柱,经套管注入液态Cem-OsteticTM纳米人工骨(伯克利生物材料公司,美国,主要成分为60%硫酸钙、24%羟基磷灰石和16% β-磷酸三钙)。安装连接棒拧紧螺帽,放置引流管,逐层缝合切口。对照组术中摄X线片评估骨折复位情况,骨折椎体根据术前CT是否存在椎弓根骨折进行选择性置钉,不采用纳米人工骨填充。对照组术前存在神经损伤者术中接受症状侧椎板开窗减压,保留棘突及韧带。2组术中均未行椎间融合。
术后予以预防感染治疗,切口引流管于48 ~ 72 h拔除,2周拆线,拆线后可在胸腰椎支具保护下下床活动。
1.3 观察指标
记录手术时间、术中出血量、内固定节段、术中及术后并发症情况。术前、术后3 d及末次随访时行X线及三维CT检查,记录术前、术后3 d及末次随访时局部后凸角、椎体楔形角、骨折椎体前缘高度及骨折椎体椎管占位率(以骨块占比表示)[7-8]。测量术中骨折复位后及术后3 d骨折椎体的骨缺损程度。骨缺损的诊断标准为CT显示椎体内存在被骨质包围的相对独立低密度区域。骨缺损程度以骨缺损率表示,骨缺损率(%)=骨折椎体复位后空腔体积/骨折椎体体积×100%,空腔体积与骨折椎体体积通过Mimics软件导入PACS薄层数据、采用CT值重建法计算[9]。末次随访时行三维CT检查评估骨融合情况。采用Oswestry功能障碍指数(ODI)[10]评估腰椎功能,采用Frankel分级[11]评估神经损伤程度。
1.4 统计学处理
采用SPSS 21.0软件对数据进行统计分析。符合正态分布的计量资料以表示,组内比较采用配对t检验,组间比较采用独立样本t检验;计数资料以例数或百分数表示,组间比较采用χ2检验 ;以P< 0.05为差异有统计学意义。
2 结 果
2.1 手术情况
观察组固定节段3 ~ 5个,术中出血量为190 ~ 720(360±80)mL,手术时间为75 ~ 130(95±17)min ;术后发生脑脊液漏1例,切口愈合不良2例。其中2例术前合并下肢神经症状者术中三维CT显示椎管内骨块移位仍明显,予以椎管减压术。对照组固定节段3 ~ 5个,术中出血量为160 ~ 650(320±62)mL,手术时间为60 ~ 150(85±21)min ;术后发生切口愈合不良1例。2组固定节段、术中出血量及手术时间差异无统计学意义(P> 0.05)。所有患者均未出现新的神经并发症或原有神经损伤加重。
2.2 影像学参数比较
观察组随访12 ~ 37(18.5±4.4)个月,对照组随访 12 ~ 28(16.6±4.0)个月。2 组患者术后 3 d及末次随访时局部后凸角及骨折椎体楔形角小于术前,骨折椎体前缘高度高于术前,差异均有统计学意义(P< 0.05,表1);2组术后3 d 骨折椎体椎管占位率均低于术前,差异有统计学意义(P<0.05,表1);2组末次随访时局部后凸角、骨折椎体楔形角及骨折椎体前缘高度与术后3 d相比,差异均无统计学意义(P> 0.05,表1)。观察组术后3 d骨折椎体内骨缺损率低于术中,且低于对照组,差异均有统计学意义(P< 0.05,表1)。术后3 d,2组局部后凸角、骨折椎体楔形角、骨折椎体前缘高度及椎管占位率差异均无统计学意义(P> 0.05,表1)。末次随访时观察组骨折椎体楔形角小于对照组,骨折椎体前缘高度高于对照组,差异均有统计学意义(P< 0.05,表1);末次随访时2组局部后凸角比较,差异无统计学意义(P>0.05,表1)。
表1 2组患者手术前后影像学参数Tab. 1 Radiographic parameters before and after operation in 2 groups n=32,
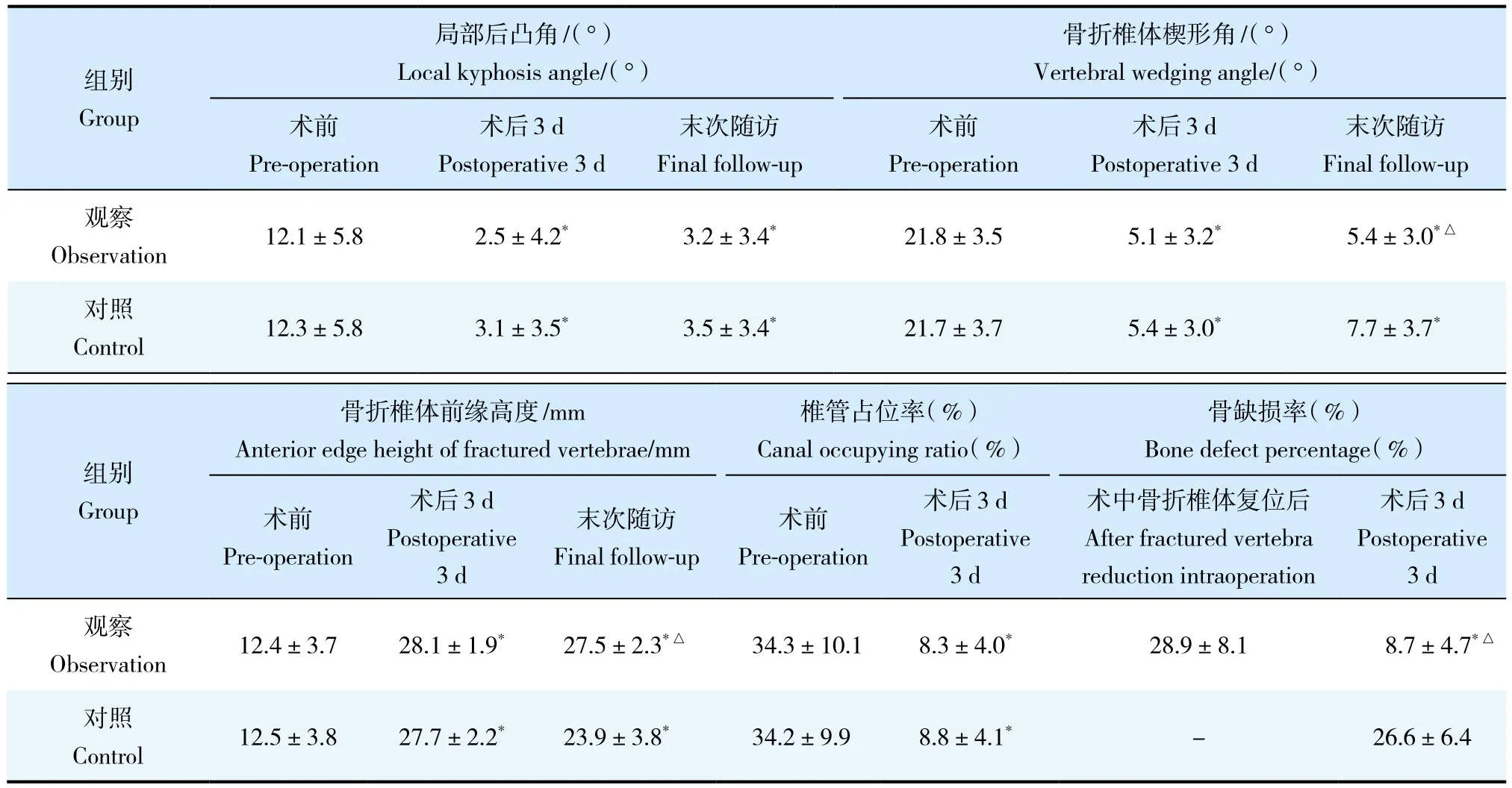
表1 2组患者手术前后影像学参数Tab. 1 Radiographic parameters before and after operation in 2 groups n=32,
注 :*与术前相比,P < 0.05 ;△与对照组相比,P < 0.05。Note :* P < 0.05,compared with pre-operation ;△ P < 0.05,compared with control group.
末次随访Final follow-up观察Observation 12.1±5.8 2.5±4.2* 3.2±3.4* 21.8±3.5 5.1±3.2* 5.4±3.0*△组别Group局部后凸角/(°)Local kyphosis angle/(°)骨折椎体楔形角/(°)Vertebral wedging angle/(°)术前Pre-operation术后 3 d Postoperative 3 d末次随访Final follow-up术前Pre-operation术后 3 d Postoperative 3 d对照Control 12.3±5.8 3.1±3.5* 3.5±3.4* 21.7±3.7 5.4±3.0* 7.7±3.7*术后 3 d Postoperative 3 d观察Observation 12.4±3.7 28.1±1.9* 27.5±2.3*△ 34.3±10.1 8.3±4.0* 28.9±8.1 8.7±4.7*△组别Group骨折椎体前缘高度/mm Anterior edge height of fractured vertebrae/mm椎管占位率(%)Canal occupying ratio(%)骨缺损率(%)Bone defect percentage(%)术前Pre-operation术后 3 d Postoperative 3 d末次随访Final follow-up术前Pre-operation术后 3 d Postoperative 3 d术中骨折椎体复位后After fractured vertebra reduction intraoperation对照Control 12.5±3.8 27.7±2.2* 23.9±3.8* 34.2±9.9 8.8±4.1* - 26.6±6.4
2.3 临床疗效及骨融合情况
观察组和对照组术前ODI分别为(42±11)%、(46±9)%,末次随访时分别为(7±2)%、(8±2)%,末次随访时均低于术前,差异有统计学意义(P< 0.05)。末次随访时观察组术前Frankel分级C级1例恢复至D级;D级2例恢复至E级1例,仍为D级1例;E级29例无变化。末次随访时对照组术前Frankel分级C级1例仍为C级;D级3例恢复至E级2例,仍为D级1例;E级28例无变化。末次随访时观察组所有椎体内骨缺损填充纳米人工骨处都有新骨形成,获得骨性融合,无螺钉移位或断棒发生。对照组末次随访时14例(43.7%)椎体内骨缺损仍存在,2例出现近端螺钉切割,1例出现螺帽松动。观察组典型病例影像学资料见图1。
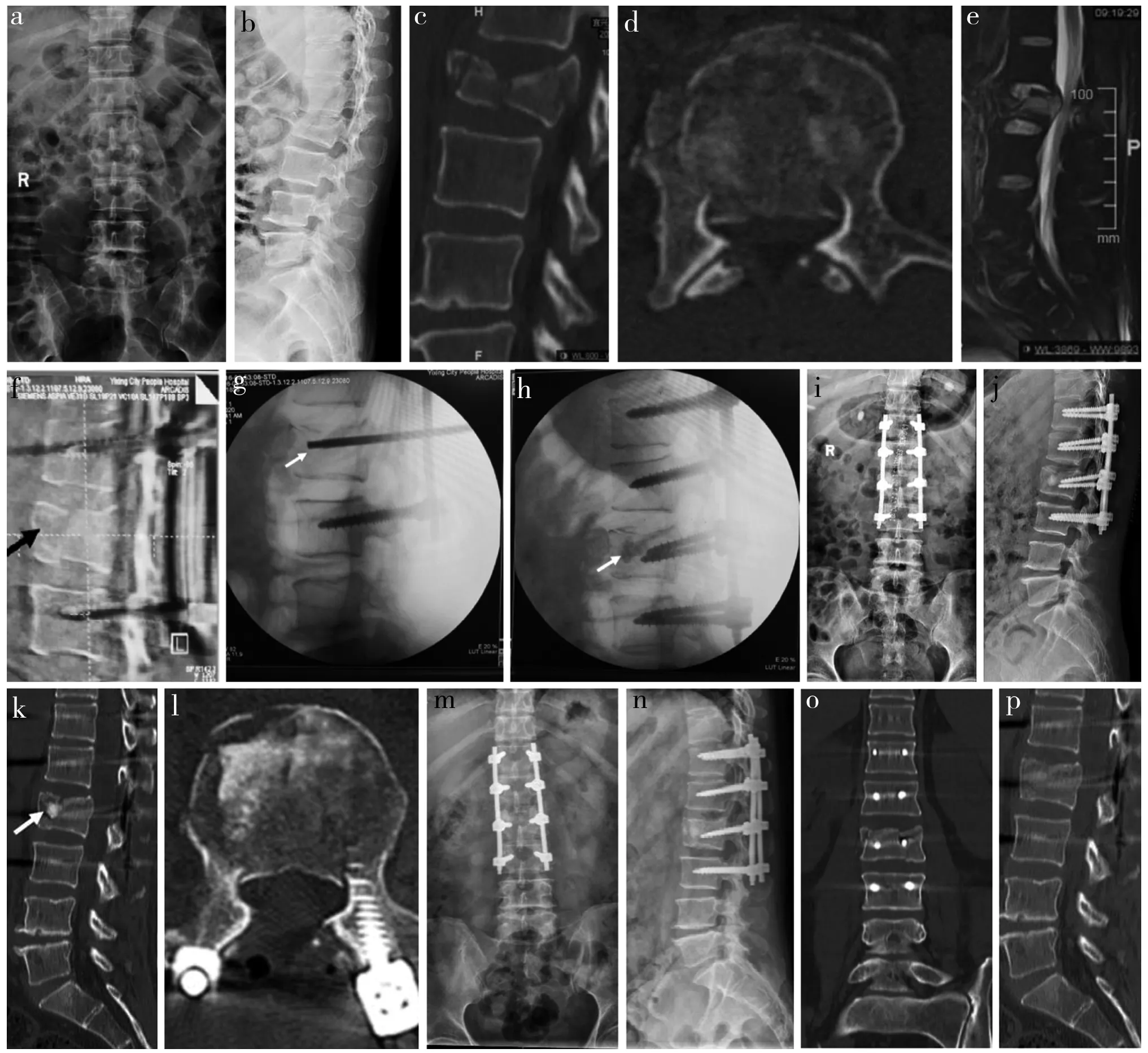
图1 观察组典型病例影像学资料Fig. 1 Imaging data of a typical case in observation group
3 讨 论
近年来,随着椎弓螺钉技术的广泛应用,后路逐渐取代前路成为脊柱外科手术的首选入路。与前路手术相比,后路椎弓根螺钉技术以三柱固定为基础提高了把持力,结合弯棒矫形技术可以更好地纠正骨折所致后凸畸形,对于椎管内占位严重且复位骨折椎体高度后椎管骨块移位仍明显者可直接减压椎管,松解脊髓及神经[12-15]。然而,胸腰椎骨折经后路钉棒复位后,椎体前柱空腔的发生率较高,文献[1,16-17]报道为52% ~ 100%。既往研究[1,18-19]指出,骨缺损的相关危险因素包括椎体压缩程度> 50%、伤椎过度撑开、术前上位椎间盘受损、骨密度T值< -2.5及骨折分型。本研究入选病例骨折分型为A3、A4及B2型,椎体压缩程度均> 50%,此类患者经钉棒撑开复位后更容易出现前柱骨缺损。
有研究[20]表明,骨缺损范围大且长期存在,可导致椎体不愈合,后期出现椎体骨不连的可能大大增加。此外,如前柱支撑不良则后方内固定应力亦增加,易导致术后椎体前方塌陷、内固定失败甚至后凸畸形复发。对于前柱压缩程度重或合并椎间盘损伤的胸腰椎骨折而言,单纯使用后路椎弓根钉棒撑开技术存在一定局限性。近年来,国内外学者[16,21-22]在使用椎弓根螺钉的基础上,通过改良手术方式以减少术后并发症的发生,主要措施包括经骨折椎椎弓根注入骨水泥、经骨折椎椎弓根植入同种异体骨、骨折椎行长钉或短钉固定加强、延长内固定节段及联合前路手术等。然而,急性胸腰椎骨折患者多为青壮年,骨水泥并不适用,且注入后无法取出;同种异体骨存在植骨排斥、感染、费用高等弊端;增加螺钉数量及延长内固定节段进一步增加了患者的经济负担,且牺牲了邻近节段的活动度,增加了邻近节段椎间盘退行性变的风险;联合前路手术则大大延长了手术时间,影响患者的术后恢复。
既往研究中的手术方式多为对急性胸腰椎骨折的预防性前柱支撑治疗,笔者认为,明确术中钉棒复位后是否存在前柱骨缺损是首要环节。本研究观察组采用术中即刻三维CT评估骨折复位情况和前方骨缺损情况,注入液态Cem-OsteticTM纳米人工骨填充,术后骨折椎体高度及椎管占位情况均获改善,骨缺损率也显著降低,末次随访时所有患者均获得骨性融合。此外,观察组有2例术前合并下肢神经症状者术中三维CT显示椎管内骨块移位仍明显,予以椎管减压术。对照组采用术中常规X线片观察骨折复位情况,术后骨折椎体高度及椎管占位情况均获改善,然而骨缺损率为(26.6±6.4)%,末次随访时14例椎体内骨缺损仍存在。由此可见,术中即刻行CT检查能有效评估骨折复位后骨缺损范围、椎管内骨折块移位程度及是否需进一步行椎管减压,明显优于常规X线片。
纳米人工骨的主要成分为羟基磷灰石,可混合硫酸钙、磷酸三钙、骨形态发生蛋白等。闫宏伟等[23]研究了人工骨浆复合骨形态发生蛋白对成年山羊椎体骨缺损的修复作用,结果显示,其具有较强的传导成骨和诱导成骨活性,而且生成的新骨有良好的强度和刚度。王冰等[24]应用钛质网笼填充人工骨辅助前路颈椎钢板治疗颈椎病,所有病例术后均获得骨性愈合,随访中未发现钛网移位、钢板断裂或螺钉松动。因此,他们认为纳米人工骨是一种较为理想的植骨融合材料,但远期效果仍需要进一步观察。本研究选用Cem-OsteticTM纳米人工骨,其具备传导成骨和诱导成骨活性,且组织相容性较好[25]。术中撑开复位骨折椎体后,经单侧椎弓根入路制备通道,放置椎体成形工作套管并注入液态人工骨,因其具备较好的流动性,可较好地充填缺损区域。本研究中观察组末次随访时所有椎体内骨缺损填充纳米人工骨处都有新骨形成,骨折愈合满意,无螺钉移位或断棒发生。
综上,术中即刻行三维CT检查明确骨缺损后采用人工骨填充获得骨性融合,可使椎体内部稳定,降低内固定应力,减少远期内固定失败的发生。但本研究病例数较少,且缺乏远期疗效对比研究,今后将通过增加样本量、延长随访时间,进一步明确该技术的远期效果。

