可变角度零切迹椎间融合器治疗单节段颈椎病的近期疗效
赵天翌,史洪洋,孙晨曦,侯 洋,史国栋
海军军医大学长征医院脊柱外科,上海 200003
颈椎病是以颈椎椎间盘退行性变及其继发的一系列颈椎失稳、髓核突出、骨赘形成、韧带肥厚和椎管狭窄等病理改变为基础的退行性疾病,根据发生原因可分为神经根型、脊髓型、交感型、椎动脉型及混合型等,是导致成人颈椎脊髓功能障碍的首要原因[1]。颈椎前路椎间盘切除融合术(ACDF)是治疗颈椎病的有效术式,其通过切除病变节段椎间盘及其他压迫因素对脊髓进行有效减压,恢复颈椎曲度,使颈椎神经和脊髓功能得到恢复[2]。但是,采用ACDF治疗的患者中约21%会出现吞咽困难和异位骨化[3-4]。为了避免上述并发症的发生,颈前路零切迹椎间融合器(Zero-P)应运而生,有研究[5-6]证实,其具有良好的手术效果和较低的术后吞咽困难发生率。但Zero-P增加了术后融合器沉降及颈椎曲度丢失的风险[7],并且螺钉置入角度固定、操作具有一定难度。可变角度零切迹椎间融合器(Zero-P VA)是新一代Zero-P,近年逐渐投入临床使用。本研究纳入82例ACDF术中采用Zero-P VA治疗的单节段颈椎病患者,观察并分析其近期临床疗效。
1 资料与方法
1.1 一般资料
纳入标准:①有脊髓型和/或神经根型颈椎病症状;②颈椎X线片、CT和MRI等影像学检查证实存在单节段脊髓或神经根压迫;③经3个月以上规范非手术治疗无效。排除标准:①有颈椎手术史;②合并后纵韧带骨化、严重颈椎后凸畸形;③合并肿瘤或任何严重的全身性疾病(如心力衰竭等)。根据上述标准,纳入2017年5月—2019年3月采用Zero-P VA行颈椎前路椎间盘切除融合术(ACDF)治疗的单节段颈椎病患者82例,所有手术由同一医师团队完成。其中男35例、女47例,年龄 27 ~ 66(47.6±10.7)岁,手术节段C3/C419 例、C4/C520 例、C5/C628例、C6/C715例。
1.2 手术方法及术后处理
患者全身麻醉成功后留置导尿管,取仰卧位,肩背部稍垫高,颈部自然背伸。按常规颈前右侧入路暴露手术节段椎体及其两侧椎间盘前部。透视下明确定位无误后,用Caspar撑开器撑开,对病变椎间隙彻底减压,用大量生理盐水冲洗创腔。随后置入1枚装有人工骨和自体骨混合物的合适大小的Zero-P VA(强生公司,美国;图1)。取出椎体撑开器,以骨蜡封闭骨孔。分别在手术节段上下椎体钻孔,按合适角度置入融合器和螺钉各1枚,透视确认内固定位置良好后锁紧螺钉。透视确认螺钉和融合器位置良好后,冲洗切口并止血,切口上下各另切1个小口置入负压引流管,常规缝合切口。患者术后第1天可于颈托保护下坐起进食并下床行走,颈部制动4周后可去除颈托。
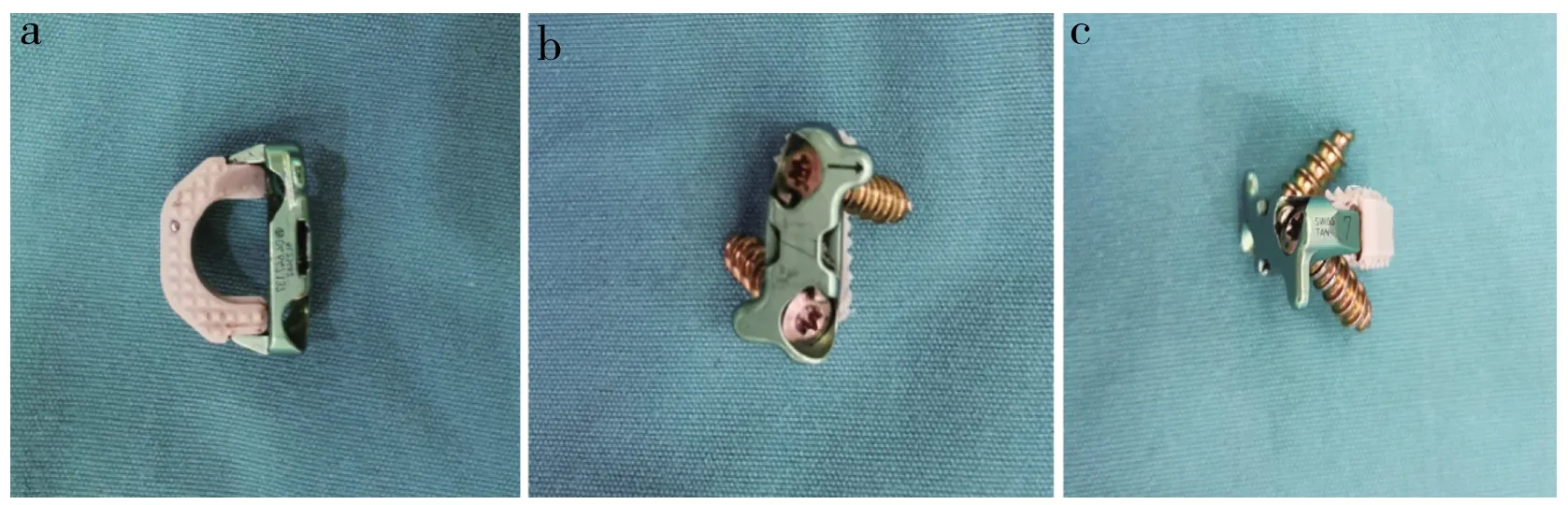
图1 Zero-P VAFig. 1 Zero-P VA
1.3 评估指标
记录手术时间及术中出血量。采用Bazaz评分[8]评估患者术后吞咽困难情况,分为无吞咽困难、轻度吞咽困难、中度吞咽困难及重度吞咽困难。采用疼痛视觉模拟量表(VAS)评分(0 ~ 10分)[9]评估患者术前、术后颈部及上肢疼痛程度。采用日本骨科学会(JOA)评分(0 ~ 17分)[10]评价患者术前、术后神经功能。在术前及术后颈椎侧位X线片上测量C2~7Cobb角和手术节段Cobb角,评估患者手术前后颈椎生理曲度的改变。为了校正影像学测量的观察者内和观察者间的一致性,由3名有经验的观察者独立评估,每人测量3次(若测量差值过大则放弃该次测量数据重新测量),取平均值。
1.4 统计学处理
采用SPSS 20.0软件对数据进行统计分析。符合正态分布的计量资料以表示,采用配对t检验进行手术前后数据的比较;计数资料以例数和百分数表示,采用χ2检验进行手术前后数据的比较;以P< 0.05为差异有统计学意义。
2 结 果
所有手术顺利完成,手术时间为(60.5±6.7)min,术中出血量为(52.3±3.3)mL。所有患者随访18 ~ 24(20.6±2.6)个月。所有患者术后临床症状和神经功能改善满意,术后3个月及末次随访时,患者C2~7Cobb角和手术节段Cobb角均较术前增大,JOA评分较术前增高,VAS评分较术前降低,差异均有统计学意义(P< 0.05,表1)。所有患者术后均未发生吞咽困难。至末次随访时,所有患者均未出现螺钉松动,融合器滑脱、松动或沉降(图2)。
表1 手术前后颈椎曲度、JOA评分及VAS评分Tab. 1 Cervical curvature,JOA score and VAS score at pre- and post-operation N=82,
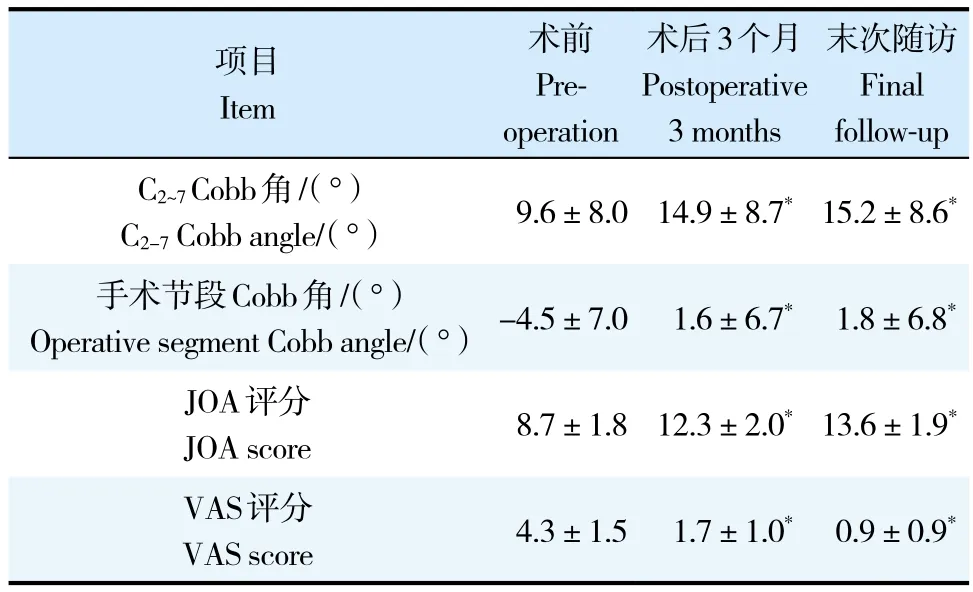
表1 手术前后颈椎曲度、JOA评分及VAS评分Tab. 1 Cervical curvature,JOA score and VAS score at pre- and post-operation N=82,
注 :*与术前相比,P < 0.05。Note :* P < 0.05,compared with pre-operation.
末次随访Final follow-up C2~7 Cobb角/(°)C2-7 Cobb angle/(°)9.6±8.014.9±8.7*15.2±8.6*项目Item术前Preoperation术后3个月Postoperative 3 months手术节段Cobb角/(°)Operative segment Cobb angle/(°)-4.5±7.01.6±6.7*1.8±6.8*JOA评分JOA score 8.7±1.8 12.3±2.0*13.6±1.9*VAS评分VAS score 4.3±1.5 1.7±1.0* 0.9±0.9*
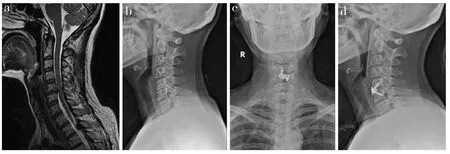
图2 典型病例影像学资料Fig. 2 Imaging data of a typical case
3 讨 论
ACDF作为治疗颈椎病的经典术式,在有效减压、椎间植骨融合基础上联合应用钛板内固定,可直接解除压迫、恢复颈椎曲度,使颈椎神经和脊髓功能得到恢复。但钛板的使用对于前纵韧带的暴露范围要求高,增加了神经和软组织损伤风险,同时也会增加吞咽困难发生的可能性,ACDF术后吞咽困难的发生率一直高居不下,严重影响了患者的日常生活[3-4]。有研究[11]表明,钛板厚度与吞咽困难发生率呈正相关,钛板厚度从2.6 mm减至1.6 mm时,吞咽困难发生率可从22%降至14%[12]。Zero-P于2008年进入临床应用,其在单节段颈椎病颈椎曲度、病变节段曲度、JOA评分、VAS评分的改善方面取得与传统颈椎前路钛融合器系统相似的临床疗效,患者术后颈椎曲度恢复较好,融合率较高,近期随访安全性较好,且术后吞咽困难发生率低[5-6]。本研究中82例患者术后颈椎曲度、疼痛程度、神经功能均明显改善,随访18 ~ 24个月均未见吞咽困难发生。Zero-P降低吞咽困难发生率的可能原因:①Zero-P的零切迹设计避免了传统钛板与食管及软组织的直接接触,减少了术后内置物对食管的刺激;②与传统钛板相比,Zero-P置入时需要暴露的空间更小,术中对肌肉的牵拉损伤更小,减少了局部组织水肿、炎性反应及对食管的刺激[13-15];③本组手术主刀医师操作熟练,能够保证Zero-P前缘良好地置入椎间隙内,减少了对食管及软组织的直接接触和刺激;④本组患者术前均常规行气管推移训练,这可能有助于手术的顺利进行并降低吞咽困难的发生率[16]。
一般认为ACDF术后邻近节段退行性变(ASD)的发生是由于手术本身影响了颈椎的正常生物力学,使手术邻近节段应力负荷明显增加,进而导致退行性变发生,且单节段手术比多节段手术更容易导致颈椎ASD的发生,也有学者[17-18]认为这是颈椎自然退行性变的结果。据统计,Zero-P较钛板内固定系统有着更低的ASD发生率,可能因为Zero-P使颈椎整体活动度得到了一定程度的保存,减少了手术邻近节段的压力负荷,延缓了ASD的发生[15,19-20]。Zero-P同时还可减少异位骨化的产生,颈椎异位骨化的发生主要与术中钛板与相邻节段椎间盘的距离有关,Zero-P的零切迹设计避免了钛板放置时与邻近节段的椎间盘距离过近,从而有助于预防骨赘形成和异位骨化[21]。
然而,Zero-P也有不足,其最大的缺点是较钛板内固定系统增加了术后融合器沉降及颈椎曲度丢失的风险[7]。一项荟萃分析[22]结果显示,Zero-P术后发生沉降的概率约为17.8%,而钛板组的沉降率仅为5.0%,融合器沉降可能会导致术后颈椎曲度的丢失。再有,Zero-P使用4枚固定角度的钛合金螺钉通过终板固定,每个椎体的上终板或下终板均须置入2枚螺钉,螺钉的角度固定,这对术中操作造成一定困难,并且对终板的结构及稳定性造成一定影响[23]。Zero-P VA 作为Zero-P的新一代产品,由聚醚醚酮(PEEK)椎间融合器、带限深的钛合金固定板及可变角度螺钉3部分组成。它改善了Zero-P的置钉方式,每枚融合器在上、下终板仅需要各置入1枚螺钉,且螺钉角度可变,其螺钉置入角度范围为头尾端成角27° ~ 44°、内外侧成角15° ~29°,术后螺钉还可随着应力的变化发生成角角度变化,防止潜在的应力遮挡。而且,Zero-P VA采用了带有限深的的钛合金固定板,这种对角线上的限深设计可防止置入物过度置入椎间隙,保持与椎体前缘的平行。
综上所述,本研究在ACDF术中采用Zero-P VA治疗单节段颈椎病,所有患者术后临床症状和神经功能改善满意,术后均未发生吞咽困难,至末次随访时,所有患者均未出现螺钉松动,融合器滑脱、松动及沉降。但本研究为回顾性研究,未设立对照组、样本量较小、随访时间较短,且未能对ASD及异位骨化等术后并发症的发生情况进行详细统计,未发现融合器沉降、移位等情况也可能与随访时间较短、随访病例数较少有关。关于Zero-P VA对于单节段颈椎病的中远期疗效、安全性和稳定性仍需长期大样本对照研究进一步观察。

