单孔加腹腔镜根治性全胃切除术的初步经验
刘文居,滕文浩,姜键平,陈梅梅,臧卫东
(福建医科大学附属肿瘤医院,福建省肿瘤医院胃肠肿瘤外科,福建 福州,350014)
随着国民经济的发展,人们防癌意识也不断增强,早期胃癌的诊断率逐步提高,目前腹腔镜技术已广泛应用于早期胃癌的手术治疗并得以规范[1-4]。在腹腔镜技术不断发展的过程中,腹腔镜胃癌根治术从腹腔镜小切口辅助发展到完全腹腔镜手术,熟练掌握完全腹腔镜胃癌根治术的学者进一步推动手术微创化,单孔腹腔镜胃癌手术同结直肠手术一样应运而生,并成为腹腔镜技术的热门话题[5-7]。单孔腹腔镜手术(single incision laparoscopic surgery,SILS)是充分利用取标本的小切口置入单孔操作平台完成手术,理论上,戳孔越少,腹壁完整性越好,美容效果越好,切口疼痛越轻,但由于操作空间狭窄,存在同轴效应、暴露困难等问题,SILS在胃癌淋巴结清扫及消化道重建方面确实存在难以逾越的障碍。近年,单孔加一个戳孔腹腔镜手术(single incision plus one port laparoscopic surgery,SILS+1)逐渐受到腹腔镜胃肠外科医师的关注,许多学者将其应用于远端胃癌根治术[5,8-12],但在全胃切除术中却鲜有报道[13-18]。笔者将SILS+1技术熟练应用于远端胃癌手术后,继续对全胃切除术进行微创探索,现将2018年7月至2021年11月我们利用单孔加腹腔镜行根治性全胃切除术的经验总结如下。
1 资料与方法
1.1 临床资料 采用回顾性描述性研究方法,收集2018年7月至2021年11月福建省肿瘤医院单一主诊组施行的46例单孔加腹腔镜根治性全胃切除术的患者,其中SILS+1根治性全胃切除术30例,术中采用直线切割器行食管-空肠功能性端端吻合(functional end-to-end esophagojejunostomy,FETE);单孔加两孔腹腔镜手术(single incision plus two ports laparoscopic surgery,SILS+2)16例,采用管状吻合器行食管空肠Roux-en-Y吻合。纳入标准:(1)术前经胃镜、腹盆腔CT等检查诊断为胃癌,排除远处转移,依据第7版美国癌症联合委员会癌症分期手册[19],临床分期为cT1b~3N0~1M0,拟行腹腔镜手术;(2)肿瘤直径≤5 cm;(3)无中上腹部手术史;(4)美国麻醉医师协会分级Ⅰ~Ⅱ级;(5)术中探查需行全胃切除术;(6)D2淋巴结清扫术;(7)患者及其家属术前均签署手术知情同意书。
1.2 手术方法 均由我院同一组手术医师施行单孔加腹腔镜根治性全胃切除术,手术组医师已具有丰富的完全腹腔镜胃癌根治术及SILS+1远端胃癌根治术操作经验[12,20-21]。采用静吸复合气管插管全身麻醉,患者取仰卧位,右下肢外展50°,右上肢外展90°,似“才”字形体位,见图1。脐上做约1.5 cm小切口穿刺12 mm Trocar,建立气腹,探查后确认可行单孔加腹腔镜根治性全胃切除术,沿脐周自然皱褶处经脐或绕脐延长小切口至4 cm,置入多通道单孔装置,重建气腹,压力维持在13 mmHg,置入30°腹腔镜;左腋前线肋下约2 cm处做1.5 cm小切口,穿刺一辅助12 mm Trocar,作为主刀主操作孔,置入超声刀,多通道单孔装置剩余通道作为主刀辅助操作孔与助手主操作孔,置入无损伤抓钳等普通腹腔镜操作器械;SILS+2为右腋前线肋下约3 cm处加一辅助5 mm Trocar,作为助手主操作孔。常规悬吊肝脏,采用反“()”式完成根治性全胃淋巴结清扫,即先左后右,由下而上的方式,先从大网膜中段稍偏右向脾侧游离,悬吊胃后壁,离断胃网膜左动静脉,清扫No.4sb,见图2。胰腺上缘清扫No.7脾侧,裸化脾动脉,清扫No.11、No.4sa、No.2;然后清扫右侧,游离肝侧大网膜,分离横结肠系膜与胃系膜,裸化胃网膜右动静脉,清扫No.6,见图3。在十二指肠上动静脉与胃右动静脉间的三角形无血管系膜剪开肝十二指肠韧带,清扫No.5,离断十二指肠,上提近断端,清扫No.8a、No.12a、No.9、No.7组肝侧至膈脚。沿肝下缘切除小网膜囊,清扫No.1、No.3,游离食管下段。SILS+1采用FETE吻合不再详述,见图4、图5。SILS+2采用管状吻合器吻合:经单孔快速放入预置提拉7号丝线的吻合器抵钉座,食管下段拟切除线取一小口,完整置入抵钉座,丝线末段位于食管外,用直线切割器闭合切断食管,完成根治性全胃切除,借助丝线拉出抵钉座柄,见图6。定位距Treitz韧带远端20 cm处空肠,关闭气腹,取出标本,经单孔切口拉出空肠,直线切割器闭合并切断空肠,近断端空肠与远断端空肠远端约50 cm处用直线切割器完成空肠侧侧吻合。剪去手套两指,吻合器机身穿过其中一指后经远断端空肠置入约8 cm,用橡皮筋套紧,见图7。腹腔镜穿过另一指后将手套套紧切口保护圈,重建气腹,迅速完成食管空肠吻合,见图8;剪断橡皮筋,见图9,退出吻合器机身,重新建立多通道单孔装置,直线切割器闭合远断端空肠,腹腔镜下缝合加固食管空肠吻合口,包埋空肠远断端,经左右戳孔各留置一细引流管,超声刀经单孔通道解除悬吊,逐层关腹并固定引流管,见图10。

图1 患者体位 图2 结扎胃网膜左血管,清扫No.4sb

图3 结扎胃网膜右血管,清扫No.6 图4 FETE吻合
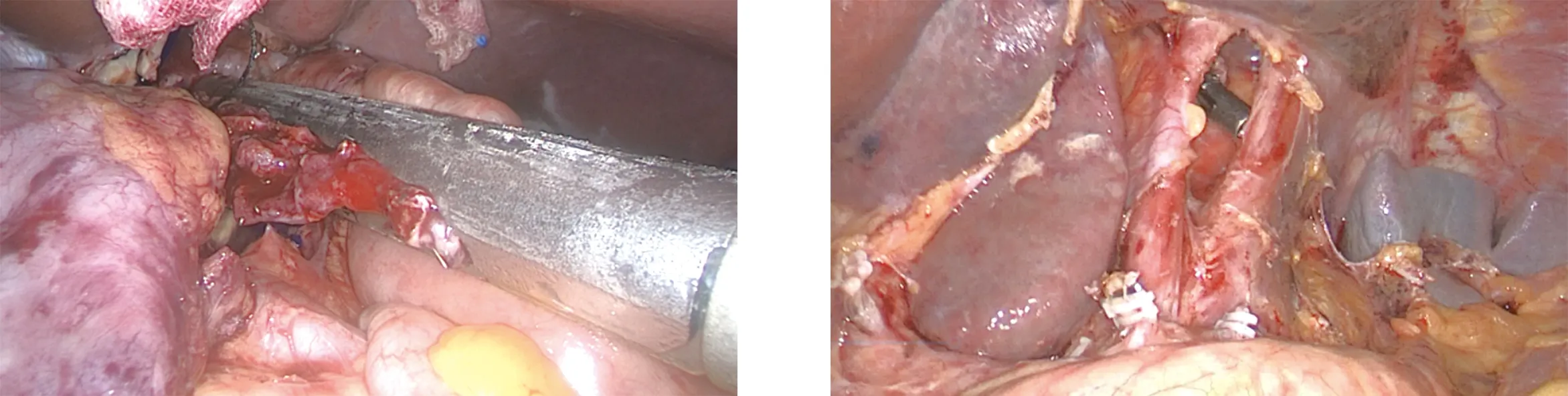
图5 FETE关闭共同开口 图6 清扫结束并置入吻合器抵钉座

图7 远断端空肠置入吻合器机身后橡皮筋套紧 图8 腔镜下完成食管空肠吻合

图9 腔镜下剪断橡皮筋 图10 SILS+2术后切口
1.3 观察指标 观察并记录围手术期情况。术中观察指标:手术时间、术中出血量、术中输血量、增加戳孔率、中转开腹率、切口长度。术后观察指标:术后首次下床活动时间、术后首次进流食时间、术后首次排气时间、术后前3 d疼痛评分[22]、美容评分[23]、术后住院时间及术后30 d内并发症发生率[24]等。术后病理情况:TNM分期、淋巴结清扫数量、肿瘤近切缘距离、肿瘤大小等。详细记录十二指肠残端漏、吻合口漏、吻合口出血、吻合口狭窄、肠梗阻等吻合相关并发症及胰瘘、淋巴瘘、膈下脓肿、胸腔积液、腹腔、肺部感染等与吻合无关的并发症。采用门诊与电话方式随访至术后30 d,了解患者术后生存情况,随访截至2021年12月20日。
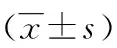
2 结 果
本组46例患者中男36例,女10例,平均(61.6±10.5)岁,体质指数(body mass index,BMI)平均(21.3±3.0)kg/m2,美国麻醉医师协会分级Ⅰ级43例、Ⅱ级3例,11例合并高血压,5例合并2型糖尿病,1例合并慢性阻塞性肺病,临床分期Ⅰ期18例、Ⅱ期28例(cTNM分期基于第7版美国癌症联合委员会癌症分期手册)。46例单孔加腹腔镜根治性全胃切除术均获成功,无一例中转开腹或增加切口。手术时间平均(208.4±31.4)min,术中出血量中位数30(四分位间距为20.0)mL,无术中并发症发生。术后前3 d疼痛评分为(2.3±0.5)分、(1.9±0.6)分、(1.4±0.6)分,术后首次排气时间(53.4±12.1)h,术后腹腔引流管拔除时间(74.3±15.1)h,术后平均住院(8.5±1.3)d,辅助切口长度(4.2±0.5)cm,肿瘤近切缘距离为(3.7±2.3)cm,淋巴结清扫数量为(42.2±14.1)枚。术后30 d并发症发生率为8.7%(4/46),其中肺部感染2例,左胸腔积液、腹腔感染各1例,经保守治疗后患者治愈出院;无明显吻合口相关并发症发生。术后病理切缘均为阴性,术后美容评分(20.1±1.7)分。随访至术后30 d,患者均生存良好。
3 讨 论
相较传统开腹手术,腹腔镜辅助胃癌根治术具有手术创伤小、术后疼痛轻、下床活动早、术后首次排气时间短、住院时间短等优点。腹腔镜远端胃癌根治术早已被第4版日本胃癌治疗指南定为早期胃癌的标准手术[3]。目前国内外已有多个大型随机对照试验证实,腹腔镜远端胃癌根治术在进展期胃癌治疗方面同样具有微创效果,而且手术安全性、肿瘤学疗效与开腹手术相当[25-27]。对于早期胃癌的腹腔镜全胃切除术也已牢固地确立了微创优势[28]。
随着腹腔镜技术水平的不断提高、外科医生的不懈努力及患者对美容的不断追求,单孔腹腔镜外科技术近年逐渐兴起并成为热点。脐周切口可较大程度避开交感神经第1级神经元,疼痛轻微,愈合后瘢痕纤细,切口隐蔽,具有很好的美容效果。利用脐周3~4 cm的单孔完成手术操作,术后腹壁完整性更好,利于早期下床活动,康复更快,术后切口相关并发症更少,同时更美观,住院时间缩短[29]。然而SILS技术在胃癌领域极难推广,利用放置引流管孔道的SILS+1技术逐渐在远端胃癌根治术中得到应用,而在全胃切除方面却鲜有报道,因为安全地完成高位食管空肠吻合是极为困难的。SILS+1技术相较传统5孔法完全腹腔镜手术实际上减少了3个戳孔,总切口长度明显缩小,且腹壁的完整性更好,具有一定的美容效果;但却明显增加手术难度、延长手术时间,相较微创效果,其减少的创伤与手术主要程序增加的创伤孰轻孰重有待商榷。笔者认为,如果手术时间明显延长带来的创伤可能超过微创手术所减少的创伤,腹腔镜手术确实难以进行,为保证手术的安全与质量,应果断中转开腹。笔者主张,应在保证肿瘤根治性原则及手术安全的前提下进行微创的探索,因此,笔者积累丰富的SILS+1远端胃癌根治术操作经验后,将SILS+1技术应用于全胃切除术,并且对于肿瘤位置较高、BMI较大的病例,采用SILS+2技术进行管状吻合器吻合,既确保近端切缘阴性,同时又未延长手术时间,近期效果良好。
我们体会,首先应积累丰富的完全腹腔镜胃癌根治术及SILS+1远端胃癌根治术的操作经验,培养微创意识及精益求精的精神。微创外科医生应始终考虑肿瘤学疗效与手术安全性,在此基础上通过不懈努力稳步实现进一步的微创,进而达到美容的目的,而非为了切口的微创,导致手术的巨创。因此,对于胃部病灶位置较高,肿瘤大体分型为Borrmann Ⅲ型、Ⅳ型,BMI较大的病例,笔者个体化地采用SILS+2技术,并使用管状吻合器吻合,既实现了肿瘤的安全切缘,又保证了微创手术的安全性;本研究中,46例患者行单孔加腹腔镜根治性全胃切除术,无Ⅲ级及以上并发症发生,近端切缘比较满意,手术时间也未见延长,而且术后切口疼痛较轻,美容效果好,患者下床活动早,利于肠道功能的恢复。其次,优化手术流程,不断改进手术步骤:(1)采用“才”字形手术体位,由于主刀左手位于多通道单孔处,采用该体位可改善术者对左侧部分的操作,同时左侧站位为国内多数学者传统腹腔镜站位,更容易接受与推广;(2)常规悬吊肝脏,减轻助手的暴露困难,不仅利于小网膜淋巴结的清扫,而且更有助于食管空肠吻合、加固吻合口;(3)悬吊胃后壁,起到助手左手的作用,使No.4sb、No.4sa、No.7、No.11淋巴结易于清扫,因悬吊更稳固,甚至较传统5孔手术更简单易行;(4)采用反“()”式清扫淋巴结,先左后右,由下而上,减少重新牵拉暴露次数,节省手术时间;(5)前期选择BMI较小、临床分期较早且无腹部手术史的病例;(6)术中证实手术难度高时可采用SILS+2技术,此时助手主操作孔为独立戳孔,与腔镜及主刀左手器械不会互相干扰,助手操作难度未增加,手术难度降低,手术时间不会明显延长,保证了手术的安全,易于推广;(7)充分利用腔镜纱布挡、垫等方式实现局部微暴露,如清扫No.4sb时,可用纱布挡起胃后壁;清扫No.5时,预先于背侧垫一纱布;亦可通过调节体位,利用重力作用协助暴露;(8)橡皮筋套紧固定空肠与吻合器时,可将橡皮筋末圈处置一丝线,方便吻合后腹腔镜下迅速剪断橡皮筋以退出管状吻合器。最后,因单孔的扶镜难度相对较大,建议固定扶镜手,将腔镜置于操作杆上方,有条件时可使用一体机,以减少手柄与光纤的互相影响,在暴露及视野尚可时,勿频繁变动,尤其不必追求完美视野而急于调整镜身,利用30°镜娴熟地调整光纤获得适合角度,更好地暴露术野且不干扰主刀左手操作。
综上,本研究结果初步表明,选择适合的病例,对于具备娴熟SILS+1腹腔镜远端胃癌根治术的术者,单孔加腹腔镜根治性全胃切除术是安全、可行的,且具有疼痛轻、美容等优势。然而,本研究为单中心、小样本、回顾性、非对照的研究,且随访时间较短,其安全性、长期疗效尚待前瞻性随机对照研究证实。

