2-氨基-5-芳基-1,3,4-噁二唑的合成
尹大伟,王龙瑞,刘玉婷*,李金泽,刘 英
(1.陕西科技大学前沿科学与技术转移研究院,陕西 西安 710021;2.陕西科技大学化学与化工学院,教育部轻化工助剂化学与技术重点实验室,陕西 西安 710021)
1,3,4-噁二唑是一类含N、O的五元芳杂环化合物。由于杂原子的存在,这类化合物及其衍生物具有非常特殊的应用活性,因而备受人们关注。在医药领域,1,3,4-噁二唑及其衍生物具有优良的生物活性,如抗癌[1-3]、杀菌[4-5]、抑菌活性[6]等。农药方面,可作为杀虫剂[7-9]和植物生长调节剂[10]。除此之外,1,3,4-噁二唑具有电子传输性质,可用作电致发光材料、有机发光二极管材料等[11-13]。
2-氨基-5-芳基-1,3,4-噁二唑是1,3,4-噁二唑的重要衍生物之一,其结构中有活性氨基,可以进在氨基氮上进行烷基化、酰基化等反应,从而衍生出很多结构,是重要的有机化工中间体和原料。2-氨基-5-芳基-1,3,4-噁二唑的合成一般采用芳醛为原料,先和氨基脲发生缩合反应得到芳醛缩氨脲,然后,在乙酸中以乙酸钠和溴将芳醛缩氨脲自身环合得到[15]。但是该法最大的缺点是需要低温下缓慢滴加溴,温度要求严苛,反应时间长。由于溴易挥发,高温不仅会造成溴的挥发,而且会产生大量副产物。同时,溴具有毒性,会对人身造成伤害,在实验室中不便操作。有鉴于基,本课题组首先以(取代)苯甲醛与盐酸氨基脲为原料合成(取代)苯甲醛缩氨脲,然后将其在1,4-二氧六环中加碘及无水K2CO3催化环合得到一系列2-氨基-5-芳基-1,3,4-噁二唑,并优化反应条件,为噁二唑衍生物的合成提供高效、安全的方法。合成路线见图1。
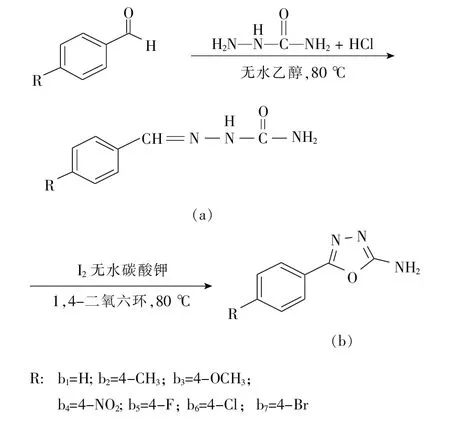
图1 2-氨基-5-芳基-1,3,4-噁二唑的合成路线
1 实 验
1.1 试剂及仪器
芳醛缩氨脲参照文献[14]方法合成。所有试剂均为市售分析纯。
VECTOR-22傅里叶红外光谱仪,德国BRUKER公司;ADVANCE Ⅲ 400 MHz核磁共振仪(DMSO-d6为溶剂,TMS为内标)德国BRUKER公司;X-4型数字显示显微熔点仪(温度计未校正),北京泰克仪器有限公司。
1.2 2-氨基-5-苯基-1,3,4-噁二唑的合成
在干燥的三口烧瓶中依次加入0.1 mmol芳醛缩氨脲、15 mL 1,4-二氧六环、0.15 mmol K2CO3,搅拌均匀后,加入0.06 mmol I2,升温,在80 ℃反应一定时间(TLC监测反应,展开剂为V(乙酸乙酯)∶V(石油醚)=3∶1。反应结束后,冷却至室温,向反应液中滴加10 mL 5% Na2S2O3,并用10 mL CH2Cl2/MeOH[V(CH2Cl2)∶V(MeOH)=10∶1)]萃取3次,合并萃取液,干燥,蒸除溶剂,得到粗产物。无水乙醇重结晶得纯品2-氨基-5-芳基-1,3,4-噁二唑。
2 结果与讨论
2.1 反应机理
经芳醛缩氨脲合成2-氨基-5-芳基-1,3,4-噁二唑,属于分子内的亲核加成-消除反应。实验采用在1,4-二氧六环溶剂中,加入K2CO3和I2,使体系处于碱性条件进行环合,最终得到目标化合物。可能的机理见图2。

图2 2-氨基-5-芳基-1,3,4-噁二唑合成机理
在溶液状态下,芳醛缩氨脲互变为化合物(1);而化合物(1)有一定的酸性,因此会和K2CO3反应而得到化合物(2);化合物(2)发生分子内亲核加成反应成环(3);化合物(3)与I2结合,再脱去HI,得到化合物(4);化合物(4)经互变最终得到2-氨基-5-芳基-1,3,4-噁二唑。
2.2 反应条件的优化
以2-氨基-5-苯基-1,3,4-噁二唑(b1)的合成为模板,讨论反应温度、苯甲醛缩氨脲与无水碳酸钾的摩尔比、溶剂种类、碱的种类及加碘量对产率的影响。
2.2.1 反应温度
在n(苯甲醛缩氨脲)∶n(无水碳酸钾)∶n(碘)=1.0∶1.5∶0.6的条件下,改变反应温度,考察反应温度对产率的影响。结果见图3。
由图3可以看出,随着反应温度的升高,2-氨基-5-苯基-1,3,4-噁二唑的产率升高,80 ℃时产率最高。因为温度过高,反应的副产物增多,会有氧化和碳化现象。因此80 ℃为适宜反应温度。
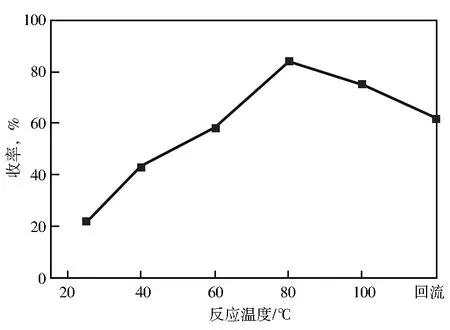
图3 反应温度对b1收率的影响
2.2.2 无水碳酸钾用量
在n(苯甲醛缩氨脲)∶n(碘)=1.0∶0.6,在反应温度为80 ℃时,考察n(苯甲醛缩氨脲)∶n(无水碳酸钾)对收率的影响,结果见图4。
由图4可见,2-氨基-5-苯基-1,3,4-噁二唑的收率会随着无水碳酸钾用量的增加而增加。这是因为随着无水碳酸钾用量增大,反应生成的水及时被吸收,有利于反应向右进行。苯甲醛缩氨脲与无水碳酸钾摩尔比在1∶1.5后,产率变化不大。故适宜n(苯甲醛缩氨脲)∶n(无水碳酸钾)为=1∶1.5。

图4 n(苯甲醛缩氨脲)∶n(无水碳酸钾)对收率的影响
2.2.3 碘用量
在n(苯甲醛缩氨脲)∶n(无水碳酸钾)=1∶1.5,反应温度80 ℃条件下,考察n(苯甲醛缩氨脲)∶n(碘)对收率的影响,其结果见图5。

图5 n(苯甲醛缩氨脲)∶n(碘)对收率的影响
由图5可见,收率随着碘用量的增加而增加,增加到一定比例后收率反而呈下降趋势。从本反应的反应机理可以看出,作为催化剂的碘,先在反应成环过程中与中间体(3)中的氮负离子结合,然后再脱除HI而形成目标产物。但随着碘量的增加,其会与中间体(3)中的氢形成副产物。因此,适宜n(苯甲醛缩氨脲)∶n(碘)为1∶0.6。
2.2.4 溶 剂
在n(缩氨脲)∶n(无水碳酸钾)∶n(碘)=1∶1.5∶0.6,反应温度80 ℃条件下,考察了乙酸、1,4-二氧六环、四氢呋喃、无水乙醇、甲醇对产率的影响,结果见图6。
从图6可以看出,以环状结构的溶剂1,4-二氧六环、THF为溶剂时产率较高,而以乙酸和醇为溶剂时产率较低。本文的反应属于环合反应,因此具有环状结构的溶剂更有利于反应的进行,因此选择1,4-二氧六环为反应的溶剂。

图6 溶剂种类对收率的影响
2.2.5 碱的种类
在n(缩氨脲)∶n(无水碳酸钾)∶n(碘)=1∶1.5∶0.6、1,4-二氧六环为溶剂、反应温度80 ℃ 条件下,考察了乙酸钠、无水K2CO3、Na2CO3、NaOH、KOH对产率的影响,结果见图7。

图7 碱对收率的影响
碱在本反应中的作用是与具有一定酸性的中间体(1)反应得到中间体(2),其碱性不能太强。从图7可以看出,碱为无水K2CO3、Na2CO3时,产率最高;而其他几种碱因碱性强而使产量较低,不利于反应的进行。无水K2CO3在反应中除了起到碱的作用外,还有脱水作用,其效果比Na2CO3更强,因此选择无水K2CO3为反应的碱催化剂。
2.3 底物的拓展
为了验证上述最佳条件的合理性及适用性,利用合成2-氨基-5-苯基-1,3,4-噁二唑优化条件分别合成了一系列2-氨基-5-芳基-1,3,4-噁二唑,其物理性质、产率见表1。
由表1可以看出,实验所得出的优化反应条件适用性较好,所得其他2-氨基-5-芳基-1,3,4-噁二唑的收率均高于2-氨基-5-苯基-1,3,4-噁二唑。从表1也见,当苯环上有推电子基时(b2,b3),产率较低;而当苯环上有吸电子基时,产物的产率更高(b4,b5,b6,b7),吸电子基的吸电子性越强,产率越高。这是因为吸电子基的存在,使苯环上其对位所连的亚胺基的碳正电性增强,有利于亲核取代反应的进行,因此反应产率较高。
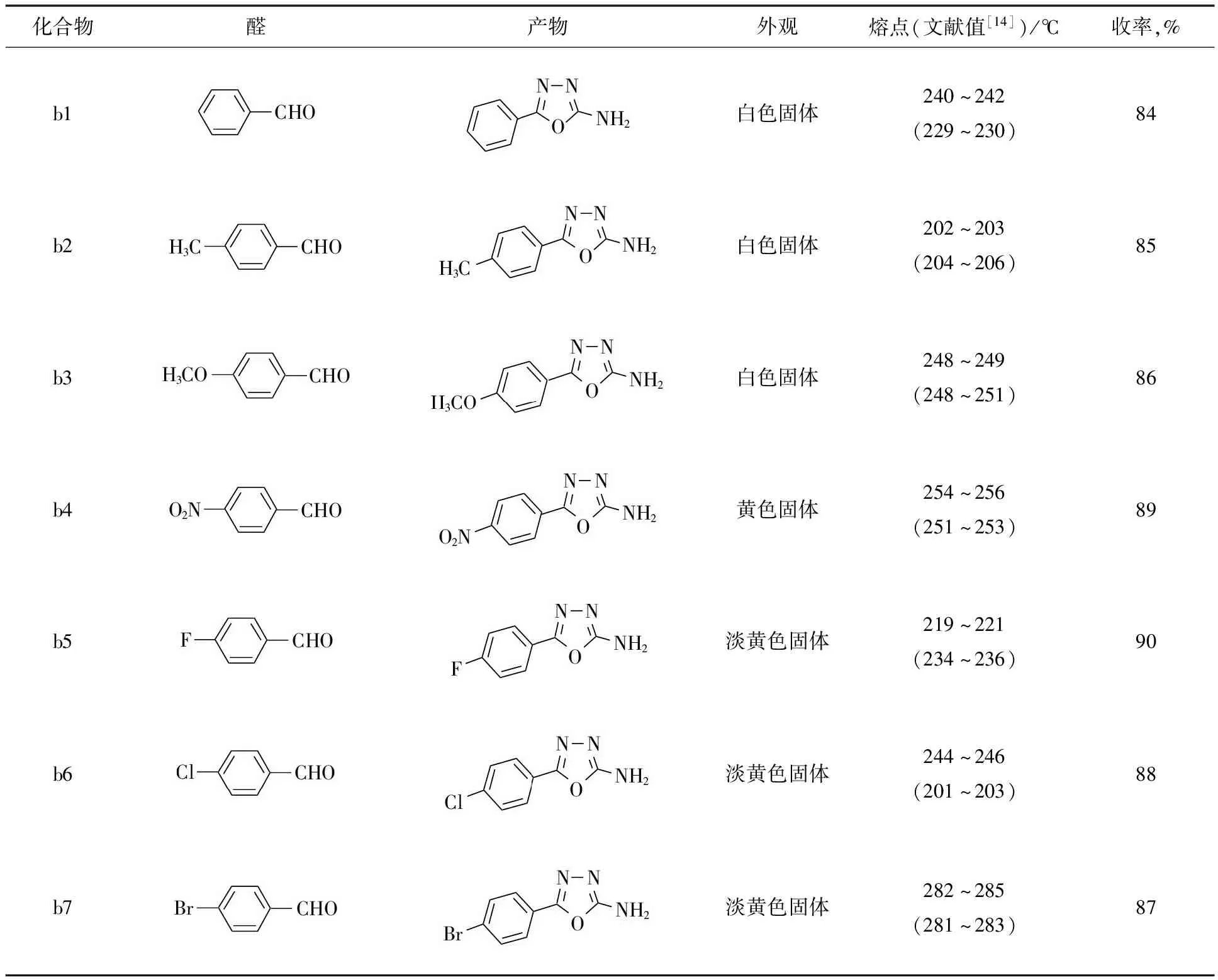
表1 2-氨基-5-苯基-1,3,4-噁二唑的物理性质和产率
3 结 论
以芳醛缩氨脲在1,4-二氧六环中,以无水碳酸钾和碘为试剂反应生成2-氨基-5-芳基-1,3,4-噁二唑。优化合成条件为:n(芳醛缩氨脲)∶n(无水碳酸钾)∶n(碘)的=1.0∶1.5∶0.6,反应温度80 ℃,产率达到84%以上。本方法简便、安全、高效,为1,3,4-噁二唑衍生物的合成及其在医药、农药、材料等领域应用提供了一定参考。

