复合脉冲磁性治疗仪辅助治疗小儿肺炎疗效观察
张新红 新泰市第三人民医院儿科 (山东 泰安 271212)
内容提要:目的:探讨复合脉冲磁性治疗仪对小儿肺炎的辅助治疗价值。方法:选择2017 年10 月~2020 年4 月本院收治的90 例肺炎患儿,以随机数字表法分为对照组和观察组。对照组予以常规治疗,观察组在对照组基础上加用复合脉冲磁性治疗仪,记录两组临床疗效、恢复情况、不良反应等指标。结果:观察组治疗总有效率为93.33%,对照组为91.11%,数据对比P>0.05;观察组治愈患儿退热、湿罗音、喘憋、咳嗽等症状消失时间及住院时间均少于对照组治愈患儿,数据对比P<0.05;治疗前两组血气分析指标、肺功能及炎症因子检测值对比P>0.05,治疗后两组上述指标均较治疗前有所改善(组内对比P<0.05),但治疗后组间对比P>0.05;观察组、对照组各项治疗相关不良反应发生情况对比均P>0.05。结论:复合脉冲磁性治疗仪应用于小儿肺炎辅助治疗中有利于促进患儿尽快恢复健康。
肺炎是儿科常见病,多发病之一,也是严重威胁患儿生活质量、生命安全的主要原因之一[1]。既往临床针对肺炎患儿多采用单纯药物治疗方案,治疗方法单一所产生的弊端(如病程长、痛苦大等)不可避免。近年来,复合脉冲磁性治疗仪的推广使用为小儿肺炎治疗工作提供了新思路,有研究认为针对肺炎患儿加用该仪器或可获得更优辅助治疗效果。本文将以2017年10月~2020年4月作为本次研究时间区间,选取上述区间内90例前来本院就诊的肺炎患儿进行分组研究,探讨复合脉冲磁性治疗仪应用于小儿肺炎的辅助治疗作用,目的在于为提高此类患儿疗效、预后提供相应参考,现总结如下。
1.资料与方法
1.1 临床资料
纳入2017年10月~2020年4月90例肺炎患儿予以随机数字表法分组,其中观察组(n=45),男24例,女21例,年龄3~9岁,平均(5.69±0.21)岁;对照组(n=45),男23例,女22例,年龄3~10岁,平均(5.71±0.20)岁。两组上述数据对比均P>0.05(即分组有可比性)。
纳入标准:①经实验室检验、影像学(胸部X射线片、CT等)检查结合患儿各项体征符合《儿科学》[2]中关于小儿肺炎诊断标准;②意识清醒,家属能够配合患儿积极遵医嘱治疗;③对本次研究内容中涉及的治疗措施均具有良好耐受性;④家属及患儿对本次研究内容具有知情权,自愿参与本次分组研究。排除标准:①出现心力衰竭、呼吸衰竭、中毒性脑病等严重并发症;②合并其他呼吸系统疾病;③恶性肿瘤;④免疫、内分泌等系统异常;⑤心脏、肝脏、肾脏等人体重要脏器严重病变(功能不全);⑥精神类疾病;⑦家属无法配合患儿遵医嘱治疗;⑧对本次研究中涉及的治疗方案无法耐受;⑨非自愿进入本次研究分组。
1.2 方法
对照组:行静脉补液维持人体内环境(具体指标为水、电解质、酸碱度等)平衡、吸氧(低流量,1~2L/min)、根据患儿具体病情给予对症药物(如止咳、抗感染、抗病毒、祛痰等)等。
观察组:在对照组基础上加用复合脉冲磁性治疗仪。具体如下:①仪器由河南省瑞禾医疗设备有限公司提供,配套专用肺炎电极贴片组成成分包括柴胡、金银花、鱼腥草、柴胡、杏仁、川贝、板蓝根等;②常规清洁患儿两侧肺俞穴局部皮肤,之后将专用肺炎电极贴片分别贴于2个治疗仪输出电极板上,电极板分别置于左、右肺俞穴并有效固定;③根据患儿实际情况(如年龄、病情等)调整仪器相关参数,其中温度设定为36~37°C、强度6~8、时间20~30min,待上述操作完成后接通电源开始治疗;④治疗结束后夏季可直接将专用肺炎电极贴片丢弃(无需保留),其他季节建议保留在肺俞穴局部皮肤4h左右方可揭掉,以利于皮肤充分吸收专用肺炎电极贴片上药物,但应注意若患儿出现局部皮肤过敏则不宜保留专用肺炎电极贴片;⑤治疗1次/d、每疗程5~7d,根据患儿实际病情变化情况决定治疗疗程数。
1.3 观察指标
①治疗效果:记录两组临床疗效(涉及治愈、好转、无效等情况),各组总有效率为治愈率+好转率;②恢复情况:记录两组治愈患儿症状消失时间、住院时间,其中症状包括退热、湿罗音、喘憋、咳嗽等;③肺功能:记录两组肺炎患儿治疗前后第1秒用力呼气容积(Forced Expiratory Volume in One Second,FEV1)、用力肺活量(Forced Vital Capacity,FVC)等肺功能指标变化情况;④血气分析指标:记录两组肺炎患儿治疗前后血气分析相关指标变化情况,具体包括血氧饱和度(Oxygen Saturation,SaO2)、动脉血氧分压(Partial Pressure of Oxygen,PaO2)、动脉二氧化碳分压(Partial Pressure of Carbon Dioxide,PaCO2)等;⑤炎症因子指标:两组治疗前后均进行实验室炎症因子检测,记录其白细胞介素-6(Interleukin-6,IL-6)、白细胞介素-8(Interleukin-8,IL-8)、肿瘤坏死因子-α(Tumor Necrosis Factor-α,TNF-α)等指标具体检测结果;⑥不良反应:记录两组治疗期间胃肠道反应(恶心、呕吐)、皮肤过敏(又称药物疹)、面色潮红等不良反应发生情况。
1.4 判定标准
①治愈:治疗7d内发热、肺部啰音、咳嗽、喘憋等症状均消失,实验室检查白细胞计数正常,复查胸部影像可见炎性病灶消失或显著减少;②好转:治疗7d内各项症状好转,实验室检查白细胞计数较之前下降,复查胸部影像可见炎性病灶减少;③无效:治疗7d内各项症状未改善甚至加重,实验室检查白细胞计数较之前未降低甚至升高,复查胸部影像可见炎性病灶未减少甚至增加。
1.5 统计学分析
计量资料数据由±s形式体现,计数资料数据由n、%形式体现,利用SPSS.26软件对各组数据实施相应检验(即t/χ2),结果P<0.05则对比结果差异有统计学意义。
2.结果
2.1 两组治疗效果比较
观察组治疗总有效率相较于对照组对比无统计学意义(P>0.05),见表1。

表1.两组疗效对比(n=45,n/%)
2.2 两组治愈患儿恢复情况比较
观察组治愈患儿肺炎相关症状消失时间、住院时间少于对照组治愈患儿,数据对比存在统计学意义(P<0.05),见表2。
表2.两组恢复情况相关数据对比(n=45,±s,d)
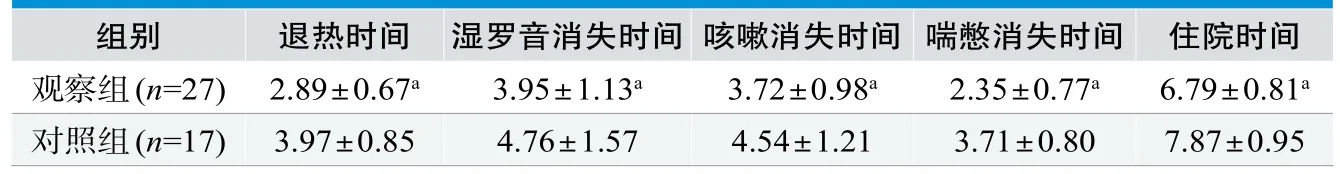
表2.两组恢复情况相关数据对比(n=45,±s,d)
注:与对照组相比,aP<0.05
组别 退热时间 湿罗音消失时间 咳嗽消失时间 喘憋消失时间 住院时间观察组(n=27) 2.89±0.67a 3.95±1.13a 3.72±0.98a 2.35±0.77a 6.79±0.81a对照组(n=17) 3.97±0.85 4.76±1.57 4.54±1.21 3.71±0.80 7.87±0.95
2.3 两组患儿肺功能比较
治疗前两组FEV1、FVC检测值对比结果无统计学意义(P>0.05);治疗后两组FEV1、FVC检测值均高于治疗前,即各组治疗前后肺功能指标组内对比差异有显著性意义(P<0.05),观察组治疗后上述肺功能指标检测值与对照组对比P均>0.05,组间两组治疗后肺功能指标对比无统计学意义,见表3。
表3.两组肺炎患儿治疗前后FEV1、FVC检测值对比(n=45,±s,L)

表3.两组肺炎患儿治疗前后FEV1、FVC检测值对比(n=45,±s,L)
注:与对照组相比,aP>0.05;与治疗前相比,bP<0.05
组别 FEV1 FVC治疗前 治疗后 治疗前 治疗后观察组 1.96±0.52 2.70±0.30ab 2.13±0.44 2.90±0.29ab对照组 1.97±0.51 2.68±0.31b 2.10±0.43 2.88±0.26b
2.4 两组患儿血气分析比较
治疗前两组SaO2、PaO2、PaCO2检测值对比无统计学意义(P>0.05);治疗后两组SaO2、PaO2、PaCO2检测值均较之前有所提升,组内各组治疗前、后数据对比差异有显著性意义(P均<0.05),但两组治疗后血气分析指标组间对比无统计学意义(P>0.05),见表4。
表4.两组肺炎患儿治疗前后SaO2、PaO2、PaCO2检测值对比(n=45,±s)

表4.两组肺炎患儿治疗前后SaO2、PaO2、PaCO2检测值对比(n=45,±s)
注:与对照组相比,aP>0.05;与治疗前相比,bP<0.05
组别 SaO2(%) PaO2(mmHg) PaCO2(mmHg)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 88.57±4.02 96.84±1.29ab 75.36±5.41 94.33±3.24ab 54.36±5.17 37.98±2.36ab对照组 88.59±3.98 96.87±1.27b 75.39±5.39 94.36±3.21b 54.35±5.16 37.99±2.33b
2.5 炎症因子
两组治疗前各项炎症因子水平(包括IL-6、IL-8、TNF-α)检测值对比不存在统计学意义(P均>0.05);治疗后,观察组、对照组IL-6、IL-8、TNF-α水平均较之前有所下降,数据组内各组治疗前后对比均存在统计学意义(P<0.05),但治疗后两组组间各炎症因子水平对比均无统计学意义(P>0.05),见表5。
表5.两组肺炎患儿治疗前后IL-6、IL-8、TNF-α水平变化情况对比(n=45,±s,ng/L)

表5.两组肺炎患儿治疗前后IL-6、IL-8、TNF-α水平变化情况对比(n=45,±s,ng/L)
注:与对照组相比,aP>0.05;与治疗前相比,bP<0.05
组别 IL-6 IL-8 TNF-α治疗前 治疗后 治疗前 治疗后 治疗前 治疗后18.65±2.11 7.54±1.02ab 4.90±0.44 1.09±0.18ab 16.98±2.32 6.99±0.88ab 18.64±2.09 7.58±1.01b 4.91±0.42 1.07±0.17b 17.01±2.33 6.96±0.91b观察组对照组
2.6 不良反应
观察组、对照组各项治疗相关不良反应发生情况对比均无统计学意义(P>0.05),见表6。

表6.两组不良反应对比(n=45,n/%)
3.讨论
肺炎患儿大多起病急、病情复杂多变,若未及时治疗可能危及其生命安全。既往临床治疗小儿肺炎以药物方案为主,通过使用止咳、祛痰、抗感染等药物从而阻碍或延缓病程进展,缓解/消除患儿相关症状[3]。但应注意的是,单一应用药物治疗小儿肺炎具有一定的局限性,由于个体差异客观存在,部分患儿用药治疗效果欠佳,若增加内用药物种类、剂量等势必对其用药安全性造成影响。
复合脉冲磁性治疗仪属于一种叠加治疗措施,将药物与局部皮肤接触后利用电极加热局部温度并实现激发,能够对血液循环、皮肤通透性等起到改善作用,促进药物由皮肤吸收至人体并发挥相应药效。本文中观察组使用复合脉冲磁性治疗仪时,配套专用肺炎电极贴片各药物组成具有消炎行气、通经活血、止痛活络、化痰镇咳、清热散结等功效,通过外用方式有效减少药物相关不良反应,因此与常规药物方案联用并不会对临床用药安全性造成严重影响,同时能够与常规治疗方案通过不同途径共同达到疾病治疗目的[4]。本文也已通过分组研究证实,加用复合脉冲磁性治疗仪的观察组临床总有效率及治疗前后血气分析指标、肺功能及炎症因子指标变化情况与未加用此法的对照组对比并无显著差异,但观察组痊愈患儿症状消失时间、住院时间等恢复情况相关指标优于对照组,此结论与苏爱芳等[5]研究结果相符。但不可否认本文存在一定的弊端(如纳入样本容量、篇幅等),因此并未开展两组远期疗效、预后等内容的对比分析,在今后工作中仍需加强对复合脉冲磁性治疗仪在小儿肺炎治疗中的价值研究。
综上所述,复合脉冲磁性治疗仪应用于小儿肺炎辅助治疗中有利于促进患儿尽快恢复健康。

