氢氧化钠改性丝光沸石吸附二氯甲烷的研究
王心愿,张 佳,2,王鹏飞,2,余金鹏,2
(1.上海化工研究院有限公司,上海 200062;2.上海绿强新材料有限公司,上海 201806)
0 前言
二氯甲烷是一种应用广泛的优良溶剂,是含氯挥发性有机物(Cl-VOCs)的主要来源之一,具有较高毒性和致癌性[1],并且会破坏臭氧层[2]。二氯甲烷废气的处理方法主要有冷凝法、燃烧法、吸附法等[3],其中吸附法是处理高浓度二氯甲烷的有效方法[4-6]。吸附法的关键是选择高效的吸附剂,目前主要吸附剂有活性炭和分子筛两大类[6]。活性炭不耐高温,脱附再生困难[7]。分子筛热稳定性好,易于再生。DENG H等[8-12]使用Y型沸石吸附二氯甲烷,静态吸附量为216~357 mg/g,但是Y型沸石主要是人工合成,合成步骤多,并且吸附多种挥发性有机物(VOCs),吸附二氯甲烷的选择性差。笔者选择来源广泛、成本低、合成容易[13],且孔径与二氯甲烷接近的丝光沸石作为吸附剂[14,4],研究其吸附分离二氯甲烷的性能。
丝光沸石属于正交晶系,孔径为6.5 Å×7.0 Å[15]。GROEN J C等[16]通过研究发现,适当浓度的碱处理丝光沸石可以产生介孔,大幅增加介孔的数量,形成多级孔结构。多级孔沸石中介孔有利于扩散,微孔有利于吸附,两者存在可以提升吸附VOCs的能力[17-18]。目前有关丝光沸石吸附VOCs的文献较少,缺少对丝光沸石动态吸附VOCs的研究[19-22]。笔者采用无机原料合成丝光沸石,使用不同浓度的NaOH溶液脱硅改性丝光沸石,考察其吸附二氯甲烷的性能,以期开发出高效的二氯甲烷吸附剂。
1 实验部分
1.1 实验试剂
碱性硅溶胶,工业纯,w(SiO2)=25.8%,上海硅缘科技有限公司;
偏铝酸钠,化学纯,w(Al2O3)≥41%,上海展云化工有限公司;
氢氧化钠,分析纯,w(NaOH)≥95%,江苏强盛功能化学股份有限公司;
实验室三级水,自制;
二氯甲烷,分析纯,国药集团化学试剂有限公司。
1.2 丝光沸石的合成及改性
丝光沸石的合成方法见文献[23],按照20SiO2∶Al2O3∶2Na2O∶300H2O配制浆液,搅拌均匀,倒入均相反应釜中,170 ℃反应72 h。使用质量为150 g,浓度分别为0.20 mol/L、0.50 mol/L、1.00 mol/L、1.50 mol/L的NaOH溶液,与5 g合成的沸石在60 ℃下共同搅拌0.5 h,获得样品AT-MOR-x,其中x表示NaOH浓度,原粉样品编号为AT-MOR-0.00。
1.3 主要设备与仪器
X射线衍射仪,D/MAX 2500型,日本理学株式会社;
荧光发射光谱仪,S2型,德国布鲁克公司;
红外光谱仪,Nicolet iS50,赛默飞世尔科技公司;
场发射扫描电镜,Merlin Compact,ZEISS集团;
物理吸附仪,ASAP 2020,美国Micromeritics公司。
1.4 样品表征
使用X射线衍射仪分析产品物相,测试条件为:CuKα射线,电压40 kV,电流40 mA,扫描范围5°~50°,数据步长0.02°,扫描速率10°/min。
物质的元素组成使用荧光发射光谱仪测定产品成分,用于表征硅铝比。
固体成键情况在分辨率为4 cm-1的红外光谱仪上测定,测试范围为450~4 000 cm-1,扫描次数为32。
N2吸脱附等温线采用物理吸附仪进行测定。取50~100 mg待测样品置于脱气管中,在350 ℃下真空脱气4 h,然后在液N2温度下进行N2吸附和脱附。使用BET方法由吸附等温线计算样品中总比表面积,通过t-plot法计算样品中的孔径和孔容。
1.5 吸附性能评价
1.5.1 静态水吸附
参考GB 6287—2021 《分子筛静态水吸附测定方法》中饱和氯化钠溶液法测试测定分子筛静态水的吸附。
1.5.2 静态VOCs吸附
选取二氯甲烷为VOCs吸附物种。首先,取1个干燥的称量瓶,使用电子天平称重记录质量m1。其次,装入1 g左右的分子筛样品,200 ℃活化1 h,然后抽真空脱气1 h,再取出称重,记录质量m2。最后,将称量瓶转移到底部倒有足量的VOCs污染物的干燥器中,室温下静态放置24 h后,盖好称量瓶盖子将称量瓶取出,再次称重,记录质量m3。
静态吸附量q静的计算方法为:
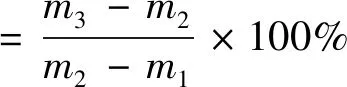
(1)
1.5.3 动态VOCs吸附
动态吸附VOCs测试系统由VOCs发生器、载气控制系统、固定床和气相色谱组成。分子筛先成型,然后制成20~40目的颗粒状样品。获得的颗粒样品先200 ℃脱气1 h,然后真空抽气0.5 h,最后取1 g样品加入到固定床中。使用N2作为载气,流速控制在630 mL/min,负载体积分数为1 000×10-6的二氯甲烷进入固定床吸附,使用气相色谱测试吸附后尾气中二氯甲烷的含量(见图1)。

1—高纯氮气瓶;2—减压阀;3—针型阀;4—VOCs发生器;5—固定床;6—气体流量计;7—气相色谱;8—废气回收塔。
动态测试得到穿透曲线中流出废气的二氯甲烷质量浓度co高于起始进气中二氯甲烷质量浓度ci(取3 794.64 mg/m3)的5%即为穿透;co等于ci的95%即为饱和。
单位吸附质饱和吸附量的计算公式为:
(2)
穿透吸附量qb计算公式:
(3)
式中:q为单位吸附质饱和吸附量,mg/g;qV为体积流量,测试时在0.63 L/min;W为样品质量,g;tc为吸附达到饱和所需时间,min;t为时间,min;qb为穿透吸附量,mg/g;tb为吸附穿透所需时间,min。
为了更好地阐释VOCs吸附过程,使用Yoon-Nelson模型(Y-N模型)拟合穿透曲线,Y-N模型的表示形式[24]为:
(4)
式中:κ为速率常数,min-1,取决于传质区的扩散特性;τ0为50%穿透吸附所需时间,min。
2 实验结果与数据讨论
2.1 碱改性丝光沸石表征
对NaOH改性的沸石进行X射线衍射测试,结果见图2。由图2可以看出:碱改性后的沸石晶型保持,原有的晶体长程有序未破坏,但是衍射峰强度下降;随着NaOH溶液浓度提升,结晶度持续下降,而且下降速率加快,AT-MOR-1.00的结晶度为88.20%,而AT-MOR-1.50的结晶度下降到67.23%。因为碱改性会脱除分子筛结构中的硅,破坏丝光沸石结构,所以NaOH溶液浓度越高,反应越快,溶解硅溶解,造成结晶度快速下降[16,25]。通过X射线荧光光谱测试碱改性的丝光沸石硅铝比,结果见表1。由表1可以看出:原粉的硅铝比为18.35,AT-MOR-1.00的硅铝比为16.93,AT-MOR-1.50的硅铝比为12.14,说明了1.50 mol/L的NaOH溶液会大量脱硅,破坏丝光沸石拓扑结构。

图2 NaOH改性MOR沸石X射线衍射图

表1 NaOH改性丝光沸石前后物性表
NaOH改性丝光沸石N2吸脱附等温线见图3。

图3 NaOH改性丝光沸石N2吸脱附等温线图
由图3可以看出:从AT-MOR-0.00到AT-MOR-1.00,比表面积从361 m2/g增加到375 m2/g,总孔容从0.201 cm3/g增加到0.267 cm3/g,介孔孔容从0.040 cm3/g增加到1.63 cm3/g,微孔孔容从0.162 cm3/g下降到0.119 cm3/g。因为在低浓度NaOH溶液改性时,NaOH溶液不仅会清理孔道内物质,而且还会脱除孔壁组成中的硅原子,破坏微孔孔壁,造成微孔缺陷,微孔相互连接形成介孔,丝光沸石中的小的五元环和四元环微孔参与形成介孔,介孔孔容增加,总孔容对应增加(见图4),圈中即为微孔缺陷后形成的介孔[26-28]。1.50 mol/L的NaOH处理丝光沸石时,对丝光沸石孔道结构损坏过大,可能造成孔道坍塌,因此AT-MOR-1.50的比表面积下降到290 m2/g,总孔容下降到0.205 cm3/g。

图4 碱改性后丝光沸石孔结构变化示意图
不同浓度的NaOH溶液改性的丝光沸石场发射扫描电镜图见图5。由图5可以看出:从AT-MOR-0.00到AT-MOR-1.00,丝光沸石从平整光滑到出现空洞,再产生裂纹,而AT-MOR-1.50表面出现不溶物,如图5中AT-MOR-1.50圈出部分,其他样品则未发现,说明高浓度NaOH溶液处理丝光沸石会生成不溶物,造成沸石孔道堵塞。

(a) AT-MOR-0.00
2.2 静态吸附
丝光沸石对于水、二氯甲烷的静态吸附结果见表2。对于AT-MOR-0.00到AT-MOR-1.00,静态水吸附量从112.9 mg/g增加到122.7 mg/g,二氯甲烷静态吸附量从148.9 mg/g增加到295.2 mg/g。NaOH改性丝光沸石对于二氯甲烷的静态吸附量提升最大。AT-MOR-1.50由于结构破坏和孔道堵塞,相比AT-MOR-1.00,其静态水吸附量明显下降。AT-MOR-1.50的静态水吸附量为108.6 mg/g,静态二氯甲烷吸附量为135.3 mg/g。由表2可以看出:1.00 mol/L NaOH溶液改性丝光沸石的效果最好,静态吸附量提升明显。

表2 NaOH改性丝光沸石的静态吸附
丝光沸石吸附水主要与沸石表面的极性位点,即—OH相关,使用碱液改性后其酸性位点总量未减少,形成介孔和表面空洞使得可接触—OH量增加(见图6),傅里叶红外光谱图上改性后沸石—OH峰明显增强[29-30]。二氯甲烷分子动力学直径为0.33 nm,且分子极性较大[4],丝光沸石吸附二氯甲烷时不存在筛分效应,并能在改性后产生的介孔内发生多层吸附[8],而且表面增加的极性位点也有利于吸附更多的二氯甲烷分子。

图6 NaOH改性丝光沸石傅里叶红外光谱图
2.3 动态吸附
改性前后丝光沸石动态吸附结果和N-Y模型拟合结果见表3。

表3 改性前后丝光沸石动态吸附结果和N-Y模型拟合结果
由表3可以看出:按穿透吸附量从大到小排列依次为AT-MOR-1.00、AT-MOR-0.05、AT-MOR-1.50、AT-MOR-0.20、AT-MOR-0.00,与静态吸附结果一致。AT-MOR-1.00穿透吸附量为86.66 mg/g,饱和动态吸附量为111.71 mg/g,与AT-MOR-0.00样品对比,穿透吸附量提升了196%,饱和动态吸附量提升了124%。穿透吸附量增加幅度大于饱和吸附量增加幅度,说明NaOH溶液改性丝光沸石不仅提升了二氯甲烷的动态吸附量,也提升了丝光沸石吸附二氯甲烷的速率。
为了进一步研究丝光沸石的吸附性能,研究相关沸石的动态吸附,利用Y-N模型进行拟合,结果见图7。

图7 碱改性丝光沸石穿透测试及Y-N模型拟合曲线
动态吸附测试结果与Y-N模型拟合较好,相关系数R2最低为0.965。从AT-MOR-0.00到AT-MOR-1.50,传质区扩散特性的速率常数随着NaOH溶液浓度增加而逐步加大,变化趋势与介孔孔容变化趋势一致,其中AT-MOR-0.00的扩散特性的速率常数为0.197 min-1,而介孔最多的AT-MOR-1.50的扩散区速率常数为0.274 min-1。说明随着丝光沸石介孔的增加,二氯甲烷在沸石内的传质得到改善。
3 结语
(1) 使用合适浓度的NaOH溶液改性,可以制备出分级孔丝光沸石;改性丝光沸石使用NaOH的最佳浓度为1.00 mol/L,反应温度为60 ℃,反应时间为0.5 h。改性的丝光沸石比表面积从361 m2/g增加大375 m2/g;总孔容从0.201cm3/g增加到0.267 cm3/g,其中微孔孔容从0.162 cm3/g下降到0.119 cm3/g,介孔孔容从0.040 cm3/g增加到0.159 cm3/g。
(2) 1.00 mol/L的NaOH溶液改性后的丝光沸石,对二氯甲烷的静态吸附量从148.9 mg/g提升到295.2 mg/g,穿透吸附量从29.29 mg/g提升到86.66 mg/g,饱和吸附量从49.68 mg/g提升到111.71 mg/g;丝光沸石吸附二氯甲烷过程符合Y-N模型,从拟合结果看,碱改性的方法提升了二氯甲烷在丝光沸石中的传质扩散能力,Y-N模型中用于描述传质区扩散特性的速率常数从0.197 min-1提升到0.267 min-1。

