罗沙司他对不同铁代谢状态维持性血液透析患者贫血的影响
郑光毅 洪大情 李贵森 何敬东 张 萍 张振华 邓 菲 魏锦曦 何 东 周莲卉 杨冬梅0 张 燕 薛 痕
肾性贫血是慢性肾脏病(CKD)患者最常见的并发症之一,也是CKD患者发生心血管事件的独立危险因素[1]。补充铁剂和红细胞生成刺激剂(ESAs)是纠正肾性贫血的常用治疗手段。然而,临床上存在部分铁过载的维持性血液透析(MHD)患者,他们由于自身铁代谢调节的异常或者不合理的补铁治疗,导致铁在体内过度蓄积。据报道,使用ESAs和静脉铁剂治疗的透析患者,铁过载发生率可高达84%,并且有30%的患者肝铁负荷可达到血色素沉积的程度[2]。过度蓄积的铁会增加患者体内的氧化应激反应,加重贫血[3];增加感染及心血管事件发生的风险,使患者的死亡率增高[4]。罗沙司他上市以来,已有多项研究结果证实,可有效纠正透析或非透析CKD患者肾性贫血[5-6]。那么,对于铁过载的MHD肾性贫血患者,罗沙司他是否能够有效地改善其肾性贫血?目前尚缺乏针对性研究。为此,本研究前瞻性收集了96例MHD肾性贫血患者资料,分析不同铁代谢状态下使用罗沙司他纠正贫血的疗效和安全性。
对象和方法
研究对象选取2019年8月至2020年9月四川省10个透析中心的MHD肾性贫血患者为研究对象,共纳入资料齐全符合入选条件的患者96例。纳入标准:(1)成年男性血红蛋白(Hb)<130 g/L,女性Hb <120 g/L;(2)年龄>18岁;(3)正在接受维持性血液透析至少3个月的CKD患者;(4)干体重≥45 kg。排除标准:(1)患有由CKD以外的疾病引起的任何其他贫血,例如地中海贫血、镰状细胞性贫血、纯红细胞再生障碍、骨髓增生异常综合征等;(2)恶性肿瘤患者;(3)合并明显感染;(4)无法完成随访研究的患者。促红细胞生成素(EPO)抵抗的定义为EPO治疗≥3个月,治疗剂量≥300 IU/(kg·周),而Hb<110 g/L。本试验获得参加研究的各透析中心伦理委员会批准,所有参试者均签署知情同意书(临床试验注册号:ChiCTR1900025765)。
研究设计本研究为前瞻性临床研究。根据受试者治疗前血清铁蛋白(SF)水平分为SF正常组(SF≤500 ng/L)和铁过载组(SF>500 ng/L)[7]。试验期间,患者可继续使用降压药物、磷结合剂、钙制剂、钙敏感受体激动剂,参考Provenzano等[8]的研究,停用铁剂,禁用已知会影响Hb浓度的药物,如人重组促红细胞生成素(rHuEPO)、雄激素、免疫抑制剂。罗沙司他每周3次口服给药,疗程12周。起始剂量:体重45~60 kg每次100 mg;体重60~160 kg则每次120 mg。若正在接受EPO治疗的患者必须有适当的停药期(如3次/周EPO治疗,停药3d;如1次/周EPO治疗,停药7d)。根据Hb水平对罗沙司他的剂量进行调整(表1),使Hb水平达到并维持在110~120 g/L,最大限度地降低对输血的需求。

表1 罗沙司他剂量调整方案
研究药物罗沙司他胶囊:美国FibroGen公司(批准文号:EHJ-GAS0018321),规格50 mg/粒、20 mg/粒。
血清学指标测定治疗前及治疗结束时,抽取外周静脉血,检测Hb、SF、转铁蛋白饱和度(TSAT)、总铁结合力(TIBC)、血清尿素氮(BUN)、血清肌酐(SCr)、谷丙转氨酶(ALT)、谷草转氨酶(AST)、总胆红素(TBIL)、间接胆红素(IBIL)、直接胆红素(DBIL)、血钾等指标。
疗效评估12周时两组Hb水平和铁代谢指标较基线的变化值。不良反应包括消化道不良反应、电解质紊乱、肝功能损害,过敏反应等。
统计学方法采用《SPSS 25.0》软件进行统计学分析。正态分布的计量资料采用均数±标准差表示,非正态分布的计量资料采用中位数(四分位间距)表示;组间比较采用独立样本t检验(正态分布)或Wilcoxon秩和检验(非正态分布);罗沙司他治疗前后检测指标采用配对样本t检验(正态分布)或Wilcoxon符号秩检验(非正态分布);计数资料采用频数及率描述,组间比较采用χ2检验或Fisher精确概率法;P<0.05为差异有统计学意义。
结 果
受试者基本情况96例患者中男性52例(54.2%)、女性44例(45.8%),平均年龄为54±15岁,54例患者SF≤500 ng/L,42例患者SF>500 ng/L。两组基线指标相较,SF正常组高血压肾病患者少于铁过载组(0vs11.9%,P=0.014),SF正常组患者干体重更低(53vs58 kg,P=0.018),两组年龄、性别差异无统计学意义(表2)。
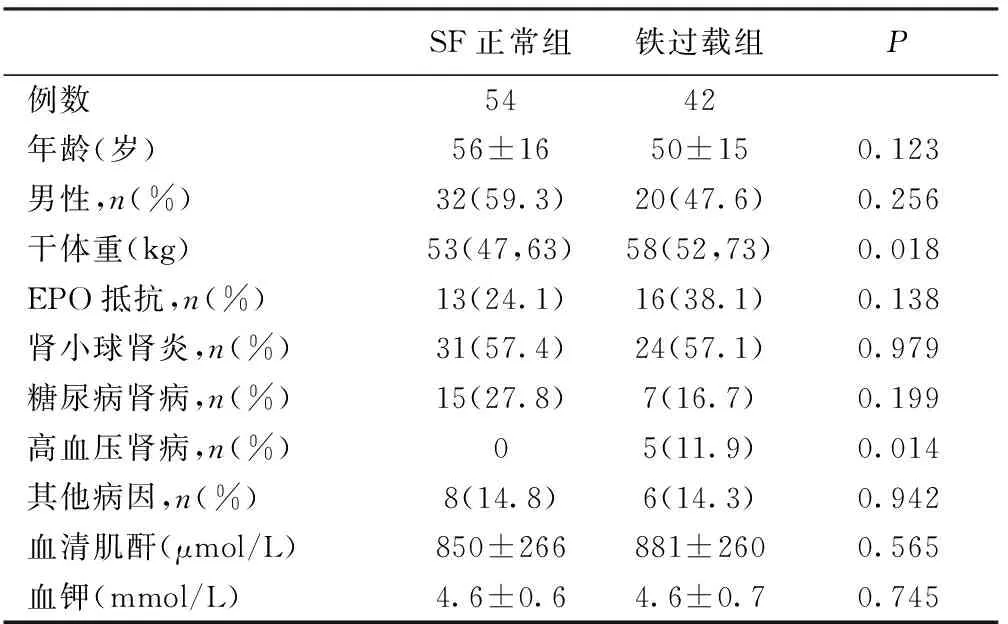
表2 96例患者一般临床资料
Hb的变化口服罗沙司他治疗后,SF正常组平均Hb由92±15 g/L增至105±14 g/L,铁过载组平均Hb由88±20 g/L增至102±20 g/L,差异均有统计学意义;治疗前后两组间Hb水平差异无显著性。两组患者Hb变化情况见图1。
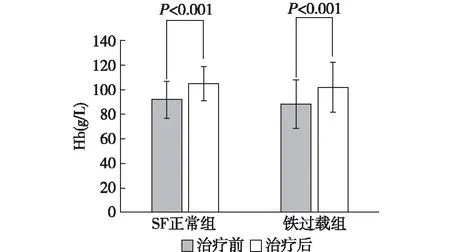
图1 两组受试者治疗前后Hb水平变化Hb:血红蛋白;SF:血清铁蛋白
罗沙司他治疗12周,SF正常组平均Hb增加了13±14 g/L,铁过载组平均Hb增加了13±17 g/L,两组受试者平均Hb变化量的差异无统计学意义(P=0.897)。
铁代谢的变化两组罗沙司他治疗后血清铁蛋白水平均较治疗前显著下降,而总铁结合力水平显著升高,差异均有统计学意义。两组患者治疗前后TSAT比较均无统计学意义(表3)。
罗沙司他治疗12周,两组患者的SF和TIBC改变量存在差异(P<0.05),提示不同基础铁代谢状态下罗沙司均能降低MHD患者SF水平,升高TIBC且保持TSAT稳定,但铁过载组SF下降幅度更大,TIBC上升幅度较小(表3)。
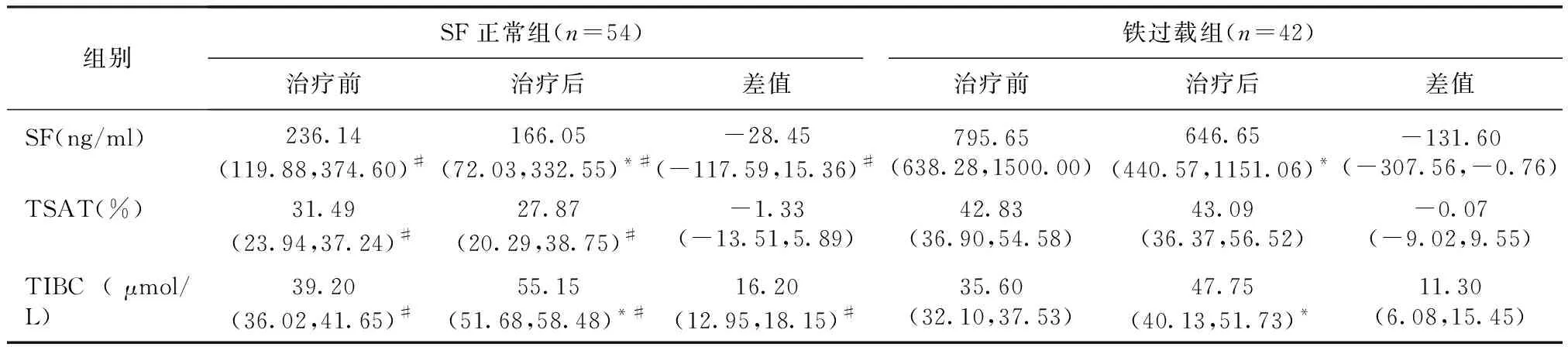
表3 治疗前后的铁代谢指标比较
按罗沙司他治疗后Hb<100 g/L和Hb≥100 g/L分组,对两组患者基线铁代谢指标进行对比分析,发现≥100 g/L组患者的SF水平较<100 g/L组患者低(P=0.019),TIBC水平更高(P<0.001),而TSAT差异无统计学意义(P=0.102)。
铁过载合并EPO抵抗的肾性贫血患者Hb及铁代谢变化本研究中铁过载组有16例EPO抵抗患者,口服罗沙司他治疗12周,Hb平均水平由77±14 g/L升至96±22 g/L(图2A),SF由819.55(560.73,1469.60)ng/ml降至623.38(444.32,1073.64)ng/ml(图2B),TIBC由35.85(32.83,37.73)μmol/L增至51.20(41.45,52.13)μmol/L(图2C),差异均有统计学意义。TSAT平均水平由49.16%(39.91%,60.44%)降至44.02%(36.42%,55.82%)(图2D),差异无统计学意义。

图2 铁过载合并EPO抵抗患者罗沙司他治疗前后实验室指标变化Hb:血红蛋白;SF:血清铁蛋白;TIBC:总铁结合力;TSAT:转铁蛋白饱和度;EPO:促红细胞生成素;A:治疗前后Hb水平变化;B:治疗前后SF水平变化;C:治疗前后TIBC水平变化;D:治疗前后TSAT水平变化
安全性评估所有患者均完成本试验,其中SF正常组1例胃肠道反应,铁过载组2例有胃肠道反应,1例出现高钾血症;两组患者不良反应发生率无明显差异。胃肠道不良反应主要包括腹痛、腹泻、恶心、呕吐,程度多为轻、中度,经干预后症状可消失或改善。1例患者于治疗4周和8周时出现高钾血症(血钾分别为6.11 mmol/L和5.48 mmol/L),予以常规降钾治疗后恢复正常。
讨 论
肾性贫血是各种肾脏病致肾功能恶化,肾脏生成EPO不足及血浆中有害物质干扰红细胞生成,缩短红细胞寿命导致的贫血。铁是人体Hb合成的重要原料,在胃肠道吸收、由转铁蛋白运输、以铁蛋白形式储存。SF和TSAT是最常用的评估铁状态的指标。铁蛋白的转录、翻译受到铁调节蛋白1(IRP1)调控,当细胞中铁含量高时,IRP1能使铁蛋白高效表达;而当细胞内铁水平低时,IRP1会导致铁蛋白表达降低。因此,SF是反映患者体内铁负荷情况的主要指标[9]。铁的利用需要转铁蛋白协助运输,TIBC是血清转铁蛋白能结合的最大铁量,反映的是转铁蛋白的实际水平;TSAT是指血液循环中蛋白结合铁的百分比,反映体内可利用铁的数量。
铁代谢紊乱是MHD患者发生贫血的重要原因之一。无论是绝对性铁缺乏(铁储备减少,循环中铁浓度降低)还是功能性铁缺乏(储存铁不低,但循环铁浓度降低)都可导致红细胞合成障碍。MHD患者可因凝血机制异常、反复血液净化管路失血以及食欲差等导致绝对性缺铁。此外,CKD患者由于机体微炎症反应和肾脏功能下降,体内铁调素水平异常升高,可导致铁利用障碍,出现功能性缺铁[10]。对于绝对性铁缺乏的肾性贫血患者,补充铁剂可以改善贫血,减少ESAs使用剂量,但对于功能性缺铁的患者,补铁治疗对于贫血纠正帮助不大反而增加了铁过载的风险[11]。铁过载会造成严重的并发症,包括自由铁通过促进活动性氧化物的产生[3],损伤肝细胞造成肝脏炎症反应和纤维化;通过损伤人内皮细胞,促进动脉粥样硬化的发生[12];通过抑制淋巴细胞的增殖,从而影响人体免疫系统[13]。因此,日本透析协会发布的指南对静脉铁剂的潜在毒性提出了警告[14],改善全球肾脏病预后组织也指出铁化合物可能造成铁过载及氧化应激等不良反应,并提出TSAT上限为30%,SF为500 ng/L[15]。
罗沙司他是一种口服的低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI),它能够维持HIF的稳定,上调EPO和EPO受体的表达,增加铁的吸收及利用,从而改善肾性贫血。以往的研究报道显示,相比于rHuEPO,罗沙司他治疗MHD患者肾性贫血效果更佳[5]。Akizawa等[16]的Ⅲ期临床试验显示,使用rHuEPO治疗的腹膜透析肾性贫血患者,更换为罗沙司他治疗后,能够进一步提高患者Hb水平。铁代谢方面,一项荟萃分析结果显示,在透析患者中,与ESAs组相比,罗沙司他组铁调素和SF水平降低,而TIBC和TSAT升高[17]。本研究结果显示,罗沙司他治疗后SF正常组和铁过载组SF均下降,TIBC水平均增加,TSAT保持稳定,与荟萃分析的结果基本一致。这表明不同铁代谢状态下,罗沙司他均可使患者体内铁储备释放,进而被骨髓利用;但铁过载组SF下降幅度更明显,TIBC上升幅度较小,提示在不同铁代谢状态下使用罗沙司他治疗MHD肾性贫血,铁代谢得到改善的程度不同,铁过载组铁负荷减轻更明显。同时,本研究发现,罗沙司他治疗后两组患者Hb水平均较基线上升,且两组患者Hb的改变量相当,这表明对于不同铁代谢状态的MHD患者,罗沙司他纠正贫血的效果相当。但是,进一步的分析发现,经罗沙司他治疗12周后Hb≥100 g/L组患者,其基线SF水平较<100 g/L组患者低,TIBC水平更高,提示适当提高患者转铁蛋白水平,合理的SF水平可能更有利于使用罗沙司他达到Hb治疗靶目标。此外,本研究中的16例铁过载合并EPO抵抗的患者,根据其相关辅助检查,排除了活动性炎症、肝脏疾病及肿瘤等致铁过载的原因,给予罗沙司他治疗后近期疗效显著,Hb和TIBC水平上升,SF水平下降,TSAT保持稳定提示对肾性贫血使用大剂量EPO,仍不能达到Hb靶目标者,为避免长期大剂量使用EPO带来的不良反应,可选择口服罗沙司他纠正贫血。本研究中患者对罗沙司他耐受良好,无心脑血管事件、血栓栓塞、死亡等严重不良事件。
综上所述,对于不同铁代谢状态的MHD患者,罗沙司他治疗可有效纠正贫血和改善铁代谢,但铁代谢得到改善的程度有所不同,铁过载患者铁负荷减轻更加明显。

