药学监护在抗肿瘤药物治疗中的作用研究
李国誉,关洁妍,冯昌文,唐慧妍
(肇庆市第一人民医院,广东 肇庆 526060)
0 引言
恶性肿瘤严重影响患者的身体健康,其发病率日趋增加,已成为严重威胁人类健康的重要公共卫生问题之一[1]。近年来,恶性肿瘤的治疗已从化疗、靶向治疗时代迈向免疫治疗时代。而无论选择何种药物进行治疗,其疗效、安全性以及患者生活质量的评价都是临床上最值得关注的问题[2-3]。因此,在抗肿瘤药物治疗中,除了医疗方面的诊治以外,更需要临床药师的参与并实施药学方面的监护。本文通过研究恶性肿瘤患者实施药学监护后的疗效评价结果、不良反应发生情况,以及用药前后生活质量评分,以探讨药学监护在抗肿瘤药物治疗中的作用。
1 资料与方法
1.1 一般资料
纳入标准:年龄≥18岁;肿瘤诊断明确;所有患者或其法定代理人均签署治疗知情同意书。排除标准:伴有严重心血管、慢性自身免疫性疾病;需长期服用免疫抑制剂;肝肾功能严重损害;慢性感染;器官移植者。选取肇庆市第一人民医院2019年10月—2021年3月期间肿瘤诊治中心150例实施药学监护的肿瘤患者作为研究组,其中男67例,女83例,年龄32—76岁,平均(55.83±3.67)岁,病程平均(2.35±0.57)年;另随机选取我院同期肿瘤诊治中心150例未实施药学监护的肿瘤患者作为对照组,其中男69例,女81例,年龄34—78岁,平均(57.19±3.96)岁,病程平均(2.44±0.62)年。两组资料具有可比性(P>0.05)。
1.2 方法
对照组患者予常规抗肿瘤药物治疗,未实施药学监护。研究组患者则在用药后实行药学监护,内容包括:①参与临床查房,监测患者用药全过程,对药物治疗做出综合评价,发现和报告药物不良反应;②实时审核用药医嘱,保证合理用药;③对医护人员进行用药指导,提供有关药物的信息咨询服务;④为患者提供用药教育,提高其治疗依从性;⑤注意患者以往病史,如是否合并糖尿病和高血压等疾病,若有需要确保联合用药的合理性,并定期关注患者的血压和血糖的控制情况等[4]。
1.3 评价标准
比较两组患者在药物治疗后的疗效评价结果、不良反应发生情况,以及用药前后睡眠质量、生活质量评分。根据irRECIST1.1标准评价疗效,分为完全缓解(complete reponse,CR)、部 分 缓 解(partial response,PR)、疾 病 稳定(stabledisease,SD)和疾病进展(progressive disease,PD),客观缓解率(objective response rate,ORR)=(CR + PR)/ 总例数×100%,疾病控制率(disease control rate,DCR) =(CR + PR + SD)/ 总例数×100%。不良反应监测包括全身乏力、皮肤反应、消化道反应、发热、肝肾功能异常、免疫功能异常、血液毒性、肾脏毒性等,并根据《常见不良事件评价标准》(CTCAE)5.0版对不良反应的严重程度进行分级。睡眠质量以匹兹堡睡眠质量指数(PSQI)评分评估,6项评价,总分为 21分,分数越高表示睡眠障碍越严重,就也就是睡眠的状态越差。生活质量评价采用“癌症患者生命质量核心量表(EORTCQLQ-C30)”自评,共有六项,得分越高表示生活质量越高。
1.4 统计学方法
2 结果
2.1 两组患者在用药治疗后的疗效评价结果、不良反应发生情况比较
研究组患者在用药治疗后的ORR与DCR均高于对照组,而不良反应发生率以及不良反应分级明显低于对照组,结果均有显著性差异(P<0.05)。详见表1。
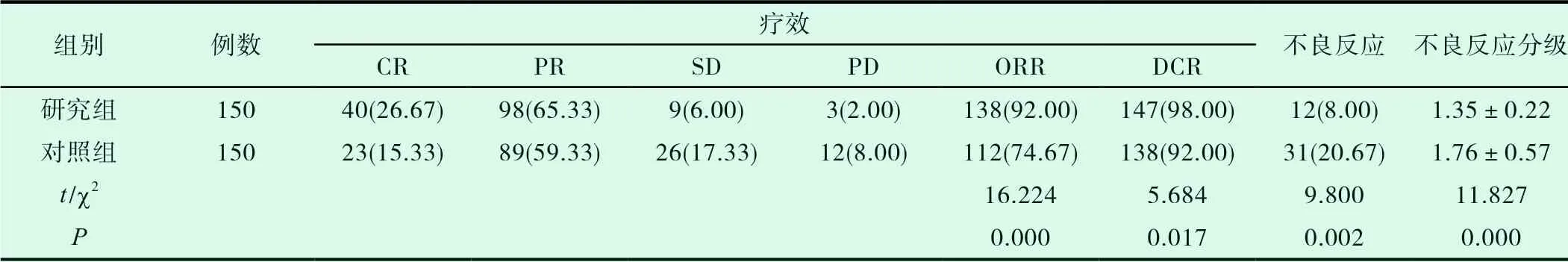
表1 两组患者在用药后的实体瘤疗效评价结果、不良反应发生情况比较[n,(%)]
2.2 两组患者用药前、后睡眠质量评分比较
两组患者用药前睡眠质量评分相比,差异(P>0.05)无意义。经用药后两组睡眠质量评分均有着明显下降,其中研究组患者各评分均显著低于对照组,差异(P<0.05)有意义。详见表2。
表2 两组患者用药前、后睡眠质量评分比较(±s,分)
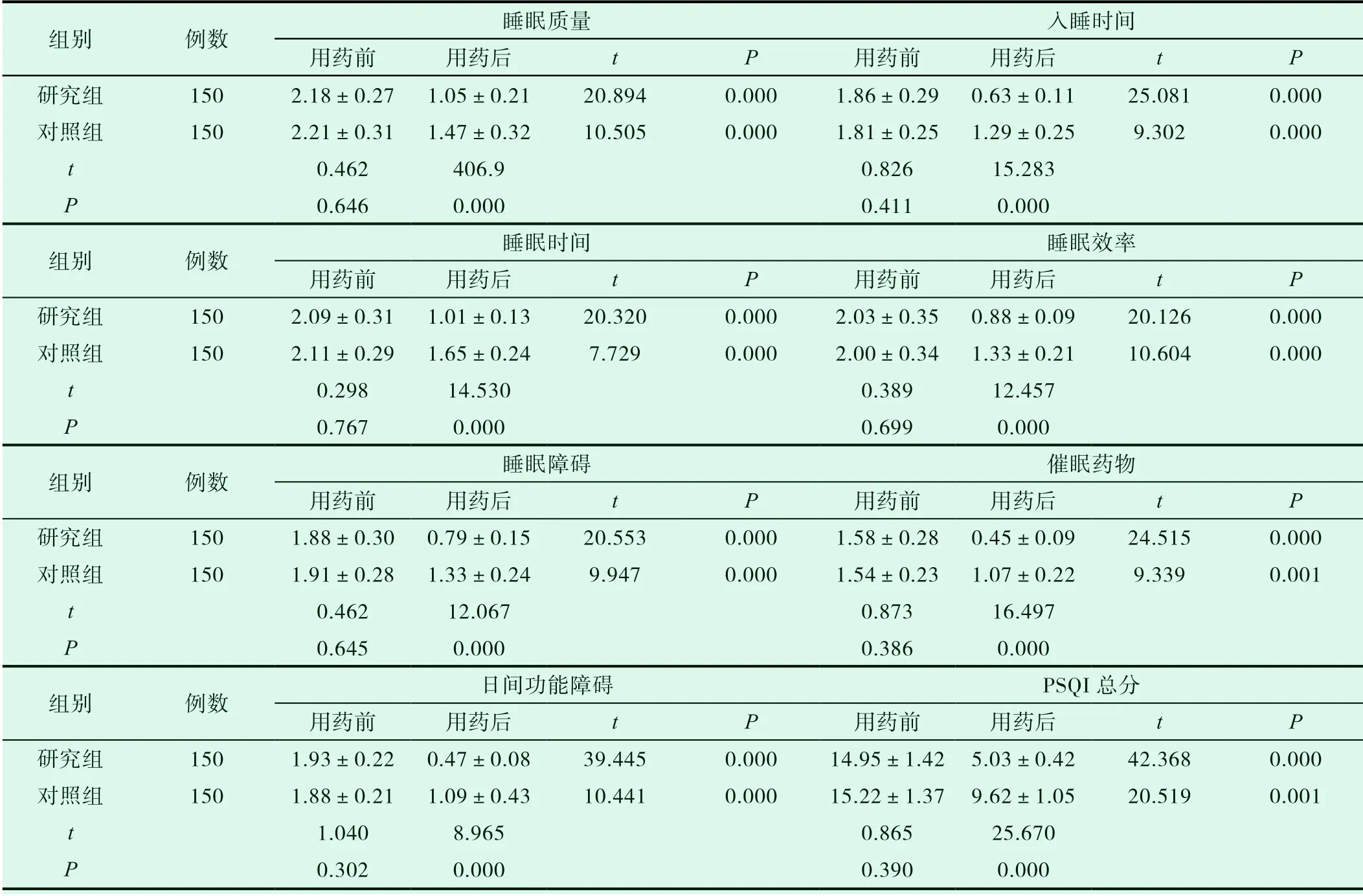
表2 两组患者用药前、后睡眠质量评分比较(±s,分)
组别 例数 睡眠质量 入睡时间用药前 用药后 t P 用药前 用药后 t P研究组 150 2.18±0.27 1.05±0.21 20.894 0.000 1.86±0.29 0.63±0.11 25.081 0.000对照组 150 2.21±0.31 1.47±0.32 10.505 0.000 1.81±0.25 1.29±0.25 9.302 0.000 t 0.462 406.9 0.826 15.283 P 0.646 0.000 0.411 0.000组别 例数 睡眠时间 睡眠效率用药前 用药后 t P 用药前 用药后 t P研究组 150 2.09±0.31 1.01±0.13 20.320 0.000 2.03±0.35 0.88±0.09 20.126 0.000对照组 150 2.11±0.29 1.65±0.24 7.729 0.000 2.00±0.34 1.33±0.21 10.604 0.000 t 0.298 14.530 0.389 12.457 P 0.767 0.000 0.699 0.000组别 例数 睡眠障碍 催眠药物用药前 用药后 t P 用药前 用药后 t P研究组 150 1.88±0.30 0.79±0.15 20.553 0.000 1.58±0.28 0.45±0.09 24.515 0.000对照组 150 1.91±0.28 1.33±0.24 9.947 0.000 1.54±0.23 1.07±0.22 9.339 0.001 t 0.462 12.067 0.873 16.497 P 0.645 0.000 0.386 0.000组别 例数 日间功能障碍 PSQI总分用药前 用药后 t P 用药前 用药后 t P研究组 150 1.93±0.22 0.47±0.08 39.445 0.000 14.95±1.42 5.03±0.42 42.368 0.000对照组 150 1.88±0.21 1.09±0.43 10.441 0.000 15.22±1.37 9.62±1.05 20.519 0.001 t 1.040 8.965 0.865 25.670 P 0.302 0.000 0.390 0.000
2.3 两组患者用药前后生活质量评分比较
两组患者用药前生活质量评分相比,无显著性差异(P>0.05);对照组用药后生活质量各项评分均明显低于用药前,也低于研究组,均有显著性差异(P<0.05);而研究组用药后生活质量各项评分同样较低于药前,但无显著性差异(P>0.05)。详见表3。
表3 两组患者用药前、后生活质量评分比较(±s)

表3 两组患者用药前、后生活质量评分比较(±s)
组别 例数 社会 认知用药前 用药后 t P 用药前 用药后 t P研究组 150 73.13±7.34 71.67±5.72 1.922 0.056 75.63±4.81 73.96±9.46 1.927 0.055对照组 150 74.09±7.29 68.64±5.03 7.536 0.000 76.22±4.39 70.58±6.21 9.083 0.000 t 1.137 4.872 1.110 3.658 P 0.267 0.000 0.268 0.000组别 例数 角色 情绪用药前 用药后 t P 用药前 用药后 t P研究组 150 66.82±3.96 65.93±6.67 1.405 0.161 74.75±5.57 73.28±7.58 1.914 0.057对照组 150 67.02±4.33 60.55±5.96 10.756 0.000 75.34±5.67 68.68±7.94 8.360 0.000 t 0.417 7.366 0.909 5.132 P 0.677 0.000 0.364 0.000组别 例数 躯体 总体用药前 用药后 t P 用药前 用药后 t P研究组 150 73.25±4.46 71.94±7.42 1.853 0.065 81.64±5.78 80.87±7.64 0.984 0.326对照组 150 74.13±4.67 67.86±5.98 10.121 0.000 82.81±5.81 70.64±4.78 19.811 0.000 t 1.669 5.244 1.748 13.903 P 0.096 0.000 0.081 0.000
3 讨论
药学监护是直接由临床药师为患者提供药物相关监护服务的服务模式,包括对给药途径、给药剂量、药物选择适应性、给药速度、配伍稳定性、药物替代疗法、溶媒选择适宜性等内容的审核有助于最大限度地降低给药风险。临床药师参与用药医嘱的审核和点评是当前临床合理用药的重要保障,同时还有助于医药工作者之间的沟通和交流,通过医师和药师会将之间的相互协作达到优化抗肿瘤治疗方案、减少辅助药物不合理应用、降低药源性不良事件发生率、限制不必要医疗费用等目的,通过系统且完善的事前干预全面促进合理用药。以提高用药安全性、合理性,降低用药不良反应率,改善其预后效果与生活质量为目的[5]。多项究[6-10]表明,临床药师干预抗肿瘤药物的临床应用,并参与患者的用药指导和用药教育,可提高药物治疗效果,减少不良反应的发生。研究结果显示,在药物治疗后研究组患者的客观缓解率(ORR)与疾病控制率(DCR)均高于对照组,而不良反应发生率以及不良反应分级则低于对照组,结果均有显著性差异(P<0.05)。两组患者用药前睡眠质量评分相比,差异(P>0.05)无意义。经用药后两组睡眠质量评分均有着明显下降,其中研究组患者各评分均显著低于对照组,差异(P<0.05)有意义。两组患者用药前生活质量评分相比,无显著性差异(P>0.05);对照组用药后生活质量各项评分均明显低于用药前,也低于研究组,均有显著性差异(P<0.05);而研究组用药后生活质量各项评分同样较低于药前,但无显著性差异(P>0.05)。说明了药学监护对于提高抗肿瘤药物的疗效,减少不良反应的发生,改善患者的预后与生活质量等均有很好的促进作用。研究结论与国内其他文献结论具有一致性。因此,在抗肿瘤药物治疗中实施药学监护是提高肿瘤患者治疗效果和依从性、减少不良反应、改善生存率和生活质量的重要举措[11-13],是肿瘤综合治疗的重要组成部分,也是保证肿瘤规范化治疗水平、医疗质量和医疗安全的关键所在。
综上所述,在抗肿瘤药物治疗中,通过实施药学监护,可较为有效的提升客观缓解率和疾病控制率,减少在用药期间不良反应的发生,以及改善患者的预后、睡眠质量和生活质量。

