高容量CoFe2O4@V3O7复合电极材料的制备及其电化学性能
李谓群,李睿智,朱圣远,巴 鑫,周盈科
(1.武汉科技大学省部共建耐火材料与冶金国家重点实验室,湖北 武汉,430081;2.武汉科技大学材料与冶金学院,湖北 武汉,430081;3.湖北省产品质量监督检验研究院,湖北 鄂州,436070)
超级电容器功率密度大、充放电速度快且维护成本低,在便携电子产品领域具有广阔的应用前景[1]。该类电容器常以炭材料、过渡金属氧化物或导电聚合物作为其电极材料,其中,过渡金属氧化物铁酸钴(CoFe2O4)具有良好的倍率性能和较强的各向异性,易磁化且结构稳定,是一种极具发展潜力的二元金属氧化物[2]。
已有研究表明,使用Co、Fe二元金属氧化物作为电极材料并将其微观形貌设计为片状[3]、针状[4]或盒状[5]时,能明显增大电极比表面积、增加活性位点、增强电子的传输能力和离子的扩散能力。此外,以二元金属氧化物为基材制备复合材料电极也是一种能有效提升电极性能的可行性方案,例如Zhao等[6]采用溶胶-凝胶法结合热处理工艺将CoFe2O4与炭材料复合,Song等[7]在CoFe2O4材料表面包覆导电聚合物PEDOT,都获得了电化学性能更佳的电极材料。不过,将过渡金属氧化物与炭材料或导电聚合物复合虽有助于氧化物骨架内的电子转移,在一定程度上提高电极材料的导电性能,但因炭材料、导电聚合物自身容量较低,所制复合材料电极容量相比单一过渡金属氧化物电极容量提升幅度有限。有鉴于此,本文结合电极材料微观形貌设计及复合材料电极制备这两种电极性能优化措施,首先借助简单水热合成法在碳布上生长CoFe2O4纳米棒阵列材料,再基于过渡金属氧化物中的钒氧化物(VOx)具有离子脱嵌空间大、理论容量高、价态多样且储量丰富等特点[8-10],利用水热法将比电容较高的V3O7[11]包覆于CoFe2O4纳米棒表面制备CoFe2O4@V3O7复合电极材料,重点分析二次水热反应时间及相关反应物浓度对所制电极电化学性能的影响,以期为更高容量电极材料的研发提供参考。
1 实验
1.1 试剂
九水合硝酸铁(Fe(NO3)3·9H2O)、六水合硝酸钴(Co(NO3)2·6H2O)、氟化氨(NH4F)、尿素(CO(NH2)2)、偏钒酸铵(NH4VO3)等均为分析纯;W0S1009-亲水型碳布产自台湾碳能科技股份有限公司。
1.2 样品的制备
1.2.1 CoFe2O4纳米棒阵列的制备
利用简单水热反应结合退火工艺制备纯CoFe2O4纳米棒阵列。首先将碳布裁剪为2 cm× 4 cm的长方形,依次置于丙酮、乙醇、去离子水中超声清洗20 min;量取35 mL去离子水,向其中加入2 mmol Fe(NO3)3·9H2O、1 mmol Co(NO3)2·6H2O、4 mmol NH4F及10 mmol CO(NH2)2并搅拌均匀,将清洗过的碳布完全浸入该混合溶液,随后移至反应釜中于90 ℃温度下反应10 h;待水热反应结束、反应釜冷却至室温后,取出长有前驱体的碳布清洗、烘干,再将其置于管式炉中,在Ar气氛下以10 ℃/min的升温速率升至450 ℃并保温2 h,之后自然冷却至室温得到纯CoFe2O4纳米棒阵列材料。
1.2.2 CoFe2O4@V3O7复合电极材料的制备
基于所制纯CoFe2O4纳米棒阵列材料前驱体,在不同NH4VO3浓度、不同反应时间条件下,再次利用水热法在CoFe2O4纳米棒阵列上生长V3O7来制备CoFe2O4@V3O7复合电极材料。首先,量取NH4VO3投放至80 mL乙二醇中于80 ℃下搅拌至完全溶解,得到具有一定NH4VO3浓度(0.005、0.01、0.02 mol/L)的混合溶液,将长有前驱体CoFe2O4的碳布浸入该混合溶液并一同移至反应釜中于180 ℃温度下反应一定时间(18、24、30 h),待反应釜冷却至室温后取出碳布,依次使用去离子水及乙醇将其清洗干净,烘干后再置于管式炉中,在Ar气氛下以5 ℃/min的升温速率升至400 ℃并保温2 h,之后自然冷却至室温得到CoFe2O4@V3O7复合电极材料。
1.3 样品的表征
利用PHILIPSXL30TMP型扫描电子显微镜(SEM)及其附带的能量色散 X 射线荧光光谱仪(EDX)对样品形貌、结构及成分进行表征;使用装备有Cu靶Kα射线(λ =0.154 18 nm)的PHILIPS X’Pret MPD Pro型X射线衍射仪(XRD)对样品的物相及晶体结构进行表征;借助VG Multilab 2000型X射线光电子能谱仪(XPS)对样品中铁、钴、钒等元素的价态进行表征。
1.4 样品电化学性能测试
通过连接在VMP3型多通道电化学工作站(法国Bio-Logic公司)上的三电极体系对相关样品进行循环伏安(CV)、恒流充放电(GCD)以及电化学阻抗(EIS)等电化学性能测试。在三电极体系中以本研究所制样品为工作电极活性材料、铂片电极为对电极、Ag/AgCl电极为参比电极,测试所用KOH溶液浓度为3 mol/L。CV测试中的扫描速率分别为1、2、5、10、20、50、100 mV/s。GCD测试中的电流密度分别为2、3、4、5、6、10 mA/cm2,测试电位为-1.2~0 V。EIS测试时的频率范围为10 mHz至1 MHz,交流扰动电压为10 mV。
2 结果与讨论
2.1 样品的表征结果分析
图1所示为水热法所制前驱体样品的SEM照片及XRD图谱。由图1(a)可见,所制样品呈现均匀的纳米棒阵列形貌,单根纳米棒直径约为30 nm,长度约为80~120 nm;从图1(b)可以看出,样品XRD图谱中的特征衍射峰与JCPDS(No.22-1086)中CoFe2O4的标准数据相符且无其它杂峰出现,证实所制前驱体为纯CoFe2O4纳米棒阵列材料。
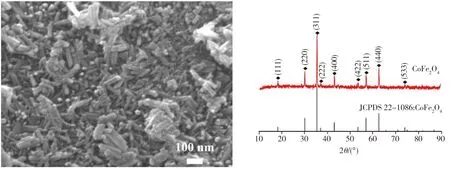
(a)SEM照片 (b)XRD图谱图1 前驱体的SEM照片及XRD图谱Fig.1 SEM image and XRD spectrum of precursor
在成功制备纯CoFe2O4纳米棒阵列材料前驱体的基础上,利用二次水热反应于不同反应条件下所制复合材料的SEM照片如图2所示。设定NH4VO3浓度为0.01 mol/L,当水热反应时间为18 h时,从所制复合材料中可以观察到由大量细颗粒连接组成的多孔骨架结构覆盖于CoFe2O4纳米棒表面(见图2(a));当水热反应时间增至24 h时,所制复合材料中的颗粒数量增多且尺寸增大,骨架结构间的空隙几乎被完全填充,大量近似立方体(边长约为100 nm)的颗粒组成均匀致密的壳层将纳米棒包裹其中,整个复合材料表面趋于平整(见图2(b));当水热反应时间延长至30 h时,所制复合材料表面附着的颗粒状物质进一步增多且颗粒团聚现象严重,地毯式包裹住每一根纳米棒(见图2(c))。比较图2(a)~图2(c)所示的样品SEM照片可知,当NH4VO3浓度不变时,水热反应24 h所制复合材料样品的微观形貌最佳。设定水热反应时间为24 h,将NH4VO3浓度调整为0.005 mol/L时,所制复合材料中的纳米棒表面一部分被片状物质覆盖,剩余部分则裸露在外(见图2(d));将NH4VO3浓度进一步增至0.02 mol/L时,所制复合材料表面出现大面积块状团聚物(见图2(e))。经分析比较图2(b)、图2(d)及图2(e)所示的样品SEM照片可知,当水热反应时间不变时,在NH4VO3浓度为0.01 mol/L的条件下所制复合材料的微观形貌最佳。综合复合材料SEM微观组织分析结果表明,设定NH4VO3浓度为0.01 mol/L、二次水热时间为24 h时,所制复合材料微观形貌最理想。

(a)NH4VO3 0.01 mol/L,水热18 h (b)NH4VO3 0.01 mol/L,水热24 h
在NH4VO3浓度为0.01 mol/L、二次水热时间为24 h条件下所制复合材料的元素分布图及XRD图谱如图3所示。从图3(a)中可以看出,Fe、Co、V三种金属元素均匀分布在复合材料表面;由图3(b)可知,样品XRD图谱中除了2θ为26.54°附近的宽峰归属于碳布基底中的碳以外,其余衍射峰则分别对应于CoFe2O4(JCPDSNO.22-1086)和V3O7(JCPDSNO.71-1591)的标准衍射数据。上述结果充分证明,经二次水热反应所制样品为CoFe2O4、V3O7所组成的复合材料,且V3O7覆盖于CoFe2O4纳米棒表面。
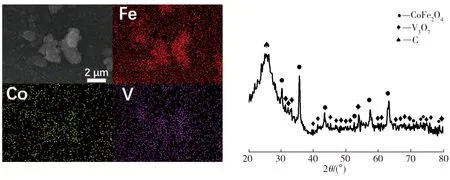
(a)元素分布 (b)XRD图谱图3 复合材料的元素分布及XRD图谱Fig.3 Element distribution and XRD spectrum of composites
所制复合材料样品的XPS测试结果如图4所示。由图4(a)可知,样品的组成元素有Fe、Co、O、C和V;由图4(b)可见,Co2p精细谱中位于782.1、796.8 eV处的主峰分别对应于CoFe2O4
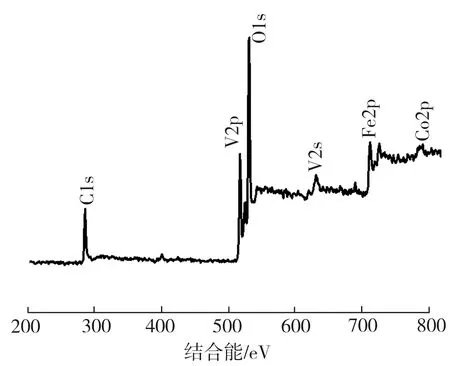
(a)总谱图
中的Co2p3/2和Co2p1/2,位于781.73、796.27 eV处的分峰均与Co3+相对应,位于785.7、803.4 eV处的分峰则对应于Co2+[12];由图4(c)可见,Fe2p精细谱中位于711.1、725 eV处的峰分别对应于Fe2p3/2和Fe2p1/2,表明复合材料中同时存在+2价与+3价的Fe[3];由图4(d)可见,V2p精细谱中位于517.3、524.2 eV 处的主峰分别对应于V2p3/2和V2p1/2,其中的分峰表明复合材料中存在V5+,在516.2 eV处的分峰则是V4+存在的明显证据[13],这是因退火过程中以氩气为保护气氛而导致水热反应生成的V4+没有完全被氧化;由图4(e)可见,O1s精细谱中位于530.4、531.6 eV处的峰依次对应于复合材料中的M—O键(M表示金属)及O—H键,这可能是因样品在存放与测试过程中吸水所致[14]。上述XPS表征结果进一步证实CoFe2O4已与V3O7成功复合。
2.2 样品的电化学性能分析
纯CoFe2O4和不同二次水热反应条件下所制CoFe2O4@V3O7复合材料样品在扫描速率为20 mV/s时的CV曲线以及不同扫描速率下的比电容变化曲线如图5所示。由图5(a)可见,在NH4VO3浓度为0.01 mol/L、不同水热反应时间条件下所制复合材料的CV曲线积分面积均明显大于纯CoFe2O4材料CV曲线相应值,表明将CoFe2O4与V3O7复合有效地提升了电极材料的比电容,其中在水热反应时间为24 h条件下所制CoFe2O4@V3O7复合材料样品的CV曲线积分面积最大,表明其比电容也最大;由图5(b)可知,在水热反应时间为24 h、不同NH4VO3浓度条件下所制复合材料的CV曲线积分面积也都明显大于纯CoFe2O4材料相应值,并且仍以NH4VO3浓度为0.01 mol/L、水热反应时间为24 h条件下所制复合材料的CV曲线积分面积为最大。此外,从图5(a)及图5(b)中还注意到,对纯CoFe2O4电极进行CV测试的电压窗口为-1.3~-0.2 V,对CoFe2O4@V3O7复合材料电极进行CV测试的电压窗口为-1.3~0 V,这是因为V3O7的引入拓宽了电极材料的工作电压区间;由图5(c)可见,在NH4VO3浓度为0.01 mol/L、不同水热反应时间条件下所制复合材料电极在同一扫描速率下的比电容均大于纯CoFe2O4电极相应值,并且复合材料电极比电容随水热反应时长的增加而先增大后减小,其中以反应24 h条件下所制复合材料的比电容为最大,其容量性能较纯CoFe2O4材料提升约90%。这是因为钒氧化物的引入拓宽了电极的工作区间,加之CoFe2O4和V3O7间的协同作用能有效增加电极材料的比电容,所以相较于纯CoFe2O4电极材料,复合材料电极的比电容明显增大,不过制备复合材料时的水热反应时间过长会造成V3O7包覆物过多,这将阻碍电荷的传输和电解液的渗入,进而影响电极材料与电解液中离子的反应,导致电极材料比电容下降;由图5(d)可见,在水热反应时间为24 h、不同NH4VO3浓度条件下所制复合材料电极在同一扫描速率下的比电容随NH4VO3浓度的增加呈先增大后减小的变化趋势,并且仍以NH4VO3浓度为0.01 mol/L、水热反应时间为24 h条件下所制复合材料电化学性能为最佳。综合上述分析并结合图2所示的样品微观形貌观察结果可以确定,CoFe2O4@V3O7复合电极材料的最佳制备条件是NH4VO3浓度为0.01 mol/L、二次水热反应时间为24 h。
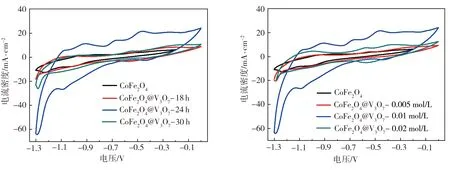
(a)不同水热反应时间下所制样品的CV曲线 (b)不同NH4VO3浓度下所制样品的CV曲线
最佳制备条件下所制CoFe2O4@V3O7复合电极材料的电化学性能测试结果如图6所示。由图6(a)可见,复合材料电极在不同扫描速率下的CV曲线中均存在明显的氧化还原峰,表明该电极为典型的赝电容电极,且所有的峰都与金属元素的M—O/M—O—OH(M为Co、Fe、V)转化过程相关[15],主要的反应式有[14,16-17]:

(1)

(2)

(3)

(4)

(5)
此外,扫描速率的变化并没有导致相应的样品电极CV曲线图形出现明显失真,这也反映出所制复合电极材料具有良好的倍率性能,样品电极CV曲线中的峰位随扫描速率增加而产生的少许偏移应是电极在高速扫描条件下极化所致。根据样品CV测试结果,计算出该电极在扫描速率为1、100 mV/s时的面积比电容依次为4.28、0.30 F/cm2,由此可见,即使扫描速率增大100倍,样品电极仍具有一定的比电容。因CoFe2O4@V3O7复合材料电极活性物质负载量为2.9 mg/cm2,故该电极在扫描速率为1 mV/s时的面积比电容值(4.28 F/cm2)可换算为1475.86 F/g(质量比电容),其电容性能相比核壳CoFe2O4@MnO2纳米片阵列(3.59 F/cm2)[14]、多孔纳米棒CoFe氧化物材料(1.23 F/cm2)[18]、CoFe2O4/CoOOH复合材料(1208 F/g)[19]、无定形氧化钒纳米片阵列(554 mF/cm2)[20]、PEDOT∶PSS/V2O5材料(60 mF/cm2)[21]、V3O7·H2O/CNT/rGO复合材料(685 F/g)[22]等均有一定程度的提升。由图6(b)可见,复合材料电极GCD曲线出现明显的平台,证实了该电极的赝电容特性,同时,类三角形的GCD曲线图形也表明所制电极材料具有良好的转化反应可逆性。经计算,CoFe2O4@V3O7复合材料电极在电流密度分别为2、3、4、5、6、10 mA/cm2条件下的面积比电容依次为2.29、1.02、0.67、0.46、0.36、0.25 F/cm2。由图6(c)可见,复合材料电极EIS曲线由高频、中频、低频3部分组成,高频区中电极EIS曲线与实轴的交点表示电极材料内阻Rs,局部放大图显示,纯CoFe2O4材料电极Rs(1.48 Ω)明显大于CoFe2O4@V3O7复合电极相应值(1.21 Ω);中频区中电极EIS曲线经Zview软件拟合后可求得CoFe2O4@V3O7电极与CoFe2O4电极的电子转移与扩散阻抗Rct分别为0.04、0.12 Ω,表明纯CoFe2O4纳米棒阵列材料与V3O7复合后,材料中电荷迁移速度得到明显提升;低频区中电极EIS曲线经Zview软件拟合后的直线斜率越大则表示电极在电解液中发生赝电容氧化还原反应时离子的扩散阻抗Zw越小,图中CoFe2O4@V3O7电极EIS曲线经拟合后的直线斜率较纯CoFe2O4电极更大,表明CoFe2O4@V3O7电极具有较小的扩散阻抗Zw。因此,CoFe2O4@V3O7复合材料电极的Rs、Rct及Zw均低于纯CoFe2O4电极相应值,表明V3O7包覆有效改善了电极材料的电导率。由图6(d)可见,在50 mV/s扫描速率下分别对CoFe2O4@V3O7复合材料电极和纯CoFe2O4电极进行1000次循环测试的过程中,复合材料电极始终展示出较纯CoFe2O4电极更高的比电容,并且随着循环次数的增加,前者比电容的降幅较后者更小,与第1次循环测试后的电极电容相比,进行第1000次循环后CoFe2O4@V3O7电极的电容保持率为62%,而纯CoFe2O4电极的相应值为44%,表明V3O7包覆可有效提升电极的容量保持率,在一定程度上改善了单一材料电极循环性能较差的状况。
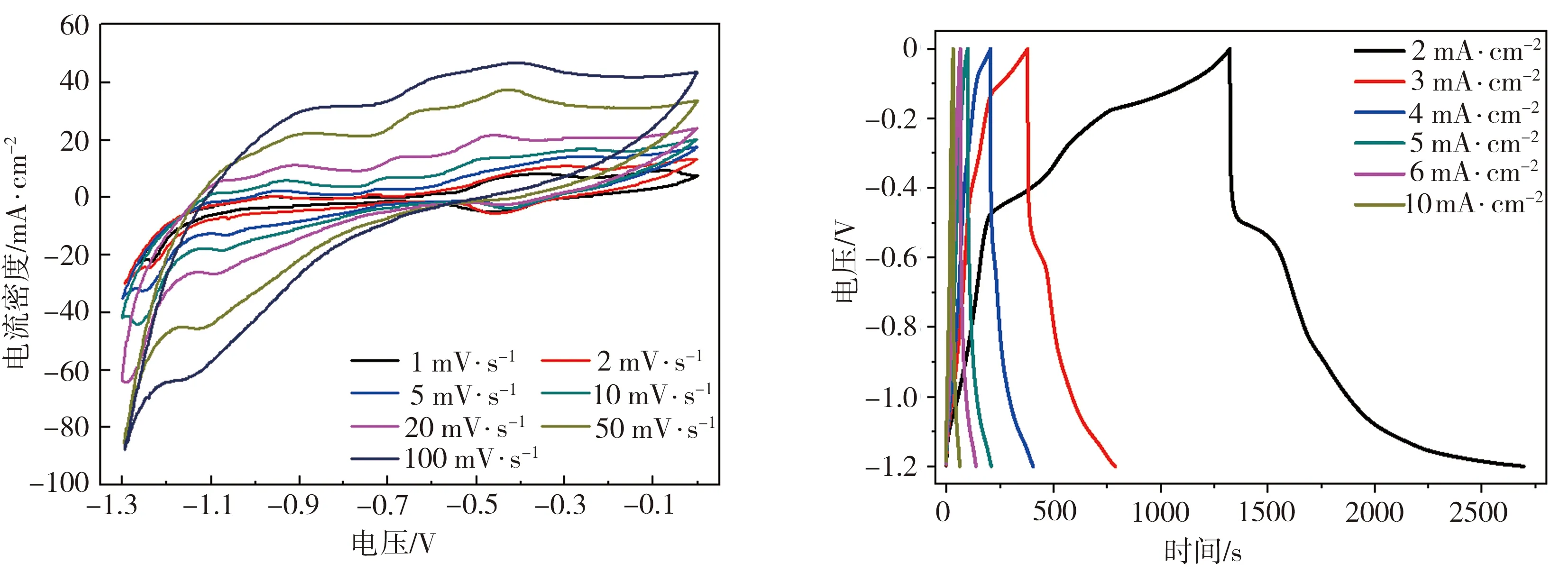
(a)CV曲线 (b)GCD曲线
3 结论
(1)在利用简单水热法制备纯CoFe2O4纳米棒阵列材料前驱体的基础上,可利用二次水热法成功制备CoFe2O4@V3O7复合电极材料。
(2)当NH4VO3浓度为0.01 mol/L、二次水热反应时长为24 h时,所制CoFe2O4@V3O7复合材料具有均匀、平整的微观形貌,以其为电极时,相应电极容量较纯CoFe2O4电极提升约90%,在1 mV/s的扫描速率下,该电极最大比电容达到4.28 F/cm2(1475.86 F/g),并且在50 mV/s的扫描速率下循环1000次后,其容量保持率为62%。

